Comment faire pour stabiliser les protéines : écrans de stabilité thermique décaler dosages et Nano différentielle Fluorimétrie dans le projet Virus-X à balayage
Summary
Un protocole est présenté pour tester rapidement la stabilité thermique des protéines dans une variété de conditions par décalage thermique et nano différentielle à balayage fluorimétrie. Systèmes tampon, de sels et d’additifs, ensemble comprenant trois écrans de stabilité unique, sont dosés avec des protéines afin d’identifier des tampons adaptés pour des études fonctionnelles et structurelles.
Abstract
Le projet Horizon2020 Virus-X a été mis en place en 2015 pour explorer la virosphere de certains biotopes extrêmes et découvrir de nouvelles protéines virales. Afin d’évaluer la valeur potentielle de biotechnique de ces protéines, l’analyse des protéines, structures et fonctions est un défi central dans ce programme. La stabilité de l’échantillon de protéine est essentielle pour fournir des résultats significatifs et augmenter le crystallizability des cibles. Le dosage de décalage thermique (TSA), une technique axée sur la fluorescence, est établi comme une méthode populaire pour optimiser les conditions pour la stabilité des protéines à haut débit. En CST, les fluorophores indépendants sont des colorants extrinsèques, sensible à l’environnement. Une alternative, technique semblable est nano différentielle à balayage fluorimétrie (nanoDSF), qui s’appuie sur la fluorescence natif de protéine. Nous présentons ici un roman osmolyte écran, un écran de 96-condition d’additifs organiques conçu pour guider les essais de cristallisation à travers des expériences préliminaires de TSA. Ainsi que des écrans sels et pH développés précédemment, l’ensemble des trois écrans fournit une analyse complète de la stabilité des protéines dans un large éventail de systèmes de tampon et d’additifs. L’utilité des écrans est démontrée dans l’analyse de la TSA et nanoDSF de lysozyme et protéine X, une protéine cible du projet Virus-X.
Introduction
De nombreuses enzymes biotechnologique-utiles proviennent de sources virales, telles que le tabac etch virus (TEV) protéase1 et le rhinovirus humain type 3C (VRC 3c) protéase2. Le projet (Figure 1) de Horizon2020 Virus-X3. Ce programme vise b d’élargir la palette des propriétés de familles d’enzymes connus et (b) de caractériser de nouveaux enzymes de fonction encore inconnue (Enzyme X). Détermination de la structure cristallographique joue un rôle central dans la caractérisation des protéines cibles, en particulier dans les cas où les séquences de protéines ont évolué au-delà de la reconnaissance de4. Stabilité des protéines est un facteur clé dans le processus de cristallisation ; échantillons doivent être conformationnellement homogènes et charpentées sur une période de temps de forme haute qualité, diffractant cristaux. En outre, il est essentiel pour les tests d’activité qui les protéines existent dans leur conformation active, qui peut également être facilitée par un environnement favorable moléculaire.
Malgré le développement de la technologie disponible pour cristallographes, cristallisation de protéines demeure un processus empirique de longues et fastidieuses5. Des expériences préliminaires biophysiques pour améliorer la stabilité des protéines en solution donnent clairement un meilleur point de départ pour la cristallisation de protéines et consomment habituellement seulement une infime quantité de protéine échantillon6,7, 8,9. Le grand nombre de protéines cibles à étudier dans ce projet nécessite également des essais de stabilité évolutive et à haut débit. L’une des méthodes plus populaires pour la caractérisation biophysique avant la cristallisation des protéines est l’analyse de décalage thermique (également connu sous le nom TSA ou différentielle à balayage fluorimétrie, DSF)10,11.
CST employer un colorant fluorescent sensible à l’environnement pour suivre la dénaturation thermique d’échantillons de protéines. Beaucoup de colorants couramment utilisés ont une activité fluorescence variable selon la polarité de leur environnement, souvent affichant un rendement de fluorescence élevée dans un environnement hydrophobe mais subissant un trempage rapide dans les milieux polaires12. Les protéines provoquent généralement des augmentations prononcées fluorescence colorant comme leurs cœurs hydrophobes deviennent exposées au cours de la dénaturation, souvent suivie d’une diminution de la fluorescence du colorant à très haute température comme protéines commencent à s’agréger (Figure 2).
Alors qu’un colorant hydrophobicité sensible est souvent un bon choix pour une teinture TSA d’usage général, il peut être impropre à être grandes, exposés au solvant régions hydrophobes, qui présentent souvent la fluorescence de fond négativement élevé des protéines. Fluorophores avec d’autres modes d’action existent (voir Discussion), mais il peut au contraire être souhaitable de suivre la dénaturation par fluorescence intrinsèque de protéine avec nanoDSF.
Résidus de tryptophane qui sont enterrés dans des régions non polaires d’une protéine sont fluorescents avec une émission maximale de 330 nm. Comme un échantillon de la protéine se déroule et ces résidus deviennent exposés à un solvant polaire, leur émission maximale subit un déplacement bathochrome à 350 nm13. nanoDSF exploite ce changement d’émission maximale pour sonder le déroulement d’un échantillon de protéines sans nécessiter de fluorophores extrinsèque14.
Faire fondre les courbes montrant étapes de dénaturation unique peuvent être analysés en ajustant les données pour un modèle sigmoïde de Boltzmann. La température au point d’inflexion de la transition qui se déroule (Tm) est utilisée comme une mesure quantitative de la stabilité thermique des protéines et un point de repère pour comparer la favorabilité de différentes conditions.
Courbes de fusion de la protéine même dans des conditions différentes possèdent parfois un degré d’hétérogénéité qui peut faire un raccord sigmoïde de Boltzmann infaisable. Pour discerner les valeursm T de données qui s’écarte de la topologie de la courbe classique, méthodes numériques peuvent être utilisées comme celles employées en NAMI, un open source TSA/data analysis programme11. Autres cadres thermodynamiques permet également d’analyser les courbes plus complexes avec plusieurs étapes de dénaturation, tels que la méthodologie de ProteoPlex15.
Les écrans de stabilité ont été conçus pour une utilisation dans des expériences de TSA et nanoDSF d’identifier rapidement les conditions favorables pour une protéine cible (Figure 3, compositions d’écran sont disponibles dans les informations complémentaires). Informations recueillies avec les écrans peuvent être utilisées à plusieurs étapes du pipeline cristallographique, y compris : l’échantillon de stockage ; purification, réduisant au minimum les pertes de rendement par l’intermédiaire de protéines qui se déroulent au cours du processus de purification ; design, fonctionnalité de protéine dans les tests d’activité avec stabilisant thermique tampons et, enfin, cristallisation, guidant les essais de cristallisation conçu rationnellement d’armature de dosage.
Choisir une base de système tampon adapté pour un échantillon de protéine est vitale ; valeurs de pH incompatible peuvent entraîner la désactivation ou la dénaturation d’une protéine. Cependant, la présence de molécules cocristallisés tampon résolu dans un grand nombre de structures radiocristallographiques (tableau 1) pourrait également être indicative d’un effet stabilisateur qui est séparée de la régulation du pH simple et au lieu de cela découle de la substance chimique caractéristiques de la molécule de tampon.
Formulé en utilisant plusieurs de tampons17,18,19 , aux côtés d’autres systèmes couramment biologiquement compatible avec tampon de Good, l’écran de pH est conçu pour deconvolute l’effet chimique d’une molécule tampon sur stabilité des protéines de la réelle pH de la solution obtenue. En fournissant les trois valeurs de pH pour chaque système de tampon et incorporant la redondance de valeur de pH entre les différents systèmes, l’écran de pH peut identifier les valeurs de pH favorable et systèmes tampon favorable pour une protéine cible.
L’écran de sel contient généralement sels de laboratoire ainsi que chaotropes, chelants, métaux lourds et les agents réducteurs. L’écran peut donner une indication générale de l’affinité d’un échantillon de protéines pour les environnements avec des forces ioniques élevées, mais chaque sous-groupe des composés peut également fournir des informations sur la structure potentielle d’une protéine. Par exemple, un chélateur considérablement déstabiliser une protéine pourrait être révélateur de métaux structurels importants au sein de l’échantillon. Si l’échantillon est également fortement stabilisé par un cation métallique dans l’écran, cela peut fournir un point de départ prometteur pour autres structurels expériences.
Osmolytes sont des composés solubles qui affectent les propriétés osmotiques de leur environnement. Dans la nature, il peuvent être utilisés comme « chaperons chimiques », appliquer le repliement des protéines désordonnées et stabiliser, surtout dans des conditions de stress20,21,22. Ces caractéristiques rendent attrayants additifs en cristallographie des protéines ; utilisable comme cryoprotecteurs pendant la récolte du cristal, montage et stockage traite23. Utilisation potentielle des osmolytes s’étend également à la purification des protéines. Une proportion importante des protéines recombinantes exprimée chez e. coli peut être difficile de le récupérer à l’état natif à l’aide de méthodes de purification standard et insolubles. Osmolytes peuvent servir à stabiliser et à récupérer des protéines des fractions insolubles, purification croissante conduit à24.
L’écran osmolyte a été conçu à l’aide d’établies composés présents dans la Protein Data Bank entrées25 et la base de données de26 Dragon Explorer of Osmoprotection-Associated voies (DEOP) et optimisé par itération à l’aide de protéines standard. L’écran est construit autour de huit sous-classes d’osmolyte : glycérol, sucres et polyols, non détergente sulfobétaïnes (NDSBs), bétaïnes et leurs analogues, organophosphorés, dipeptides, acides aminés et leurs dérivés et un dernier groupe divers. Chaque osmolyte est présent dans plusieurs concentrations basées sur sa solubilité et les plages de concentration efficace aux fins de comparaison.
Protocol
Representative Results
Discussion
Aspects critiques au sein du protocole incluent l’étape de centrifugation et une bonne étanchéité de la plaque à 96 puits pour des expériences TSA (étape 1.5). Centrifugation veille à ce que la condition d’échantillon et écran de protéines entrent en contact et mélanger. En outre, si l’on utilise une plaque non scellée pour une expérience TSA, il y a un risque important de solvant d’évaporation tout au long de l’expérience, causant une augmentation de la concentration de l’échantillon et augmenter les chances d’agrégation de la protéine prématurée.
CST et nanoDSF se prêtent à une vaste gamme d’échantillons de protéines ; la grande majorité des échantillons peut produire des courbes de fusion interprétable avec un colorant journaliste hydrophobie ou par l’intermédiaire de nanoDSF sans colorant. Si les sources standard fluorescence ne conviennent pas à votre protéine, la simple modification du protocole qui pourrait être explorée est le choix de fluorophore. Plusieurs colorants alternatives pourraient être appropriés pour les expériences TSA. Les exemples incluent N-[4-(7-diethylamino-4-methyl-3-coumarinyl)phenyl]maleimide (CPM), un composé qui émet une fluorescence après réaction avec un thiol27et 4-(dicyanovinyl) julolidine (DCVJ), un composé qui varie sa fluorescence basée sur la rigidité de son environnement, augmentant sa fluorescence comme un échantillon de protéines déroule le28,29 (la teinture ce dernier nécessite souvent des concentrations élevées d’échantillon).
Autres méthodes d’analyse des courbes de fusion sont disponibles si Tm n’est pas calculé automatiquement par le logiciel de l’instrument. Si les données sont homogènes et qu’une seule étape de dénaturation est apparente dans les courbes de fusion, un ensemble de données tronqué peut être monté sur un Boltzmann sigmoïde avec l’équation suivante :
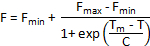
Où F est l’intensité de la fluorescence à la température T, Fmin et Fmax est les intensités de fluorescence avant et après la transition de dénaturation, respectivement, Tm est la température du point médian de la transition de la dénaturation et la C est la pente au Tm. Alors que cette méthode fonctionne bien pour les procédés de dénaturation simple en deux étapes, il ne convient pas pour les courbes de fusion complexe avec plusieurs transitions.
Un des avantages majeurs de la TSA est son accessibilité ; TSA expériences peuvent être effectuées dans n’importe quel système de RT-PCR avec filtres à des longueurs d’onde appropriées pour la teinture de fluorescence employées. Ceci couplé avec le faible coût des consommables, facilité d’utilisation et relativement faible quantité de protéines nécessaire, faire des TSA une technique précieuse pour une large gamme d’échelles de projet, aussi bien dans l’industrie et les universités.
Ainsi que ce qui indique des conditions favorables de tampon, les écrans contiennent certains puits qui peuvent donner des indices de la présence de métaux structures au sein d’une protéine de l’échantillon. Puits pouvant être d’un intérêt particulier dans l’écran de sel sont G6 et G7, qui contiennent de l’EDTA de 5 mM et 5 mM EGTA, respectivement. La déstabilisation thermique importante dans ces puits peut être le signe d’importantes ions métalliques dans la protéine qui sont séquestrées par la chelants. Composés dans l’écran osmolyte peuvent également potentiellement fournir des indices à la fonction d’une protéine. Bon nombre de ces composés dans l’écran appartiennent aux classes de molécules qui sont communs substrats d’enzymes. Par exemple, la stabilisation générale offerte par saccharides (présents dans les puits A11-B10) pour lysozyme pourrait être attribuée à leur similarité structurelle à établi des substrats de l’enzyme, la N-acétylglucosamine oligomères30.
Les protocoles TSA et nanoDSF décrites ci-dessus peuvent être adaptées à l’étude des interactions protéine-ligand. Les ligands qui se lient spécifiquement à une protéine peuvent augmenter sa stabilité thermique en introduisant de nouvelles interactions au sein du complexe. Un changement positif de dose-dépendante de protéine Tm est un signe prometteur d’une interaction de protéine-ligand réussie. La vitesse, de débit et de faible coût du dépistage des banques de composés avec CST a fait une méthode très populaire dans la découverte de médicaments de stade précoce.
Optimiser les conditions de tampon de protéines cibles et leurs complexes de ligand peut être essentielle pour la réussite d’un projet, comme le montrent de nombreux exemples de littérature31,32,33,34. Avec un essai typique prenant moins de 2 h, y compris le temps d’installation, CST et nanoDSF couplé avec des écrans de stabilité représentent une technique rapide et peu coûteuse pour les optimisations de mémoire tampon.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Ce projet est financé depuis le Conseil européen de recherche (CER) en vertu du programme de recherche et d’innovation Horizon 2020 de l’Union européenne (subvention contrat n ° 685778). Ce travail a été soutenu par le Biotechnology and Biological Sciences Research Council (BBSRC, subvention nombres BB/M011186/1, BB/J014516/1). DB merci le BBSRC doctorat formation partenariat Newcastle-Liverpool-Durham pour une bourse d’étude et Durham University département de Biosciences de contribuer vers le financement de ces travaux. Nous remercions Ian Edwards pour son aide et le service de spectrométrie de masse Durham University département de chimie pour leur analyse instrumentale de protéine X. Nous sommes reconnaissants à Arnthor Ævarsson pour son travail avec le projet Virus-X et merci aussi à Claire Hatty et NanoTemper GmbH de prêts et d’aider avec le système NT.48 de Prométhée pour ce projet. Enfin, merci à Frances Gawthrop et Tozer graines pour leur soutien dans le cadre du prix BBSRC iCASE.
Materials
| Lysozyme | Melford Laboratories | L38100 | Crystallised and lyophilised chicken egg white lysozyme. |
| The Durham pH Screen | Molecular Dimensions | MD1-101 | 96-well protein stability screen. See above for contents. |
| The Durham Salt Screen | Molecular Dimensions | MD1-102 | 96-well protein stability screen. See above for contents. |
| The Durham Osmolyte Screen | Various | #N/A | 96-well protein stability screen, not commercially available at the time of publication. See above for contents. |
| SYPRO Orange | Invitrogen | S6651 | Widely used fluorescent dye for protein staining in gels and DSF. |
| 96-well PCR Plate | Starlab | 1403-7700 | Semi-skirted clear plastic for use with AB 7500 Fast RT-PCR System. |
| 7500 Fast Real-time PCR System | Applied Biosystems | 4362143 | 96-well format RT-PCR system. Alternative systems can be used. Analysis of data performed using free, open-access software NAMI. AB software tailored to DSF experiments using the 7500 Fast available at additional cost. |
| Prometheus NT.48 | NanoTemper Technologies | #N/A | Label-free DSF system with up to 48-sample capacity. Can calculate unfolding temperatures (Tm and Tonset), critical denaturant concentrations (Cm), free folding energy (ΔG and ΔΔG), and aggregation results (Tagg) using built-in software. |
| Prometheus NT.48 Series nanoDSF Grade Standard Capillaries | NanoTemper Technologies | PR-C002 | Prometheus NT.48 Series nanoDSF Grade Standard Capillaries. "High sensitivity" variants are available at a higher cost for use with low-concentration samples (<200 µg ml-1). |
References
- Kapust, R. B., Waugh, D. S. Controlled intracellular processing of fusion proteins by TEV protease. Protein Expression and Purification. 19 (2), 312-318 (2000).
- Cordingley, M. G., Register, R. B., Callahan, P. L., Garsky, V. M., Colonno, R. J. Cleavage of small peptides in vitro by human rhinovirus 14 3C protease expressed in Escherichia coli. Journal of Virology. 63 (12), 5037-5045 (1989).
- Hjorleifsdottir, S., Aevarsson, A., Hreggvidsson, G. O., Fridjonsson, O. H., Kristjansson, J. K. Isolation, growth and genome of the Rhodothermus RM378 thermophilic bacteriophage. Extremophiles. 18 (2), 261-270 (2014).
- Alva, V., Nam, S. Z., Söding, J., Lupas, A. N. The MPI bioinformatics Toolkit as an integrative platform for advanced protein sequence and structure analysis. Nucleic Acids Research. 44, 410-415 (2016).
- McPherson, A. Protein Crystallization. Methods in molecular biology. 1607, 17-50 (2017).
- Ericsson, U. B., Hallberg, B. M., DeTitta, G. T., Dekker, N., Nordlund, P. Thermofluor-based high-throughput stability optimization of proteins for structural studies. Analytical Biochemistry. 357 (2), 289-298 (2006).
- Reinhard, L., Mayerhofer, H., Geerlof, A., Mueller-Dieckmann, J., Weiss, M. S. IUCr Optimization of protein buffer cocktails using Thermofluor. Acta Crystallographica Section F Structural Biology and Crystallization Communications. 69 (2), 209-214 (2013).
- Boivin, S., Kozak, S., Meijers, R. Optimization of protein purification and characterization using Thermofluor screens. Protein Expression and Purification. 91 (2), 192-206 (2013).
- Kozak, S., Lercher, L., Karanth, M. N., Meijers, R., Carlomagno, T., Boivin, S. Optimization of protein samples for NMR using thermal shift assays. Journal of Biomolecular NMR. 64 (4), 281-289 (2016).
- Semisotnov, G. V., Rodionova, N. A., Razgulyaev, O. I., Uversky, V. N., Gripas’, A. F., Gilmanshin, R. I. Study of the “molten globule” intermediate state in protein folding by a hydrophobic fluorescent probe. Biopolymers. 31 (1), 119-128 (1991).
- Grøftehauge, M. K., Hajizadeh, N. R., Swann, M. J., Pohl, E. Protein-ligand interactions investigated by thermal shift assays (TSA) and dual polarization interferometry (DPI). Acta Crystallographica Section D: Biological Crystallography. 71, 36-44 (2015).
- Steinberg, T. H., Jones, L. J., Haugland, R. P., Singer, V. L. SYPRO Orange and SYPRO Red Protein Gel Stains: One-Step Fluorescent Staining of Denaturing Gels for Detection of Nanogram Levels of Protein. Analytical biochemistry. 239, 223-237 (1996).
- Burstein, E. A., Vedenkina, N. S., Ivkova, M. N. Fluorescence and the location of tryptophan residues in protein molecules. Photochemistry and Photobiology. 18 (4), 263-279 (1973).
- Haffke, M., Rummel, G., Boivineau, J., Münch, A., Jaakola, V. -. P. nanoDSF: label-free thermal unfolding assay of G-protein-coupled receptors for compound screening and buffer composition optimization. Application Note NT-PR-008. , (2016).
- Chari, A., et al. ProteoPlex: stability optimization of macromolecular complexes by sparsematrix screening of chemical space. Nature Methods. 12 (9), 859-865 (2015).
- Laskowski, R. A. PDBsum: summaries and analyses of PDB structures. Nucleic Acids Research. 29 (1), 221-222 (2001).
- Good, N. E., Winget, G. D., Winter, W., Connolly, T. N., Izawa, S., Singh, R. M. Hydrogen ion buffers for biological research. 生物化学. 5 (2), 467-477 (1966).
- Good, N. E., Izawa, S. Hydrogen ion buffers. Methods in enzymology. 24, 53-68 (1972).
- Ferguson, W. J., et al. Hydrogen ion buffers for biological research. Analytical biochemistry. 104 (2), 300-310 (1980).
- Welch, W. J., Brown, C. R. Influence of molecular and chemical chaperones on protein folding. Cell stress & chaperones. 1 (2), 109-115 (1996).
- Diamant, S., Eliahu, N., Rosenthal, D., Goloubinoff, P. Chemical chaperones regulate molecular chaperones in vitro and in cells under combined salt and heat stresses. The Journal of biological chemistry. 276 (43), 39586-39591 (2001).
- Yancey, P. H. Organic osmolytes as compatible, metabolic and counteracting cytoprotectants in high osmolarity and other stresses. Journal of Experimental Biology. 208 (15), 2819-2830 (2005).
- Garman, E. F., Owen, R. L. Cryocooling and radiation damage in macromolecular crystallography. Acta Crystallographica Section D Biological Crystallography. 62 (1), 32-47 (2006).
- de Marco, A., Vigh, L., Diamant, S., Goloubinoff, P. Native folding of aggregation-prone recombinant proteins in Escherichia coli by osmolytes, plasmid- or benzyl alcohol- overexpressed molecular chaperones. Cell Stress & Chaperones. 10 (4), 329 (2005).
- Berman, H. M., et al. The protein data bank. Nucleic acids research. 28 (1), 235-242 (2000).
- Bougouffa, S., Radovanovic, A., Essack, M., Bajic, V. B. DEOP: A database on osmoprotectants and associated pathways. Database. 2014, 1-13 (2014).
- Alexandrov, A. I., Mileni, M., Chien, E. Y. T., Hanson, M. A., Stevens, R. C. Microscale Fluorescent Thermal Stability Assay for Membrane Proteins. Structure. 16 (3), 351-359 (2008).
- Kung, C. E., Reed, J. K. Fluorescent molecular rotors: a new class of probes for tubulin structure and assembly. 生物化学. 28 (16), 6678 (1989).
- Iio, T., Itakura, M., Takahashi, S., Sawada, S. 9-(Dicyanovinyl)julolidine binding to bovine brain calmodulin. Journal of biochemistry. 109 (4), 499-502 (1991).
- Veros, C. T., Oldham, N. J. Quantitative determination of lysozyme-ligand binding in the solution and gas phases by electrospray ionisation mass spectrometry. Rapid Communications in Mass Spectrometry. 21 (21), 3505-3510 (2007).
- Kean, J., Cleverley, R. M., O’Ryan, L., Ford, R. C., Prince, S. M., Derrick, J. P. Characterization of a CorA Mg2+ transport channel from Methanococcus jannaschii using a Thermofluor-based stability assay. Molecular membrane biology. 25 (8), 653-661 (2008).
- Geders, T. W., Gustafson, K., Finzel, B. C. Use of differential scanning fluorimetry to optimize the purification and crystallization of PLP-dependent enzymes. Acta Crystallographica Section F. 68 (5), 596-600 (2012).
- Morgan, H. P., Zhong, W., McNae, I. W., Michels, P. A., Fothergill-Gilmore, L. A., Walkinshaw, M. D. Structures of pyruvate kinases display evolutionarily divergent allosteric strategies. Royal Society open science. 1 (140120), (2014).
- Moretti, A., Li, J., Donini, S., Sobol, R. W., Rizzi, M., Garavaglia, S. Crystal structure of human aldehyde dehydrogenase 1A3 complexed with NAD+ and retinoic acid. Scientific reports. 6 (35710), (2016).

