NRCC 패치 - 클램프 칩에 대한 세포의 Culturing 및 전기 생리학
Summary
우리는 세포와 도금 매체로 읽어 좋았 냐고 물어 봤어, 캐나다의 국립 연구 협의회 소독하고,,,,에서 가공 및 electrophysiological 녹음에 사용하는 방법 평면 패치 – 클램프 칩 보여줍니다.
Abstract
그 섬세한 감성과 이온 채널의 레벨에서 각각의 세포를 모니터하고 제어할 수있는 능력으로 인해, 패치 – 고정은 전기 생리학의 황금 표준 모두 한 질병 모델과 제약 화면에 적용됩니다. 방법은 전통적으로 부드럽게 그 정점이 아래 멤브레인의 패치를 분리하기 위해 생리적 용액으로 채워진 유리 피펫으로 세포에 문의하는 것입니다. 피펫에 삽입 전극은 전체 세포를 위해 파열 멤브레인 패치하거나 내에서 이온 채널의 활동을 캡처합니다. 지난 10 년, 패치 – 클램프 칩은 대안 3, 4로 제안되었습니다 정지 필름 배지에서 생리 매체를 분리하고, 영화 microfabricated 조리개는 피펫의 꼭대기를 대체합니다. 패치 – 클램프 칩은 자동화 시스템에 통합과 높은 처리량 검사 5 상용화되었습니다. incr하기처리량을 완화, 그들은 휴대 프로브 바다표범를 검색하고 전체 세포 모드로 들어가는 유체 정지에서 세포의 전달, 흡입에 의한 조리개에서 자신의 위치, 그리고 자동화된 루틴을 포함합니다. 우리는 최적화된 임피던스와 교양 달팽이 뉴런의 행동 잠재력 6 고품질 녹음을 허용하는 오리피스 형태로 실리콘 패치 – 클램프 칩의 제조에보고에 따르면, 최근에, 우리는 또한 포유류의 뉴런에게 7 심문으로 진행 상황을보고했습니다. 저희 패치 – 클램프 칩은 캐나다 Photonics 제작 센터 8, 상용 공장에 가공, 대형 시리즈에서 사용할 수 있습니다. 우리는 서로 다른 모델 NRCC 기술의 사용을 확인할 electrophysiologists와 협력에 종사하는 열망입니다. 칩은 그림 1에 나타나 일반적인 방식에 따라 사용됩니다 : 실리콘 칩은 플렉시 글라스 문화 유리병와 조리개의 뒷면 하단의 것은 지하 chann에 연결되어엘은 패키지의 양쪽 끝에 튜브가 장착되어. 전지는 유리병에 배양해되며 프로브 위에 세포는 유체 포트가 세포에 최소한의 방해와 솔루션 교류를 촉진 밖 channel.The 두 삽입 측정 전극에 의해 모니터링되고,이 세포 내 용 유리 pipettes에 비해 장점이다 재관류.
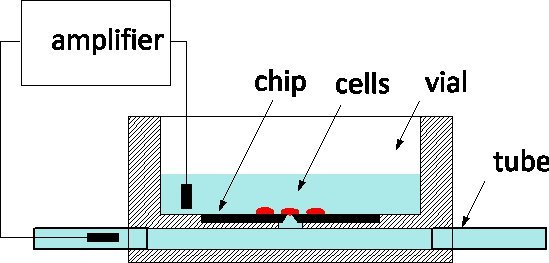
그림 1. NRCC 패치 – 클램프 칩을 사용하여 측정의 원리
여기서 우리는 세부 소독 및 주요 칩, 세포와 매체, 판 그들과 함께 그들을로드하고, 마지막으로 electrophysiological 음반들을 위해 사용하는 프로토콜.
Protocol
Discussion
NRCC의 패치 – 클램프 칩 심문 플랫폼은 높은 정보량 제약 assays를위한 잠재적으로 강력한 도구이며, 질병의 체외 모델에서 조사를. 유리 pipettes에 비해 그것의 장점은 대형 세포를 알아내기 위해 장점은 낮은 접속 저항이며, 약간 더 큰 정전 용량에도 불구하고 작은 세포에 대한 비교 역학집니다. 개구 물개의 자연 세포는 정기적으로 취득했으며, 전체 셀 항목은 자발적인 14 것으로 관찰되었습니다. 칩 및 유리 피펫 방법 사이의 명확한 차이는 프로브는 세포 배양 접시의 일부이며 수동으로 세포막과 접촉 가져되지 않는다는 사실입니다. Culturing 세포, 기능적 네트워크의 가능성이 일부 질병 모델로서보다 생물학적으로 관련성이 높은 모델 결과와 바다표범 16을 알아내기 위해 높은 셀 보안을위한 다른 메커니즘. 그러나, 세포 현탁액과 대조적으로 흡인 cannoT는 프로브의 셀을 배치하는 데 사용됩니다. 달팽이 뉴런은 다른 대형 세포로 프로브의 꼭대기에서 수동 위치 결정 의무가 있습니다. 에서 세포의 이상 문화 시간을 필요로하는 작은 세포 들어, 우리는 어떠한 조작에 대한 필요성을 obviated와 프로브 위에 세포를 배치하는 프로브 위에 patterning의 유착 polypeptides에 의해 도장을 얻기의 높은 확률을 유지하고, 증명 배치 프로브 17,18.
NRCC 또한 유리 피펫의 비교 용량으로 microfluidic 패치 – 클램프 칩 19 polyimide 개발하고있다. 그 프로젝트의 궁극적인 목적은 허용 개별 이온 채널 14 해상도에서 네트워크 행동에 종사하는 여러 뉴런의 electrophysiological 활동의 동시 모니터링.에게 여러 프로브 패치 – 클램프 칩입니다 이 방법은 다중 전극 배열 20 ~ 고해상도 보완적인 방법입니다.
Divulgations
The authors have nothing to disclose.
Acknowledgements
저자는 어셈블리와 도움을 패치 – 클램프 CPFC에서 칩, 그리고 색조 트란, 탁구 조 및 마태복음 Shiu의 제조를 위해 알렉세이 Bogdanov을 인정하고 싶습니다. Naweed 셰야드는 보건 연구 (CIHR) 교부금의 캐나다 학회에 의해 지원되었다. 콜린 도르바은 NSERC과 의학 연구 (AHFMR) studentships 대한 알버타 헤리티지 재단의 수상자이다.
References
- Walz, W. Patch-Clamp Analysis: Advanced Techniques. Neuromethods. , 38 (2007).
- Neher, E., Sakmann, B. Single-channel currents recorded from membrane of denervated frog muscle fibers. Nature. 260, 799-802 (1976).
- Behrends, J. C., Fertig, N. Ch. 14: Planar Patch-clamp. Neuromethods. , (2007).
- Fertig, N., Tilke, A., Blick, R. H. Stable integration of isolated cell membrane patches in a nanomachined aperture. Applied Physics Letters. 77, 1218-1220 (2000).
- Dunlop, J., Bowlby, M., Peri, R., Vasilyev, D., Arias, R. High-throughput electrophysiology: an emerging paradigm for ion-channel screening and hysiology. Nat. Rev. Drug. Discov. 7 (4), 358-368 (2008).
- Py, C., Denhoff, M., Martina, M. A novel silicon patch-clamp chip permits high-fidelity recording of ion channel activity from functionally defined neurons. Biotechnology and Bioengineering. 107 (4), 593-600 (2010).
- Martinez, D., Martina, M., Kremer, L. Development of patch-clamp chips for mammalian cell applications. Micro and Nanosystems. 2 (4), (2010).
- Py, C., Salim, D., Monette, R. Cell to aperture interaction in patch-clamp chips visualized by fluorescence microscopy and focused-ion beam sections. Biotechnology & Bioengineering. 108, 1395-1403 (2011).
- Martina, M., Luk, C., Py, C. Interrogation of Cultured Neurons using Patch-Clamp Chips. Journal of Neural Engineering. 8, 034002 (2011).
- Bell, H. J., Syed, N. I. Hypoxia-induced modulation of the respiratory CPG. Frontiers in bioscience : a journal and virtual library. 14, 3825-3835 (2009).
- Syed, N. I., Bulloch, A. G. M., Lukowiak, K. In vitro reconstruction of the respiratory central pattern generator of the mollusk Lymnaea. Science. 250, 282-285 (1990).
- Syed, N. I., Zaidi, H., Lovell, P., Windhorst, U., Johansson, H. In vitro reconstruction of neuronal circuits: A simple model system approach. Modern techniques in neuroscience research. , (1999).
- Martina, M., Luk, C., Py, C. Interrogation of Cultured Neurons using Patch-Clamp Chips. Journal of Neural Engineering. 8, 034002 (2011).
- Py, C., Denhoff, M., Martina, M., et al. Silicon patch-clamp chip suitable for high-fidelity recording of ion channel activity from cultured neurons. Biotechnology and Bioengineering. 107 (4), (2010).
- Ong, W. -. L., Yobas, L., Ong, W. -. Y. A missing factor in chip-based patch clamp assay: gigaseal. Journal of Physics: Conference Series. 34, 187 (2006).
- Charrier, A., Martinez, D., Monette, R. Cell placement and guidance on substrates for neurochip interfaces. Biotechnology and Bioengineering. 105, 368-373 (2010).
- Diaz-Quijada, D., Maynard, C. C. o. m. a. s., Monette, T., Py, R., A, C. K. r. a. n. t. i. s., Mealing, G. Surface Patterning with Chemisorbed Chemical Cues for Advancing Neurochip Applications. Industrial & Engineering Chemistry Research. 50 (17), 10029-10035 (2011).
- Martinez, D., Py, C., Denhoff, M., et al. High-fidelity patch-clamp recordings from neurons cultured on a polymer microchip. Biomedical Microdevices. 12, 977-97 (2010).
- Taketani, M., Baudry, M. . Advances in Network Electrophysiology: Using Multi-Electrode Arrays. , (2006).

