Productie van Apolipoprotein C-III Knockout Konijnen behulp Zinc Finger Nucleasen
Summary
Recente ontwikkeling in gentargeting instrumenten maakt de productie van knock-out (KO) konijnen mogelijk. In het onderhavige werk, genereerden we vijf Apolipoprotein (Apo) C-III KO konijnen met behulp van Zinc Finger Nucleasen (ZFN). Dit werk heeft aangetoond dat ZFN is een zeer efficiënte methode om KO konijnen.
Abstract
Apolipoproteïne (Apo) C-III (apoCIII) zich op het oppervlak van plasma chylomicronen (CM), zeer lage dichtheid lipoproteïne (VLDL) en lipoproteïnen met hoge dichtheid (HDL). Het is bekend dat hoge niveaus van plasma apoCIII constitutea risicofactor voor cardiovasculaire ziekten (CVD). Verhoogde plasma apoCIII niveau vaak correleert met insulineresistentie, obesitas en hypertriglyceridemie. Onschatbare kennis over de rol van ApoCIIIin lipide metabolisme en CVD is verkregen van transgene muismodellen zoals apoCIII knockout (KO) muizen, maar wordt opgemerkt dat het metabolisme van lipoproteïne bij muizen verschilt van die van mensen in vele aspecten. Het is niet bekend tot nu of verhoogde plasma apoCIII is direct atherogene. We werkten aan apoCIII KO konijnen ontwikkelen in de huidige studie op basis van de hypothese dat konijnen kan dienen als een reasonablemodelfor studie van de menselijke vetmetabolisme en atherosclerose. Zinkvinger nuclease (ZFN) sets targeting konijn ApoCIIIgene werden onderworpen aan in vitro validatie vóór embryo micro-injectie. Het mRNA werd geïnjecteerd om het cytoplasma van 35 konijn pronucleaire stadium embryo's, en evalueerden de mutatie tarieven bij de blastocyst staat. Zestien blastocysten die werden getest, een bevredigende 50% mutaties (8/16) en het richten plaats werd bereikt, die het gebruik van set 1 in vivo experimenten. Vervolgens hebben we gemicroinjecteerd 145 embryo's met Set 1 mRNA, en overgebracht deze embryo's tot 7 ontvanger konijnen. Na 30 dagen dracht, werden 21 kits geboren, waarvan er vijf werden bevestigd als apoCIII KO konijnen na PCR sequencing assays. De KO dier tarief (# KO kits / totaal geboren) was 23,8%. De totale productie-efficiëntie is 3,4% (5 kits/145 embryo's). De huidige werk aangetoond dat ZFN is een zeer efficiënte methode om KO konijnen. Deze apoCIII KO konijnen zijn nieuwe middelen om de rollen van apoCIII studeren in lipide stofwisseling.
Introduction
Apolipoproteïne (Apo) C-III (apoCIII) is een kleine O-geglycosyleerde secretorische eiwit dat voornamelijk wordt gesynthetiseerd in de lever en de darmen. Het bevindt zich op het oppervlak van plasma chylomicronen (CM), zeer lage dichtheid lipoproteïne (VLDL) en lipoproteïnen met hoge dichtheid (HDL). ApoCIII is erkend als een risicofactor voor cardiovasculaire ziekte 1. Patiënten met een erfelijke deficiëntie van apoCIII hebben lage plasma triglyceride (TG) en een dalende subklinische coronaire atherosclerose 2,3. Verhoogde plasma apoCIII niveau, anderzijds vaak correleert met insulineresistentie, obesitas en hypertriglyceridemie (HTG) 4,5.
Knockout (KO) is een krachtig middel om de functie van een gen te bestuderen. In overeenstemming met de waarnemingen in menselijke populaties mutant, knockout van de apoCIII gen in muizen leidde tot een verlaging van plasma TG en bescherming tegen postprandiale HTG 6. Dergelijke positieve rol van apoCIII verschenenonafhankelijk te zijn van Apolipoprotein E (ApoE), zoals muizen die een tekort van zowel ApoE en apoCIII ook worden beschermd tegen postprandiale hyperlipidemie 7. Hoewel deze apoCIII KO muizen waardevolle informatie heeft verstrekt over de mogelijke functies van apoCIII bij de mens, wordt opgemerkt dat het metabolisme van lipoproteïne van muizen verschilt van die van mensen in vele aspecten. Bijvoorbeeld, muis ontbreekt plasma cholesteryl ester transfer proteïne (CETP), een belangrijke enzym betrokken bij het transport van VLDL, LDL en HDL 8. Daarom moet een geschikt diermodel ontwikkeld met als doel de fysiologische rol van apoCIII in vivo.
Het konijn is een klassieke model diersoorten 9-11. Het heeft een korte dracht (30-31 dagen), grote worpgrootte (4-12/litter) en kan gemakkelijk worden ondergebracht in een indoor faciliteit. In vergelijking met muizen, konijnen fylogenetisch dichter bij de mens 10. Belangrijk is, zoals human, maar in tegenstelling tot muizen, konijnen zijn LDL-rijk zoogdieren en hebben aanzienlijke niveaus van CETP 10,12. Bovendien zijn ze gevoelig voor cholesterol-rijk dieet geïnduceerde atherosclerose de laesies gelijk aan die in menselijke atherosclerose 13. Daarom veronderstelden we dat apoCIII KO konijnen kan dienen als een beter model dan hun tegenhangers muis om de rol van ApoCIIIplay vetmetabolisme en atherosclerose bij mensen te onderzoeken.
Productie van gen gerichte transgene (GTT) konijnen is een uitdaging. Dit is voornamelijk te wijten aan het ontbreken van kiembaan verzenden van embryonale stamcellen (ESC) en de extreem lage rendement van somatische celkernen (SCNT) bij konijnen. ESC is het belangrijkste instrument om GTT muizen te genereren, terwijl en SCNT is met succes toegepast op KO dieren te genereren in soorten ontbreekt germline verzenden van SER's, met inbegrip van varkens, schapen en runderen, maar niet konijnen. Onlangs Zinc Finger Nuclease (ZFN), Transchrijving Activator-Like Effector Nuclease (TALEN) 14, en RNA Guided Endonuclease (RGEN) 15 ontpopt als krachtig middel voor het genoom bewerken. Deze nucleasen, zogenaamde "moleculaire scharen", zijn efficiënt in het genereren van dubbelstrengs breuken (DSB) in het genoom die kan leiden tot een functioneel KO van het doelgen of worden gebruikt om een DNA sequentie te integreren op een specifieke locus in het genoom een aantal soorten 16. In 2011, een van de eerste aanpassing van de ZFN technologie genereerden wij peroxisoomproliferator-activated receptor gamma (PPARy) KO varkens cellen via deze aanpak en met succes gegenereerd PPARy KO varkens na het gebruik van deze cellen voor SCNT 17. In hetzelfde jaar, efficiënte immunoglobuline gendisruptie en gerichte vervanging bij konijnen ook met behulp ZFN werd gemeld 18.
In deze studie werden vijf apoCIII KO konijnen gegenereerd zoals bevestigd door PCR sequencing, met ZFN Set 1 (zie figuur 1 </sTrong>. voor stroomschema illustratie). Deze dieren zijn nieuwe middelen om de rollen van apoCIII studeren in lipide stofwisseling.
Protocol
Representative Results
Discussion
In het onderhavige werk, werden vijf apoCIII KO konijnen gegenereerd met behulp van de ZFN technologie. Voorheen het enige rapport van de productie van GTT konijnen ook de ZFN technologie 18. De huidige werk bevestigde dat ZFN nuttig is om effectief te richten genen in konijnen.
In deze studie, de transgene tarief (positieve kits / totaal geboren) is23.8% (5/21), die vergelijkbaar is met die van het vorige verslag ZFN bij konijnen (30,8%, 16/52) 18 en die gerapporteerd van het gebruik van ZFN bij andere diersoorten, waaronder zebravis 19, 20 muizen, ratten 21 en varkens 17. Dit percentage is zelfs hoger dan de percentages veel conventionele transgene konijnen productie studies, die normaal vallen in het traject van 5-20%. Bijvoorbeeld, in een poging om het product apoCIII transgene konijnen via conventionele DNA micro-injectie, Ding et al.. Verkregen 3 positieve oprichters van de 54 pups geboren (5,6%) 22.
In overeenstemming met eerdere bevindingen, de mutaties op de targeting sites zijn variabel, zoals deleties of inserties bestaande verschillend aantal basen (variërend 1-21 in vijf konijnen KO). Op basis van de specifieke sequentie informatie van de grondlegger dieren wordt voorspeld dat tenminste vier (dwz. Die met Δ1, 1, 1, of Δ20 mutaties) functieverlies van apoCIII hebben. Animal R-16 met Δ21 niet functieverlies weergegeven, aangezien deze mutatie is voorspeld enige oorzaak verlies van zeven aminozuren, maar geen leesraam verschuiving. Uiteindelijk fenotype assays worden nagegaan of deze grondlegger dieren werkelijk verlies van apoCIII functies weer.
Geen van de vijf KO konijnen opgewekt in de huidige studie bevatten biallelisch wijzigingen. Interessant is ook het geval in het vorige ZFN konijn verslag. Wanneer daarentegen ZFNs gericht α1 ,3-galactosyltransferase werden op varkenscellen, de frequentie gericht op een allel varieerde 7-46%, met ongeveer een derde van mutaties creëren eenstaps biallele knockouts 23. Consistent hiermee bij TALEN werd toegepast op varkens fibroblastcellen, de biallele wijzigingen werden gevonden bij ongeveer 15-40% van de totale positieve klonen 14. Het is mogelijk dat het niet biallele KO konijnen genereren in deze studie species (verschil konijnen versus varkens) voor deze capaciteit van nuclease genexpressie targeting vermeldt. Het is echter meer waarschijnlijk dat dit is gewoon omdat het aantal KO konijnen gegenereerd in dit project is relatief klein. Wij geloven dat ZFN kan genereren bialleic mutaties in konijnen, die moet worden beschouwd als een ander potentieel voordeel van ZFN gebaseerd GTT konijnenproductie. Verdere experimenten nodig om deze capaciteit van ZFN bij konijnen bevestigen.
Kortom, de huidige werk toont aan dat ZFN gebaseerd gene targeting aanpak effectief is in het produceren van KO konijnen. In het bijzonder, we gegenereerd vijf apoCIII KO konijnen met een bevredigend transgene tarief van 23,8%. Deze dieren worden beschouwd als meer betekenisvolle informatie over de rol van lipide metabolisme bij mensen deze eiwitten dan de overeenkomstige muismodellen geven. Wij voorspellen ZFN gebaseerde gen targeting, evenals andere nuclease gebaseerde technologieën zoals TALEN en RGEN in nonmurine dieren aanzienlijk de ontwikkeling van nieuwe diermodellen voor diverse menselijke ziekten te bestuderen vergemakkelijken.
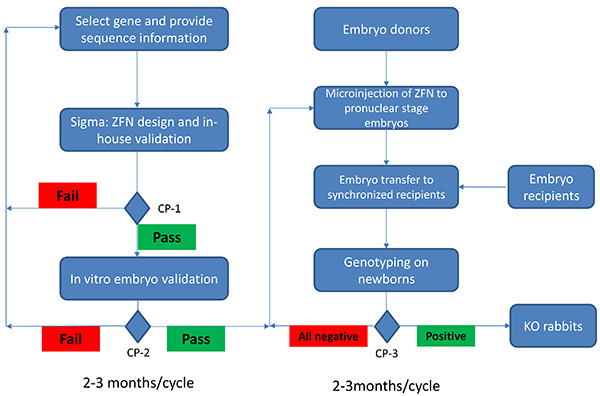
Figuur 1. Stroomschema van de productie van knock-out konijnen met behulp ZFN technologie. Productie van KO konijnen middels ZFN techniek begint met de selectie van het gen van belang. De sequentie-informatie wordt verstrekt, ZFN sets zijn ontworpen, en subjected om op basis van gist validatie. Bij de check point (CP) 1 (CP-1), alleen die sets voorbij interne validatie (50% of meer van de interne positieve controle) zal worden aan de gebruikers voor selectie aangeboden. Als er geen sets voorbij CP-1, kunnen aanvullende volgorde nodig zijn voor het ontwerpen van effectieve ZFN sets. Een embryo's in vitro validatie wordt gevolgd om ervoor te zorgen de geselecteerde ZFN set kan mutaties veroorzaken op geselecteerde sites (CP-2). ZFN set (s) zal alleen gebruikt worden als het passeert CP-2 (> = 10% mutatie prijzen in embryo's in vitro). Mislukking op CP-2 zal een herontwerp van de ZFN sets nodig. Embryo donoren zullen worden voorbereid en pronucleaire stadium embryo wordt gemicroinjecteerd met de gevalideerde ZFN sets. Deze gemicroinjecteerd embryo's zullen worden overgedragen aan gesynchroniseerd embryo ontvangers. Na een maand draagtijd wordt pasgeborenen genotyperen (CP-3). Als geen van de pasgeborenen positief zijn, zal extra micro-injectie worden uitgevoerd. Het duurt 2-3 maanden na aanvang van het project tot CP-2, uitgaande van no falen tijdens het proces. Het duurt nog 2-3 maanden van CP-2 naar CP-3. Daarom is het mogelijk om een knock-out konijn in een 4-6 maanden tijd met behulp van de ZFN technologie genereren. Klik hier voor grotere afbeelding .
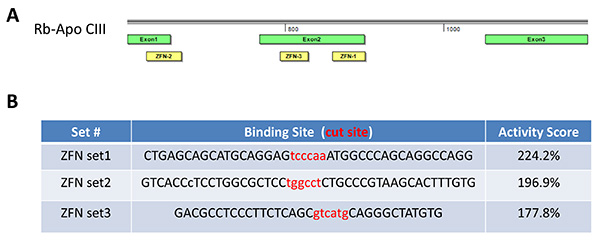
Figuur 2. ZFN ontwerp. Drie ZFN sets (Set 1, 2, en 3) werden ontworpen gericht is op verschillende sequenties op Exon 1 of Exon 2 van konijn apoCIII (A). Alle drie sets werden onderworpen aan de gist MEL-1 reporter assay de ZFN activiteiten te bepalen. Volgens protocollen van de fabrikant worden ZFNs dat> 50% van de activiteiten die van de interne positieve controle voor de vervaardiging tonen geacht bruikbaar voor in vitro en in vivo experimenten genoom bewerken.De ZFN activiteiten waren 224,2% voor Set 1, 196,9% voor Set 2 en 177,8% voor Set 3 (B), dus Set 1 werd geselecteerd in de huidige studie. Klik hier voor grotere afbeelding .
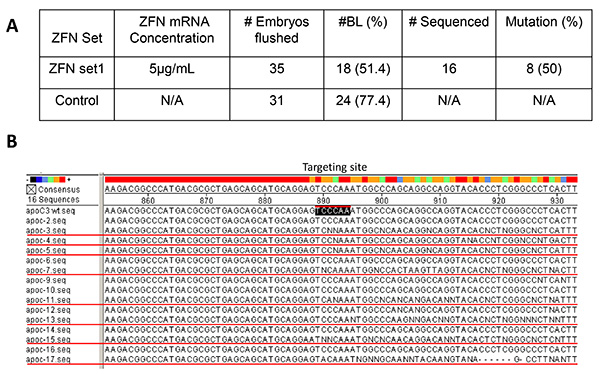
Figuur 3. Embryo's in vitro validatie van ZFN. De mRNA (5 ug / ml) Set 1 werd gemicroinjecteerd het cytoplasma van 35 pronucleaire fase konijn embryo (A). Gespoeld embryo zonder microinjectie behandeling (n = 31) werden gebruikt als controlegroep. Het BL ontwikkeling bedroeg 77,4% in de controlegroep. In de gemicroinjecteerd groep, de BL bedroeg 51,4%. Van 16 BLs onderworpen aan PCR sequencing, 8 (50%) werden geïdentificeerd als positief, wat aangeeft Set 1 is een effectieve ZFN set om mutaties op de targeting plaats (B, apoc3wt.seq, zwart-boxed) van apoCIII bij konijnen. De BLs bevattende mutaties BL # apoc-3, 4, 5, 7, 11, 13, 15, en 17 (B, rood onderstreept). De resterende BLs (# apoc-2, 6, 9, 10, 12, 14 en 16) hebben geen mutaties op de targeting website. Klik hier voor grotere afbeelding .

Figuur 4. Productie van apoCIII KO konijnen. Honderd en vijfenveertig embryo gemicroinjecteerd met ZFN Set 1 mRNA's werden overgebracht naar 7 pseudo-zwangere konijnen ontvanger (A). Vers gespoeld embryo's (n = 75) zonder ZFN microinjectie werden doorgegeven aan ontvangers (n = 6) als controlegroep. De term tarief berekend als totale looptijd kits / totaal embryo experiment groep 140,5% (21/145), terwijl het tarief is 29,3% (22/75) in de controlegroep (A). Van de 21 kits geboren in de gemicroinjecteerd groep, vijf (R1, R9, R11, R12 en R16) werden geïdentificeerd als positief KO kits na PCR sequencing (B). De INDELs bij de targeting site zijn twee inserties (1 voor zowel R9 en R11) en drie deleties (Δ1, Δ 20 Δ 21 voor R1, R12 en R16, respectievelijk). Klik hier voor grotere afbeelding .
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dit werk werd deels gefinancierd door subsidies van de National Institutes of Health (HL105114, HL088391, NS066652 en HL068878 te YEC), de American Heart Association (Nationale Scientist Development 0835237N om JZ). YEC wordt financieel ondersteund als begiftigd Frederick Huetwell hoogleraar Cardiovasculaire Geneeskunde aan de Universiteit van Michigan Medical Center (UMMC). Dit werk gebruikt Core Services ondersteund door Center for Advanced Models for Translational Sciences and Therapeutics (CAMTraST) bij UMMC.
Materials
| APOC3-ZFN | Sigma Aldrich | CSTZFNY-1KT | Target Gene: APOC3, Lot Number: 12201118MN |
| mMESSAGE kit | Invitrogen | AM1344M | mRNA synthesis |
| MEGAclear Kit | Invitrogen | AM1908M | mRNA purification |
| Follicle-stimulating hormone | Bioniche Life Sciences | Folltropin-V | Treating embryo donor rabbits |
| Human chorionic gonadotropin | Intervet | Chorulon | Treating embryo donor rabbits |
| Gonadotropin-releasing hormone | Prospecbio | HOR-255 | Treating embryo recipient rabbits |
| Earle's Balanced Salt Solution (EBSS) | Thermo Fisher Scientific | SH30029.02 | Embryo culture, base medium |
| MEM (nonessential amino acid) | Sigma Aldrich | M7145 | Embryo culture, supplements |
| BME AMINO ACIDS solution | Sigma Aldrich | B6766 | Embryo culture, supplements |
| Glutamine | Gibco | 25030-149 | Embryo culture, supplements |
| Sodium pyruvate | Gibco | 11360-070 | Embryo culture, supplements |
| Fetal bovine serum | Sigma Aldrich | 12003C | Embryo culture, supplements |
| HEPES buffered TCM 199 | Gibco | 12350039 | Embryo manipulation medium |
| Incubator | Eppendorf | Galaxy 170 | Embryo culture equipment |
| Micromanipulator | Eppendorf | TransferMan NK 2 | Embryo manipulation equipment |
| Micropipette puller | Sutter Instruments Inc. | P-1000 | Embryo manipulation equipment |
| Microinjector | Tritech Research | MINJ-D | Embryo manipulation equipment |
| Borosilicate glass capillary tubes | World Precision Instruments, Inc. | TW100F-6 | Embryo manipulation supply |
| Euthasol (pentobarbitol sodium) | Virbac AH, Inc. | ANADA#200-071 | Euthanization of embryo donor rabbits |
References
- Ooi, E. M., Barrett, P. H., Chan, D. C., Watts, G. F. Apolipoprotein C-III: understanding an emerging cardiovascular risk factor. Clinical Science. 114, 611-624 (2008).
- Pollin, T. I., et al. A null mutation in human APOC3 confers a favorable plasma lipid profile and apparent cardioprotection. Science. 322, 1702-1705 (2008).
- Ginsberg, H. N., et al. Apolipoprotein B metabolism in subjects with deficiency of apolipoproteins CIII and AI. Evidence that apolipoprotein CIII inhibits catabolism of triglyceride-rich lipoproteins by lipoprotein lipase in vivo. The Journal of Clinical Investigation. 78, 1287-1295 (1986).
- Cohn, J. S., et al. Increased apoC-III production is a characteristic feature of patients with hypertriglyceridemia. Atherosclerosis. 177, 137-145 (2004).
- Cohn, J. S., Patterson, B. W., Uffelman, K. D., Davignon, J., Steiner, G. Rate of production of plasma and very-low-density lipoprotein (VLDL) apolipoprotein C-III is strongly related to the concentration and level of production of VLDL triglyceride in male subjects with different body weights and levels of insulin sensitivity. The Journal of Clinical Endocrinology and Metabolism. 89, 3949-3955 (2004).
- Maeda, N., et al. Targeted disruption of the apolipoprotein C-III gene in mice results in hypotriglyceridemia and protection from postprandial hypertriglyceridemia. The Journal of Biological Chemistry. 269, 23610-23616 (1994).
- Jong, M. C., et al. Apolipoprotein C-III deficiency accelerates triglyceride hydrolysis by lipoprotein lipase in wild-type and apoE knockout mice. Journal of Lipid Research. 42, 1578-1585 (2001).
- James, J. F., Hewett, T. E., Robbins, J. Cardiac physiology in transgenic mice. Circ. Res. 82, 407-415 (1998).
- Duranthon, V., et al. On the emerging role of rabbit as human disease model and the instrumental role of novel transgenic tools. Transgenic Research. 21, 699-713 (2012).
- Fan, J., Watanabe, T. Transgenic rabbits as therapeutic protein bioreactors and human disease models. Pharmacol. Ther. 99, 261-282 (2003).
- Shiomi, M., Ito, T. The Watanabe heritable hyperlipidemic (WHHL) rabbit, its characteristics and history of development: a tribute to the late Dr. Yoshio Watanabe. Atherosclerosis. 207, 1-7 (2009).
- Morehouse, L. A., et al. Inhibition of CETP activity by torcetrapib reduces susceptibility to diet-induced atherosclerosis in New Zealand White rabbits. Journal of Lipid Research. 48, 1263-1272 (2007).
- Getz, G. S., Reardon, C. A. Animal models of atherosclerosis. Arteriosclerosis, Thrombosis, and Vascular Biology. 32, 1104-1115 (2012).
- Carlson, D. F., et al. Efficient TALEN-mediated gene knockout in livestock. Proceedings of the National Academy of Sciences of the United States of America. , (2012).
- Jiang, W., Bikard, D., Cox, D., Zhang, F., Marraffini, L. A. RNA-guided editing of bacterial genomes using CRISPR-Cas systems. Nature Biotechnology. 31, 233-239 (2013).
- Petersen, B. Update on ‘molecular scissors’ for transgenic farm animal production. Reproduction, Fertility, and Development. 25, 317-318 (2012).
- Yang, D., et al. Generation of PPARgamma mono-allelic knockout pigs via zinc-finger nucleases and nuclear transfer cloning. Cell Research. 21, 979-982 (1038).
- Flisikowska, T., et al. Efficient immunoglobulin gene disruption and targeted replacement in rabbit using zinc finger nucleases. PLoS ONE. 6, e21045 (2011).
- Foley, J. E., et al. Targeted mutagenesis in zebrafish using customized zinc-finger nucleases. Nature Protocols. 4, 1855-1867 (2009).
- Carbery, I. D., et al. Targeted genome modification in mice using zinc-finger nucleases. Génétique. 186, 451-459 (2010).
- Mashimo, T., et al. Generation of knockout rats with X-linked severe combined immunodeficiency (X-SCID) using zinc-finger nucleases. PLoS ONE. 5, e8870 (2010).
- Ding, Y., et al. Hypertriglyceridemia and delayed clearance of fat load in transgenic rabbits expressing human apolipoprotein CIII. Transgenic Research. 20, 867-875 (2011).
- Hauschild, J., et al. Efficient generation of a biallelic knockout in pigs using zinc-finger nucleases. Proceedings of the National Academy of Sciences of the United States of America. 108, 12013-12017 (2011).

