Internalisering og Observation af fluorescerende biomolekyler i levende mikroorganismer via Elektroporation
Summary
Studies of biomolecules in vivo are crucial for understanding molecular function in a biological context. Here we describe a novel method allowing the internalization of fluorescent biomolecules, such as DNA or proteins, into living microorganisms. Analysis of in vivo data recorded by fluorescence microscopy is also presented and discussed.
Abstract
The ability to study biomolecules in vivo is crucial for understanding their function in a biological context. One powerful approach involves fusing molecules of interest to fluorescent proteins such as GFP to study their expression, localization and function. However, GFP and its derivatives are significantly larger and less photostable than organic fluorophores generally used for in vitro experiments, and this can limit the scope of investigation.
We recently introduced a straightforward, versatile and high-throughput method based on electroporation, allowing the internalization of biomolecules labeled with organic fluorophores into living microorganisms. Here we describe how to use electroporation to internalize labeled DNA fragments or proteins into Escherichia coli and Saccharomyces cerevisiæ, how to quantify the number of internalized molecules using fluorescence microscopy, and how to quantify the viability of electroporated cells. Data can be acquired at the single-cell or single-molecule level using fluorescence or FRET. The possibility of internalizing non-labeled molecules that trigger a physiological observable response in vivo is also presented. Finally, strategies of optimization of the protocol for specific biological systems are discussed.
Introduction
De fleste fluorescens undersøgelser inde levende celler afhænger af proteinfusioner med fluorescerende proteiner (fps), såsom GFP 1. Disse fluorescerende tags kan studier af kopitallet, diffusion mønster eller lokalisering af proteiner involveret i processer som genekspression eller membran transport 2-7. Rammeprogrammer tilbyde høj mærkning specificitet, nem implementering, og fås i en stor beholdning af varianter med forskellige fotofysiske og kemiske egenskaber 1. Men organiske fluoroforer forbliver det primære valg for in vitro-forsøg på grund af deres større fotostabilitet (op til 100 gange mere stabil end rammeprogrammerne) 8,9, lille størrelse (op til 100 gange mindre volumen end RP) og nem intramolekylær mærkning (især gennem anvendelse af cysteinrester). Alle disse faktorer er særligt vigtige for enkelt-molekyle fluorescens og FRET studerer 10.
Adskillige internalisering metoder Combining fordelene ved økologisk mærkning og in vivo detektion er blevet indført i det seneste årti; Imidlertid er sådanne metoder enten anvende relativt store polypeptider tags (f.eks TMP, halogen eller 20 kDa SNAP tags) 11-14, kræver anvendelse af unaturlige aminosyrer 15, eller er begrænset til store, single-membran eukaryote celler (f.eks. , skrabe lastning, sprøjte lastning, mikroinjektion) 16-19.
Denne protokol beskriver en roman, ligefrem og højt gennemløb internalisering metode, par fordelene af organiske fluoroforer med in vivo observation. At udvikle denne teknik, vi tilpasset elektroporation procedure almindeligvis anvendes til at transformere celler med plasmid-DNA 20,21 med henblik på at indlæse mikroorganismer, såsom E. coli eller S. cerevisiae med økologisk mærkede biomolekyler. Protokollen består af 4 trin: inkubering af celler med mærkede biomolekyler,elektroporation, celle opsving, og celle vask for at fjerne ikke-internaliserede biomolekyler. Her præsenterer vi denne elektroporation protokol, samt cell imaging og dataanalyse processer for at studere cellebaserede og single-molekyle fluorescens og ærgre signaler.
Elektroporation afhængig udleder en høj spænding elektrisk felt over en lav ionstyrke cellesuspension at danne forbigående membranporer hvorigennem biomolekyler kan indtaste celler (figur 1) 20,21. Ligesom med transformation af bakterier eller gær med plasmid-DNA, skal være forberedt før elektroporering at sikre deres electrocompetency celler. Denne procedure, som består af flere vasketrin med vand, øger membranpermeabilitet og sænker ionstyrken af cellen løsning til at undgå lysbuedannelse i elektroporation cuvette. I denne protokol, kan celler fremstilles som beskrevet nedenfor (se PROTOKOL: 1.1) eller købt fra kommerciel udbyders.
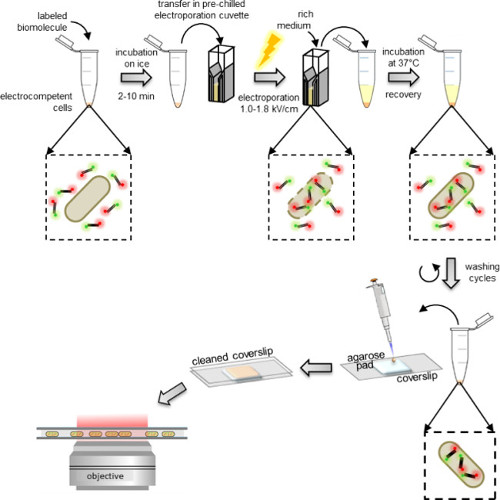
Figur 1: Skematisk repræsentation af internalisering protokollen Fra venstre til højre:. Tilføje et par mikroliter mærkede biomolekyler til alikvot af elektrokompetente celler (dobbelt-mærkede DNA-fragmenter og bakterier i dette eksempel); inkuberes 1 til 10 minutter på is og overføre til en forud afkølet elektroporation cuvette; elektroporere og derefter tilføje 0,5-1 ml rigt medium til cellerne umiddelbart efter; inkuberes ved 37 ° C (eller den ønskede temperatur af organismen, fx 29 ° C for gær) at lade cellerne inddrive; udføre 5 vasketrin for at fjerne overskydende ikke-internaliserede mærkede molekyler; resuspenderes slutpelleten i 100-200 ml PBS-buffer og pipette 10 pi på en agarose pad; dække puden med en renset dækglas og billede på et fluorescens mikroskop (i bredt felt tilstand eller HILO tilstand).
Mens DNA internalisering er ligetil (figur 2), der skal tages, når internalisere mærkede proteiner ved hjælp af elektroporation forholdsregler. For det første kan bestanden prøve af økologisk mærkede protein stadig indeholde en lille procentdel af gratis farvestof. Gratis farvestofmolekyler er meget mindre end proteiner, og måske derfor internaliseres fortrinsvis. For at sikre, at størstedelen af de observerede internaliserede fluorescerende molekyler svarer til proteinet af interesse, bør den oprindelige proteinprøve indeholde mindre end ~ 2% fri farvestof (figur 5) 22. Overskuddet af ikke-internaliserede mærkede proteiner kan også holde sig til den ydre cellemembran efter elektroporation; dette fænomen er protein-specifik og skal kontrolleres for hvert nyt protein. Vi foreslår flere muligheder, der tillader fjernelse af ikke-internaliserede proteiner fra den indlæste celleprøve (Se PROTOKOL: 3.3.3).
Endelig celler resuspenderes i et lille volumen af phosphatbuffer og pipetteret på en agarose pad, så deres billeddannelse på et fluorescensmikroskop. Immobilisering på agarose puder er en simple og effektiv måde at billeddannelse celler på et dækglas uden at skade deres integritet. Puden bør indeholde en lav fluorescens dyrkningsmedium.
Cell imaging kan udføres enten i Vidvinklet, total intern refleksion fluorescens (TIRF) eller ved hjælp HILO (Highly krængning og lamineret Optical Sheet) mikroskopi. I Hilo konfiguration laserstrålen trænger dybere ind i prøven end i TIRF, endnu ikke belyse hele prøven som for Vidvinklet, som tillader en større signal-støj-forhold 23. Afhængigt af laser magt og tidsopløsning bruges kan internaliserede biomolekyler tælles (ved hjælp af trinvis-fotoblegning analyse, figur 3), lokaliseret, eller spores 24-28. Internalisering af dobbelt mærkede konstruktioner med et FRET par fluoroforer tillader kvantificering af FRET både enkelt celle eller et enkelt molekyle niveauer (figur 6).
Forskellige parametre kan varieresafhængig af den ønskede effekt og det biologiske system undersøgt. For det første kan mængden af internaliseret materiale per celle indstilles ved at ændre koncentrationen af mærkede biomolekyler tilsat til cellerne før elektroporering (figur 2). Elektroporering feltstyrke vil også påvirke både lastning effektivitet og levedygtighed celle; som forventet, mens stiger belastningseffektivitet med stigende feltstyrke, levedygtigheden af elektroporerede celler aftager (figur 4A). Begge parametre kan kvantificeres ved at registrere den procentdel af lastet og delende celler efter elektroporering. Denne levedygtighedsassay kombineret med fluorescensimagografi også kontrollerer observation af internaliserede biomolekyler i levende celler og tillade kontinuerlig observation over flere generationer (figur 4B).
Sammenfattende denne protokol tillader internalisering af fluorescensmærkede DNA og proteinmolekyler iE. coli eller S. cerevisiae 26. Enkelte molekyler mærket med økologiske fluoroforer kan spores med høj spatiotemporale opløsning til tidshorisonter en størrelsesorden længere end rammeprogrammer. Endelig er denne metode er kompatibel med Vidvinklet, TIRF og konfokal afsløring, samt pulserende excitation ordninger såsom ALEX (skiftevis laserexcitation 28,29).
Protocol
Representative Results
Discussion
Mange parametre kan varieres under celle elektroporation og dataopsamling afhængig biologiske system af interesse og den præcise karakter af forsøget (celle-niveau eller single-molekyle analyse). For eksempel, når elektroporering DNA i bakterier, 0,25-5 pmol mærket dsDNA fragmenter fører til en lav internalisering effektivitet, der muliggør direkte påvisning single-molekyle (dvs.., Uden behov for fotoblegning forhånd). Over 5 pmol dsDNA, celler tendens til at være tungt lastet, en ordning bedre egnet til encellede analyse. Alle mærkede DNA'er bør også være tidligere geloprenset for at fjerne ethvert spor af frit farvestof (ikke-reageret fluorofor) fra DNA stamopløsning. Desuden potentielle problemer med DNA-nedbrydning, især for smFRET eksperimenter, kan løses ved anvendelse af DNA'er med unaturlige nukleinsyrer eller motiver, der beskytter exonuklease-tilgængelige termini såsom hairpin-loops.
En anden adjustable parameter i elektroporation er feltstyrken påføres under elektroporation. Lav feltstyrke (~ 1 kV / cm) vil føre til en lav belastningseffektivitet egnet til enkelt-molekyle studier. Højere feltstyrker (op til 1,8 kV / cm) vil øge lastning effektivitet; Imidlertid er der en omvendt korrelation mellem feltstyrke og cellelevedygtighed efter elektroporation (se figur 4). For reference, en normal feltstyrke anvendes for bakterier og gær elektroporation er ~ 1,5 kV / cm. Tidskonstanten, repræsenterer længden af dette henfald er en bekvem parameter til følge, eftersom tidskonstanten dråber, så snart nogen gnistdannelse fænomen forekommer i kuvetten. Under normale indstillinger bør tidskonstanten være større end 4 ms; lavere værdier vil føre til lav belastningseffektivitet eller endog ikke-loaded beskadigede celler. De fleste electroporators tilbyde andre frihedsgrader (såsom "puls trunkering" eller "puls form"), som kan ændres til at tune bådecelle lastning og levedygtighed. Vi anvendte denne fremgangsmåde for både bakterier og gær, men lignende procedurer bør også tillade internalisering af mærkede biomolekyler i pattedyrceller ved hjælp af passende elektroporator indstillinger da deres membran er faktisk mindre kompleks (enkelt lipiddobbeltlag), og da elektroporation er allerede blevet anvendt med sådanne celler 21.
Når internalisere mærkede proteiner, skal fjernes fra den kendte elektroporering mærkede protein stamopløsning alle frie farvestof. Free farvestofmolekyler, på grund af deres mindre størrelse, kan internaliseres fortrinsvis over proteiner af interesse, og er vanskelige at skelne under dataanalyse (trods deres forventede hurtigere diffusion). Som en vejledning, for en prøve af økologisk mærkede protein at være egnet til elektroporation, bør mængden af tilbageværende fri farvestof være under 2% (påvist ved hjælp af fluorescerende scanning af en SDS-PAGE) 22. Denne proces er særlig vigtigt,som nogle molekyler kan holde sig til de ydre membraner af elektroporerede bakterier eller gær. I denne forbindelse bør den negative kontrolprøve vise fluorescensintensitet per celle klart lavere end elektroporerede celler, ideelt så lavt som autofluorescens niveau af tomme celler (celler, som ikke er blevet inkuberet med eventuelle fluorescensmærkede biomolekyler eller elektroporeret, figur 2).
Som med dsDNA er internalisering effektivitet mærkede proteiner bundet til mængden af biomolekyler tilsat til cellerne før elektroporering. Men andre parametre, såsom størrelse og ladning, spiller en rolle i internalisering. Små proteiner udviser høje internalisering effektiviteten, mens større proteiner (op til 98 kDa) med held kan internaliseres, men med lavere effektivitet (figur 5) 26. Det isoelektriske punkt af proteinet potentielle vekselvirkninger med cellemembranen og andre fysisk-kemiske parametre ogsåindflydelse celle loading under elektroporering. Som et resultat, brugerne nødt til at optimere eksperimenter for deres eget system, vel vidende, at en høj initial koncentration af mærket protein (> 50 uM) vil give den bedste chance for vellykket belastning. Elektroporation tilbyder også et nyt redskab til at forstyrre og analysere cellulær funktion ved at indføre proteiner og andre biomolekyler i celler (enten mærket eller umærket). T7 RNA-polymerase eksperimenter (figur 5C) forelægge en sådant eksempel på et eksperiment, hvor vi kan indføre et biomolekyle, der kan ændre genekspression in vivo ved hjælp af elektroporering.
Ved udførelse af enkelt-molekyle fluorescens eksperimenter er TIR belysning sædvanligvis begunstiget i forhold til andre illumination tilstande, fordi den giver det bedste signal-til-støj-forholdet af spændende kun fluoroforer inden for en tynd sektion over dækglasset overflade (~ 100 nm). Men imaging mærkede biomolekyler spredende inde levende mikroorganismer kan rekoret dybere belysning (op til 0,8 um for E. coli). Dybere belysning opnås i Hilo tilstand, mens et højt signal-til-støjforhold opretholdes. På den anden side, bredt felt billeddannelse er særlig vigtig for trinvis fotoblegning analyse, hvor brugeren at anslå antallet af internaliserede molekyler ved fotoblegning en hel loaded celle med høj laser power og dividere den første celle fluorescensintensitet af ensartet intensitet produceret af et enkelt molekyle (enkelt fotoblegning trin, figur 3). Vidvinklet billeddannelse er også påkrævet til langsigtet molekyle sporing for at lokalisere de spredende molekyler af interesse, selv om deres baner dækker cellevolumen hele.
I denne protokol, præsenterer vi, hvordan elektroporation, en standard teknik til biologer og biokemikere til at levere nukleinsyrer i celler, er en simpel metode til at levere fluorescerende biomolekyler i forskellige celletyper. Ther roman, high-throughput teknik giver et unikt værktøj til at observere mærkede molekyler i deres naturlige miljø. Derudover biomolekyler mærket med fluoroforer dækker en bred vifte af bølgelængder, elektroporation kan levere molekyler modificeret med mange kemiske grupper, såsom unaturlige nukleotider og aminosyrer, metalchelatorer, tværbindere og anbringelse i bur grupper. Hvis det biologiske system af interesse er ikke afgørende for udvikling cellen, kan det gen, der koder for målproteinet også blive slettet (eller bankede-down), der sikrer, at proteinerne observeret efter internalisering repræsenterer alle (eller de fleste) af det intracellulære protein pool . I det væsentlige, kan elektroporation "transplantation" fleksibiliteten af in vitro biokonjugater i levende celler og derfor en fordel indsats i syntetisk biologi, systembiologi og in vivo enkelt molekyle detektion.
Divulgations
The authors have nothing to disclose.
Acknowledgements
We thank Stephan Uphoff for discussions.
R.C. was supported by Linacre College, Oxford University. A.P. was supported by the German Academic Exchange Service (DAAD), the German National Academic Foundation and EPSRC. M.S. was supported by the Wellcome Trust. A.N.K. was supported by a UK BBSRC grant (BB/H01795X/1), and a European Research Council Starter grant (261227).
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| ElectroMax DH5-alpha Comptent cells | Invitrogen | 11319-019 | or any other commercial or lab-mage electrocompetant bacteria or yeast. |
| EZ Rich Defined Madia | Teknova | M2105 | low fluorescence rich media |
| MicroPulser Electroporation Apparatus | Biorad | 165-2100 | or any classical electroporator for microorganism transformation |
| Certified Molecular Biology agarose | Biorad | 161-3100 | low fluorescence agarose for agarose pad |
| Microscope coverslips No 1.5 thickness | Menzel | BB024060SC | remove background particles by heating slides in furnace at 500 °C for 1h |
| Single-molecule fluorescence microscope | Home-built | described in REFs | |
| Localization software | Custom-written, available online | MATLAB and C++ software package that can be adapted for localization analysis. | |
| Tracking software | Available online | MATLAB implementation by Blair and Dufresne. |
References
- Tsien, R. Y. The green fluorescent protein. Annu Rev Biochem. 67, 509-544 (1998).
- Leake, M. C., et al. Stoichiometry and turnover in single, functioning membrane protein complexes. Nature. 443, 355-358 (2006).
- Taniguchi, Y., Kawakami, M. Application of HaloTag protein to covalent immobilization of recombinant proteins for single molecule force spectroscopy. Langmuir. 26, 10433-10436 (2010).
- Xie, X. S., Choi, P. J., Li, G. W., Lee, N. K., Lia, G. Single-molecule approach to molecular biology in living bacterial cells. Annual review of biophysics. 37, 417-444 (2008).
- Lee, J. H., et al. Highly multiplexed subcellular RNA sequencing in situ. Science. 343, 1360-1363 (2014).
- Miesenbock, G., De Angelis, D. A., Rothman, J. E. Visualizing secretion and synaptic transmission with pH-sensitive green fluorescent proteins. Nature. 394, 192-195 (1998).
- Sauer, M. Localization microscopy coming of age: from concepts to biological impact. J Cell Sci. 126, 3505-3513 (2013).
- Dempsey, G. T., Vaughan, J. C., Hao Chen, K., Zhuang, X. Evaluation of fluorophores for optimal performance in localizationbased super-resolution imaging. Nat Meth. 8, 1027-1041 (2011).
- Shaner, N. C., Steinbach, P. A., Tsien, R. Y. A guide to choosing fluorescent proteins. Nat Meth. 2, 905-909 (2005).
- Landgraf, D., Okumus, B., Chien, P., Baker, T. A., Paulsson, J. Segregation of molecules at cell division reveals native protein localization. Nat. Methods. 9, 480-482 (2012).
- Jaitin, D. A., et al. Massively Parallel Single-Cell RNA-Seq for Marker-Free Decomposition of Tissues into Cell Types. Science. 343, 776-779 (2014).
- Aldridge, S., et al. AHT-ChIP-seq: a completely automated robotic protocol for high-throughput chromatin immunoprecipitation. Genome Biol. 14, R124 (2013).
- Keppler, A., et al. A general method for the covalent labeling of fusion proteins with small molecules in vivo. Nat Biotechnol. 21, 86-89 (2003).
- Wombacher, R., et al. Live-cell super-resolution imaging with trimethoprim conjugates. Nat. Methods. 7, 717-719 (2010).
- Zhang, Z., et al. A new strategy for the site-specific modification of proteins in vivo. Biochimie. 42, 6735-6746 (2003).
- McNeil, P. L., Murphy, R. F., Lanni, F., Taylor, D. L. A method for incorporating macromolecules into adherent cells. J Cell Biol. 98, 1556-1564 (1984).
- Clarke, M. S., McNeil, P. L. Syringe loading introduces macromolecules into living mammalian cell cytosol. J Cell Sci. 102, 533-541 (1992).
- Sakon, J. J., Weninger, K. R. Detecting the conformation of individual proteins in live cells. Nat. Methods. 7, 203-205 (2010).
- Taylor, L. S. Electromagnetic syringe. IEEE Trans. Biomed. Eng. 25, 303-304 (1978).
- Dower, W. J., Miller, J. F., Ragsdale, C. W. High efficiency transformation of E. coli by high voltage electroporation. Nucleic Acids Res. 16, 6127-6145 (1988).
- Neumann, E., Schaefer-Ridder, M., Wang, Y., Hofschneider, P. H. Gene transfer into mouse lyoma cells by electroporation in high electric fields. EMBO J. 1, 841-845 (1982).
- Sustarsic, M., et al. Optimized delivery of fluorescently labeled proteins in live bacteria using electroporation. Histochem Cell Biol. , (2014).
- Tokunaga, M., Imamoto, N., Sakata-Sogawa, K. Highly inclined thin illumination enables clear single-molecule imaging in cells. Nat. Methods. 5, 159-161 (2008).
- Sinha, A., et al. A cascade of DNA-binding proteins for sexual commitment and development in Plasmodium. Nature. 000, 1-5 (2014).
- English, B. P., et al. Single-molecule investigations of the stringent response machinery in living bacterial cells. Proc Natl Acad Sci U S A. 108, E365-E373 (2011).
- Crawford, R., et al. Long-lived intracellular single-molecule fluorescence using electroporated molecules. Biophys J. 105, 2439-2450 (2013).
- Uphoff, S., Reyes-Lamothe, R., Garza de Leon, F., Sherratt, D. J., Kapanidis, A. N. Single-molecule DNA repair in live bacteria. Proc Natl Acad Sci U S A. 110, 8063-8068 (2013).
- Uphoff, S., Sherratt, D. J., Kapanidis, A. N. Visualizing Protein-DNA Interactions in Live Bacterial Cells Using Photoactivated Single-molecule Tracking. J Vis Exp. , (2014).
- Hohlbein, J., Gryte, K., Heilemann, M., Kapanidis, A. N. Surfing on a new wave of single-molecule fluorescence methods. Phys Biol. 7, 031001 (2010).
- Xie, X. S., Yu, J., Yang, W. Y. Perspective – Living cells as test tubes. Science. 312, 228-230 (2006).
- Santoso, Y., et al. Conformational transitions in DNA polymerase I revealed by single-molecule FRET. Proc Natl Acad Sci U S A. 107, 715-720 (2010).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature communications. 4, 2131 (2013).

