Hakket Væv i Komprimeret Collagen: A Cell-holdige Biotransplant for Single-iscenesat rekonstruktionskirurgi Repair
Summary
Tissue engineering omfatter ofte in vitro ekspansion for at skabe autotransplantater til vævsregenerering. I denne undersøgelse blev udviklet en fremgangsmåde til vævsekspansion, regenerering og genopbygning in vivo for at minimere behandlingen af celler og biologiske materialer uden for kroppen.
Abstract
Conventional techniques for cell expansion and transplantation of autologous cells for tissue engineering purposes can take place in specially equipped human cell culture facilities. These methods include isolation of cells in single cell suspension and several laborious and time-consuming events before transplantation back to the patient. Previous studies suggest that the body itself could be used as a bioreactor for cell expansion and regeneration of tissue in order to minimize ex vivo manipulations of tissues and cells before transplanting to the patient. The aim of this study was to demonstrate a method for tissue harvesting, isolation of continuous epithelium, mincing of the epithelium into small pieces and incorporating them into a three-layered biomaterial. The three-layered biomaterial then served as a delivery vehicle, to allow surgical handling, exchange of nutrition across the transplant, and a controlled degradation. The biomaterial consisted of two outer layers of collagen and a core of a mechanically stable and slowly degradable polymer. The minced epithelium was incorporated into one of the collagen layers before transplantation. By mincing the epithelial tissue into small pieces, the pieces could be spread and thereby the propagation of cells was stimulated. After the initial take of the transplants, cell expansion and reorganization would take place and extracellular matrix mature to allow ingrowth of capillaries and nerves and further maturation of the extracellular matrix. The technique minimizes ex vivo manipulations and allow cell harvesting, preparation of autograft, and transplantation to the patient as a simple one-stage intervention. In the future, tissue expansion could be initiated around a 3D mold inside the body itself, according to the specific needs of the patient. Additionally, the technique could be performed in an ordinary surgical setting without the need for sophisticated cell culturing facilities.
Introduction
De fleste væv engineering undersøgelser om transplantation til huden og urogenitale tarmkanalen omfatter autologe celle høst fra sundt væv og celler ekspansion i særligt udstyrede celle-dyrkning faciliteter 1,2.
Efter celleekspansion celler sædvanligvis opbevares til senere anvendelse, når patienten er parat til at modtage autograft. Nitrogenholdige frysere tillader langtidsopbevaring ved lave temperaturer på -150 ° C eller lavere. Processen med frysning skal være forsigtig og kontrolleret for ikke at miste cellerne. En risiko for celledød er krystallisering af intracellulær vand under optøningsprocessen, hvilket kan føre til sprængning af cellemembranerne. Celle frysning udføres sædvanligvis ved langsom og kontrolleret afkøling (-1 ° C pr min), ved anvendelse af en høj koncentration af celler, føtalt bovint serum og dimethylsulfoxid. Efter optøning skal bearbejdes igen ved at fjerne frysning medium og dyrkning på cellekultur plast eller et cellernebiomaterialet før transplantation tilbage til patienten.
Alle de ovennævnte trin er tidskrævende, arbejdskrævende og bekostelig 3. Derudover alle in vitro-behandling af celler beregnet til patient transplantation er stærkt reguleret og kræver veluddannede og akkrediterede personale og laboratorier 4. Alt i alt, at skaffe en sikker og pålidelig fremstillingsproces, teknikken kunne kun være etableret i et meget lille antal teknisk avancerede centre og en bredere brug i almindelige kirurgiske lidelser er tvivlsomt.
For at overvinde begrænsningerne ved celledyrkning i laboratoriemiljøet er begrebet transplantere hakket væv for celle ekspansion in vivo indført ved hjælp af kroppen selv som en bioreaktor. Til disse formål, vil de autotransplantater fortrinsvis skal transplanteres på et 3D støbeform i overensstemmelse med formen, der er nødvendig ved den endelige rekonstruktion af organet af interest 5-7.
Oprindeligt var ideen om at transplantere hakket epitel præsenteret af Meek i 1958, da han beskrev, hvordan epitel vokser fra kanterne af et sår. Han påviste, at et lille stykke hud vil øge sine marginer og dermed dens potentiale for celle ekspansion med 100% ved at skære det stykke to gange i vinkelrette retninger (figur 1) 8. Teorien er blevet støttet af brugen af i indgreb delvise tykkelse hudtransplantationer for hudtransplantation 9 og i huden sårheling modeller 10.
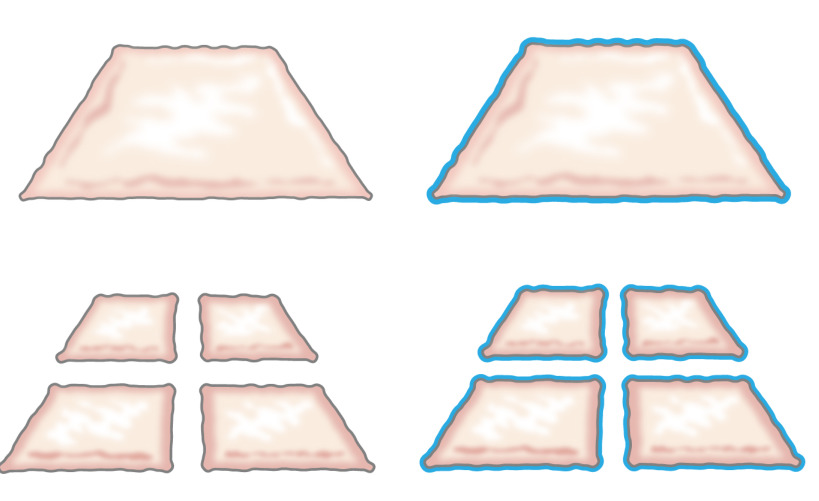
Figur 1:. Meek teori Ifølge Meek teori, epitel vokser fra kanterne af et sår. Ved at øge området afsløret af hakningen teknologi, hakket væv epithelializes sår fra mange vinkler.
Den foreliggende undersøgelse er baseret på den hypotese, at det samme princip kunne anvendes til det subkutane væv ved at placere hakket epitel omkring en form. Epitelcellerne ville mobilisere fra hakket transplantationer (reorganisere), dække såret områder (migrere) og dividere (udvide) for at danne en kontinuerlig neoepithelium der dækker sårområdet og adskiller fremmedlegeme (formen) fra det indre legeme ( figur 2).

Figur 2:. Tegning af en 3D-form med hakket epitel til in vivo intracorporal vævsekspansion ifølge teorien om Meek Ved at bruge hakket væv anbringes på en form og derefter transplanteres til det subkutane væv, er hypotesen, at epitelcellerne vandrer fra kanter af det hakkede væv, omorganisere og ekspandere for således at danne en kontinuerlig neoepithelium der dækker sårområdet og adskiller fremmedlegeme (formen) fra det indre legeme.
Selvom tidligere in vivo undersøgelser viser lovende resultater, kunne yderligere forbedringer opnås ved at styrke de autotransplantater så regenereret epitel kunne modstå mekanisk traume bedre 7. Til disse formål, blev vigtige forudsætninger for en vellykket biomateriale identificeret, såsom: let diffusion af næringsstoffer og affaldsprodukter, mulighed for skimmel i en 3D måde og lethed af kirurgisk håndtering. Konklusioner blev foretaget, at disse behov kan opfyldes ved at tilføje et sammensat biomateriale til det hakkede væv.
Den nuværende undersøgelse med henblik på at udvikle et stillads bestående af hakket væv i plast-komprimeret collagen indeholdende en forstærkende kerne af en bionedbrydelig stof. Ved hjælp af disse, kan levedygtige celler migrere fra hakket vævspartikler og proliferere med morfologiske træk er karakteristiske for den oprindelige epitel (hud eller urothelium). Ved hjælp af plast kompression, skafottet var reducered i størrelse fra 1 cm til ca. 420 um som hakket partikler blev indkapslet i det øvre lag collagen. Kernen stof kunne være nogen polymer men skal ændres med en hydrofil overflade for at forbinde med de dækker kollagenlagene 11.
Den fremgangsmåde, en forbedret stillads integritet ved at indarbejde en strikket maske bestående af poly (ε-caprolacton) (PCL) inden for to plast komprimeret kollagengeler bruger det som et stillads til dyrkning hakket blære slimhinde eller hakket hud fra svin. Konstruktionen blev opretholdt i celledyrkningsbetingelser i op til 6 uger in vitro, hvilket viser vellykket dannelse af en lagdelt, flerlaget urothelium eller squamous hud epitel på toppen af en velkonsolideret hybrid konstruktion. Konstruktionen var let at håndtere og kan sutureres på plads til blære augmentation formål eller dækning af overfladefejl. Alle dele af vævet stillads er FDA-godkendt, og teknikkenkunne anvendes til procedurer ettrins ved vævshøst, hakning, plast kompression, og omplantning tilbage til patienten som en enkelt-iscenesat intervention. Proceduren kan udføres for væv ekspansion og genopbygning under sterile forhold i enhver almen kirurgi enhed.
Protocol
Representative Results
Discussion
Denne undersøgelse viser en let-at-bruge tilgang til frembringelse blærevæggen pletter med autologt væv til transplantation på operationsbordet. Plastrene er dannet ved kombinationen af en biologisk nedbrydelig polymer strikning i midten og kollagen med og uden hakket væv i de ydre overflader i kombination med plast kompression. Plastic komprimering er en metode, der tidligere er beskrevet af andre forfattere og kan defineres som en hurtig uddrivning af fluid fra kollagengeler 12,13. Hakket væv a…
Divulgations
The authors have nothing to disclose.
Acknowledgements
The authors thank the Swedish Society for Medical Research, the Promobilia Foundation, the Crown Princess Lovisa Foundation, the Freemason Foundation for Children’s Welfare, the Swedish Society of Medicine, the Solstickan Foundation, Karolinska Institutet, and the Stockholm City Council for financial support.
Materials
| Silicone catheter 10-French | Preparing the animal for surgery , Section 1 | ||
| DMEM 10X | Gibco | 31885-023 | Plastic compression section 4 |
| 24 well plates | Falcon | 08-772-1 | Plastic compression section 4 |
| 3'3,'5-Triiodothyronine | Sigma-Aldrich | IRMM469 | In vitro culture; Section 5 |
| 4% PFA | Labmed Solutions | 200-001-8 | Immunocytochemistry; Section 6 |
| 70% ethanol | Histolab | Immunocytochemistry; Section 6 | |
| ABC Elite kit: Biotin -Streptavidin detection kit | Vector | PK6102 | Immunocytochemistry; Section 6 |
| Absolute ethanol | Histolab | 1399.01 | Immunocytochemistry; Section 6 |
| Adenine | Sigma-Aldrich | A8626 | In vitro culture; Section 5 |
| Atropine 25 μg/kg | Temgesic, RB Pharmaceuticals, Great Britain | Preparing the animal for surgery , Section 1 | |
| Azaperone 2 mg/kg | Stresnil, Janssen-Cilag, Pharma, Austria | Preparing the animal for surgery , Section 1 | |
| Biosafety Level 2 hood | Plastic compression; Section 4 | ||
| Blocking solution: Normal serum from the same species as the secondary secondary antibody was generated in. | Vector | The blocking solution depends of the origin of first antibody | Immunocytochemistry; Section 6 |
| Buprenorphine 45 μg/kg | Atropin, Mylan Inc, Canonsburg, PA | Preparing the animal for surgery , Section 1 | |
| Carprofen 3 mg/kg | Rimadyl, Orion Pharma, Sweden | Preparing the animal for surgery , Section 1 | |
| Chlorhexidine gluconate | Hibiscrub 40 mg/mL, Regent Medical, England | Preparing the animal for surgery , Section 1 | |
| Cholera toxin | Sigma-Aldrich | C8052 | In vitro culture; Section 5 |
| Coplin jar: staining jar for boiling | Histolab | 6150 | Immunocytochemistry; Section 6 |
| Stainless mold (33x22x10 mm) custom made | Plastic compression; Section 4 | ||
| DMEM | Gibco | 3188-5023 | Plastic compression section 4. Keep on ice when using it in plastic compression |
| Epidermal growth factor | Sigma-Aldrich | E9644 | In vitro culture; Section 5 |
| Ethilon (non-absorbable monofilament for skin sutures) | Ethicon | Surgery, Section 1 | |
| Fetal bovine serum (FBS) | Gibco | 10437-036 | Plastic compression section 4 |
| Forceps (Adison with tooth) | Preparing the animal for surgery , Section 1 | ||
| Gauze (Gazin Mullkompresse) | Preparing the animal for surgery , Section 1 | ||
| Ham´s F12 | Gibco | 31765-027 | Plastic compression section 4 |
| Hematoxylin | Histolab | 1820 | Immunocytochemistry; Section 6 |
| Humidity chamber | DALAB | Immunocytochemistry; Section 6 | |
| Hydrocortisone | Sigma-Aldrich | H0888 | In vitro culture; Section 5 |
| Hydrogen peroxide Solution 30% | Sigma-Aldrich | H1009 | Immunocytochemistry; Section 6 |
| Insulin | Sigma-Aldrich | I3536 | In vitro culture; Section 5 |
| Isoflurane | Isoflurane, Baxter, Deerfield, IL | Preparing the animal for surgery , Section 1 | |
| Lidocaine 5 mg/ml | Xylocaine, AstraZeneca, Sweden | Preparing the animal for surgery , Section 1 | |
| Lucose 25 mg/mL | Baxter, Deerfield, IL | Preparing the animal for surgery , Section 1 | |
| Marker pen pap pen | Sigma-Aldrich | Z377821-1EA | Immunocytochemistry; Section 6 |
| Medetomidine 25 μg/kg | Domitor, Orion Pharma, Sweden | Preparing the animal for surgery , Section 1 | |
| Mincing device | Applied Tissue Technologies LLC | Minced tissue preparation, section 2 | |
| Monocryl (absorbable monofilament) | Ethicon | Surgery, Section 1 | |
| NaCl | Sigma-Aldrich | S7653 | Immunocytochemistry; Section 6 |
| NaOH 1N | Merck Millipore | 106462 | Plastic compression section 4 and cell culture |
| Nylon mesh, 110 uM thick pore size 0.04 sqmm | Plastic compression; Section 4 | ||
| Oculentum simplex APL: ointment for eye protection | APL | Vnr 336164 | Surgery, Section 1 |
| PBS | Gibco | 14190-094 | Plastic compression section 4 |
| Penicillin-Streptomycin | Gibco | 15140-122 | Plastic compression section 4 |
| Phenobarbiturate 15 mg/kg | Pentobarbital, APL, Sweden | Preparing the animal for surgery , Section 1 | |
| PLGA Knitted fabric | Plastic compression; Section 4 | ||
| Rat-tail collagen | First LINK, Ltd, UK | 60-30-810 | Plastic compression section 4, keep on ice |
| Scalpel blade – 15 | Preparing the animal for surgery , Section 1 | ||
| Shaving shears | Preparing the animal for surgery , Section 1 | ||
| Stainless stell mesh, 400 uM thick pore size | Plastic compression; Section 4 | ||
| Steril gloves | Preparing the animal for surgery , Section 1 | ||
| Sterile gowns | Preparing the animal for surgery , Section 1 | ||
| Sterile drapes | |||
| Sterilium | Bode Chemie HAMBURG | Preparing the animal for surgery , Section 1 | |
| Suture Thread Ethilon | Preparing the animal for surgery , Section 1 | ||
| TE-solution (antigen unmasking solution) consist of 10 mM Tris and 1 mM EDTA, pH 9.0 | 10 mM Tris/1 mM EDTA, adjust pH to 9.0 | ||
| Tiletamine hypochloride 2,5 mg/kg | Preparing the animal for surgery , Section 1 | ||
| Transferrin | Sigma-Aldrich | T8158 | In vitro culture; Section 5 |
| Trizma Base, H2NC | Sigma-Aldrich | T6066 | Immunocytochemistry; Section 6 |
| Vector VIP kit: Enzyme peroxidase substrate kit | Vector | SK4600 | Immunocytochemistry; Section 6 |
| Vicryl (absorbable braded) | Ethicon | Surgery, Section 1 | |
| Tris buffer pH 7.6 (washing buffer) | TE solution: Make 10X (0,5M Tris, 1,5M NaCl) by mixing: 60,6 g Tris (Trizma Base, H2NC(CH2OH)3, M=121.14 g/mol), add 800 ml distilled water adjust the pH till 7.6, add 87,7 g NaCl and fill to 1000 ml with distilled water. Dilute to 1X with distilled water. | ||
| X-tra solv (solvent) | DALAB | 41-5213-810 | Immunocytochemistry; Section 6. Use under fume hood |
| Zolazepam hypochloride | Zoletil, Virbac, France | Preparing the animal for surgery , Section 1 | |
| Depilatory wax strips | Veet | Preparing the animal for surgery , Section 1 | |
| Pentobarbital sodium | Lundbeck | Termination, Section 3 |
References
- Rheinwald, J. G., Green, H. Serial cultivation of strains of human epidermal keratinocytes: the formation of keratinizing colonies from single cells. Cell. 6, 331-343 (1975).
- Fossum, M., Nordenskjold, A., Kratz, G. Engineering of multilayered urinary tissue in vitro. Tissue Engineering. 10, 175-180 (2004).
- Salmikangas, P., et al. Manufacturing, characterization and control of cell-based medicinal products: challenging paradigms toward commercial use. Regen Med. 10, 65-78 (2015).
- Fossum, M., et al. Minced skin for tissue engineering of epithelialized subcutaneous tunnels. Tissue Engineering. Part A. 15, 2085-2092 (2009).
- Fossum, M., et al. Minced urothelium to create epithelialized subcutaneous conduits. The Journal of Urology. 184, 757-761 (2010).
- Reinfeldt Engberg, G., Lundberg, J., Chamorro, C. L., Nordenskjold, A., Fossum, M. Transplantation of autologous minced bladder mucosa for a one-step reconstruction of a tissue engineered bladder conduit. BioMed Research International. 2013, 212734 (2013).
- Meek, C. P. Successful microdermagrafting using the Meek-Wall microdermatome. Am J Surg. 96, 557-558 (1958).
- Tanner, J. C., Vandeput, J., Olley, J. F. The Mesh skin graft. Plastic and Reconstructive Surgery. 34, 287-292 (1964).
- Svensjo, T., et al. Autologous skin transplantation: comparison of minced skin to other techniques. The Journal of Surgical Research. 103, 19-29 (2002).
- Ajalloueian, F., Zeiai, S., Rojas, R., Fossum, M., Hilborn, J. One-stage tissue engineering of bladder wall patches for an easy-to-use approach at the surgical table. Tissue Engineering. Part C, Methods. 19, 688-696 (2013).
- Engelhardt, E. M., et al. A collagen-poly(lactic acid-co-varepsilon-caprolactone) hybrid scaffold for bladder tissue regeneration. Biomaterials. 32, 3969-3976 (2011).
- Brown, R. A., Wiseman, M., Chuo, C. B., Cheema, U., Nazhat, S. N. Ultrarapid engineering of biomimetic materials and tissues: fabrication of nano- and microstructures by plastic compression. Adv Funct Mater. 15, 1762-1770 (2005).
- Fumagalli Romario, U., Puccetti, F., Elmore, U., Massaron, S., Rosati, R. Self-gripping mesh versus staple fixation in laparoscopic inguinal hernia repair: a prospective comparison. Surg Endosc. 27, 1798-1802 (2013).
- Muangman, P., et al. Complex Wound Management Utilizing an Artificial Dermal Matrix. Annals of Plastic Surgery. 57, 199-202 (2006).
- Ajalloueian, F., Zeiai, S., Fossum, M., Hilborn, J. G. Constructs of electrospun PLGA, compressed collagen and minced urothelium for minimally manipulated autologous bladder tissue expansion. Biomaterials. 35, 5741-5748 (2014).
- Orabi, H., AbouShwareb, T., Zhang, Y., Yoo, J. J., Atala, A. Cell-seeded tubularized scaffolds for reconstruction of long urethral defects: a preclinical study. Eur Urol. 63, 531-538 (2013).
- Blais, M., Parenteau-Bareil, R., Cadau, S., Berthod, F. Concise review: tissue-engineered skin and nerve regeneration in burn treatment. Stem Cells Transl Med. 2, 545-551 (2013).
- Serpooshan, V., Muja, N., Marelli, B., Nazhat, S. N. Fibroblast contractility and growth in plastic compressed collagen gel scaffolds with microstructures correlated with hydraulic permeability. J Biomed Mater Res A. 96, 609-620 (2011).

