Ljusdriven Enzymatisk Dekarboxylering
Summary
Vi beskriver ett protokoll för ljuskatalyserade generation av väteperoxid – en kofaktor för oxidativa omvandlingar.
Abstract
Oxidoreduktaser tillhör de mest tillämpade industriella enzymer. Ändå måste de externa elektroner vars försörjning är ofta kostsamt och utmanande. Återvinning av den elektrondonatorer NADH eller NADPH kräver användning av ytterligare enzymer och offersubstrat. Intressant, flera oxidoreduktaser accepterar väteperoxid som elektrondonator. Samtidigt som den är billig, reducerar denna reagens ofta stabiliteten hos enzymer. En lösning på detta problem är in situ-genereringen av kofaktorn. Den kontinuerliga tillförseln av kofaktorn vid låg koncentration driver reaktionen utan att försämra enzymstabilitet. Detta papper demonstrerar en metod för den ljuskatalyse alstring in situ av väteperoxid med exemplet av heme-beroende fettsyra dekarboxylas olet JE. Fettsyra dekarboxylas olet JE upptäcktes på grund av sin unika förmåga att producera långkedjiga 1-alkener från fettsyror, en hittills okänd enzymatiskreaktion. 1-alkener används allmänt tillsatser för mjukningsmedel och smörjmedel. Olet JE har visat att acceptera elektroner från väteperoxid för oxidativ dekarboxylering. Medan tillsats av väteperoxid skadar enzymet och resulterar i låga utbyten, alstring in situ av kofaktorn kringgår detta problem. Den photobiocatalytic systemet visar tydliga fördelar vad gäller enzymaktivitet och utbyte, vilket resulterar i ett enkelt och effektivt system för fettsyra dekarboxylering.
Introduction
Klimatförändringen och överskådlig utarmning av förnybara resurser utgör ett allvarligt hot mot vårt samhälle. I detta sammanhang representerar enzymkatalys en ännu inte utnyttjas fullt ut potential för utveckling av hållbar och "grönare" kemi 1. Oxidoreduktaser har förmågan att katalysera införande och ändring av funktionella grupper under milda reaktionsbetingelser och tillhör de viktigaste biokatalysatorer 2. Flesta redox transformationer kräver tillförseln av externt av kofaktorer såsom NAD (P) H. Metoder för kofaktor regenerering har använts i industriell skala. Men de fortfarande resultera i höga processkostnader, vilket begränsar deras tillämpning främst till högvärdiga produkter. Intressant nog flera peroxidaser 3,4 och P450 monooxygenases 5 acceptera elektroner från väteperoxid via den så kallade peroxid shunten. Medan H2O 2 är en billig samreagens, är det enligt uppgift harmful för många enzymer. En stadig in situ-bildning av låga koncentrationer av väteperoxid är en framkomlig väg för att driva reaktionen utan att försämra den operativa stabiliteten hos enzymet.
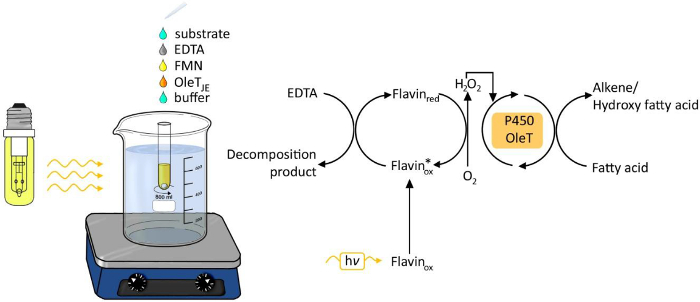
Figur 1. Experimentell uppställning av photobiocatalytic dekarboxylering av fettsyror genom olet JE. Klicka här för att se en större version av denna siffra.
Användningen av ljus som energikälla för kemiska och biologiska processer har fått ökad uppmärksamhet under de senaste åren 6. Ljusdriven generation av väteperoxid har visat sig vara en enkel och robust metod för att tillföra väteperoxid för redox transformationer (Figur 1). En fotokatalysator såsom flavin-adenin-månonucleotide (FMN) möjliggör reduktion av molekylärt syre till väteperoxid, som sedan används som kofaktor för den enzymatiska oxyfunctionalization reaktionen. Möjliga elektrondonatorer är etylendiamintetraättiksyra (EDTA), askorbat eller den billiga formiat. Metoden är allmänt tillämpbar för H2O 2 -beroende enzymer, inklusive peroxidaser 3,4 och P450 monooxygenases 5.
Vi har nyligen undersökt tillämpningen av en ny bakterie dekarboxylas 7 för omvandling av naturliga fetter i olefiner 8. Detta skulle vara en hållbar väg för syntes av vanligt förekommande plattformskemikalier från en biobaserad källa. Dekarboxylas olet JE från den grampositiva bakterien Jeotgalicoccus sp. katalyserar den oxidativa dekarboxyleringen av fettsyror och bildar 1-alkener som produkter. Olet JE är nära besläktad med bakteriella P450 monooxygenases och behöver elektroner from väteperoxid för reaktionen.
Tyvärr, tillsats av H2O 2 till en lösning av substrat och enzym resulterade i låga omvandlingar och en dålig reproducerbarhet av resultaten, förmodligen på grund av en skadlig effekt av väteperoxid på stabiliteten hos olet JE. Generering av ett fusionsprotein med NADPH-reduktas RhFred gjort en NADPH-beroende dekarboxylering möjlig. 9 Trots det höga priset på NADPH och den nuvarande begränsade möjligheter till en kostnadseffektiv regenerering fick oss att undersöka billigare elektrondonatorer. Inspirerad av likheten mellan olet JE med P450 monooxygenases använde vi den ljuskatalyserade generation H2O 2. Vi var glada att få höga omvandlingar (upp till> 95%) med hjälp av cellfria extrakt eller renade enzymlösningar.
Med exempel på fettsyra dekarboxylering, presenterar vi en allmän protokoll för ljusdrivna enzymATIC redox transformationer använder FMN som fotokatalysator och väteperoxid som kofaktor. De presenterade metoder innefattar produktionen av enzymet i rekombinant cell av E. coli, rening av enzymet, ansökan för syntes av 1-alkener och analys av reaktionsprodukterna.
Protocol
Representative Results
Discussion
Ljusdriven generation av väteperoxid kan användas för en rad redox transformationer, inklusive peroxygenases 3, chloroperoxidases 10 och P450 monooxygenases 5. Det är ett enkelt och praktiskt tillvägagångssätt. På lång sikt, användning av synligt ljus öppnar perspektivet att utnyttja solljus under kemiska transformationer, som är ett hållbart alternativ för energirika reaktioner.
Metoden kan användas med renat enzym eller med cellfritt extrakt. Medan den senare kräver mindre kostnader och arbete, bör det noteras att små molekyler i råextraktet kan störa ljuset katalyserade omvandlingen. En praktiskt tillvägagångssätt är att ta bort dessa små komponenter med en mikromembran (dvs genom centrifugering i en centrifugal filterenhet eller genom dialys). Koncentrationen av det ljus-skörd molekyl FMN bestämmer koncentrationen av väteperoxiden. Beroende på Affinity av oxidoreduktas, är denna koncentration avgörande för den enzymatiska aktiviteten. En annan viktig faktor är koncentrationen av offerelektrondonator EDTA. Den viktigaste parametern är emellertid den operativa stabiliteten och aktiviteten av enzymet.
Den olefinization av fettsyror är en elegant reaktion för omvandling av biobaserade fettsyror i olefiner som hör till de stora råvaror för kemisk industri. Ljusdriven biokatalytisk dekarboxylering kan utföras vid rumstemperatur och vid neutralt pH, vilket ger tydliga fördelar när det gäller hållbarhet.
Våra resultat visar att in situ-alstring av väteperoxid är en strategi för att tillföra kofaktorn utan att försämra enzymstabilitet, vilket leder till en hög omvandling. Nuvarande metoder för kofaktor regenerering använda jordbruksprodukter eller bensinbaserade kemikalier. Ljusdriven reaktioner framstår som förnybart alternativ. Framtidaforskning kommer att ägnas åt metoder för substitution av offerreagens EDTA av billigare molekyler och för att minska mängden av ljus skörd molekyl FMN.
Divulgations
The authors have nothing to disclose.
Acknowledgements
R.K. and F.H. are grateful for the EU-commision for financial support within the Marie-Sklodowska ITN Biocascades (Nr. 634200).
Materials
| Chemicals | |||
| Ampicillin | Sigma Aldrich | 69-52-3 | |
| Bradford reagent | Roth | K015.1 | |
| BSA | Sigma Aldrich | 90604-29-8 | |
| DMSO | Sigma Aldrich | 67-68-5 | |
| Ethyl acetate | Fisher Chemical | 141-78-6 | |
| Ethylenediaminetetraacetic acid (EDTA) | Roth | 8043.1 | |
| Riboflavin 5-monophosphate sodium salt hydrate | Sigma Aldrich | 130-40-5 | |
| Hydrochlorid acid 37% | Sigma Aldrich | 7647-01-0 | |
| Hydrogen peroxide 30% | Sigma Aldrich | 7722-84-1 | |
| δ-Amino levulinic acid | Sigma Aldrich | 5451-09-2 | |
| N-Methyl-N-(Trimethylsilyl)trifluoro acetamide (MSTFA) | Sigma Aldrich | 24589-78-4 | |
| Myristic acid >99% | Sigma Aldrich | 208-875-2 | |
| Imidazole | Sigma Aldrich | 288-32-4 | |
| Sodium chloride | Fisher Chemical | 7647-14-5 | |
| Stearic acid >99% | Sigma Aldrich | 57-11-4 | |
| Tetracycline | Sigma Aldrich | 60-54-8 | |
| Tergitol | Sigma Aldrich | MFCD01779855 | |
| Tris(hydroxymethyl)-aminomethan | Sigma Aldrich | 77-86-1 | |
| Name | Company | Catalog Number | Comments |
| Device | |||
| Incubator shaker | G-25CK | New Brunswick Scientific | |
| Ecotron | Infors HT | ||
| Centrifugation | Labofuge 400R | Heraeus | |
| RC 5B Plus | Sorvall | ||
| Fresco 17 | Thermo Scientific | ||
| Centrifugation rotors | SS34 | Sorvall | |
| SLA | Sorvall | ||
| Clean bench | Envirco | Ceag Schirp Reinraum technik | |
| Column GC-FID | CP-Sil 5CB (30 m x 0.25 mmx 0.25 µm) | Agilent Technologies | |
| Column GC-MS | FactorFour Capillary Coloumn (VF-5 ms + 5 m EZ Guard) | Varian | |
| GC-FID | GC-2010 plus | Shimadzu | |
| GC-MS | IST-40 | Varian | |
| Magnetic stirrer | RCT classic | IKA | |
| pH meter | SevenEasy | Mettler toledo | |
| Sonicator | Branson Sonifier 250 | Branson | |
| Spectral photometer | FLUOstar Omega | BMG Labtech | |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Affinity chromatography column | His Pur Ni-NTA spin column | Thermo Scientific | |
| Centricon | Vivaspin turbo 15 | VWR International | |
| Microtiter plates | 96 Well Multiply®PCR Plates | Sarstedt |
References
- Kourist, R., Domìnguez de Marìa, P., Miyamoto, K. Biocatalytic strategies for the asymmetric synthesis of profens – recent trends and developments. Green Chem. , 2607-2618 (2011).
- Holtmann, D., Fraaije, M. W., Arends, I. W., Opperman, D. J., Hollmann, F. The taming of oxygen: biocatalytic oxyfunctionalisations. Chemical Comm. 50, 13180-13200 (2014).
- Churakova, E., et al. Specific photobiocatalytic oxyfunctionalization reactions. Ang. Chem. In. Ed. 123, 10904-10907 (2011).
- Hollmann, F., Arends, I., Buehler, K. Biocatalytic Redox Reactions for Organic Synthesis: Nonconventional Regeneration Methods. ChemCatChem. 2, 762-782 (2010).
- Girhard, M., Kunigk, E., Tihovsky, S., Shumyantseva, V. V., Urlacher, V. B. Light-driven biocatalysis with cytochrome P450 peroxygenases. Biotechnol. Appl. Biochem. 60, 111-118 (2013).
- Bartsch, M., et al. Photosynthetic production of enantioselective biocatalysts. Microb. Cell. Fact. 14, 53 (2015).
- Rude, M. A., et al. Terminal olefin (1-alkene) biosynthesis by a novel P450 fatty acid decarboxylase from Jeotgalicoccus species. Appl. Environ. Microbiol. 77, 1718-1727 (2011).
- Zachos, I., et al. Photobiocatalytic decarboxylation for olefin synthesis. Chem. Comm. 51, 1918-1921 (2015).
- Liu, Y., et al. Hydrogen peroxide-independent production of α-alkenes by OleTJE P450 fatty acid decarboxylase. Biotechnol. Biofuels. 7, 28 (2014).
- Perez, D. I., Grau, M. M., Arends, I. W., Hollmann, F. Visible light-driven and chloroperoxidase-catalyzed oxygenation reactions. Chem. Comm. 40 (44), 6848-6850 (2009).

