Ontwikkeling en onderhoud van een preklinisch Patient Afgeleid Tumor xenograft model voor onderzoek naar nieuwe anti-Cancer Therapies
Summary
Gebruik makend van de patiënt afgeleide tumoren in een subcutane preklinisch model is een uitstekende manier om de effectiviteit van nieuwe therapieën, voorspellende ontdekking van biomarkers, en resistente paden te bestuderen. Dit model, in de ontwikkeling van geneesmiddelen, is essentieel voor het bepalen van het lot van vele nieuwe anti-kankerbehandelingen voorafgaand aan klinisch onderzoek.
Abstract
Patient derived tumor xenograft (PDTX) models provide a necessary platform in facilitating anti-cancer drug development prior to human trials. Human tumor pieces are injected subcutaneously into athymic nude mice (immunocompromised, T cell deficient) to create a bank of tumors and subsequently are passaged into different generations of mice in order to maintain these tumors from patients. Importantly, cellular heterogeneity of the original tumor is closely emulated in this model, which provides a more clinically relevant model for evaluation of drug efficacy studies (single agent and combination), biomarker analysis, resistant pathways and cancer stem cell biology. Some limitations of the PDTX model include the replacement of the human stroma with mouse stroma after the first generation in mice, inability to investigate treatment effects on metastasis due to the subcutaneous injections of the tumors, and the lack of evaluation of immunotherapies due to the use of immunocompromised mice. However, even with these limitations, the PDTX model provides a powerful preclinical platform in the drug discovery process.
Introduction
Colorectale kanker (CRC) is een belangrijke bijdrage aan kanker sterfgevallen in de Verenigde Staten. In 2015 waren er naar schatting 132.700 nieuwe gevallen van CRC met 49.700 sterfgevallen 1. Hoewel de prognose bij patiënten met gelokaliseerde ziekte is uitstekend, patiënten met gevorderde ziekte slechte resultaten, waardoor dit een hoge prioriteit bij de ontwikkeling van nieuwe therapieën. Ondanks de kwaliteit van de zorg chemotherapeutische behandelingen en nieuwere biologics die worden ingezet tegen deze ziekte, is er slechts een stapsgewijze toename van de totale overleving. Dienovereenkomstig is er een aanzienlijke inspanning in het begrijpen van de bestuurder die betrokken zijn bij het vergemakkelijken van tumorgroei bij deze ziekte. De Cancer Genome Atlas Network heeft onlangs veel belangrijke routes die zijn betrokken bij CRC ontregeling en omvatten: WNT, phosphoinositide 3-kinase (PI3K), RAS, transforming growth factor-β (TGF-β) en TP53 2. Samen met onderzoeken beschrijven othaar routes die de groei versterken in CRC hebben de ontwikkeling van de nieuwere therapieën die gericht zijn op een aanzienlijke verbetering van de overlevingskansen in deze patiëntenpopulatie 3-5 ontstoken. Gebruik makend van preklinische modellen in de oncologie de ontwikkeling van geneesmiddelen zijn van essentieel belang geweest in dit proces in het voorspellen van de klinische activiteit van deze nieuwe verbindingen.
Diverse preklinische modellen zijn gebruikt bij de ontwikkeling van geneesmiddelen. Aangezien preklinische transgene diermodellen en geïmmortaliseerde cellijnen niet succesvol bij het bepalen van de klinische activiteit van nieuwe kanker therapieën geweest, voornamelijk omdat het niet mogelijk om de complexiteit van menselijke tumoren tijdens zijn patiënt afgeleide tumor xenograft (PDTX) modellen opgezet. Het grootste voordeel van dit model is dat de tumor heterogeniteit intact blijft en sluit nauw aan bij de moleculaire kenmerken en clonaliteit van de oorspronkelijke tumor patiënt 6-9. PDTX modellen bieden een uitstekende in vivopreklinische platform om nieuwe agenten, resistentie tegen geneesmiddelen paden, combinatorische strategieën en kanker stamcel biologie 10 bestuderen.
Een algemeen overzicht van de PDTX werkwijze wordt geïllustreerd in figuur 1. Het begint in de kliniek, instemmende patiënten deel van hun overcapaciteit tumorweefsel worden gebruikt voor dit onderzoek toe. Vervolgens, in de spreekkamer van een stuk van de tumor wordt geëxtrapoleerd door een patholoog en in te transporteren media te onderzoekspersoneel. Direct daarna een deel van de tumor wordt in kleine stukjes gesneden en getransplanteerd in immunodeficiënte muizen subcutaan. Zodra de tumor groeit wordt doorgekweekt in verschillende generaties muizen om de tumor 10 te handhaven. Gewoonlijk nadat de F3 generatie de tumor kan worden uitgebreid tot een behandelingsstudie waarbij nieuwe verbindingen en / of combinatorische therapieën worden geëvalueerd. Gebruik makend van Next Gen Seq (exome Seq, RNA Seq en SNP array) potentieel predictieve biomarkers zijn ontdekted die helpen bij de selectie van patiënten die voordeel kunnen halen uit een bepaalde behandeling.
De overkoepelende doelstellingen van het gebruik van PDTX modellen zijn: 1) een evaluatie van de effectiviteit van nieuwe therapieën als monotherapie of in combinatie en 2) het identificeren van voorspellende biomarkers voor de gevoeligheid of weerstand voorafgaand aan klinisch onderzoek. In dit manuscript, bieden wij de methodologie bij het initiëren en onderhouden van een CRC PDTX bank en bieden de voordelen en beperkingen van dit model in de ontwikkeling van geneesmiddelen ontdekking.
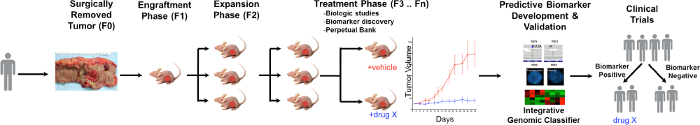
Figuur 1. Overzicht van de CRC PDTX Model Protocol. Een patiënt afgeleid tumor wordt ontvangen van operatie en direct geïnjecteerd in athymische naakt muizen subcutaan. Zodra de tumor groeit het wordt uitgebreid naar de volgende generaties en uiteindelijk uitgebreid voor de behandeling studies. behandeling Responses worden beoordeeld en predictieve biomarkers zijn geïdentificeerd die kunnen helpen bij de selectie van patiënten. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
De PDTX drug discovery platform biedt een verbeterd model om de tekortkomingen van andere preklinische modellen die onbetrouwbaar voorspellen van de klinische activiteit van nieuwe verbindingen. Belangrijk is dat tumoren in dit model zijn biologisch stabiel, behouden metastatische potentieel, en vertonen vergelijkbare drug responsiviteit van generatie op generatie. In dit model worden afgeleid patiënt tumoren geïnjecteerd in athymische naakt muizen gepasseerd en vervolgens gebruikt in therapeutische evalueren. Er zijn…
Divulgations
The authors have nothing to disclose.
Acknowledgements
This work was supported by grant 1R01CA152303-01.
Materials
| RPMI or DMEM | Corning | 10-040-CV | |
| Penicillin-Streptomycin | Corning | 30-002-CI | |
| Non-essential Amino Acids | Corning | 25-025-CI | |
| Fetal Bovine Serum | Corning | 35-010-CV | Thaw in -4 °C, then activate for 30 minutes at 60 °C water bath |
| CPT blood tube | BD vacutainer | 362761 | |
| Microcentrifuge tube | Surelock | A-7002 | |
| Phospate-Buffered Saline | Corning | 21-040-CV | |
| Cyrogenic vials | Cyroking | C0732901 | |
| Plastic tumor cutting dish | Trueline | TR4001 | |
| Scissors | Roboz | RS-5881 | |
| Forceps | Roboz | RS-5135 | |
| Matrigel (gelatinous protein mixture) | Corning | 354234 | Store at -20 or -80 °C, then thaw on ice, do not leave at room temperature |
| 10% Formalin cups | Protocol | 032-059 | |
| Liquid Nitrogen Dewar Storage | Thermolyne | CY50900 | |
| Portable liquid nitrogen dewar | Nalgene | 4150-2000 | |
| Dimethyl Sulfoxide | Fischer | 67-68-5 | |
| Freezing container: Mr Frosty | Nalgene | 5100-0001 | |
| Isopropyl Alcohol | Decon | 64-17-5 | |
| Trocars | Innovative Research of America | MP-182 | |
| Anesthesia machine | Patterson Veterinary | none | |
| Anesthesia box | Patterson Veterinary | none | |
| Isoflurane | Vet one | 1038005 | |
| F-Air Canister | Bickford Omnicon | 80120 | |
| Meloxicam | Vet one | 5182-90C | |
| Calipers | Fowler | 54-100-167 | |
| Weight scale | Ohaus | Scout Pro SP601 |
References
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics. 2015. CA Cancer J Clin. 65 (1), 5-29 (2015).
- . Comprehensive molecular characterization of human colon and rectal cancer. Nature. 487 (7407), 330-337 (2012).
- Arcaroli, J. J., et al. Tumours with elevated levels of the Notch and Wnt pathways exhibit efficacy to PF-03084014, a gamma-secretase inhibitor, in a preclinical colorectal explant model. Br J Cancer. 109 (3), 667-675 (2013).
- Hubbard, J., Grothey, A. Antiangiogenesis agents in colorectal cancer. Curr Opin Oncol. 22 (4), 374-380 (2010).
- van Es, J. H., et al. Notch/gamma-secretase inhibition turns proliferative cells in intestinal crypts and adenomas into goblet cells. Nature. 435 (7044), 959-963 (2005).
- Cassidy, J. W., Caldas, C., Bruna, A. Maintaining Tumor Heterogeneity in Patient-Derived Tumor Xenografts. Cancer Res. 75 (15), 2963-2968 (2015).
- Jin, K., et al. Patient-derived human tumour tissue xenografts in immunodeficient mice: a systematic review. Clin Transl Oncol. 12 (7), 473-480 (2010).
- Julien, S., et al. Characterization of a large panel of patient-derived tumor xenografts representing the clinical heterogeneity of human colorectal cancer. Clin Cancer Res. 18 (19), 5314-5328 (2012).
- Siolas, D., Hannon, G. J. Patient-derived tumor xenografts: transforming clinical samples into mouse models. Cancer Res. 73 (17), 5315-5319 (2013).
- Tentler, J. J., et al. Patient-derived tumour xenografts as models for oncology drug development. Nat Rev Clin Oncol. 9 (6), 338-350 (2012).
- Carson, F. L. . Histotechnology: A Self-Assessment Workbook. , (1996).
- Arcaroli, J. J., et al. Common PIK3CA mutants and a novel 3′ UTR mutation are associated with increased sensitivity to saracatinib. Clin Cancer Res. 18 (9), 2704-2714 (2012).
- Arcaroli, J. J., et al. A NOTCH1 gene copy number gain is a prognostic indicator of worse survival and a predictive biomarker to a Notch1 targeting antibody in colorectal cancer. Int J Cancer. 138 (1), 195-205 (2016).
- Arcaroli, J. J., et al. Gene array and fluorescence in situ hybridization biomarkers of activity of saracatinib (AZD0530), a Src inhibitor, in a preclinical model of colorectal cancer. Clin Cancer Res. 16 (16), 4165-4177 (2010).
- Lieu, C. H., et al. Antitumor activity of a potent MEK inhibitor, TAK-733, against colorectal cancer cell lines and patient derived xenografts. Oncotarget. 6 (33), 34561-34572 (2015).
- Pitts, T. M., et al. Association of the epithelial-to-mesenchymal transition phenotype with responsiveness to the p21-activated kinase inhibitor, PF-3758309, in colon cancer models. Front Pharmacol. 4, 35 (2013).
- Song, E. K., et al. Potent antitumor activity of cabozantinib, a c-MET and VEGFR2 inhibitor, in a colorectal cancer patient-derived tumor explant model. Int J Cancer. 136 (8), 1967-1975 (2015).
- Tentler, J. J., et al. Identification of predictive markers of response to the MEK1/2 inhibitor selumetinib (AZD6244) in K-ras-mutated colorectal cancer. Mol Cancer Ther. 9 (12), 3351-3362 (2010).
- Bardelli, A., et al. Amplification of the MET receptor drives resistance to anti-EGFR therapies in colorectal cancer. Cancer Discov. 3 (6), 658-673 (2013).
- Bertotti, A., et al. A molecularly annotated platform of patient-derived xenografts (“xenopatients”) identifies HER2 as an effective therapeutic target in cetuximab-resistant colorectal cancer. Cancer Discov. 1 (6), 508-523 (2011).
- Davis, S. L., et al. Combined inhibition of MEK and Aurora A kinase in KRAS/PIK3CA double-mutant colorectal cancer models. Front Pharmacol. 6, 120 (2015).
- Morelli, M. P., et al. Preclinical activity of the rational combination of selumetinib (AZD6244) in combination with vorinostat in KRAS-mutant colorectal cancer models. Clin Cancer Res. 18 (4), 1051-1062 (2012).
- Pitts, T. M., et al. Dual pharmacological targeting of the MAP kinase and PI3K/mTOR pathway in preclinical models of colorectal cancer. PLoS One. 9 (11), e113037 (2014).
- Spreafico, A., et al. Rational combination of a MEK inhibitor, selumetinib, and the Wnt/calcium pathway modulator, cyclosporin A, in preclinical models of colorectal cancer. Clin Cancer Res. 19 (15), 4149-4162 (2013).
- Arcaroli, J. J., et al. ALDH+ tumor-initiating cells exhibiting gain in NOTCH1 gene copy number have enhanced regrowth sensitivity to a gamma-secretase inhibitor and irinotecan in colorectal cancer. Mol Oncol. 6 (3), 370-381 (2012).
- Hoey, T., et al. DLL4 blockade inhibits tumor growth and reduces tumor-initiating cell frequency. Cell Stem Cell. 5 (2), 168-177 (2009).
- Ikebuchi, F., et al. Dissociation of c-Met phosphotyrosine sites in human cells in response to mouse hepatocyte growth factor but not human hepatocyte growth factor: the possible roles of different amino acids in different species. Cell Biochem Funct. 31 (4), 298-304 (2013).
- Zhang, Y. W., et al. Enhanced growth of human met-expressing xenografts in a new strain of immunocompromised mice transgenic for human hepatocyte growth factor/scatter factor. Oncogene. 24 (1), 101-106 (2005).

