治療用途のためのツールとしてのRGD官能ヒドロゲルの合成
Summary
We present a protocol for the synthesis of RGD-functionalized hydrogels as devices for cell and drug delivery. The procedure involves copper catalyzed alkyne-azide cycloaddition (CuAAC) between alkyne-modified polyacrylic acid (PAA) and a RGD-azide derivative. The hydrogels are formed using microwave-assisted polycondensation and their physicochemical properties are investigated.
Abstract
The use of polymers as biomaterials has provided significant advantages in therapeutic applications. In particular, the possibility to modify and functionalize polymer chains with compounds that are able to improve biocompatibility, mechanical properties, or cell viability allows the design of novel materials to meet new challenges in the biomedical field. With the polymer functionalization strategies, click chemistry is a powerful tool to improve cell-compatibility and drug delivery properties of polymeric devices. Similarly, the fundamental need of biomedicine to use sterile tools to avoid potential adverse-side effects, such as toxicity or contamination of the biological environment, gives rise to increasing interest in the microwave-assisted strategy.
The combination of click chemistry and the microwave-assisted method is suitable to produce biocompatible hydrogels with desired functionalities and improved performances in biomedical applications. This work aims to synthesize RGD-functionalized hydrogels. RGD (arginylglycylaspartic acid) is a tripeptide that can mimic cell adhesion proteins and bind to cell-surface receptors, creating a hospitable microenvironment for cells within the 3D polymeric network of the hydrogels. RGD functionalization occurs through Huisgen 1,3-dipolar cycloaddition. Some PAA carboxyl groups are modified with an alkyne moiety, whereas RGD is functionalized with azido acid as the terminal residue of the peptide sequence. Finally, both products are used in a copper catalyzed click reaction to permanently link the peptide to PAA. This modified polymer is used with carbomer, agarose and polyethylene glycol (PEG) to synthesize a hydrogel matrix. The 3D structure is formed due to an esterification reaction involving carboxyl groups from PAA and carbomer and hydroxyl groups from agarose and PEG through microwave-assisted polycondensation. The efficiency of the gelation mechanism ensures a high degree of RGD functionalization. In addition, the procedure to load therapeutic compounds or biological tools within this functionalized network is very simple and reproducible.
Introduction
ヒドロゲルは天然または合成された親水性架橋ポリマーで形成された三次元ネットワークであり、独特の三次元構造によって特徴付けられます。これらのデバイスは、薬物送達、組織工学、遺伝子キャリアとスマート・センサ1,2の生物医学分野でますます魅力的です。実際、その高い水含有量、ならびにそれらのレオロジーおよび機械的性質は、それらの適切な候補が軟組織微小環境を模倣し、水溶性のサイトカインまたは増殖因子の送達のためにそれらの効果的なツールにするために行います。最も有望な使用の一つは、細胞および生物活性化合物を運ぶ注射用生体材料としてです。 インビトロおよびインビボ実験3,4で観察されたようなヒドロゲルは、保持して正確な生理学的関連性の様式で幹細胞の調節シグナルを送達することによって、細胞の生存および制御幹細胞の運命を改善することができます。このの主要な利点は、可能性であります体の上にすべてを移行し、目標の目標5を失って 、循環急流にエリアとextravasatesを離れる細胞の量を最小限に抑え、( その場で )接種のゾーン内注入した細胞を維持します。三次元ハイドロゲルネットワークの安定性は、ポリマー鎖の6間の共有結合または凝集力によって形成され、その架橋部位です。
このフレームワークでは、直交選択的化学は、ポリマー鎖に適用されるが、ヒドロゲル公演7を向上させることができる汎用性の高いツールです。実際、適切な化学基を有するポリマーの修飾は、細胞生存率および組織形成におけるそれらの使用を強化するために適切な化学的、物理的および機械的特性を提供するのに役立つ可能性があります。同様に、ゲルマトリックス内の細胞または成長因子をロードするための技術のうち、RGDペプチドの使用は、細胞接着及び生存の改善を可能にします。 RGDは構成されるトリペプチドでありますアルギニン、グリシン、およびはるかに複数の細胞接着受容体と細胞アンカー、行動および生存8,9にその生物学的影響に対処する能力のために最も効果的でしばしば用いられるトリペプチドであるアスパラギン酸の。この作業では、RGD官能ヒドロゲルの合成は、もてなしの細胞微小環境のために十分な生化学的特性によって特徴付けネットワークを設計することを目的として検討されています。
ヒドロゲルの合成におけるマイクロ波照射の使用は、副反応を最小限に抑え、従来の熱プロセス10に比べて短時間でより高い反応速度と収率を得るための簡単な手順を提供します。この方法は、ポリマーとの相互作用及び反応システム11中の有機溶媒の非存在に起因する精製工程及び収率滅菌ヒドロゲルを必要としません。したがって、それは、MODためのポリマーネットワークに結合されたRGDの高い割合を確保しますificationsは、ゲル形成に関与するポリマーの化学基に必要とされます。カルボキシル基は、PAAおよびカルボマー、ならびにヒドロキシル基、PEGから、アガロースから、重縮合反応によりヒドロゲルの三次元構造を生じます。言及されたポリマーは、脊髄損傷の修復処理12におけるヒドロゲルの合成のために使用されます。以前に報告されているようにこれらのデバイスは、高い生体適合性だけでなく、多くの生体組織のとチキソトロピー性のものと似ている機械的および物理化学的特性を示し、13,14を動作します。さらに、それらは、注射ゾーンで、 その場に局在したままです。
この研究では、PAAのカルボキシル基は、アルキン部分( 図1)を用いて修飾され、及びRGD -アジド化合物は、構造を用いて調製化合物とトリペプチドの末端基-NH 2(CH 2)の反応性を利用するn個合成されます- N 3(<強い>図2)。その後、変更されたPAAはCuAACのクリック反応15-17( 図3)を介してRGD-アジド誘導体と反応します。銅(I)触媒の使用は、反応速度及び位置選択性の両方の主要な改善につながります。 CuAAC反応は広く、有機合成およびポリマー科学において使用されます。これは、官能基を高効率、高耐性を兼ね備え、かつ、有機溶剤を使用することによって影響を受けません。高選択性、速い反応時間および簡単な精製手順は、所望の部分18を移植する星型ポリマー、ブロックコポリマーまたは鎖の取得を可能にします。このクリック戦略は、最終的な生化学的用途に応じて物理化学的性質をカスタマイズするために重合後のポリマーを修正することが可能となります。 CuAAC実験条件は簡単に(銅の酸化を最小限に発生する可能性があるのに対し、反応は、水の影響を受けない)、再現性、および自然のです形成されたトリアゾールは、製品の安定性を確保します。銅金属の使用は、細胞に対する潜在的な毒性効果および生物学的微小環境において、臨界点と考えることができるが、透析は、触媒残留物の完全な除去を可能にするための精製方法として使用されます。最後に、PAAは、RGD細胞または薬物担体としてのこれらのシステムの潜在的な機能を確認するために、検討されているヒドロゲルの合成( 図4)、得られたネットワークの物理化学的特性で使用される修飾しました。
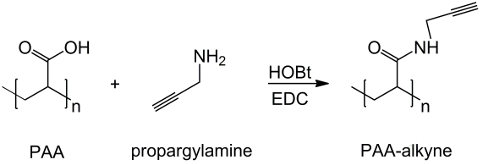
図1:PAAは、アルキンの合成を修正アルキン基とPAAの官能化のスキームを;。 「n」はプロパルギルアミンと反応するカルボキシル基を有するモノマーを示しています。 ご覧になるにはこちらをクリックしてください。この図の拡大版。
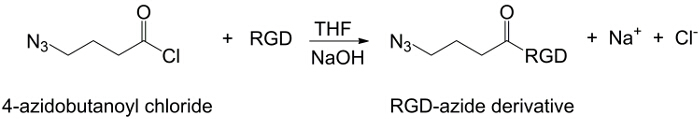
図2:RGD- アジド合成 RGD-アジド誘導体の合成この図の拡大版をご覧になるにはこちらをクリックしてください。
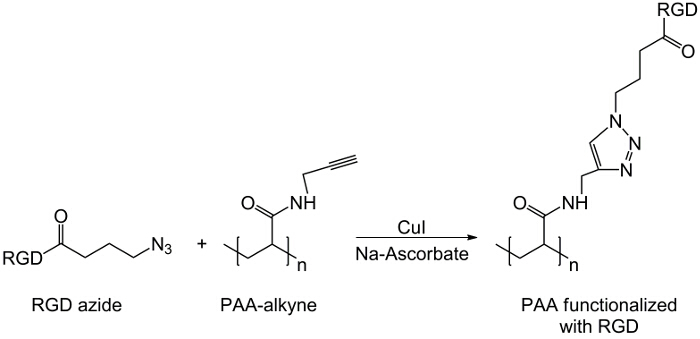
図3:RGD-アジド誘導体とアルキン-PAA間のクリック反応の反応スキームをクリックしてください 。 この図の拡大版をご覧になるにはこちらをクリックしてください。
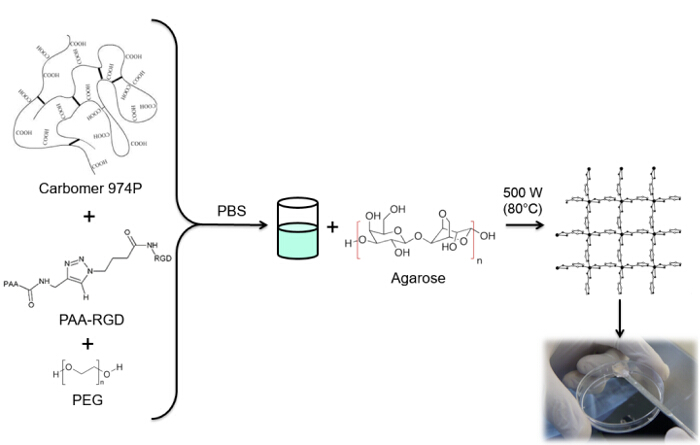
図4:ハイドロゲルSYNThesis。RGD官能ヒドロゲルの合成手順。 この図の拡大版をご覧になるにはこちらをクリックしてください。
Protocol
Representative Results
Discussion
The PAA post-polymerization modification with alkyne moieties and the RGD functionalization with the azide group guarantee the formation of a stable bond between the polymer and the peptide. Indeed, triazole serves as a rigid linking unit among the carbon atoms, attached to the 1,4 positions of the 1,2,3-triazole ring and it cannot be cleaved hydrolytically or otherwise. In addition, triazole is extremely difficult to oxidize and reduce, unlike other cyclic structures such as benzenoids and related aromatic heterocycles<…
Divulgations
The authors have nothing to disclose.
Acknowledgements
著者は、言語の編集のために実りある議論のための教授マウリツィオ瑪斯とミスキアラAllegrettiに感謝したいと思います。本研究は、坂東GIOVANI Ricercatori 2010(MinisteroデッラサルーテGR-2010- 2312573)によってサポートされています。
Materials
| Poly(acrylic acid) solution average Mw ~ 100,000, 35 wt % in H2O | Sigma Aldrich | 523925 | CAS 9003-01-4 |
| Poly(ethylene glycol) 2,000 | Sigma Aldrich | 84797 | CAS 25322-68-3 |
| Carbomeer 974P | Fagron | 1387083 | |
| Agarose | Invitrogen Corp. | 16500-500 | UltraPure Agarose |
| RGD peptide | abcam | ab142698 | |
| 4-azidobutanoic acid | Aurum Pharmatech | Z-2421 | CAS 54447-68-6 |
| Oxalyl chloride | Sigma Aldrich | O8801 | CAS 79-37-8 |
| Propargylamine hydrochloride 95% | Sigma Aldrich | P50919 | CAS 15430-52-1 |
| Copper(I) iodide | Sigma Aldrich | 3140 | CAS 7681-65-4 |
| Sodium ascorbate | Sigma Aldrich | Y0000039 | CAS 134-03-2 |
| Phosphate buffered saline | Sigma Aldrich | P4417 | |
| Dialysis Membrane | Spectrum Laboratories, Inc. | 132725 | Spectra/Por 3 Dialysis Membrane Standard RC Tubing MWCO: 3,5 kD |
References
- Slaughter, B. V., Khurshid, S. S., Fisher, O. Z., Khademhosseini, A., Peppas, N. A. Hydrogels in Regenerative Medicine. Adv. Mater. 21 (32-33), 3307-3329 (2009).
- Rossi, F., Perale, G., Papa, S., Forloni, G., Veglianese, P. Current options for drug delivery to the spinal cord. Expert Opin. Drug Deliv. 10 (3), 385-396 (2013).
- Huebsch, N., et al. Harnessing traction-mediated manipulation of the cell/matrix interface to control stem-cell fate. Nat. Mater. 9 (6), 518-526 (2010).
- Mothe, A. J., Tam, R. Y., Zahir, T., Tator, C. H., Shoichet, M. S. Repair of the injured spinal cord by transplantation of neural stem cells in a hyaluronan-based hydrogel. Biomaterials. 34 (15), 3775-3783 (2013).
- Khetan, S., et al. Degradation-mediated cellular traction directs stem cell fate in covalently crosslinked three-dimensional hydrogels. Nat. Mater. 12 (5), 458-465 (2013).
- Ashley, G. W., Henise, J., Reid, R., Santi, D. V. Hydrogel drug delivery system with predictable and tunable drug release and degradation rates. Proc. Natl. Acad. Sci. U S A. 110 (6), 2318-2323 (2013).
- Rossi, F., van Griensven, M. Polymer Functionalization as a Powerful Tool to Improve Scaffold Performances. Tissue Eng. Part A. 20 (15-16), 2043-2051 (2014).
- Gould, S. T., Darling, N. J., Anseth, K. S. Small peptide functionalized thiol-ene hydrogels as culture substrates for understanding valvular interstitial cell activation and de novo tissue deposition. Acta Biomater. 8 (9), 3201-3209 (2012).
- Azagarsamy, M. A., Anseth, K. S. Wavelength-Controlled Photocleavage for the Orthogonal and Sequential Release of Multiple Proteins. Angew. Chem. Int. Edit. 52 (51), 13803-13807 (2013).
- Larrañeta, E., et al. Microwave-Assisted Preparation of Hydrogel-Forming Microneedle Arrays for Transdermal Drug Delivery Applications. Macromol. Mater. Eng. 300 (6), 586-595 (2015).
- Cook, J. P., Goodall, G. W., Khutoryanskaya, O. V., Khutoryanskiy, V. V. Microwave-Assisted Hydrogel Synthesis: A New Method for Crosslinking Polymers in Aqueous Solutions. Macromol. Rapid Comm. 33 (4), 332-336 (2012).
- Perale, G., et al. Multiple drug delivery hydrogel system for spinal cord injury repair strategies. J. Control. Release. 159 (2), 271-280 (2012).
- Rossi, F., Perale, G., Storti, G., Masi, M. A Library of Tunable Agarose Carbomer-Based Hydrogels for Tissue Engineering Applications: The Role of Cross-Linkers. J. Appl. Polym. Sci. 123 (4), 2211-2221 (2012).
- Frith, J. E., et al. An injectable hydrogel incorporating mesenchymal precursor cells and pentosan polysulphate for intervertebral disc regeneration. Biomaterials. 34 (37), 9430-9440 (2013).
- Kolb, H. C., Finn, M. G., Sharpless, K. B. Click chemistry: Diverse chemical function from a few good reactions. Angew. Chem. Int. Edit. 40 (11), (2001).
- Sacchetti, A., Mauri, E., Sani, M., Masi, M., Rossi, F. Microwave-assisted synthesis and click chemistry as simple and efficient strategy for RGD functionalized hydrogels. Tetrahedron Lett. 55 (50), 6817-6820 (2014).
- Ossipov, D. A., Hilborn, J. Poly(vinyl alcohol)-based hydrogels formed by "click chemistry". Macromolecules. 39 (5), 1709-1718 (2006).
- Truong, V., Blakey, I., Whittaker, A. K. Hydrophilic and Amphiphilic Polyethylene Glycol-Based Hydrogels with Tunable Degradability Prepared by "Click" Chemistry. Biomacromolecules. 13 (12), 4012-4021 (2012).
- Hou, R. Z., et al. New synthetic route for RGD tripeptide. Prep. Biochem. Biotechnol. 36 (3), 243-252 (2006).
- Rossi, F., Chatzistavrou, X., Perale, G., Boccaccini, A. R. Synthesis and Degradation of Agar-Carbomer Based Hydrogels for Tissue Engineering Applications. J. Appl. Polym. Sci. 123 (1), 398-408 (2012).
- Mauri, E., Rossi, F., Sacchetti, A. Tunable drug delivery using chemoselective functionalization of hydrogels. Mater. Sci. Eng. C. 61, 851-857 (2016).
- Joaquin, A., Peppas, N. A., Zoldan, J. Hydrogel Polymer Library for Developing Induced Pluripotent Stem Cell Derived Cardiac Patches. Tissue Eng. Part A. 20, S55-S55 (2014).
- Rossi, F., et al. Tunable hydrogel-Nanoparticles release system for sustained combination therapies in the spinal cord. Colloids Surf. B Biointerfaces. 108, 169-177 (2013).
- Kolb, H. C., Sharpless, K. B. The growing impact of click chemistry on drug discovery. Drug Discov. Today. 8 (24), 1128-1137 (2003).
- Ossipov, D. A., Yang, X., Varghese, O., Kootala, S., Hilborn, J. Modular approach to functional hyaluronic acid hydrogels using orthogonal chemical reactions. Chem. Commun. 46 (44), 8368-8370 (2010).
- Anderson, S. B., Lin, C. C., Kuntzler, D. V., Anseth, K. S. The performance of human mesenchymal stem cells encapsulated in cell-degradable polymer-peptide hydrogels. Biomaterials. 32 (14), 3564-3574 (2011).
- Caron, I., et al. A new three dimensional biomimetic hydrogel to deliver factors secreted by human mesenchymal stem cells in spinal cord injury. Biomaterials. 75, 135-147 (2016).
- Lee, J. W., Kim, H., Lee, K. Y. Effect of spacer arm length between adhesion ligand and alginate hydrogel on stem cell differentiation. Carbohyd. Polym. 139, 82-89 (2016).
- Liu, Y., Fan, Z., Wang, Y., Yu, L. Controlled Release of Low Molecular Protein Insulin-like Growth Factor-1 through Self-Assembling Peptide Hydrogel with Biotin Sandwich Approach. J.Biomed. Eng. 32 (2), 387-392 (2015).

