प्रक्रिया और एक स्वचालित केशिका Electrophoretic-आधारित Immunoassay विधि के लिए कुंजी ऑप्टिमाइज़ेशन रणनीतियाँ
Summary
कुल प्रोटीन की तैयारी से लक्ष्य प्रोटीन को मापने के लिए एक वाणिज्यिक मंच का उपयोग कर एक केशिका आधारित immunoassay का प्रदर्शन किया है । इसके अलावा, प्रदर्शन समय के परख मापदंडों, प्रोटीन एकाग्रता, और एंटीबॉडी कमजोर पड़ने एक सेल संस्कृति मॉडल प्रणाली के लिए अनुकूलित कर रहे हैं ।
Abstract
नई प्रौद्योगिकियों कि केशिका आधारित immunoassays का उपयोग तेजी से और अधिक मात्रात्मक प्रोटीन मूल्यांकन पारंपरिक immunoassays की तुलना में वादा करता हूं । हालांकि, अंय एंटीबॉडी के समान-आधारित प्रोटीन परख, केशिका का अनुकूलन-आधारित immunoassay मानकों, प्रोटीन एकाग्रता, एंटीबॉडी कमजोर पड़ने के रूप में, और जोखिम समय सार्थक और विश्वसनीय की पीढ़ी के लिए एक महत्वपूर्ण शर्त है डेटा. माप जहां संकेत में परिवर्तन सीधे lysate एकाग्रता में परिवर्तन करने के लिए आनुपातिक है परख के रैखिक रेंज के भीतर गिर चाहिए । उचित lysate सांद्रता, एंटीबॉडी कमजोर पड़ने का चयन करने की प्रक्रिया, और जोखिम बार मानव के रूप में, उपकला सेल लाइन, ब्यास-बी. ए., यहां प्रदर्शन किया है । परख रैखिकता p53 और α-tubulin एंटीबॉडी के साथ पूरे सेल निकालने प्रोटीन सांद्रता की एक सीमा से अधिक दिखाया गया है । संकेत burnout का एक उदाहरण लंबे समय जोखिम समय के साथ उच्चतम सांद्रता पर देखा जाता है, और एक α-tubulin एंटीबॉडी कमजोर पड़ने वक्र संतृप्ति का प्रदर्शन दिखाया गया है । इसके अलावा, उदाहरण प्रयोगात्मक परिणाम अनुकूलित मापदंडों का उपयोग डॉक्सोरूबिसिन-इलाज कोशिकाओं के लिए रिपोर्ट कर रहे हैं ।
Introduction
केशिका electrophoretic immunoassays माप प्रोटीन अभिव्यक्ति कोशिका lysates में आकार या चार्ज जुदाई प्रणालियों का उपयोग कर और पारंपरिक immunoassays पर कई लाभ प्रदान करते हैं । उदाहरण के लिए, पश्चिमी दाग की तुलना में, स्वचालित केशिका-आधारित प्रक्रिया जैल, स्थानांतरण उपकरणों, और मैनुअल बहाकर की आवश्यकता को समाप्त कर देती है । इसके अलावा, आवश्यक प्रोटीन की निरपेक्ष राशि लगभग 10 गुना कम है, केशिका आधारित सिस्टम दुर्लभ कोशिका प्रकार या सीमित नमूना1,2के साथ प्रयोग के लिए आदर्श बना । परिणाम में प्राप्त कर रहे है के रूप में छोटे 3 स्वचालित प्रणाली का उपयोग एच और पहले से अधिक मात्रात्मक और पारंपरिक पश्चिमी दाग प्रक्रियाओं3,4,5से प्रतिलिपि हो प्रदर्शन किया गया है । आकार आधारित परख के लिए प्रक्रिया में सोडियम dodecyl सल्फेट (एसडीएस), dithiothreitol (डीटीटी), और फ्लोरोसेंट के ढेर और जुदाई मैट्रिक्स युक्त केशिका कॉलम में आणविक वजन मार्करों से युक्त नमूनों लदान के होते हैं । वोल्टेज केशिकाओं के लिए लागू आकार के अनुसार नमूनों में प्रोटीन अलग करता है, और यूवी प्रकाश केशिका दीवार को अलग प्रोटीन मैटीरियल । केशिका तो bliss-लक्ष्य-विशिष्ट प्राथमिक एंटीबॉडी और सहिजन peroxidase (एचआरपी)-संयुग्मित माध्यमिक एंटीबॉडी के साथ जांच की है । Luminol और पेरोक्साइड उत्प्रेरित chemiluminescent प्रकाश पीढ़ी जो एक आरोप युग्मित डिवाइस (सीसीडी) कैमरे से मापा जाता है और quantitate प्रोटीन के लिए विश्लेषण किया ।
रिश्तेदार आसानी और एक स्वचालित केशिका आधारित electrophoretic immunoassay मंच की गति के बावजूद, ऐसे प्रोटीन एकाग्रता, एंटीबॉडी कमजोर पड़ने के रूप में परख शर्तों के अनुकूलन, और जोखिम समय सही प्राप्त करने के लिए महत्वपूर्ण है, प्रतिलिपि परिणाम. सामांय में, निंनलिखित प्रक्रियाओं के लिए इन प्रणालियों के लिए एक परख का अनुकूलन किया जाना चाहिए:
1) एक स्क्रीन का मूल्यांकन करने के लिए और प्रोटीन लक्ष्य के लिए संकेत और विशिष्टता के लिए एंटीबॉडी का चयन किया जाना चाहिए । यदि उपलब्ध हो, शुद्ध प्रोटीन या लक्ष्य epitope विशिष्टता का आकलन करने के लिए इस्तेमाल किया जा सकता है; हालांकि, यह अभी भी मॉडल प्रणाली से स्रोत कुल प्रोटीन में संभावित गैर विशिष्ट संकेत का आकलन करने के लिए महत्वपूर्ण है ।
2) अगले, परख के गतिशील रेंज के लिए निर्धारित की जरूरत है । एक आदर्श स्थिति में, संकेत दोहरीकरण (पीक क्षेत्र का उपयोग कर मापा जाता है) नमूना एकाग्रता दोगुनी हो जाती है के रूप में मनाया जाता है; हालांकि, व्यवहार में, एक अनुमानित तरीके से इनपुट के लिए संकेत में आनुपातिक परिवर्तन (उदा, रेखीय फ़िट) प्रोटीन ठहराव के लिए पर्याप्त है । इसके अतिरिक्त, इस अनुकूलन उच्च संकेत के साथ प्रोटीन एकाग्रता को परिभाषित लेकिन अभी भी प्रयोगात्मक मॉडल के लिए रैखिक सीमा के भीतर होगा ।
3) तय प्रोटीन एकाग्रता अनुकूलन चरण 2 में चुना का उपयोग कर इष्टतम एंटीबॉडी एकाग्रता का निर्धारण । के रूप में एंटीबॉडी एकाग्रता बढ़ जाती है, संकेत बढ़ जाती है जब तक यह संतृप्ति पर पठार । इस संतृप्ति के स्तर के पास एक एंटीबॉडी एकाग्रता प्रोटीन एकाग्रता का सही माप के लिए आवश्यक है ।
प्रक्रिया प्रोटीन सांद्रता, एंटीबॉडी कमजोर पड़ने, और एक स्वचालित केशिका आधारित आकार परख के लिए जोखिम समय का अनुकूलन करने के लिए प्रयोग किया जाता है 6 पूरे सेल ब्यास से अलग अर्क का उपयोग कर प्रदर्शन है-2 बी, एक एसवी-४० मानव दमा बदल उपकला कोशिका लाइन. कोशिका या ऊतक निष्कर्षों से प्रोटीन अलगाव प्रकाशित प्रोटोकॉल की एक संख्या का उपयोग किया जा सकता है7,8,9 और यहां कवर नहीं किया जाएगा । एक परीक्षण अनुकूलित शर्तों का उपयोग कर प्रयोग के परिणाम भी कुल और phosphorylated के लिए रिपोर्ट कर रहे है (serine 15, serine 20) डॉक्सोरूबिसिन को उजागर संस्कृतियों में p53 (एक आम कीमोथेरेपी एजेंट है कि १.२, १.८ पर सेल apoptosis10लाती है), और २.४ µ g/एमएल मीडिया 4 एच के लिए फसल से पहले । p53 पीक क्षेत्रों ɑ-tubulin, जो एक लोडिंग नियंत्रण के रूप में प्रयोग किया जाता है के लिए सामान्यीकृत हैं ।
Protocol
नोट: यह सुनिश्चित करें कि नीचे उल्लिखित सभी रिएजेंटों और नमूनों को निर्माता & #39; s प्रोटोकॉल के अनुसार तैयार किया गया है । कृपया इस प्रक्रिया है, जो नाइट्राइल दस्ताने, लैब कोट, बंद पंजे जूते, और सुरक्षा चश्मे शामिल है के दौरान उचित व्यक्तिगत सुरक्षा उपकरण पहनते हैं । विशिष्ट सामग्री, रिएजेंट और आवश्यक उपकरणों की एक मेज अलग से प्रदान की जाती है । नमूनों की कुल प्रोटीन एकाग्रता पहले से स्थापित तरीके कि lysate बफर के साथ संगत कर रहे हैं का उपयोग कर निर्धारित किया जाना चाहिए, जैसे ब्रैडफोर्ड परख 11 .
1. निर्माता द्वारा आपूर्ति के रूप में मानक पैक से नमूने और रिएजेंट की तैयारी dithiothreitol (डीटीटी) के ४०० mM काम समाधान तैयार करने के लिए, ४० & #181; L से युक्त साफ़ ट्यूब को पानी के लिए निर्माता से स्टॉक की आपूर्ति की । यह धीमी और कोमल pipetting के साथ समाधान मिश्रण से समाधान के लिए बुलबुले को शुरू करने से बचने के लिए महत्वपूर्ण है । Add 20 & #181; l 10x नमूना बफर और 20 & #181; l तैयार ४०० मिमी डीटीटी के लिए समाधान गुलाबी ट्यूब फ्लोरोसेंट 5x मास्टर मिश्रण से युक्त (सामग्री की तालिका देखें). नोट: मास्टर मिश्रण (मिमी) एक पन्नी कवर के साथ निर्माता द्वारा बंद कर दिया है और एक पिपेट टिप से छेदा जाना चाहिए. पिपेट में डीटीटी छप से बचने के लिए धीमी गति से pipetting से धीरे मिलाएं । अगले, add 16 & #181; l क जल, 2 & #181; की आपूर्ति की गई 10x नमूना बफर के एल, और 2 & #181; एल के तैयार ४०० mM डीटीटी समाधान के लिए सफेद biotinylated सीढ़ी ट्यूब निर्माता द्वारा आपूर्ति की । मिश्रण धीरे और denaturing. के लिए एक ०.६ मिलीलीटर ट्यूब में स्थानांतरण पानी के साथ आपूर्ति की 10x समाधान 1:100 कमजोर द्वारा 0.1 x नमूना बफर तैयार करते हैं । पर्याप्त 0.1 x नमूना बफर सभी नमूनों को पतला करने के लिए तैयार करें । 0.1 x नमूना बफर है कि एक नमूना है, जो कुल प्रोटीन की अंतिम वांछित एकाग्रता पर निर्भर करेगा करने के लिए जोड़ा जाता है की राशि की गणना । मिश्रण 1 हिस्सा 5x फ्लोरोसेंट मिमी 4 के साथ वांछित अंतिम प्रोटीन एकाग्रता प्राप्त करने के लिए नमूना पतला भागों । निम्नानुसार वॉल्यूम की गणना: (i) वॉल्यूम 5x फ्लोरोसेंट MM = (वांछित अंतिम प्रोटीन एकाग्रता)/ (ii) प्रोटीन स्टॉक की मात्रा = (वांछित अंतिम प्रोटीन एकाग्रता x कुल मात्रा की जरूरत)/ (iii) आयतन 0.1 x नमूना बफर = कुल मात्रा-5x & #160; मिमी मात्रा-प्रोटीन स्टॉक मात्रा.
2. नमूनों और सीढ़ी की विकार जगह तैयार नमूनों और biotinylated सीढ़ी में एक ९५ & #176; सी हीट ब्लॉक के लिए 5 min. भंवर ट्यूबों तुरंत के बाद मशीन, एक के लिए स्पिन निष्पादित ~ 5 एक तालिका के अंदर की ओर केंद्रापसारक, और बर्फ पर जगह. नोट: प्रोटीन एकत्रीकरण को रोकने और केशिका मैट्रिक्स में प्रवास में सुधार करने के लिए कुछ प्रोटीन gentler denaturing स्थितियों ( उदा , ७० o C 10 मिनट के लिए) की आवश्यकता हो सकती है । इस विकल्प पर विचार अगर वहां भारी उच्च आणविक भार पर धब्बा है (उदाहरण के लिए वीडियो देखें) ।
3. एंटीबॉडी की तैयारी के रूप में अनुकूलन द्वारा निर्धारित ( प्रतिनिधि परिणाम और वीडियो देखें), प्राथमिक एंटीबॉडी ( जैसे , 1:50, 1:100) के वांछित कमजोर पड़ने (ओं) को तैयार एंटीबॉडी मंदक 2. नोट: एंटीबॉडी आम तौर पर पारंपरिक पश्चिमी सोख्ता के लिए की तुलना में केशिका आधारित immunoassay के लिए उच्च सांद्रता में इस्तेमाल कर रहे हैं । आपूर्ति किए गए द्वितीयक एंटीबॉडी कमजोर पड़ने के बिना उपयोग करने के लिए तैयार है ।
4. Luminol की तैयारी-एस और पेरोक्साइड Luminol-s और पेरोक्साइड का एक 1:1 मिश्रण तैयार. भंवर मिश्रण करने के लिए और बर्फ पर दुकान. नोट: यह महत्वपूर्ण है कि इस मिश्रण प्रत्येक प्रयोगात्मक परख के लिए नए सिरे से तैयार है । फुल प्लेट चलाने के लिए 250ul टोटल मिक्स की जरूरत होती है ।
5. तैयारी की परख प्लेट के रूप में दिखाया चित्रा 1 , नमूने और परख प्लेट में ऊपर तैयार reएजेंट लोड । प्रत्येक पंक्ति के लिए नीचे विस्तृत निर्देश देखें । कुओं से वाष्पीकरण को कम करने के लिए, सुनिश्चित करें कि प्लेट ढक्कन रिएजेंट अतिरिक्त के बीच बदल दिया गया है । में पंक्ति A, प्लास्टिक 5 & #181; Biotinylated सीढ़ी के वेल A1 में एल. शेष पंक्ति के लिए, प्लास्टिक तैयार नमूनों (5 & #181; L प्रत्येक) कुओं में A2-A25. नोट: यह आवश्यक है कि A1 अच्छी तरह से हमेशा सीढ़ी होता है, कारतूस में पहली केशिका के रूप में इस मानक चलाने के लिए अनुकूलित है. पंक्ति B में , प्लास्टिक 10 & #181; L का एंटीबॉडी मंदक 2 में प्रत् येक वेल (B1-B25). पंक्ति C में , प्लास्टिक 10 & #181; L की एंटीबॉडी मंदक 2 में अच्छी तरह से C1. शेष पंक्ति C कुओं में, प्लास्टिक 10 & #181; L का प्राथमिक एंटीबॉडी (वेल्स C2-C25). में पंक्ति D, प्लास्टिक 10 & #181; L के Streptavidin-एचआरपी में well D1. शेष पंक्ति D कुओं में, प्लास्टिक 10 & #181; माध्यमिक एंटीबॉडी (वेल्स D2-D25) के एल. पंक्ति म E, प्लास्टिक 10 & #181; प्रत्येक वेल (E1-E25) में ताज़े तैयार luminol-पेरोक्साइड मिश्रण के एल. तत, add ५०० & #181; L धो बफ़र कुओं की शीर्ष 3 पंक्तियों में से प्रत्येक के लिए डिब्बे प्रति । नोट: यह बुलबुले केशिका लोड हो रहा है और चलाने के साथ हस्तक्षेप कर सकते हैं के रूप में टिप से धीरे pipetting और अंतिम मात्रा निष्कासित नहीं द्वारा बुलबुला गठन को कम करने के लिए महत्वपूर्ण है. एक बार सभी कुओं भरी हुई हैं, कमरे के तापमान पर 5 मिनट के लिए ~ १००० x g पर थाली के लिए बुलबुले को हटाने और तरल कुओं के नीचे में है सुनिश्चित करें । एक छोटे से पिपेट टिप या साफ सुई के साथ किसी भी दिखाई बुलबुले पॉप ( जैसे , 25 गेज बाँझ & #34; प्रतिनिधि शीर्ष & #34; सुई).
6. शुरू केशिका immunoassay साधन सुनिश्चित करें कि उपकरण और साथ कंप्यूटर चालू हैं । कोई गर्म समय की जरूरत है । कंप्यूटर पर इंस्ट्रूमेंटेशन सॉफ़्टवेयर खोलें । सबसे पहले, & #34 का चयन करें; परख & #34; विंडो के दाईं ओर टैब और & #34; नई परख & #34; के अधीन & #34; फ़ाइल मेनू & #34; बाईं ओर । आकार का चयन करें, आकार रेंज ( जैसे , 12-230 केडीए), और कारतूस प्रकार ( जैसे , 25 केशिका) है कि विशेष रूप से परख के लिए इस्तेमाल किया गया था । नोट: एक भी इनपुट परख पैरामीटर, प्रोटीन एकाग्रता, एंटीबॉडी प्रकार, और कमजोर पड़ने सहित, अगर वांछित, हो सकता है, लेकिन इन की आवश्यकता नहीं परख शुरू कर रहे हैं । नारंगी पैनल के शीर्ष पर बटन धक्का द्वारा उपकरण पर दरवाजा खोलो । ध्यान से अपनी पैकेजिंग से केशिका कारतूस हटा दें । कांच केशिकाओं खुद को छूने के बिना, कारतूस धारक में कारतूस जगह है । नारंगी से नीले रंग के लिए आंतरिक प्रकाश परिवर्तन देख द्वारा कारतूस बैठने की पुष्टि करें । बेंच पर मजबूती से थाली पकड़ और ध्यान से थाली के निचले हिस्से से वाष्पीकरण सील छील । किसी भी एक एसएम के साथ इन जुदाई मैट्रिक्स वेल्स में देखा बुलबुले पॉपसभी प्लास्टिक टिप या साफ सुई ( जैसे , 25 गेज बाँझ & #34; प्रतिनिधि top & #34; सुई). प्लेट धारक पर परख थाली जगह है, यह सुनिश्चित करने के पूरी तरह से बैठा है, और बंद साधन दरवाजा । क्लिक करें & #34; स्टार्ट & #34; बटन सॉ. नोट: यदि कोई प्रारंभ बटन प्रकट होता है, तो इंस्ट्रूमेंट के साथ कनेक्शन खो गया है । शीर्ष बाएँ मेनू से साधन चुनें, तो कनेक्ट. एक पॉप-अप साधन सीरियल नंबर के साथ दिखाई देना चाहिए; यह चुनें, फिर कनेक्ट करें प्रारंभ करें बटन अब दिखाई देना चाहिए । जब भागो पूरा हो जाए तो थाली त्याग दें । निकास के लिए एक sharps कंटेनर में कारतूस और जगह निकालें, किसी भी सुई कि बुलबुले पॉप करने के लिए इस्तेमाल किया गया हो सकता है के साथ साथ । यदि साधन नियमित रूप से इस्तेमाल किया जा रहा है कनेक्शन समस्याओं से बचने के लिए पर सत्ता छोड़ दो ( जैसे , कम से कम साप्ताहिक). 7. प्रयोग विश्लेषण विश्लेषण से पहले, सुनिश्चित करें कि निंन गुणवत्ता जांच की जाती हैं । का चयन करके फ्लोरोसेंट मानकों का सत्यापन & #34; मानक दिखाएं & #34; चिह्न । जांच करें कि मानक सही तरीके से पहचाने जाते हैं & #34; ग्राफ़ देखें & #34; tab. यदि वे गलत हैं, तो & #34 पर जाएं; सिंगल व्यू & #34; आइकन, सही पीक पर दायां क्लिक करें, और & #34 का चयन करें; बल मानक & #34;, या सही पीक पर दायां क्लिक करें और & #34 का चयन करें; न मानक & #34; । प्रत्येक नई केशिका के लिए यह जाँच करें । पर क्लिक करके biotinylated सीढ़ी का सत्यापन करें & #34; नमूने & #34; और & #34; एकल दृश्य & #34; चिह्न । प्रयोग टैब में सीढ़ी का चयन करें । यदि किसी चोटी की गलत पहचान है, तो उस पर दायाँ क्लिक करें & #34; ग्राफ देखें & #34; और select & #34; निकाल पीक & #34;. नोट: उदाहरण के लिए, 12-230 केडीए किट के लिए उपयोग की गई biotinylated सीढ़ी 12, ४०, ६६, ११६, १८०, और २३० केडीए & #160; आकार देने वाली चोटियों को दिखाना चाहिए. यह चरण नहीं किया जाता है, तो नमूना चोटियों का आकार गलत रूप से परिकलित किया जाएगा, नकली परिणाम का उत्पादन. देखें और नमूना चोटियों का विश्लेषण. चोटियों तालिका से डेटा प्राप्त, आणविक वजन सहित, पीक क्षेत्र, पीक ऊंचाई, और शोर करने के लिए संकेत (S/एन), के रूप में प्रयोगात्मक गणना के लिए आवश्यक. 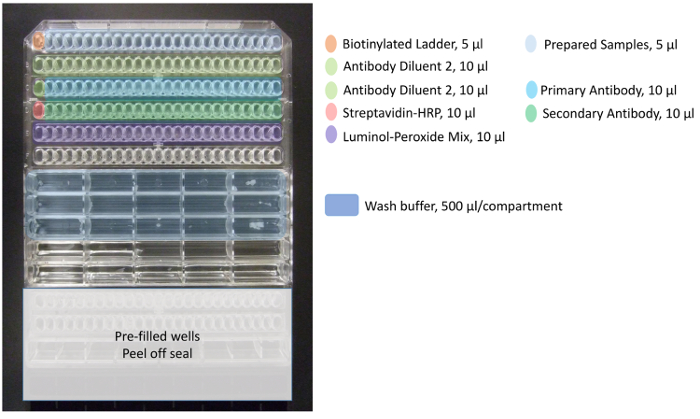 चित्रा १ . Pipetting परख प्लेट के लिए टेंपलेट । रंग कोडिंग उचित रिएजेंट और नमूनों का प्रतिनिधित्व करता है (अप करने के लिए 24 कुल) परख थाली में जोड़ा । biotinylated सीढ़ी को अच्छी तरह A1 (नारंगी) में जोड़ें, कुओं से तैयार नमूनों को A2 तक A25 (हल्का नीला), एंटीबॉडी मंदक 2 से वेल्स B1-B25 और C1 (हल्का हरा), प्राइमरी एंटीबॉडी टू वेल्स C2 तक C25 (नीला), streptavidin-एचआरपी से वेल D1 (डार्क पिंक), माध्यमिक एंटीबॉडी को वेल्स D25 अप करने के लिए D2 (डार्क ग्रीन), और luminol-पेरोक्साइड मिश्रण करने के लिए वेल्स E1 तक E25 (बैंगनी). धो बफर बड़ा मध्य प्लेट वेल्स (डार्क ब्लू) के पहले तीन पंक्तियों में जोड़ा जाता है । इस फिगर का बड़ा वर्जन देखने के लिए यहां क्लिक करें ।
चित्रा १ . Pipetting परख प्लेट के लिए टेंपलेट । रंग कोडिंग उचित रिएजेंट और नमूनों का प्रतिनिधित्व करता है (अप करने के लिए 24 कुल) परख थाली में जोड़ा । biotinylated सीढ़ी को अच्छी तरह A1 (नारंगी) में जोड़ें, कुओं से तैयार नमूनों को A2 तक A25 (हल्का नीला), एंटीबॉडी मंदक 2 से वेल्स B1-B25 और C1 (हल्का हरा), प्राइमरी एंटीबॉडी टू वेल्स C2 तक C25 (नीला), streptavidin-एचआरपी से वेल D1 (डार्क पिंक), माध्यमिक एंटीबॉडी को वेल्स D25 अप करने के लिए D2 (डार्क ग्रीन), और luminol-पेरोक्साइड मिश्रण करने के लिए वेल्स E1 तक E25 (बैंगनी). धो बफर बड़ा मध्य प्लेट वेल्स (डार्क ब्लू) के पहले तीन पंक्तियों में जोड़ा जाता है । इस फिगर का बड़ा वर्जन देखने के लिए यहां क्लिक करें ।
Representative Results
Discussion
दशकों के लिए, वहां केशिका electrophoretic के विकास में निरंतर रुचि है, क्योंकि कम नमूना और एजेंट व्यय की immunoassay तरीके आधारित है, प्रसंस्करण समय में कमी हुई जब पारंपरिक तरीकों की तुलना में, और उच्च संगतता के लिए प्रक्रिया को स्वचालित4,15। वहां प्रोटीन है कि electrophoretic, electrokinetic, बहुलक sieving, और isoelectric तरीकों, जो विभिंन गुणों से प्रोटीन को अलग सहित उपयोग केशिकाओं, के जुदाई के लिए विभिंन प्रोटोकॉल के एक नंबर रहे है (क्रमशः, इलेक्ट्रोस्टैटिक चार्ज, विभाजन संतुलन, अलग मैट्रिक्स के sieving गुण, और पीएच)16। यहां, हम एक एंटीबॉडी-आधारित (या immunoassay) केशिका ट्रो विधि का वर्णन, एक बहुलक sieving जुदाई का उपयोग कर, कि स्वचालित और व्यावसायिक रूप से अपनाया गया है3। इस प्रणाली के लाभ का उपयोग करें और आपरेशन, मानकीकृत और व्यावसायिक रूप से उपलब्ध है, और विश्वसनीय, संवेदनशील माप है कि कम रिएजेंट और पश्चिमी दाग जैसे पारंपरिक प्रोटीन परख की तुलना में नमूनों की आवश्यकता में आसानी शामिल हैं, एंजाइम से जुड़े immunoassay, और अन्य प्रारूपों3,4,5. यह इस तकनीक के पिछले आकलन में उल्लेख किया गया है कि प्रोटीन का आकार सीमा है कि मूल्यांकन किया जा सकता है उपलब्ध जुदाई मैट्रिक्स द्वारा सीमित किया गया है4, लेकिन हाल ही में प्रसाद 2 से मध्यम श्रेणी का विस्तार किया है ४४० केडीए17 . इसके अलावा, कुछ lysate बफ़र्स परख18के साथ असंगत होने के लिए जाना जाता है, इसलिए उपयोग प्रयोगात्मक एजेंट का चयन पहले से विचार किया जाना चाहिए ।
व्यावसायिक रूप से उपलब्ध घटकों के साथ एक स्वचालित प्रक्रिया का एक प्रमुख लाभ मानकीकृत विधियों और रिएजेंटों के माध्यम से परिणामों की निरंतरता है । इस प्रक्रिया के भीतर महत्वपूर्ण कदम स्वचालित द्वारा परख विफलता की संभावना को कम करता है । हालांकि, यह ध्यान दें कि कुछ प्रथाओं का पालन किया जाना चाहिए करने के लिए प्रोटोकॉल के दौरान केशिका electrophoretic-आधारित immunoassay के साथ समस्याओं को कम करने के लिए महत्वपूर्ण है । सबसे पहले, यह महत्वपूर्ण है कि luminol-S/पेरोक्साइड मिश्रण ताजा और प्लेट लदान से पहले तुरंत तैयार है । अनुरूप समय अनुरूप luminescence में ऑक्सीकरण एजेंट, जो परख के बाद एक विशेष एंटीबॉडी परख के लिए सुसंगत माप में परिणाम होगा जोड़ा जाता है के बाद परिणाम होगा । इसके अलावा, यह महत्वपूर्ण है कि गैर समय सीमा समाप्त एजेंट उपयोग किया जाता है, जो मुख्यतः ऑक्सीकरण एजेंट की शक्ति को प्रभावित करता है । इसके अतिरिक्त, यह महत्वपूर्ण है कि नमूने के लोडिंग आदेश, एंटीबॉडी, और अंय एजेंट सख्ती से पीछा किया ( चित्र 1देखें) । किसी भी repipetted जगह से बाहर परख असफलता और एक व्यर्थ चलाने में परिणाम होगा ।
इन महत्वपूर्ण कदमों के अलावा, प्राथमिक तकनीक के साथ अनुभवी मुद्दों को आम तौर पर अनुकूलन के माध्यम से दूर किया जा सकता है । दरअसल, इन शर्तों प्रत्येक मॉडल प्रणाली/एंटीबॉडी संयोजन के लिए विशिष्ट है और इसलिए प्रत्येक नए परख के लिए empirically निर्धारित किया जाना चाहिए । इस अनुच्छेद में, हम तीन आम अनुकूलन प्रक्रियाओं पर ध्यान केंद्रित: जोखिम समय, lysate अनुमापन, और प्राथमिक एंटीबॉडी कमजोर पड़ने । मध्यम श्रेणी का परिणाम उत्पंन करने की क्षमता एक जोखिम समय के विश्लेषण पर निर्भर करता है जब luminol सब्सट्रेट तेजी से समाप्त नहीं किया जा रहा है, संकेत के नुकसान में सब्सट्रेट कमी परिणाम के रूप में. Lysate अनुमापन प्रत्येक परख है, जो विभिंन मॉडल प्रणालियों के साथ अलग कर सकते है के रैखिक गतिशील रेंज निर्धारित करता है, साथ ही साथ विभिंन एंटीबॉडी, यहां तक कि एक ही प्रोटीन लक्ष्य के लिए । एंटीबॉडी कमजोर पड़ने पर या संतृप्त सांद्रता के पास चुना संकेत में परिवर्तन सुनिश्चित करने के लिए मुक्त एंटीबॉडी की कमी से प्रभावित नहीं होगा, लेकिन केवल उपलब्ध प्रोटीन लक्ष्य epitope की मात्रा अलग करके । अनुकूलन प्रक्रिया के दौरान अंय विचार एंटीबॉडी मशीन समय और स्टैकिंग/नमूना लोड समय शामिल हो सकते हैं । ज्यादातर मामलों में साधन के लिए डिफ़ॉल्ट सेटिंग्स संकल्प और संवेदनशीलता का सबसे अच्छा संतुलन प्रदान करते हैं । हालांकि, कुछ मामलों में, गरीब संकल्प या संवेदनशीलता इन मापदंडों का समायोजन करके सुधार किया जा सकता है ।
केशिका electrophoretic-आधारित immunoassay तरीकों तेज, कुशल, और प्रतिलिपि प्रोटीन माप प्रदान करते हैं । हालांकि इन तरीकों को मुख्य रूप से अनुसंधान और विकास सेटिंग्स में उपयोग किया गया है, इन प्रौद्योगिकियों की निरंतरता विनियामक और नैदानिक अनुप्रयोगों में संभावित उपयोगिता है । उदाहरण के लिए, पर्यावरणीय विषालु के लिए अतिसंवेदनशील उपजनसंख्याों की पहचान या रोग की प्रगति के साथ रोगियों को सुलभ मैट्रिक्स में मापा प्रोटीन के आधार पर कर सकते हैं, रक्त, मूत्र, और लार जैसे. के रूप में रिएजेंट और आपरेशन लागत ड्रॉप और नमूनों और लक्ष्य है कि एक साथ वृद्धि का आकलन किया जा सकता की संख्या, हम संभावना केशिका electrophoretic-आधारित immunoassay अनुप्रयोगों के इन प्रकार के लिए इस्तेमाल किया तरीकों को देखेंगे ।
Divulgations
The authors have nothing to disclose.
Acknowledgements
लेखक के लिए अमेरिकी EPA अनुसंधान और विकास के कार्यालय के कीथ Tarpley-अनुसंधान त्रिकोण पार्क (ORD-RTP) ग्राफिक और विकास, टेप, और अनुदेशात्मक वीडियो के संपादन के लिए मीडिया टीम का शुक्रिया अदा करना चाहूंगा । हम भी अपने डेटा के अनुकूलन के बारे में उपयोगी बातचीत के लिए ProteinSimple से दबोरा Pritchett शुक्रिया अदा करना चाहूंगा। जेएम Guynn अमेरिका पर्यावरण संरक्षण एजेंसी में ओक रिज विज्ञान और शिक्षा अनुसंधान/भागीदारी कार्यक्रम के लिए संस्थान द्वारा समर्थित किया गया था ।
Materials
| Wes instrument | ProteinSimple (Santa Clara, CA) | 004-600 | |
| P53 DO-1 primary antibody | Santa Cruz Biotechnology, Inc. | sc-126 | |
| phosphorylated p53 (ser 15) primary antibody | Cell Signaling Technology | 9286 | |
| phosphorylated p53 (ser 20) primary antibody | Cell Signaling Technology | 9287 | |
| alpha-tubulin primary antibody | Cell Signaling Technology | 3873 | used as a loading control |
| Compass Software | ProteinSimple (Santa Clara, CA) | provided with the Wes | |
| 12-230 kDa Master kit | ProteinSimple (Santa Clara, CA) | PS MK02 (since replaced by a new kit #) | |
| www.proteinsimple.com/consumables_sw_wes.html | INCLUDES PART NO: Wash Buffer (60 mL) 042-202 10X Sample Buffer (440 μL) 042-195 Pre-Filled Microplates (8) PS-PP01 Capillary Cartridges (8) PS-CC01 Antibody Diluent II (20 mL) 042-203 Luminol-S (1.5 mL) 042-233 Peroxide (1.5 mL) 042-234 Streptavidin-HRP (132 μL) 042-414 Standard Pack (8): Biotinylated ladder, fluorescent 5X master mix, DTT, and empty 0.6 mL tube PS-ST01 Anti-Rabbit Secondary Antibody 042-206 or Anti-Mouse Secondary Antibody 042-205 |
||
| Name | Company | Catalog Number | Comments |
| Cell culture, treatment, and harvest (using vendor recommended protocols; protocols not included in manuscript) | |||
| BEAS-2B cells | American Type Culture Collection (ATCC, Manassas, VA) | CRL-9609 | |
| keratinocyte growth medium, KGM Gold | Lonza Ltd (Basel, Switzerland) | 192152 | for cell culture |
| keratinocyte basal medium, KBM Gold | Lonza Ltd (Basel, Switzerland) | 192151 | serum free medium for chemical dosing |
| doxorubicin | Sigma-Aldrich (St. Louis, MO) | D1515 | |
| Coomassie Blue Bradford Assays | ThermoFisher Scientific (Waltham, MA) | 23200 | for protein quantification |
| Nuclear Extract kit | Active Motif (Carlsbad, CA) | D1515 | used to prepare whole cell lysates |
| INCLUDES: | |||
| Lysis Buffer AM1 | |||
| 1M dithiothreitol (DTT) | |||
| Protease Inhibitor Cocktail | |||
| 10X PBS | |||
| Phosphatase Inhibitors | |||
References
- Bradley, H. L., Sabnis, H., Pritchett, D., Bunting, K. D. . Hematopoietic stem cell protocols. 1185, (2014).
- Guo, L., Eldridge, S., Furniss, M., Mussio, J., Davis, M. Use of Human Induced Pluripotent Stem Cell-Derived Cardiomyocytes (hiPSC-CMs) to Monitor Compound Effects on Cardiac Myocyte Signaling Pathways. Curr Protoc Chem Biol. 7 (3), 141-185 (2015).
- Chen, J. Q., et al. Absolute quantitation of endogenous proteins with precision and accuracy using a capillary Western system. Anal Biochem. 442 (1), 97-103 (2013).
- Chen, J. Q., Wakefield, L. M., Goldstein, D. J. Capillary nano-immunoassays: advancing quantitative proteomics analysis, biomarker assessment, and molecular diagnostics. J Transl Med. 13, 182 (2015).
- Liu, S., et al. The Application of a Novel Nanovolume Capillary Electrophoresis- Based Protein Analysis System in Personalized & Translational Medicine Research. J Bioanal Biomed. S3 (004), (2013).
- ProteinSimple Western. . Size Assay Development Guide, Revision 1. , (2014).
- Eaton, S. L., et al. A guide to modern quantitative fluorescent western blotting with troubleshooting strategies. J Vis Exp. (93), (2014).
- Eslami, A., Lujan, J. Western blotting: sample preparation to detection. J Vis Exp. (44), (2010).
- Silva, J. M., McMahon, M. The fastest Western in town: a contemporary twist on the classic Western blot analysis. J Vis Exp. (84), e51149 (2014).
- Thorn, C. F., et al. Doxorubicin pathways: pharmacodynamics and adverse effects. Pharmacogenet Genomics. 21 (7), 440-446 (2011).
- Ernst, O., Zor, T. Linearization of the bradford protein assay. J Vis Exp. (38), (2010).
- Taira, N., Yoshida, K. Post-translational modifications of p53 tumor suppressor: determinants of its functional targets. Histol Histopathol. 27 (4), 437-443 (2012).
- Thompson, T., et al. Phosphorylation of p53 on key serines is dispensable for transcriptional activation and apoptosis. J Biol Chem. 279 (51), 53015-53022 (2004).
- Currier, J. M., Cheng, W. Y., Menendez, D., Conolly, R., Chorley, B. N. Developing a Gene Biomarker at the Tipping Point of Adaptive and Adverse Responses in Human Bronchial Epithelial Cells. PLoS One. 11 (5), e0155875 (2016).
- Moser, A. C., Hage, D. S. Capillary electrophoresis-based immunoassays: principles and quantitative applications. Electrophoresis. 29 (16), 3279-3295 (2008).
- Shintani, H. . Handbook of Capillary Electrophoresis Applications. , (1997).
- . Wes reagents and consumables :: ProteinSimple Available from: https://www.proteinsimple.com/consumables_sw_wes.html (2017)

