Comportamento de fase de vesículas carregadas em solução simétrica e assimétrica condições monitoradas com microscopia de fluorescência
Summary
Experimentos na fase separado unilamellar gigante vesículas (GUVs) frequentemente negligenciam condições de solução fisiológica. Este trabalho apresenta abordagens para estudar o efeito de buffer de alta salinidade na separação de fases líquido-líquido em GUVs multicomponentes carregadas como uma função de trans-membrana solução assimetria e temperatura.
Abstract
Vesículas separada fase gigante unilamellar (GUVs) exibindo coexistindo ordenada pelo líquidom e líquido-desordenada domínios são uma ferramenta comum de Biofísica para investigar a hipótese de balsa lipídica. Inúmeros estudos, no entanto, negligenciam o impacto de condições de solução fisiológica. Por conta disso, o trabalho atual apresenta o efeito da assimetria de solução tampão e trans-membrana alta salinidade na separação de fases líquido-líquido em GUVs carregados desenvolvidos dioleylphosphatidylglycerol, ovo esfingomielina e colesterol. Os efeitos foram estudados sob condições isotérmicas e variação de temperatura.
Descrevemos equipamentos e estratégias experimentais aplicáveis para monitorar a estabilidade dos domínios líquidos coexistentes em vesículas carregadas sob condições de solução de alta salinidade simétrica e assimétrica. Isso inclui uma abordagem para preparar GUVs multicomponentes carregados no buffer de alta salinidade, temperaturas elevadas. O protocolo implica a opção de realizar uma troca parcial da solução externa por uma etapa de diluição simples, minimizando a diluição de vesículas. Uma abordagem alternativa é apresentada utilizando um dispositivo microfluidic que permite uma troca de solução externa completa. Os efeitos da solução na separação de fases também foram estudados sob diferentes temperaturas. Para tal, apresentamos o projeto básico e a utilidade de uma câmara de controle de temperatura construído in-house. Além disso, refletimos sobre a avaliação do estado de fase GUV, armadilhas associados e como burlá-los.
Introduction
Já desde a observação dos domínios de micro-empresas em vesículas de líquido-líquido fase separada gigante unilamellar (GUVs) por microscopia de fluorescência, GUVs têm sido usados como um sistema modelo para investigar os lipídios jangada hipótese1,2 , 3 . Como a área de sua BICAMADA autônoma encontra-se no intervalo do que de células biológicas, que são imita apropriada das membranas de plasma apresentando as balsas hipotéticos. Foram realizados numerosos estudos sobre tais GUVs com vesículas dispersadas em água pura, sacarose ou soluções de baixa salinidade4,5,6,7,8. Nestas condições, no entanto, não refletem exposição fisiologicamente relevantes de biomembranas para ambientes de alta salinidade e trans-membrana solução assimetria como são as condições para as células.
Neste trabalho e em uma publicação anterior do nosso grupo9, os Estados de fase da carga GUVs multicomponentes foram examinados em função da presença de assimetria de sal e solução através da membrana. GUVs foram preparados a partir de misturas de diferentes proporções de dioleoylphosphatidylglycerol (DOPG), ovo esfingomielina (eSM) e colesterol (Chol) em solução de sacarose (com osmolaridade de 210 mOsm/kg) ou buffer de alta salinidade (100 mM de NaCl, 10 mM Tris, pH 7,5, 210 mOsm/kg). A escolha de lipídios foi justificada pelos dados já obtidos no diagrama de fase desta mistura6,8.
Um número de métodos para a preparação de GUVs está disponível na literatura10,11,12 (Observe que, aqui, não consideraremos os que envolvem a transferência de lipídios de à base de óleo para uma fase aquosa 13 , 14 por causa do perigo inerente dos restantes resíduos óleo na membrana, que pode afetar o comportamento de fase). A preparação de GUVs no buffer de alta salinidade está associada com desafios específicos. Para soluções de baixa força iônica, o método de electroformation15,16 apresenta uma maneira rápida para preparar GUVs em rendimentos elevados com pequenos defeitos de10,17. O método baseia-se depositar uma camada de lipídios sobre uma superfície condutora (eletrodo), secá-los e hidratante-los com uma solução aquosa, enquanto aplicando um campo de AC. No entanto, este método requer ajustes se o sal está presente na solução aquosa18,19. Presume-se que a força motriz para o crescimento da vesícula por electroformation é electroosmosis16 que é dificultado em altas condutividades20. Portanto, electroswelling de GUVs em soluções de alta salinidade não é uma abordagem direta como necessita de otimização para as diferentes concentrações de sal presentes na solução inchaço. Assistida por gel de vesículas inchaço21,22 é uma alternativa potencial para electroformation com tempos de formação ainda mais rápidos. Esta abordagem baseia-se a hidratação do filme lipídico reforçada quando um gel (agarose ou álcool polivinílico (PVA)) é usado como substrato. Essas abordagens, no entanto, vêm com o risco de contaminação da membrana no caso baseada em agarose inchaço23 e/ou temperatura limites como no caso do inchaço baseada em PVA. Da mesma forma, um protocolo para crescer GUVs sobre um substrato de papel de celulose foi recentemente estabelecido24. Questões gerais desse método são a falta de controle sobre a pureza do substrato, bem como o uso de grandes quantidades de lipídios. Neste trabalho, iremos apresentar e apresentar as vantagens do método mais tradicional para a preparação de chefe, nomeadamente a espontânea inchaço método25,26. Consiste de uma camada lipídica sobre um substrato lipofóbico, hidratante-lo na atmosfera de vapor de água e inchaço subsequente na solução desejada inchaço de secagem (ver Figura 1 e detalhes na seção de protocolo). Este método não oferece controle sobre a distribuição de tamanho de vesículas e resulta em vesículas no geral menores em comparação com métodos onde a produção é assistida por campo elétrico, substrato de polímero ou microfluidic significa. No entanto, a qualidade de vesículas e o tamanho é apropriado para examinar o estado de fase de membrana como explorada aqui.
Criação de assimetria entre as soluções através da membrana da vesícula está associado com determinados desafios também. Uma abordagem comumente usada é a diluição direta da suspensão vesículas na solução externa desejada27,28. No entanto, isso também diminui a densidade de distribuição de vesículas. Outra estratégia é lentamente, trocar a solução externa em torno de GUVs, estabeleceu-se na parte inferior de uma pilha de fluxo que permite a solução de em – e saída. Para evitar perturbar ou mesmo perdendo as vesículas com o fluxo, taxas de fluxo baixas são aplicadas8, que processa esta abordagem tempo-ineficiente. Além disso, nenhuma dessas abordagens garante solução completa externa troca. Uma solução óbvia é para imobilizar vesículas para evitar perdê-los durante uma troca de solução externa. Por exemplo, biotinilado GUVs pode ser amarrado em uma superfície revestida streptavidin29. No entanto, esta abordagem pode levar a variações composicionais no aderidas e daí a membrana não-aderido segmentos30,31. Da aplicação magnética ou campos elétricos para aprisionar os resultados de vesículas na membrana de impor tensão32. Empregando a Pinça óptica para interceptar uma vesícula requer ter uma alça anexada (ou seja, uma pérola), enquanto o uso de macas ópticos pode envolver aquecimento local33. Captura de GUVs também pode ser realizada por cultivá-las em fios de platina sem desprendimento final34. Isso no entanto produz vesículas que não são isolados e geralmente ligados aos fios ou outras vesículas por tubos fina lipídico (amarras).
O trabalho apresentado destaca estratégias para superar as limitações acima referidas. Primeiro, apresentamos uma descrição detalhada do método inchaço espontâneo adaptado e otimizado para a produção de GUVs nos buffers de alta salinidade. Em seguida apresentamos duas abordagens para eficientemente criar condições de solução assimétrica por simples diluição ou a utilização de um dispositivo microfluidic. Porque o nosso objectivo é a análise do estado de fase membrana de GUVs em condições diferentes da solução, as seções subsequentes descrevem critérios para a análise estatística de sucesso e dicas de presentes para evitar falsa categorização.
As análises foram realizadas em condições isotérmicas, assim como sob temperaturas diferentes. Enquanto a temperatura control é comumente empregado, detalhes sobre câmaras de temperatura-controle experimental são raramente descritos. Aqui, apresenta-se uma configuração construída in-house para observar GUVs em diferentes condições de temperatura.
Protocol
Representative Results
Discussion
Produção de sucesso de GUVs para observações de estado de fase em condições de alta salinidade simétricas e assimétricas
Os protocolos aqui apresentados apresenta uma estratégia para avaliar a influência de assimetria de buffer e a solução de alta salinidade em estado de fase de membrana de GUVs carregadas sobre uma escala larga das composições. Um dos principais desafios para alcançar este objetivo foi a produção de GUVs carregados nos buffers de alta salinidade.
Nós produzimos com sucesso GUVs em solução de sacarose e alta-solução salina tampão por uma simples abordagem inchaço espontânea, que inclui uma etapa de pré-hidratação do filme lipídico depositado e uma etapa final de hidratação durante a noite para crescimento de vesículas. É importante notar que a deposição de lipídios deve ser feita em uma placa PTFE áspera para garantir lipídico mesmo espalhar-se para produzir vesículas unilamellar. Além disso, é essencial para executar cada passo durante a preparação de vesículas em uma temperatura onde o filme lipídico está em um estado de fase fluida e homogênea. Outra coisa, a população de vesículas pode ser polydisperse na composição e influenciar a análise de estado de fase final da população. O protocolo específico para o inchaço espontâneo de GUVs rende uma moita de vesículas que por um lado, oferece a possibilidade de re-suspendê-lo em pequenos volumes para obter altamente concentrada dispersões de vesículas e por outro lado, fornece solução assimétrica condições através da membrana, minimizando a diluição das vesículas8,28. É essencial que durante a diluição de vesículas ou solução externa trocar, dentro e fora osmolarities permanecem combinado como alterações de morfologia causadas por incompatibilidades de osmolaridade podem induzir ou impedir de separação de fase Lo + Ld41 ou, no caso de hipotônica condições, pode levar à vesícula estourando.
Aqui, tenta otimizar protocolos de electroformation em solução de alta salinidade resultou na produção de não GUVs enquanto inchaço PVA-assistida rendeu vesículas multilamellar. Mesmo que ele requer mais longos tempos de preparação e resultados em lotes de vesículas de inferior qualidade10,17, o sucesso da produção de vesículas carregadas por espontânea inchaço vem com vantagens adicionais. Exige um esforço mínimo ao mesmo tempo, resultando em rendimentos suficientes para análises de estatística em lotes e, ao contrário de electroformation, sem equipamentos sofisticados ou otimização foram necessárias. Além disso, sem contaminações por oxidação lipídica têm sido observadas42,43. De acordo com a literatura não há nenhuma diferença entre as composições lipídicas das vesículas e as ações correspondentes do qual eles foram cultivados7,17. Além disso, a formação de vesículas sobre um substrato PTFE não solicita a inclusão de quaisquer contaminações em contraste com gel-assistida métodos inchaço onde moléculas estrangeiras podem ser introduzidas pelo substrato23. Electroformation vem com mais inconvenientes relacionados à diluição excessiva vesículas ao criar condições de solução assimétrica. GUVs produzidos por electroformation estão normalmente presentes como uma dispersão homogênea (em contraste com a suspensão de vesículas altamente concentrado na forma de um grupo formado durante o inchaço espontâneo). Qualquer diluição da solução externa diluiria substancialmente o número de vesículas também. Além disso, ao longo deste trabalho, observou-se que DOPG/eSM/Chol GUVs produziram pela electroformation em sacarose tornou-se instável, se diluído em tampão de alta salinidade. Fluorescência de patches de lipídios do slide de microscópio indicado que vesículas explodiriam antes sua inspeção visual foi possível. Tal instabilidade pode ser atribuída a uma tensão elevada da membrana das vesículas preparado pela electroformation em comparação com aqueles obtidos por inchaço espontâneo10.
Embora a diluição de vesícula é uma abordagem fácil e rápida para criar condições de solução GUV assimétricas, ele apenas realiza uma troca parcial solução externa, embora em uma fração de alta (aqui: 95%, Figura 2), como após diluição, vestígios de que o solução de inchaço permanecerá. A escolha do grau da troca da solução externa é um trade-off entre pipetagem até a moita de vesículas em conjunto com a solução de inchaço (seção 2) e não diluir demais. Portanto, nós introduzimos uma abordagem alternativa microfluidic discutida em outra parte em detalhe37 que permite uma troca rápida e completa solução externa durante observações de estado de fase de chefe para verificar as fase estado de observações para diluído vesículas. As observações de variações de estado de fase quando se muda de simétrica para condições de solução assimétrica de fato foram observadas para estar de acordo. Além disso, ambos os métodos para gerar condições de solução assimétrica mostradas aqui são comparativamente rápido (comparar ref.8) e vem sem riscos conhecidos de alterações de composição local (comparar referências30,31), aumento da tensão de membrana (comparar referência32), ou aquecimento local (comparar referência33), quanto os métodos alternativos discutido na introdução. Durante a captura de microfluidic, um equilíbrio osmótico entre a vesícula interior e o exterior não é apenas essenciais para evitar artefatos de estado de fase como mencionado acima, mas também causada por condições de solução hipertônica de deflação podem causar os GUVs presos a escorregar através do posts depois de uma troca de solução externa.
Mesmo que o inchaço espontâneo foi aplicado com sucesso para crescer sem carga vesículas de um sistema DOPC/eSM/Chol, em outros casos, a ausência de cargas podem afectar o GUV inchaço devido a consequente falta de repulsão entre os bilayers individuais44 . Estendendo o período pré-inchaço ou introduzindo headgroups volumosos lipídica pode contrariar esta questão45. Além disso, a estabilidade da vesícula após sua diluição em soluções diferentes daquele usado para inchaço pode diferir para composições diferentes lipídios e meios de diluição, que aqui não temos investigado. Também não exploramos a possibilidade de ajustar o diâmetro médio do chefe com o método de preparação aqui apresentado. Mas parâmetros tais como a composição de vesículas e inchaço solução são susceptíveis de influenciar os resultados. A aplicação de métodos alternativos46 pode produzir vesículas maiores para os lipídios e soluções utilizados aqui, no entanto, eles podem vir com outros inconvenientes associados com o método. A abordagem acima descritas para produzir GUVs em condições de alta salinidade simétricas e assimétricas fornece uma ferramenta potencial para estudos adicionais de vesículas constituído por composições diferentes lipídios e dispersos em diferentes meios. Que não exploramos as possibilidades, futuros julgamentos mostrará como geralmente os métodos de preparação e diluição de chefe podem ser aplicados.
Observando a separação de fases em diferentes temperaturas
Existem diferentes configurações experimentais adequadas para estudar GUVs a diferentes temperaturas. Enquanto essas configurações não são comumente descritas em detalhe dentro da literatura, o trabalho atual apresenta uma montagem básica aplicável para tais estudos.
_content “> controle medições mostram que a temperatura disto internamente projetou e construiu a câmara é precisamente controlada por um termostato e gradientes de temperatura dentro da Câmara estão dentro da resolução de temperatura experimental. Assegura-se que as condições experimentais térmicas são consistentes com a leitura do termostato.
Durante a avaliação dos Estados de fase chefe sobre uma escala de temperatura larga, é importante que as observadas vesículas são bem equilibradas após a temperatura ter sido alterada. Uma maneira de assegurar isto é para verificar se há histerese. Se houver histerese, os passos de temperatura devem ser diminuídos e/ou vezes de equilibração aumentaram. Como temperatura controle neste trabalho é estabelecida por um termóstato à base de água, a gama de temperaturas de funcionamento está idealmente limitada a 0 – 100 ° C. Este intervalo pode ser expandido usando outros líquidos de controle de temperatura como óleo ou empregando outras configurações, por exemplo, um dispositivo Peltier. Na prática, a temperatura também é limitada pela possível condensação ou evaporação. Além disso, para temperaturas longe da temperatura ambiente, a ocorrência de um gradiente de temperatura de estado estacionário em toda a câmara de observação se torna mais provável. Além disso, os equipamentos de imagem podem ser prejudicado em temperaturas extremas. Para intervalos de temperatura típico apropriados para estudos de vesículas lipídicas (~ 10-50 ° C7,9) danos ao equipamento de observação devem ser considerado, mas normalmente não é esperado.
Artefatos de observação de domínio de vesículas
Há um número de fontes para artefatos de observação usando microscopia de fluorescência de campo amplo. Primeiro de tudo, um deve estar ciente de que a resolução máxima r do objeto aplicado para a inspeção visual dos Estados de fase de vesículas determina o limite de detecção dos domínios de lipídios de acordo com:
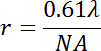
onde λ é o comprimento de onda de emissão, e nd é a abertura numérica do objectivo. Um objetivo típico com um 40 x ampliação e um at de 0,6 que detecta de emissão verde acender cerca de 560 nm atingiria uma resolução óptica de ~0.6 µm. portanto, estudos que comparam a Estados de fase de vesículas, feitas a partir de misturas de lipídios particular entre diferentes condições devem usar o mesmo objectivo para a mesma mistura de lipídios.
Outro artefato é a ocorrência de domínios de lipídios em consequência da foto-oxidação lipídica devido a uma exposição prolongada à luz de excitação41. Foto-dano ocorre preferencialmente em metades de lipídios de hidrocarboneto insaturado. Na verdade, algumas composições de lipídios, tal formação de domínio das vesículas inicialmente homogêneas foi observada aqui após um longo período de exposição à luz de excitação (~ 30 s). Para combater esse problema, a luz de excitação foi mantida focada em um campo de visão por apenas alguns segundos para a avaliação do estado de fase. Portanto, o DiIC18 era adequado para os nossos propósitos. Outros corantes, no entanto, podem ser muito mais sensíveis e podem precisar de ser tratado em intensidades de excitação mais baixas e com tempos de exposição à luz de excitação mais curtos.
Tensão de cisalhamento mecânico da transferência das vesículas pipeta mistura potencialmente domínios temporariamente, assim, distorcer o comportamento de fase de vesículas aparentes. Para alguns lotes, vesículas diferentes apresentaram comportamentos diferentes fase 0 min e 5 min após a pipeta de transferência no sentido do lamela de microscópio. Também a tensão de cisalhamento induzida pelo fluxo do fluido no dispositivo microfluidic tem demonstrado resultar em domínio47de mistura. Vesículas devem ser deixadas sem ser perturbado por uma quantidade suficiente de tempo para equilíbrio antes de observação. Dentro deste estudo, vesículas presas no dispositivo microfluidic foram deixadas sem ser perturbado por 1h após o carregamento de vesícula e as trocas de solução antes de observação.
Para evitar alguns das dificuldades acima mencionadas, bem como a restrição imposta pelo limite de difração de luz, métodos alternativos, tais como espectroscopia de ressonância magnética nuclear48 ou de técnicas de microscopia de super resolução49 poderia ser empregada.
Conclusão e perspectivas
O trabalho apresentado demonstra um conjunto de métodos que permite a análise da influência das condições de alta salinidade simétrica e assimétrica solução na separação de fases de membrana. Todos os métodos apresentados são adequados para outras aplicações. O dispositivo microfluidic, por exemplo, fornece uma plataforma para estudar a cinética de formação de domínio e desaparecimento após a indução de assimetria de solução. Além disso, aparência de domínio em função da concentração de sal poderia ser analisada assim. Todos os métodos também podem ser usados para examinar a influência sobre o comportamento de fase usando outras soluções de interesse.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Este trabalho é parte do consórcio MaxSynBio, que é financiado conjuntamente pelo Ministério Federal da educação e pesquisa da Alemanha e a sociedade Max Planck.
Materials
| 1,2-dioleoyl-sn-glycero-3-phospho-(1'-rac-glycerol), sodium salt | Avanti Polar Lipids | 840475C | abbreviated as DOPG in the text |
| chicken egg sphingomyelin | Avanti Polar Lipids | 860061 | abbreviated as eSM |
| cholesterol (ovine wool, > 98 %) | Avanti Polar Lipids | 700000 | abbreviated as Chol |
| 1,1'-dioctadecyl-3,3,3',3'-tetramethylindocarbocyanine perchlorate | Molecular Probes | D-282 | abbreviated as DiIC18 |
| Chloroform, HPLC grade (≥ 99.8 %) | Merck | ||
| NaCl (> 99.8 %) | Roth | ||
| HCl (37 %) | Roth | ||
| Tris (≥ 99.9 %) | Roth | ||
| Sucrose (≥ 99.5 %) | Sigma Aldrich | ||
| Parafilm | |||
| Threaded vial 45×27 mm, 15 mL | Kimble | Soda flat bottom, white screw cap | |
| pH meter | Mettler Toledo | MP220 | |
| Osmometer | Gonotec | Osmomat030 | |
| Epi-fluorescence microscope | Zeiss | Axio Observer D1 | |
| Confocal laser scanning microscope | Leica | TCS SP5 | |
| Objective 40x, 0.6 NA | Zeiss | LD Achroplan | |
| Objective 40x, 0.75 NA | Leica | 506174 | |
| Objective 63x, 0.9 NA | Leica | 506148 | |
| Microscope slide, 56×26 mm, 0.17 ± 0.01 mm | Menzel-Gläser | ||
| Cover slip, 22×22 mm, 0.17 ± 0.01 mm | Menzel-Gläaser | ||
| Parafilm "M" | Bremix Flexible Packaging | ||
| Syringes, 5 mL, 10 mL | Braun | ||
| 0.45 µm syringe filter | GVS North America | Cameo 25AS, 1213723 | Acetate, sterile |
References
- Dietrich, C., et al. Lipid rafts reconstituted in model membranes. Biophys J. 80 (3), 1417-1428 (2001).
- Bagatolli, L. A. To see or not to see: lateral organization of biological membranes and fluorescence microscopy. Biochim Biophys Acta. 1758 (10), 1541-1556 (2006).
- Carquin, M., D’Auria, L., Pollet, H., Bongarzone, E. R., Tyteca, D. Recent progress on lipid lateral heterogeneity in plasma membranes: From rafts to submicrometric domains. Prog Lipid Res. 62, 1-24 (2016).
- Baumgart, T., Hess, S. T., Webb, W. W. Imaging coexisting fluid domains in biomembrane models coupling curvature and line tension. Nature. 425 (6960), 821-824 (2003).
- Bacia, K., Schwille, P., Kurzchalia, T. Sterol structure determines the separation of phases and the curvature of the liquid-ordered phase in model membranes. Proc Natl Acad Sci U S A. 102 (9), 3272-3277 (2005).
- Vequi-Suplicy, C. C., Riske, K. A., Knorr, R. L., Dimova, R. Vesicles with charged domains. Biochim Biophys Acta. 1798 (7), 1338-1347 (2010).
- Blosser, M. C., Starr, J. B., Turtle, C. W., Ashcraft, J., Keller, S. L. Minimal effect of lipid charge on membrane miscibility phase behavior in three ternary systems. Biophys J. 104 (12), 2629-2638 (2013).
- Pataraia, S., Liu, Y., Lipowsky, R., Dimova, R. Effect of cytochrome c on the phase behavior of charged multicomponent lipid membranes. Biochim Biophys Acta. 1838 (8), 2036-2045 (2014).
- Kubsch, B., Robinson, T., Lipowsky, R., Dimova, R. Solution Asymmetry and Salt Expand Fluid-Fluid Coexistence Regions of Charged Membranes. Biophys J. 110 (12), 2581-2584 (2016).
- Dimova, R., et al. A practical guide to giant vesicles. Probing the membrane nanoregime via optical microscopy. J Phys Condens Matter. 18 (28), S1151-S1176 (2006).
- Liu, A. P., Fletcher, D. A. Biology under construction: in vitro reconstitution of cellular function. Nat Rev Mol Cell Biol. 10 (9), 644-650 (2009).
- Walde, P., Cosentino, K., Engel, H., Stano, P. Giant Vesicles: Preparations and Applications. Chembiochem. 11 (7), 848-865 (2010).
- van Swaay, D., deMello, A. Microfluidic methods for forming liposomes. Lab Chip. 13 (5), 752-767 (2013).
- Stein, H., Spindler, S., Bonakdar, N., Wang, C., Sandoghdar, V. Production of Isolated Giant Unilamellar Vesicles under High Salt Concentrations. Front Physiol. 8, 63 (2017).
- Angelova, M. I., Dimitrov, D. S. Liposome Electroformation. Faraday Discuss. 81, 303-311 (1986).
- Dimitrov, D. S., Angelova, M. I. Lipid swelling and liposome formation mediated by electric fields. Bioelectrochemistry and Bioenergetics. 19, 323-336 (1988).
- Rodriguez, N., Pincet, F., Cribier, S. Giant vesicles formed by gentle hydration and electroformation: a comparison by fluorescence microscopy. Colloids Surf B Biointerfaces. 42 (2), 125-130 (2005).
- Montes, L. R., Alonso, A., Goni, F. M., Bagatolli, L. A. Giant unilamellar vesicles electroformed from native membranes and organic lipid mixtures under physiological conditions. Biophys J. 93 (10), 3548-3554 (2007).
- Pott, T., Bouvrais, H., Meleard, P. Giant unilamellar vesicle formation under physiologically relevant conditions. Chem Phys Lipids. 154 (2), 115-119 (2008).
- Green, N. G., Ramos, A., Gonzalez, A., Morgan, H., Castellanos, A. Fluid flow induced by nonuniform ac electric fields in electrolytes on microelectrodes. I. Experimental measurements. Phys Rev E Stat Phys Plasmas Fluids Relat Interdiscip Topics. 61 (4 Pt B), 4011-4018 (2000).
- Horger, K. S., Estes, D. J., Capone, R., Mayer, M. Films of Agarose Enable Rapid Formation of Giant Liposomes in Solutions of Physiologic Ionic Strength. J Am Chem Soc. 131 (5), 1810-1819 (2009).
- Weinberger, A., et al. Gel-Assisted Formation of Giant Unilamellar Vesicles. Biophys J. 105 (1), 154-164 (2013).
- Lira, R. B., Dimova, R., Riske, K. A. Giant Unilamellar Vesicles Formed by Hybrid Films of Agarose and Lipids Display Altered Mechanical Properties. Biophys J. 107 (7), 1609-1619 (2014).
- Kresse, K. M., Xu, M., Pazzi, J., Garcia-Ojeda, M., Subramaniam, A. B. Novel Application of Cellulose Paper As a Platform for the Macromolecular Self-Assembly of Biomimetic Giant Liposomes. ACS Appl Mater Interfaces. 8 (47), 32102-32107 (2016).
- Reeves, J. P., Dowben, R. M. Formation and properties of thin-walled phospholipid vesicles. J Cell Physiol. 73 (1), 49-60 (1969).
- Needham, D., Evans, E. Structure and Mechanical-Properties of Giant Lipid (DMPC) Vesicle Bilayers from 20-Degrees-C Below to 10-Degrees-C above the Liquid-Crystal Crystalline Phase-Transition at 24-Degrees-C. Biochimie. 27 (21), 8261-8269 (1988).
- Manneville, J. B., et al. COPI coat assembly occurs on liquid-disordered domains and the associated membrane deformations are limited by membrane tension. Proc Natl Acad Sci U S A. 105 (44), 16946-16951 (2008).
- Wollert, T., Wunder, C., Lippincott-Schwartz, J., Hurley, J. H. Membrane scission by the ESCRT-III complex. Nature. 458 (7235), 172 (2009).
- Kuhn, P., et al. A facile protocol for the immobilisation of vesicles, virus particles, bacteria, and yeast cells. Integr Biol (Camb). 4 (12), 1550-1555 (2012).
- Sarmento, M. J., Prieto, M., Fernandes, F. Reorganization of lipid domain distribution in giant unilamellar vesicles upon immobilization with different membrane tethers. Biochim Biophys Acta. 1818 (11), 2605-2615 (2012).
- Lipowsky, R., Rouhiparkouhi, T., Discher, D. E., Weikl, T. R. Domain formation in cholesterol-phospholipid membranes exposed to adhesive surfaces or environments. Soft Matter. 9 (35), 8438 (2013).
- Korlach, J., Reichle, C., Muller, T., Schnelle, T., Webb, W. W. Trapping, deformation, and rotation of giant unilamellar vesicles in octode dielectrophoretic field cages. Biophys J. 89 (1), 554-562 (2005).
- Delabre, U., et al. Deformation of phospholipid vesicles in an optical stretcher. Soft Matter. 11 (30), 6075-6088 (2015).
- Fidorra, M., Garcia, A., Ipsen, J. H., Hartel, S., Bagatolli, L. A. Lipid domains in giant unilamellar vesicles and their correspondence with equilibrium thermodynamic phases: a quantitative fluorescence microscopy imaging approach. Biochim Biophys Acta. 1788 (10), 2142-2149 (2009).
- Bezlyepkina, N., Gracia, R. S., Shchelokovskyy, P., Lipowsky, R., Dimova, R. Phase diagram and tie-line determination for the ternary mixture DOPC/eSM/cholesterol. Biophys J. 104 (7), 1456-1464 (2013).
- Eyer, K., Kuhn, P., Stratz, S., Dittrich, P. S. A microfluidic chip for the versatile chemical analysis of single cells. J Vis Exp. (80), e50618 (2013).
- Robinson, T., Kuhn, P., Eyer, K., Dittrich, P. S. Microfluidic trapping of giant unilamellar vesicles to study transport through a membrane pore. Biomicrofluidics. 7 (4), 44105 (2013).
- Veatch, S. L., Gawrisch, K., Keller, S. L. Closed-loop miscibility gap and quantitative tie-lines in ternary membranes containing diphytanoyl PC. Biophys J. 90 (12), 4428-4436 (2006).
- Kolesinska, B., et al. Interaction of beta(3) /beta(2) -peptides, consisting of Val-Ala-Leu segments, with POPC giant unilamellar vesicles (GUVs) and white blood cancer cells (U937)–a new type of cell-penetrating peptides, and a surprising chain-length dependence of their vesicle- and cell-lysing activity. Chem Biodivers. 12 (5), 697-732 (2015).
- Robinson, T., et al. Removal of background signals from fluorescence thermometry measurements in PDMS microchannels using fluorescence lifetime imaging. Lab Chip. 9 (23), 3437-3441 (2009).
- Morales-Penningston, N. F., et al. GUV preparation and imaging: minimizing artifacts. Biochim Biophys Acta. 1798 (7), 1324-1332 (2010).
- Zhou, Y., Berry, C. K., Storer, P. A., Raphael, R. M. Peroxidation of polyunsaturated phosphatidyl-choline lipids during electroformation. Biomaterials. 28 (6), 1298-1306 (2007).
- Breton, M., Amirkavei, M., Mir, L. M. Optimization of the Electroformation of Giant Unilamellar Vesicles (GUVs) with Unsaturated Phospholipids. J Membr Biol. 248 (5), 827-835 (2015).
- Lasic, D. D., Needham, D. The “stealth” liposome: a prototypical biomaterial. Chemical Reviews. 95, 2601-2628 (1995).
- Needham, D., McIntosh, T. J., Lasic, D. D. Repulsive interactions and mechanical stability of polymer-grafted lipid membranes. Biochim Biophys Acta. 1108 (1), 40-48 (1992).
- Akashi, K., Miyata, H., Itoh, H., Kinosita, K. Preparation of giant liposomes in physiological conditions and their characterization under an optical microscope. Biophys J. 71 (6), 3242-3250 (1996).
- Sturzenegger, F., Robinson, T., Hess, D., Dittrich, P. S. Membranes under shear stress: visualization of non-equilibrium domain patterns and domain fusion in a microfluidic device. Soft Matter. 12 (23), 5072-5076 (2016).
- Veatch, S. L., Polozov, I. V., Gawrisch, K., Keller, S. L. Liquid domains in vesicles investigated by NMR and fluorescence microscopy. Biophys J. 86 (5), 2910-2922 (2004).
- Owen, D. M., Magenau, A., Williamson, D., Gaus, K. The lipid raft hypothesis revisited–new insights on raft composition and function from super-resolution fluorescence microscopy. Bioessays. 34 (9), 739-747 (2012).

