Le protocole présenté ici permet la reproduction d’une démyélinisation généralisée de la matière grise des deux hémisphères corticaux chez les rats Dark Agouti mâles adultes. La méthode comprend l’implantation intracérébrale d’un cathéter, l’immunisation subclinique contre la glycoprotéine oligodendrocytaire de myéline et l’injection intracérébrale d’un mélange de cytokines pro-inflammatoires à travers le cathéter implanté.
Research Article
Modèle de rat de démyélinisation corticale cérébrale généralisée induite par une injection intracérébrale de cytokines pro-inflammatoires
In This Article
Summary
Abstract
La sclérose en plaques (SEP) est la maladie à médiation immunitaire la plus courante du système nerveux central (SNC) et entraîne progressivement une invalidité physique et la mort, causée par des lésions de la substance blanche dans la moelle épinière et le cervelet, ainsi que par la démyélinisation dans la matière grise. Alors que les modèles conventionnels d’encéphalomyélite allergique expérimentale conviennent à l’étude de l’inflammation à médiation cellulaire dans la substance blanche spinale et cérébelleuse, ils ne parviennent pas à traiter les pathologies de la matière grise. Nous présentons ici le protocole expérimental d’un nouveau modèle de démyélinisation corticale chez le rat permettant d’enquêter sur les mécanismes pathologiques et moléculaires conduisant à des lésions corticales. La démyélinisation est induite par une immunisation avec de la glycoprotéine oligodendrocytaire de myéline (MOG) à faible dose dans un adjuvant de Freund incomplet, suivie d’une administration intracérébrale médiée par cathéter de cytokines pro-inflammatoires. De plus, le cathéter permet plusieurs cycles de démyélinisation sans provoquer de traumatisme induit par injection, ainsi que l’administration intracérébrale de médicaments thérapeutiques potentiels faisant l’objet d’une investigation préclinique. La méthode est également favorable sur le plan éthique car la douleur et la détresse ou le handicap des animaux sont contrôlés et relativement minimes. Le délai prévu pour la mise en œuvre de l’ensemble du protocole est d’environ 8 à 10 semaines.
Introduction
La SEP est une maladie inflammatoire du SNC à médiation immunitaire, qui endommage principalement les feuilles de myéline, mais conduit finalement à la perte axonale et à des lésions neuronales permanentes. La SEP est la maladie à médiation immunitaire la plus courante du SNC avec une prévalence estimée à environ 2,3 millions de personnes dans le monde, selon la National MS Society1, et représente un fardeau personnel et socio-économique majeur. L’âge moyen d’apparition de la maladie est de 30 ans et entraîne la perte d’années productives en causant une invalidité grave. La SEP est actuellement incurable, et les modalités actuelles de traitement visent à gérer les symptômes lors d’une rechute aiguë dans la SEP récurrente-rémittente et à modifier l’évolution de la maladie pour diminuer la fréquence des rechutes par un traitement immunomodulateur2,3. Aucune option de traitement ne s’est encore avérée efficace pour les typesprogressifs 4,à l’exception d’un essai clinique récent de traitement appauvrissant les cellules B, qui s’est avéré efficace chez un sous-groupe de patients atteints de SEP progressive primaire (SEP-PP) présentant une inflammation active5. Bien que plusieurs facteurs de risque génétiques6 etenvironnementaux 7 potentiels aient été identifiés, l’étiologie de la SEP reste toutefois inconnue.
La SEP est caractérisée par de grandes plaques inflammatoires démyélinisantes dans la substance blanche8,9et des lésions diffuses de la substance blanche . Les lésions focales ont été associées à une attaque étendue médiée par les lymphocytes T, à la destruction des oligodendrocytes, à l’astrogliose réactive et à la dégénérescence axonale, entraînant un déclin des motoneurones. La démyélinisation et l’atrophie de la matière grise ont été reconnues comme des caractéristiques histopathologiques supplémentaires de la maladie9,10,11. Ce dernier a été suggéré pour contribuer au dysfonctionnement neurologique et au déclin cognitif chez les patients12,13. Trois schémas de démyélinisation corticale ont été distingués, à savoir i) leucocortical, contiguë aux lésions de la substance blanche (34%), ii) petites, périvasculaires (16%) et iii) sous-pieuses (50%). Contrairement aux lésions focales de la substance blanche, il a été rapporté que ces lésions de la matière grise n’ont pas d’attaque médiée par les lymphocytes T et sont plutôt caractérisées par une activation microgliale améliorée, une apoptose et une perte neuronale12.
À ce jour, il n’a pas été possible de récapituler la SEP humaine dans un seul modèle animal, en grande partie en raison de la complexité de la maladie. Une variété de modèles animaux de SEP, chacun simulant différents aspects de la pathogenèse et de la progression de la maladie, ont plutôt été développés14,15. Les modèles animaux actuels imitent trois processus pathologiques différents : i) les lésions inflammatoires focales, ii) les lésions diffuses de la substance blanche et iii) la pathologie de la matière grise diffuse.
Des études animales sur les plaques de substance blanche de sep ont principalement été menées dans des modèles d’encéphalomyélite à rongeurs (EAE). Les animaux d’essai sont activement immunisés avec une émulsion contenant un antigène de myéline [généralement la glycoprotéine oligodendrocytaire de myéline (MOG)16,17, la protéine de base de la myéline (MBP)18, ou la protéine protéolipide (PLP)19], ainsi qu’un adjuvant complet de Freund (CFA)20. La maladie peut également être induite passivement par un transfert adoptif de lymphocytes T spécifiques de la myéline21. L’évolution de la maladie dépend de la combinaison antigène/souche de souris utilisée. MOG35-55 dans C57BL/6, par exemple, entraîne une maladie chronique monophasique22, tandis que PLP139-151 chez les souris suisses Jim Lambert (SJL) conduit à une maladie récurrente-rémittente23 d’une manière spécifique au sexe24. Le MOG35-55du rat induit en outre une réponse encéphalitogénique des lymphocytes T, tandis que le MOG35-55 humain induit une inflammation dépendante des cellules B chez les souris C57BL/625. Divers modèles EAE fournissent un excellent outil pour étudier l’inflammation à médiation cellulaire principalement dans la moelle épinière et le cervelet, mais les structures du cerveau antérieur comme le cortex, le corps calleux et les structures sous-corticales restent largement épargnées26. Ni les lésions diffuses de la substance blanche ni la démyélinisation de la matière grise ne sont, en outre, reproduites de manière adéquate dans les modèles EAE26,27. Une démyélinisation corticale associée à une induction active de l’EAE a été rapportée chez les ouistitis28,29 et dans certaines sous-souches de rats Lewis, dans ce dernier cas attribuée aux combinaisons prédominantes d’isotypes et d’allèles de classe I et de classe II du CMH30.
Le modèle cuprizone31 est un outil utile pour étudier la démyélinisation diffuse de la substance blanche et la pathologie de la matière grise avec une démyélinisation étendue des régions corticale, sous-corticale32et hippocampique33, ainsi que du corps calleux34 et du putamencaudé 35. L’intoxication à la cuprizone, qui entraîne en principe l’apoptose des oligodendrocytes induite par le stress métabolique, imite certaines caractéristiques des lésions démyélinisantes corticales du cerveau de la SEP, telles qu’une activation de la microglie, l’astrogliose et un manque relatif d’infiltration des cellules immunitaires périphériques. L’absence d’apoptose neuronale et d’atrophie thalamique, ainsi que la résolution complète de la démyélinisation avec une remyélinisation robuste observée à l’arrêt de la supplémentation alimentaire en cuprizone32,limitent toutefois l’utilisation de l’intoxication par la cuprizone comme modèle préclinique de SEP. La démyélinisation toxique peut également être induite par une injection focale de lysolécithine ou de bromure d’éthidium dans les voies de la substance blanche36,37, mais ces méthodes sont rarement utilisées. Les modèles de démyélinisation toxiques sont particulièrement adaptés à l’analyse des mécanismes complexes de la remyélinisation, tels que l’exigence de cellules progénitres oligodendrocytes et d’astrocytes38,39. Des informations détaillées sur les modèles d’EAE et d’intoxication sont fournies dans deux revues récentes15,40.
La démyélinisation induite par les cytokines a été initialement développée pour étudier les lésions de la substance blanche spinale dans EAE41. Plus tard, il a été modifié pour étudier les pathologies de la matière grise corticale chez les rats MS. Dark Agouti (DA) ou Lewis sont d’abord amorcés par une immunisation subclinique avec MOG1-12542,43 ou MOG1-11644 dans un adjuvant de Freund (IFA) incomplet. Contrairement aux modèles EAE classiques, ces animaux amorcés ne présentent pas de symptômes cliniques de lésions inflammatoires focales dans la moelle épinière. Au lieu de cela, une réponse inflammatoire et une démyélinisation dans le cerveau sont ensuite obtenues par une administration intracérébrale d’un mélange de cytokines pro-inflammatoires [facteur de nécrose tumorale alpha (TNFα) et interféron gamma (IFNγ)] une fois que les animaux ont atteint un titre stable d’anticorps anti-MOG dans le sang.
Études de Merkler et al. 42 et Gardner et coll. 44 ont prouvé l’efficacité d’une induction de démyélinisation corticale sous-piale par une immunisation MOG subclinique et une injection intracérébrale ou sous-arachnoïdienne de cytokines. La durée rapportée de la démyélinisation était cependant trop courte - une remyélinisation complète s’est produite en 14 jours ou moins, limitant ainsi la fenêtre pour tout test d’intervention pharmacologique. Les deux modèles, en outre, utilisent un modus d’injection traumatique, qui pourrait en soi provoquer un traumatisme d’injection et une dégradation de la barrière hémato-encéphalique (BHE) et ainsi conduire à un recrutement incontrôlé de cellules inflammatoires dans le parenchyme. Les deux études, en outre, ont démontré une démyélinisation limitée à une zone limitée, dans le cortex ipsilatéral, ou à proximité du site d’injection de cytokines.
Pour surmonter ces limitations, nous avons implanté un cathéter dans le cortex pariétal droit de rats DA, avec l’extrémité du cathéter située juste au-dessus du corps calleux. Pour permettre une récupération complète de l’intégrité de la BHE, les animaux ont eu droit à une période de repos de 2 semaines après l’implantation du cathéter. Par la suite, les rats ont été immunisés subcliniquement avec 5 μg de MOGrecombinant 1-125 dans l’IFA. Après l’obtention d’un titre d’anticorps anti-MOG stable après environ 4 semaines, 2 μL de mélange de cytokines ont été injectés via le cathéter en 10 minutes à l’aide d’une pompe à seringue programmable. Cette procédure a provoqué une démyélinisation corticale généralisée des hémisphères cérébral ipsi- et controlatéral en 15 jours, avec une remyélinisation partielle environ 30 jours après l’injection de cytokines43. De multiples phases de démyélinisation pourraient, en outre, être induites par l’administration répétée de cytokines pro-inflammatoires à travers le cathéter, et l’atrophie cérébrale globale, caractéristique commune des sous-types45progressifs de SEP, pourrait être induite dès la deuxième phase de démyélinisation43. Il est important de savoir que le cathéter implanté pourrait également être utilisé pour tester des interventions pharmacologiques.
Le protocole décrit ci-dessous fournit une explication détaillée des étapes expérimentales pour une génération reproductible de démyélinisation corticale généralisée dans les deux hémisphères cérébraux de rats DA à l’aide d’un cathéter intracérébral.
Protocol
Toutes les méthodes décrites ici ont été approuvées par les autorités locales (Bundesministerium für Wissenschaft und Forschung (ministère autrichien de la Science et de la Recherche); Numéro de licence : 66.010/0132-WF/V/3b/2014). Les rats DA mâles adultes (âgés de 10 à 12 semaines) ont été logés dans un cycle lumière/obscurité de 12/12 h avec un accès libre à la nourriture et à l’eau.
1. Préparation du matériel
REMARQUE: La chirurgie est effectuée dans des conditions aseptiques. Avant de commencer, assurez-vous que tous les instruments chirurgicaux, y compris les forets, sont nettoyés avec un désinfectant approprié.
- Préparer un mélange anesthésique : 0,02 mg/mL de fentanyl, 0,4 mg/mL de midazolam et 0,2 mg/mL de médétomidine (concentrations finales dans le mélange).
REMARQUE: Voir la section de discussion respective pour les anesthésiques alternatifs. - Préparer un mélange antidote : 0,07 mg/mL de flumazénil et 0,42 mg/mL d’atipamézole (concentrations finales dans le mélange).
- Assemblez le cathéter et le capuchon du cathéter avec l’entrée et la vis. Coupez le cathéter à une longueur de 2 mm avec un scalpel (Figure 1).
REMARQUE: N’utilisez pas de ciseaux pour cela, car ils compriment et déforment la forme circulaire de la section transversale de la pointe du cathéter.
2. Préparation chirurgicale
- Anesthésier le rat par une administration intrapéritonéale (i.p.) du mélange anesthésique (1,5 mL/kg de poids corporel).
- Rasez la tête du rat entre les oreilles à l’aide du rasoir électrique. Placez une couverture homéotherme sur le cadre stéréotaxique avant de positionner l’animal, pour éviter l’hypothermie tout au long de la chirurgie.
- Immobilisez la tête du rat dans le cadre stéréotaxique à l’aide des barres d’oreille et de la plaque de morsure, en veillant à ce que la tête soit horizontale et stable. Vérifiez la stabilité en appliquant une pression sur le crâne avec le doigt ou la pince.
REMARQUE: Une fixation lâche et un positionnement non horizontal dans le cadre stéréotaxique peuvent entraîner un écart par rapport aux coordonnées prévues. - Appliquez des gouttes oculaires lubrifiantes pour prévenir la sécheresse de la cornée pendant la chirurgie. Couvrez les yeux avec un matériau opaque pour éviter toute exposition chirurgicale à la lumière.
- Nettoyez la zone rasée en alternant l’application de 70% d’éthanol et de 10% de complexe povidone-iode.
REMARQUE: Suivez toutes les mesures de précaution pendant la chirurgie pour éviter l’infection. La chirurgie est réalisée dans des conditions aseptiques. Si l’asepsie est cassée, le matériau contaminé doit être remplacé.
3. Implantation de cathéter
- Faites une incision longitudinale d’environ 2 cm de longueur au milieu de la peau de la tête. Utilisez des pinces bulldog pour retenir la peau sur les côtés. Pour une vue d’ensemble de ces étapes, reportez-vous à la Figure 2.
- Retirez le sang à l’aide d’un applicateur à pointe de coton.
- Retirez le périoste du crâne. Nettoyez le tissu avec l’applicateur à pointe de coton et exposez l’os du crâne. Laissez sécher le crâne pendant environ 1 min.
- Identifiez les repères anatomiques, Lambda, Bregma et la suture médiale. Avec la perceuse installée sur le cadre stéréotaxique, positionnez la pointe de la perceuse au Bregma comme point de départ. Déplacez-vous de 2 mm postérieur à partir du Bregma et déplacez~2,4 mm latéralement vers la suture médiale.
- Percez un trou de 0,5 mm de diamètre pour le cathéter à cette position. Enlevent doucement toute poussière osseuse.
REMARQUE: Il est important que la dure-mère reste intacte pendant le forage. Pour ce faire, 1) utilisez une perceuse qui peut être installée sur le cadre stéréotaxique, 2) inspectez fréquemment le trou pendant le forage et 3) forez par petites étapes - si trop de pression est appliquée sur le crâne, la pointe de la perceuse continuera et endommagera le cerveau lorsque le crâne est complètement pénétré. - Percez 3 autres trous (~ 1,3 mm de diamètre) pour les vis d’ancrage à quelques millimètres du premier trou. Soufflez doucement la poussière d’os.
REMARQUE: Sélectionnez les emplacements des vis d’ancrage qui offrent suffisamment d’espace pour le dessus du cathéter (~ 2 mm de diamètre) et le dessus de la vis d’ancrage (~ 1 mm). - Enlever la poussière osseuse par irrigation avec environ 1 à 2 mL de solution saline tamponnée au phosphate stérile (PBS) ou de solution saline physiologique à l’aide d’une seringue. Nettoyez le crâne. Serrez les vis d’ancrage de 2 à 3 tours complets.
REMARQUE: Les vis d’ancrage sont nécessaires pour stabiliser la configuration en maintenant le ciment dentaire et, par conséquent, le cathéter en place. Tout en serrant une vis d’ancrage, assurez-vous qu’elle n’est pas facilement amovible en la soulevant doucement vers le haut avec une pince. Étant donné que l’implantation du cathéter lui-même provoque un traumatisme tissulaire, une blessure supplémentaire à la dura lors du forage ou du serrage des vis d’ancrage entraînera de multiples blessures traumatiques et entravera éventuellement la comparabilité au sein d’un groupe. Serrez d’abord les vis d’ancrage et insérez le cathéter en dernier. - Insérez le cathéter de 2 mm de longueur à travers le premier trou, perpendiculairement à la surface du crâne. Tout en maintenant le cathéter, appliquez un peu de ciment dentaire et laissez-le polymériser avec une brève exposition (~ 5 s) à la lumière de durcissement dentaire pour stabiliser le cathéter, permettant l’utilisation des deux mains à l’étape suivante.
ATTENTION: Lorsque vous travaillez avec une lumière de durcissement dentaire, évitez de regarder directement la pointe ou la lumière réfléchie par la zone d’application, car la forte intensité de cette lumière peut causer des dommages à la rétine. Utilisez des lunettes de protection appropriées. - Appliquez plus de ciment dentaire autour du cathéter, ancrez les vis et solidifiez le ciment dentaire avec la lumière de durcissement dentaire (~ 15 - 30 s). Confirmez le durcissement du ciment avec la pointe d’une pince.
4. Fermeture de la plaie et antagonisation de l’anesthésie
- Fermez la peau de la tête avec des sutures résorbables, antérieures et postérieures au cathéter.
REMARQUE: Comme il y aura une configuration bosselée sur le crâne à la fin de l’implantation, faites la fermeture de la plaie en conséquence. Soulever trop la peau entraînera un inconfort pour l’animal. - Injecter le mélange d’antidote par voie sous-cutanée (1,5 mL/kg de poids corporel) à l’aide d’une seringue de 1 mL avec une aiguille de 26 G.
- Administrer l’enrofloxacine (2,5 %) par injection sous-cutanée (7,5 mg/kg de poids corporel) pour un traitement antibiotique prophylactique. Administrer du carprofène (1 mg/mL; 5 mg/kg de poids corporel) et de la buprénorphine (1,2 mg/kg) pour soulager la douleur par injection sous-cutanée.
5. Soins postopératoires et médicaments
- Revenir l’animal dans la cage modifiée et le garder sous observation pendant 1 à 3 h, avec une application de lumière infrarouge pour éviter l’hypothermie. Observez et repositionnez constamment l’animal toutes les 5 à 10 minutes jusqu’à la récupération postopératoire. Prenez des précautions particulières pour éviter une exposition constante à la lumière des yeux jusqu’à la récupération.
- Répétez les administrations d’enrofloxacine (7,5 mg/kg de poids corporel) et de carprofène (1 mg/mL; 5 mg/kg de poids corporel) par injections sous-cutanées le lendemain de la chirurgie. La buprénorphine n’est pas nécessaire pour être rafraîchie car le traitement précédent est efficace pendant 72 heures.
6. Préparation du mélange d’immunisation (au plus tôt 14 jours après l’implantation du cathéter)
Remarque: Placez les seringues sur de la glace pendant la procédure de préparation.
- Connectez deux seringues en verre à pointe de verrouillage Luer de 10 mL aux bras courts d’un robinet d’arrêt à 3 voies et fermez la troisième sortie avec le bras long.
- Assurez-vous que les connexions sont sécurisées et sans fuite : ajoutez environ 4 mL de PBS stérile à la seringue ouverte tout en maintenant le piston 2. Insérez le piston 1 et poussez les deux pistons d’avant en arrière tout en vérifiant les fuites. Si aucune fuite ne se produit, jetez le PBS et retirez à nouveau le piston 1.
- Pipette 1 mL d’IFA et 50 μg de rMOG1-125 ensemble et ajuster le mélange à un volume final de 2 mL avec du PBS stérile (pH 7,4) dans un tube approprié.
REMARQUE: En raison des pertes d’émulsion sur les extrémités ou les parois des seringues pendant la préparation, préparez un volume plus important que celui prévu pour l’administration. Il est également plus pratique de se préparer pour plus de 1 animal à la fois. - Placer le mélange IFA et rMOG1-125 dilué dans la seringue ouverte. Insérez doucement le piston tout en maintenant une pression lâche sur le piston opposé(Figure 3A).
- Émulsionner l’inoculum en le conduisant d’une seringue à l’autre en poussant les pistons d’avant en arrière, jusqu’à ce qu’il soit blanc et visqueux (Figure 3B).
- Fixez une seringue de verrouillage Luer de 1 mL au bras court ouvert du robinet d’arrêt à 3 voies et remplissez-la d’inoculum (Figure 3C). Répartir tout l’inoculum dans des seringues de 1 mL. Gardez-le sur la glace jusqu’à l’injection. Administrer le mélange le jour de la préparation.
7. Immunisation
- Anesthésier le rat avec de l’isofluorane dans une chambre (~2 min, mélangé avec de l’oxygène 2 L/min) puis maintenir l’anesthésie à travers un masque (mélangé avec de l’oxygène 1,5 L/min).
- Injecter 200 μL d’inoculum par voie sous-cutanée à la base de la queue à l’aide d’une aiguille de 21 G.
REMARQUE: Administrer l’injection lentement car la solution est visqueuse.
8. Détermination des titres d’anticorps
- Prélever environ 200 μL de sang 4 semaines après l’immunisation afin de déterminer les titres d’anticorps anti-MOG.
- Enduire les puits d’une plaque de 96 puits de MOG (5 μg/mL en PBS) et les incuber pendant 1 h à 37 °C.
- Bloquer la plaque avec 1% d’albumine sérique bovine (BSA) dans du PBS pendant 1 h à température ambiante.
- Incuber la plaque avec du sérum de rat (1:50) et la standardiser pendant 2 h à 37 °C. Lavez la plaque 3x avec 200 μL de PBS/Polysorbate 20.
- Incuber la plaque avec un anticorps secondaire IgG conjugué à la peroxydase de raifort (1:10 000). Lavez la plaque 3x avec 200 μL de PBS/Polysorbate 20.
- Ajouter 100 μL de solution de substrat de peroxydase par puits et l’incuber pendant 20 à 30 min dans l’obscurité à température ambiante.
- Mesurez la densité optique à une longueur d’onde de 405 nm et calculez le titre d’anticorps à partir de la densité optique à l’aide d’une courbe standard.
9. Injection intracérébrale de cytokines
- Réglez la longueur de la canule du connecteur (2 mm). (Voir la figure 4 pour les étapes de préparation.)
- Remplir une seringue de 1 mL avec le mélange de cytokines (500 ng/μL de TNF-alpha, 300 U/μL d’IFN-gamma recombinant de rat dans du PBS stérile). Connectez la seringue à une canule de connexion. Remplissez la canule avec le mélange de cytokines. Évitez les bulles.
- Montez la seringue sur la pompe à seringue programmable et programmez-la pour injecter 0,2 μL/min(Figure 5A). Démarrez la pompe et maintenez-la en état de fonctionnement afin d’éviter la formation de bulles d’air à l’extrémité de la canule.
REMARQUE: La vitesse d’injection doit tenir compte du diamètre intérieur de la seringue spécifique utilisée; ainsi, le diamètre de la seringue doit être enregistré lors de la mise en place de la pompe. - Anesthésier le rat avec de l’isoflurane dans une chambre (~2 min, mélangé à 2 L/min d’oxygène) puis maintenir l’anesthésie à travers un masque (mélangé à 1,5 L/min d’oxygène)(Figures 5B et 5C). Appliquez des gouttes oculaires lubrifiantes car l’animal sera anesthésié pendant au moins 30 minutes.
- Retirez le capuchon du cathéter avec l’entrée. Insérez la canule du connecteur dans le cathéter et la vissez et serrez-la(figures 5D et 5E).
REMARQUE: Ne le serrez pas trop, car cela détruirait l’extrémité supérieure du cathéter. - Laisser l’injection se poursuivre pendant 10 min (le volume total d’injection étant de 2 μL). Arrêtez la pompe. Laissez la canule à l’intérieur du cathéter pendant 20 minutes pour permettre au volume injecté de diffuser complètement.
- Dévissez la canule du connecteur et retirez-la lentement pour éviter un effet de vide.
- Reconnectez le capuchon du cathéter à l’entrée et vissez-le. Permettre à l’animal de se remettre de l’anesthésie dans une cage.
Results
La démyélinisation corticale pourrait être évaluée à différents moments après une injection de cytokines par immunohistochimie pour la protéine protéolipide (PLP) (Figure 6). La figure 6A montre l’immunoréactivité PLP intacte au jour 15 chez un animal témoin immunisé par MOG qui n’a reçu que du PBS stérile par le biais du cathéter implanté. Le jour 1 après l’injection de cytokines, la démyélinisation pouvait déjà être détectée chez les animaux amorcés par MOG, mais seulement à proximité de la zone cathétérisée (Figure 6B). L’immunoréactivité PLP reste intacte dans le cortex controlatéral 1 jour après l’injection de cytokines. Le jour 3, une augmentation progressive de la perte de l’immunoréactivité PLP, qui se propage dans le cortex ipsilatéral(Figure 6C),a pu être observée. La démyélinisation corticale controlatérale a également pu être détectée au jour 3(Figure 6D),mais elle est plutôt limitée à la zone située sous les vis d’ancrage, peut-être en raison d’une zone de faible débit de liquide interstitiel causée par les vis d’ancrage43. L’absence d’une observation similaire chez les animaux témoins injectés de PBS exclut la possibilité d’une démyélinisation induite par un traumatisme provenant de la vis d’ancrage.
Entre les jours 9 à 15, la démyélinisation affecte de grandes parties du cortex des deux hémisphères(figures 6E, 6Fet 6G). Cela coïncide avec une observation de comportement lent, mais sans diminution statistiquement significative de la motricité dans un test de rotarod43. La démyélinisation corticale est maintenue jusqu’à 30 jours après l’injection de cytokines dans les deux hémisphères(figures 6H et 6I)avec seulement une remyélinisation partielle. La figure 6J montre une quantification de la perte de PLP dans la matière grise corticale après l’injection intracérébrale de cytokines. Il convient de noter que l’immunoréactivité PLP n’a pas encore été évaluée après des périodes de plus de 30 jours; ainsi, la résolution instantanée de la remyélinisation, s’il y en a, reste à évaluer par d’autres expérimentations. Une deuxième administration de mélange de cytokines à travers le cathéter implanté 30 jours après la première injection entraîne une atrophie cérébrale marquée au jour 15(Figure 7).

Figure 1: Préparation du cathéter. (A et B) La canule guide et la canule factice (capuchon du cathéter avec entrée) sont assemblées et vissées. (C) Ensuite, le cathéter est coupé à 2 mm de taille à l’aide d’un scalpel. L’observation microscopique a montré que l’utilisation de ciseaux à cette fin déforme la forme circulaire de la pointe de la canule et, par conséquent, doit être évitée. Veuillez cliquer ici pour voir une version agrandie de cette figure.
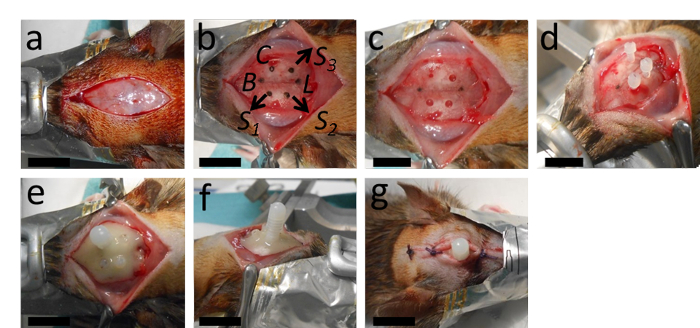
Figure 2: L’implantation du cathéter. (A) La chirurgie commence par une incision longitudinale et l’ablation du périoste. (B, C) Ce panneau montre le marquage de la place du cathéter à 2 mm postérieur de Bregma et à 2,4 mm latéral à droite de la suture sagittale; ainsi que les emplacements des trous destinés aux trois vis d’ancrage à une distance appropriée du cathéter et du Lambda. (D) Après avoir percé le trou du cathéter (un diamètre de 0,5 mm, avec une pointe de perçage ronde) et les trous pour les vis d’ancrage (1,3 mm de diamètre avec une pointe de perçage torsadée), les vis d’ancrage sont serrées. (E, F) Ensuite, le cathéter est inséré et toute la configuration est stabilisée avec du ciment dentaire polymérisant. (G) La plaie est cousue avec deux ou trois nœuds antérieurs et postérieurs au cathéter. B = Bregma; L = Lambda; C = Cathéter; S1, S2 et S3 = emplacements pour les trous des trois vis d’ancrage. Les barres d’échelle = 1 cm. Veuillez cliquer ici pour voir une version plus grande de cette figure.
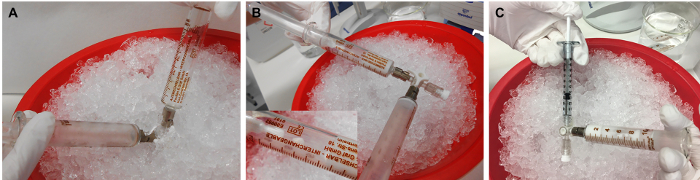
Figure 3: Préparation de l’émulsion rMOG/IFA. (A) Le mélange de rMOG, PBS et IFA est émulsionné en pressant l’inoculum d’une seringue à l’autre en poussant les pistons d’avant en arrière, (B) jusqu’à ce qu’il soit blanc et visqueux. (C) Par la suite, l’inoculum est distribué à 1 mL de seringues pour l’injection. 5 μg de rMOG sont utilisés dans 200 μL de mélange PBS/IFA pour immuniser cliniquement un rat; cependant, en raison des pertes aux extrémités et aux parois des seringues pendant la préparation, un plus grand volume doit être préparé. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 4: Préparation de la canule du connecteur. (A - D) Ces panneaux montrent comment un connecteur et un interne sont assemblés avec une canule de guidage de gabarit de 2 mm. (E) L’interne est coupé à la même taille que la canule de guidage à l’aide d’un scalpel (F) et le guide de gabarit est ensuite dévissé. (G) L’autre extrémité de la canule du connecteur est fixée à une seringue de 1 mL, qui contient le mélange d’injection, avec une aiguille de 20 G. Les barres d’échelle = 3 cm. Veuillez cliquer ici pour voir une version plus grande de cette figure.

Figure 5: Injection intracérébrale. (A) Une pompe à seringue programmable est ajustée pour une vitesse d’injection de 2 μL/min, et la seringue de 1 mL remplie de mélange de cytokines (ou pbS stérile pour les commandes) est montée sur la pompe. (B) L’animal est d’abord anesthésié dans la chambre en utilisant 5% d’isoflurane avec un débit d’oxygène de 2 L / min, puis (C) l’anesthésie est maintenue à travers le masque en utilisant 2,5% d’isoflurane avec un débit d’oxygène de 1,5 L / min. (D) Le capuchon du cathéter avec l’entrée (la canule factice) est vissé et la canule d’injection est insérée à travers le cathéter implanté. Étant donné que le volume de l’injection est très faible, l’investigateur doit être prudent pour éviter les bulles d’air à l’extrémité de la canule. Pour cette raison, il est important de commencer l’insertion pendant que la pompe est en fonctionnement et uniquement lorsqu’il y a une bulle de liquide en croissance à la pointe. Le volume supplémentaire n’ira pas dans le cerveau de toute façon, car il se décompose sur le dessus du cathéter avant l’insertion. (E) Ensuite, la canule du connecteur est serrée et la pompe est laissée fonctionner pendant 10 min. Après 10 min d’injection, la pompe est arrêtée et la canule est laissée à l’intérieur pendant 15 à 20 min pour permettre la diffusion du volume injecté dans le liquide interstitiel. Les barres d’échelle = 5 cm, sauf indication contraire. Veuillez cliquer ici pour voir une version agrandie de cette figure.
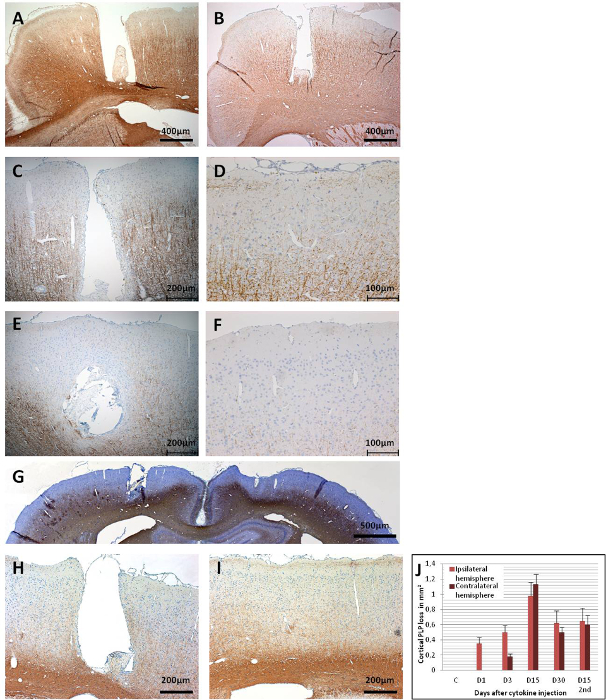
Figure 6: Immunoréactivité PLP dans les coupes coronales du cerveau. (A) Ce panel montre un cerveau témoin (MOG-amorcé) avec une injection de PBS (jour 15), qui n’entraîne pas de démyélinisation corticale. (B) Dès le jour 1 post-injection de cytokines, la démyélinisation est apparente dans la zone du cathéter. (C) Une perte plus large d’immunoréactivité PLP est observée dans le cortex ipsilatéral au jour 3, (D) ainsi qu’au niveau du côté controlatéral. Une perte généralisée de l’immunoréactivité PLP est observée dans les deux hémisphères au jour 15, car (E) ce panneau montre le cortex ipsilatéral et (F) ce panneau montre le cortex controlatéral. (G) Un aperçu des deux hémisphères est donné en montrant la perte généralisée de PLP au jour 15. Au jour 30, comme (H) ce panneau montre le cortex ipsilatéral et (I) ce panneau montre pour le cortex controlatéral, il y a encore une démyélinisation remarquable, mais aussi quelques zones remyéliniques ont pu être observées. (J) Ce panel montre la quantification de la démyélinisation (perte de PLP en mm2/hémisphère). Des coupes cérébrales coronales de 1,5 à 2 μm ont été utilisées pour la détection des PLP avec un anti-PLP contre la SEP avec un facteur de dilution de 1:500. Les sections ont été contre-colorées avec de l’hématoxyline pour les noyaux cellulaires. Pour des informations détaillées sur l’immunohistochimie, voir Ucal et al. 43. Les groupes G et J ont été modifiés à partir d’Ucal et al. 43. Veuillez cliquer ici pour voir une version agrandie de cette figure.
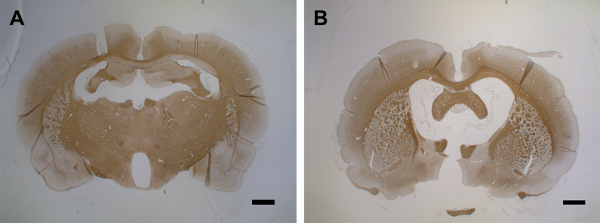
Figure 7: Atrophie cérébrale après une deuxième injection de cytokines. (A) Ce panel montre un cerveau témoin (MOG-amorcé) avec une injection de PBS (jour 15). (B) Au jour 15 après la première injection de cytokines, une deuxième injection entraîne une atrophie cérébrale dans les 15 jours. Des coupes cérébrales coronales de 1,5 à 2 μm ont été utilisées pour la détection des PLP avec un anti-PLP contre la SEP avec un facteur de dilution de 1:500. Les sections ont été contre-colorées avec de l’hématoxyline pour les noyaux cellulaires. Pour des informations détaillées sur l’immunohistochimie, voir Blakemore37. Les barres d’échelle = 500 μm. Veuillez cliquer ici pour voir une version plus grande de cette figure.

Figure 8: Cages modifiées pour empêcher le retrait du cathéter par l’animal. Dans les cages standard, l’espace du porte-nourriture sur la grille est situé plus près du fond de la cage, créant un espace étroit risqué qui augmente les chances que le cathéter s’emmêle avec la grille et, par conséquent, son retrait. Pour éviter cela, la cage doit être modifiée. Cet espace étroit était bloqué par un plan transparent, permettant le respect de l’animal. La nourriture doit être donnée à l’intérieur de la cage dans ces cages modifiées. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Discussion
Notre méthode utilise des rats DA. L’adaptation aux souris nécessitera probablement l’utilisation d’un cathéter et de vis plus petits. Il convient également de garder à l’esprit que l’évolution de la maladie, la réponse inflammatoire et l’étendue de la démyélinisation peuvent différer de ce qui est présenté ici si une espèce / souche différente est utilisée. De telles différences ont été observées avec des modèles EAE classiques utilisant différentes souches de souris. MOG92-106 d’origine rat, par exemple, a entraîné une EAE progressive primaire ou progressive secondaire chez les souris A.SW, tandis qu’elle a induit une EAE récurrente-rémittente chez les souris SJL / J46. Des animaux de la même souche devraient donc être utilisés. Des différences entre les sexes dans la manifestation de l’EAE ont également été rapportées dans diverses études antérieures24. On pourrait s’attendre à l’apparition de tels effets de genre pour le protocole décrit ici, mais il reste à valider dans d’autres expériences.
L’administration intrapéritonéale (IP) d’un mélange d’anesthésiques comprenant 0,02 mg/mL de fentanyl, 0,4 mg/mL de midazolam et 0,2 mg/mL de médétomidine est utilisée pour l’intervention chirurgicale. Les rats DA mâles adultes pesant de 270 à 300 g ont besoin d’environ 0,4 à 0,6 mL de ce mélange(c’est-à-direenviron 1,5 mL / kg) pour induire une anesthésie d’une durée de 60 à 90 min. Après la chirurgie, l’anesthésie est antagonisée par une injection sous-cutanée d’un antidote comprenant 0,07 mg/mL de flumazénil et 0,42 mg/mL d’atipamezole dans une solution saline physiologique (0,9% de NaCl). Une dose de 1 à 1,5 mL/kg antagonise l’anesthésie en 5 min. Alternativement, les animaux peuvent être autorisés à se réveiller spontanément lors d’un lavage physiologique des anesthésiques, mais dans ce cas, les animaux devraient être gardés sous observation jusqu’à ce qu’ils soient pleinement conscients.
D’autres options d’anesthésie fréquemment utilisées pour les chirurgies animales, telles qu’une injection IP de kétamine et de xylazine47 ou de pentobarbital de sodium48,ou une inhalation d’anesthésiques volatils comme l’isofluorane49 et l’halothane50,peuvent également être envisagées pour la chirurgie présentée ici. Il est toutefois essentiel de choisir un agent anesthésique qui n’interfère pas avec la ou les interventions en aval prévues.
Pendant l’immunisation et l’injection intracérébrale de cytokines, 5% d’isoflurane est utilisé pour l’anesthésie. Le modèle décrit ici a été établi à l’aide de rats, et les détails expérimentaux énumérés sont donc spécifiquement applicables au rat. Les coordonnées d’implantation du cathéter ont été sélectionnées pour permettre l’analyse simultanée d’éventuels changements de substance blanche (l’extrémité du cathéter dans le corps calleux). Alors que le site d’insertion du cathéter peut varier en fonction de la position antéropostérior et latérale, la sélection du sulcus central nécessite d’éviter d’endommager le sinus sagittal supérieur.
Une autre caractéristique de la méthode décrite est la démyélinisation équivalente des hémisphères ipsi- et controlatéral, résultant éventuellement du transport du mélange de cytokines injecté vers l’espace sous-arachnoïdien par le flux physiologique du liquide interstitiel à partir des régions corticales51. Le mode d’injection, et non l’emplacement du cathéter, provoque donc une démyélinisation dans tout le cortex cérébral, et le choix du cortex pariétal droit ou gauche devrait donc être sans importance à cet égard.
Le protocole utilise un cathéter de 26 G, qui est assez petit pour éviter une blessure traumatique étendue et assez grand pour éviter un taux accru de colmatage de la pointe du cathéter au cours de la longue période de l’expérience. Certes, l’implantation et la présence du cathéter lui-même provoquent une activation astrocytaire et microgliale, également chez les animaux témoins recevant uniquement l’implantation du cathéter; cependant, cela est mineur par rapport aux animaux injectés de cytokines. 43 Pour éviter toute interférence avec les analyses ultérieures, nous avons utilisé des cathéters compatibles IRM en poly-éther-éther-cétone (PEEK).
Une profondeur similaire de démyélinisation est, en fait, créée dans les régions ipsi- et controlatérale avec la méthode présentée. Cela implique que la profondeur / longueur du cathéter pourrait ne pas jouer un rôle majeur dans le modèle et l’étendue de la démyélinisation dans le cortex. Par conséquent, une modification de la longueur du cathéter pourrait être envisagée afin de réduire la taille de la lésion induite par le cathéter. Néanmoins, une longueur de cathéter significativement plus courte pourrait provoquer une démyélinisation corticale légèrement moins prononcée, tandis qu’une réponse concluante ne serait obtenue que par des expériences testant spécifiquement la longueur du cathéter.
L’un des avantages du modèle est que le cathéter implanté permet de tester des thérapies potentielles administrées au cortex via le cathéter pour permettre la remyélinisation au plus fort de la démyélinisation corticale histologiquement détectable (jour 15 ou plus tard), alors que dans un contexte de prétraitement, ce serait après l’immunisation mais avant l’injection de cytokines. La décision sur le délai d’administration des produits thérapeutiques dépendra donc de la question de recherche particulière et du médicament d’intérêt.
Après l’implantation du cathéter, il est important de loger les animaux seuls dans les cages modifiées (de préférence à sommet élevé) afin d’éviter le retrait du cathéter jusqu’à la fin de l’étude (Figure 8). Les animaux peuvent également dévisser le capuchon du cathéter avec l’entrée, bien que cela se produise rarement. Les animaux doivent être observés quotidiennement et les bouchons retirés doivent être remplacés par des bouchons frais, afin d’éviter le blocage de la pointe du cathéter en l’absence d’entrée et d’assurer une livraison précise dans le parenchyme après l’injection intracérébrale. Les animaux sont immunisés au plus tôt 2 semaines après l’implantation du cathéter pour permettre la guérison et la fermeture de la barrière hémato-encéphalique.
Les titres sériques d’anticorps anti-MOG doivent être mesurés après l’immunisation. Une expérience dose-réponse a montré que 5 μg de MOG1-125 (dans l’IFA) fournissaient une immunisation suffisante dans les 4 semaines chez les rats DA mâles adultes. Un titre de 5 000 μg/mL et plus serait suffisant, mais dépendra certainement de plusieurs facteurs, y compris la préparation MOG et la souche animale et, par conséquent, devra être déterminé individuellement. Il est important d’éviter des doses d’antigènes excessivement élevées présentant un phénotype EAE classique avec des membres postérieurs paralysés avant même l’injection de cytokines.
Chaque animal est immunisé avec 5 μg de glycoprotéine oligodendrocytes de myéline recombinante (rMOG1-125)émulsionnée dans 200 μL d’adjuvant de Freund (IFA) incomplet. Étant donné qu’une partie de l’émulsion est perdue dans la seringue pendant la préparation, il est conseillé de préparer plus que cette quantité pour chaque animal. Nous avons utilisé du MOG recombinant (1-125 du N-terminus du MOG de rat), qui a été exprimé dans Escherichia coli et a ensuite été purifié à homogénéité par chromatographie chélate, dissous dans de l’urée 6 M, et dialysé contre du PBS pour obtenir une préparation physiologique52,53. Cependant, le MOG disponible dans le commerce peut également être utilisé.
D’autres préparations antigéniques, telles que MOG1-116, MOG35-55 ou PLP139-151 sont utilisées dans divers modèles EAE, et les différences d’antigène et de souche animale sont connues pour induire des phénotypes de maladie distincts dans ces modèles20. Ces préparations antigéniques n’ont pas été testées chez des rats DA et, si elles sont utilisées de préférence au rMOG1-125,pourraient induire un phénotype de la maladie ou des résultats histologiques différents de ce qui est présenté ici.
Une canule de connexion de la même longueur que le cathéter est préparée avant l’injection intracérébrale. Cela peut être fait en l’assemblant avec un cathéter gabarit et en le coupant à la même taille (2 mm de longueur) (Figure 4). Il est important que la canule du connecteur soit exempte de bulles d’air pendant l’injection de cytokines - parce que le volume d’injection n’est que de 2 μL, même une minuscule bulle d’air à l’extrémité de la canule réduira considérablement le volume du liquide livré avec succès dans le cerveau. Ceci est réalisé en maintenant la pompe en marche et en insérant la canule uniquement lorsqu’une goutte croissante de liquide d’injection est présente à la pointe. Après l’insertion de la canule, le connecteur est vissé au cathéter tout en évitant un serrant excessive afin de ne pas endommager la pointe supérieure du cathéter, ce qui rendra difficile le récapitulatif après l’injection. Une vitesse d’injection de 0,2 μL/min est utilisée pour éviter les traumatismes induits par l’injection. De plus, une injection lente, combinée à une période d’attente de 20 minutes après l’injection, assure la diffusion du liquide injecté dans le liquide interstitiel et un drainage efficace dans le LCR. La canule est ensuite retirée lentement pour éviter un effet de vide.
La méthode rapportée comprend une intervention chirurgicale et, par conséquent, nécessite du personnel capable d’effectuer une chirurgie de survie stéréotaxique. Le personnel en contact direct avec les animaux aurait dû suivi les cours d’expérimentation animale appropriés. Le reste du protocole peut être effectué par des membres de laboratoire compétents.
La méthode est destinée à produire une démyélinisation du cortex cérébral déclenchée par l’inflammation et ne reproduit pas toutes les caractéristiques de la SEP humaine(par exemple,l’apparition de lésions inflammatoires focales de la substance blanche, qui est une caractéristique de la SEP humaine).
Disclosures
Les auteurs n’ont rien à divulguer.
Acknowledgements
Les auteurs tiennent à remercier tout le personnel de l’Institut de recherche biomédicale de l’Université de médecine de Graz pour leur aide et leur coopération, ainsi que Christopher John Wrighton pour la relecture du manuscrit.
Materials
| Name | Company | Catalog Number | Comments |
|---|---|---|---|
| Rats Agouti noirs mâles adultes (300 ± ; 25 g) ; | |||
| Fentanyl | Hameln pharma plus, Allemagne | ; comme le citrate de fentanyl, 50 et micro ; g/ml | |
| Midazolam | ERWO Pharma, Autriche | 50039017 | 5 mg/ml |
| Medetomidin ; | Orion Pharma, Finlande | sous forme de chlorhydrate de méthétomidine, 1mg/ml | |
| de flumazénil | Roche, Suisse | 0,1 mg/ml | |
| d’atipamézol | Orion Pharma, Finlande | sous forme de chlorhydrate d’atipamézol, 5 mg/ml | |
| 10 % de complexe de povidone iodé | Mundipharma, Autriche | ||
| Ciment dentaire ; | Heraeus Kulzer, Allemagne | 6603 7633 | |
| Solution saline physiologique ; | Fresenius Kabi, Autriche | 0,9 % de NaCl | |
| Solution saline tamponnée (PBS) | Sigma-Aldrich, Allemagne | P3813 | |
| Isofluorane ; | AbbVie, Autriche | ||
| Gouttes oculaires lubrifiantes ; | Thea Pharma, Autriche | ||
| 70 % EtOH | Merck, Allemagne | 1070172511 L’éthanol | absolu a été dilué dans du ddH2O pour la préparation de 70 % v/v |
| 2,5 % d’enrofloxacine | Bayer, Allemagne | Antibiotiques prophylactiques ; | |
| carprofène | Pfizer, États-Unis | Analgésiques, 50 mg/ml ; | |
| Préadolescent-20 ; | Sigma-Aldrich, Allemagne | P9416 | |
| Pentobarbital ; | Richter Pharma, Autriche | pentobarbital sodique, 400 mg/ml | |
| Interféron gamma | PeproTech, États-Unis | ; 400-20 | |
| Facteur de nécrose tumorale alpha | R& D Systems, | États-Unis 510-RT-050/CF | |
| rMOG1-125 | propre produit au Centre de médecine moléculaire, Institut Karolinska, Suède | Glycoprotéine oligodendrocytaire de myéline de rat recombinante, acides aminés 1-125 de l’extrémité N-terminale, également disponible dans le commerce : AnaSpec, AS-55152-500, anticorps | |
| anti-MOG | Ana Spec/Kaneka Corporation, Japon | AS-555157 | Standard de ELISA-Kit ; Ana Spec/Kaneka ; ; |
| Freund incomplet s adjuvant ; | Sigma-Aldrich, Allemagne | ; F5506 | |
| Anticorps secondaire IgG anti-rat conjugué à la peroxydase de raifort | Ana Spec/Kaneka Corporation, Japon | AS-555157 | Anticorps secondaire du kit ELISA ; Ana Spec/Kaneka Corporation |
| Albumine sérique bovine ; | Sigma-Aldrich, Allemagne | A9576 | |
| Solution de substrat de peroxydase | Vector Laboratories, États-Unis | SK-45000 | |
| Cadre stéréotaxique ; | David Kopf Instruments, États-Unis | ||
| Cathéters, IRM adapté ; | PlasticsOne, USA | 8IC315GPKXXC | |
| Canules factices ; | PlasticsOne, USA | 8IC315DCNSPC | |
| Vis en plastique, compatible IRM ; | PlasticsOne, USA | 8L080X093N01 | |
| Canule de connecteur ; | PlasticsOne, USA | 8IC313CXSPCC | |
| Tournevis avec pointe de | |||
| Perceuse avec extension d’arbre flexible ; | Proxxon, Allemagne | N° 28 472, N° 28 706, N° 28 620, ; ; | |
| Mèche ronde, 0,5 mm ; | Hager & Meisinger, Allemagne ; | REF310 104 001 001 009 | |
| Mèche torsadée 1,3 mm | Hager & Meisinger, Allemagne ; | REF350 104 417 364 013 | |
| Scalpel ; | Braun, Allemagne | BB510 | |
| Manche de scalpel ; | Fine Science Tools, Allemagne | 91003-12 | |
| Applicateur d’embout en coton ; | Henry Schein Medical, Autriche | 900-3155 | |
| Ciseaux chirurgicaux | Fine Science Tools, Allemagne | 14101-14, 14088-10 ; | |
| Pince chirurgicale | Fine Science Tools, Allemagne | 11002-12, 11251-35 | |
| Pinces Bulldog ; | Fine Science Tools, Allemagne | 18050-35 | |
| Couverture homoéotherme ; | TSE systems, Allemagne | ||
| Lampe infrarouge | Beurer, Allemagne | 616.51 | |
| Lampe à polymériser dentaire ; | Guilin Woodpecker Medical, Chine | ||
| Suture résorbable ; | Johnson & Johnson, Belgique | V792E | |
| Pousse-seringue programmable ; | World Precision Instruments, USA | AL-1000 | |
| d’examen | |||
| Blouse | |||
| Rasoir électrique | Aesculap, Allemagne | GT420 | |
| Vaporisateur d’anesthésique volatile ; | Rothacher Medical, Suisse | CV 30-301-D | |
| Source d’oxygène pour vaporisateur d’anesthésique volatil | Air Liquide, Autriche | 19,113 | |
| Chambre d’anesthésie volatile ; | Rothacher Medical, Suisse | PS-0347 | |
| Masque d’anesthésie pour rats | Rothacher Medical, Suisse | PS-0307-A | |
| Seringue de 1 ml ; | Codan, Danemark | REF 62.1612 | |
| Aiguille d’injection de calibre 26 | Braun, Allemagne | 4657683 | |
| Aiguille de calibre 20 pour l’injection de cytokines et l’immunisation ; | Braun, Allemagne | 4657519 | |
| Seringues en verre Luer lock ; | Poulten & Graf, Allemagne | 7.140-37 | |
| Robinet d’arrêt 3 voies ; | Becton Dickinson, Suède | 394600 | |
| Plaque à 96 puits ; | Thermo Fisher Scientific, États-Unis | 442404 | |
| Lecteur de plaques | Cole-Parmer, États-Unis | EW-1396-00 | |
| 37° ; C incubateur | Kendro, Allemagne | 50042301 | |
| Micropipettes ; | Gilson, États-Unis | F167350 |
References
- MS Prevalence. National Multiple Sclerosis Society. , Available from: http://www.nationalmssociety.org/About-the-Society/MS-Prevalence (2017).
- Berkovich, R. Treatment of acute relapses in multiple sclerosis. Neurotherapeutics. 10 (1), 97-105 (2013).
- Kalincik, T. Multiple Sclerosis Relapses: Epidemiology, Outcomes and Management. A Systematic Review. Neuroepidemiology. 44 (4), 199-214 (2015).
- Feinstein, A., Freeman, J., Lo, A. C. Treatment of progressive multiple sclerosis: what works, what does not, and what is needed. The Lancet Neurology. 14 (2), 194-207 (2015).
- Montalban, X., et al. Ocrelizumab versus Placebo in Primary Progressive Multiple Sclerosis. The New England Journal of Medicine. 376 (3), 209-220 (2017).
- Dyment, D. A., Ebers, G. C., Sadovnick, A. D. Genetics of multiple sclerosis. The Lancet Neurology. 3 (2), 104-110 (2004).
- Ascherio, A. Environmental factors in multiple sclerosis. Expert Review of Neurotherapeutics. 13, 12 Suppl 3-9 (2013).
- Allen, I. V., McQuaid, S., Mirakhur, M., Nevin, G. Pathological abnormalities in the normal-appearing white matter in multiple sclerosis. Neurological Sciences. 22 (2), 141-144 (2001).
- Kutzelnigg, A., et al. Cortical demyelination and diffuse white matter injury in multiple sclerosis. Brain. 128 (11), 2705-2712 (2005).
- Kutzelnigg, A., Lassmann, H. Cortical lesions and brain atrophy in MS. Journal of the Neurological Sciences. 233 (1-2), 55-59 (2005).
- Lucchinetti, C. F., et al. Inflammatory cortical demyelination in early multiple sclerosis. The New England Journal of Medicine. 365 (23), 2188-2197 (2011).
- Peterson, J. W., Bo, L., Mork, S., Chang, A., Trapp, B. D. Transected neurites, apoptotic neurons, and reduced inflammation in cortical multiple sclerosis lesions. Annals of Neurology. 50 (3), 389-400 (2001).
- Kutzelnigg, A., Lassmann, H. Cortical demyelination in multiple sclerosis: a substrate for cognitive deficits. Journal of the Neurological Sciences. 245 (1-2), 123-126 (2006).
- Procaccini, C., De Rosa, V., Pucino, V., Formisano, L., Matarese, G. Animal models of Multiple Sclerosis. European Journal of Pharmacology. 759, 182-191 (2015).
- Kipp, M., Nyamoya, S., Hochstrasser, T., Amor, S. Multiple sclerosis animal models: a clinical and histopathological perspective. Brain Pathology. 27 (2), 123-137 (2017).
- Lebar, R., Lubetzki, C., Vincent, C., Lombrail, P., Boutry, J. M. The M2 autoantigen of central nervous system myelin, a glycoprotein present in oligodendrocyte membrane. Clinical and Experimental Immunology. 66 (2), 423-434 (1986).
- Linington, C., Bradl, M., Lassmann, H., Brunner, C., Vass, K. Augmentation of demyelination in rat acute allergic encephalomyelitis by circulating mouse monoclonal antibodies directed against a myelin/oligodendrocyte glycoprotein. The American Journal of Pathology. 130 (3), 443-454 (1988).
- Panitch, H., Ciccone, C. Induction of recurrent experimental allergic encephalomyelitis with myelin basic protein. Annals of Neurology. 9 (5), 433-438 (1981).
- Tuohy, V. K., Sobel, R. A., Lees, M. B. Myelin proteolipid protein-induced experimental allergic encephalomyelitis. Variations of disease expression in different strains of mice. The Journal of Immunology. 140 (6), 1868-1873 (1988).
- Stromnes, I. M., Goverman, J. M. Active induction of experimental allergic encephalomyelitis. Nature Protocols. 1 (4), 1810-1819 (2006).
- Stromnes, I. M., Goverman, J. M. Passive induction of experimental allergic encephalomyelitis. Nature Protocols. 1 (4), 1952-1960 (2006).
- Mendel, I., Kerlero de Rosbo, N., Ben-Nun, A. A myelin oligodendrocyte glycoprotein peptide induces typical chronic experimental autoimmune encephalomyelitis in H-2b mice: fine specificity and T cell receptor V beta expression of encephalitogenic T cells. European Journal of Immunology. 25 (7), 1951-1959 (1995).
- McRae, B. L., et al. Induction of active and adoptive relapsing experimental autoimmune encephalomyelitis (EAE) using an encephalitogenic epitope of proteolipid protein. Journal of Neuroimmunology. 38 (3), 229-240 (1992).
- Bebo, B. F., Vandenbark, A. A., Offner, H. Male SJL mice do not relapse after induction of EAE with PLP 139-151. Journal of Neuroscience Research. 45 (6), 680-689 (1996).
- Oliver, A. R., Lyon, G. M., Ruddle, N. H. Rat and human myelin oligodendrocyte glycoproteins induce experimental autoimmune encephalomyelitis by different mechanisms in C57BL/6 mice. The Journal of Immunology. 171 (1), 462-468 (2003).
- Scheld, M., et al. Neurodegeneration Triggers Peripheral Immune Cell Recruitment into the Forebrain. The Journal of Neuroscience. 36 (4), 1410-1415 (2016).
- Chanaday, N. L., Roth, G. A. Microglia and astrocyte activation in the frontal cortex of rats with experimental autoimmune encephalomyelitis. Neuroscience. 314, 160-169 (2016).
- Pomeroy, I. M., Matthews, P. M., Frank, J. A., Jordan, E. K., Esiri, M. M. Demyelinated neocortical lesions in marmoset autoimmune encephalomyelitis mimic those in multiple sclerosis. Brain. 128 (11), 2713-2721 (2005).
- Merkler, D., et al. Differential macrophage/microglia activation in neocortical EAE lesions in the marmoset monkey. Brain Pathology. 16 (2), 117-123 (2006).
- Storch, M. K., et al. Cortical demyelination can be modeled in specific rat models of autoimmune encephalomyelitis and is major histocompatibility complex (MHC) haplotype-related. Journal of Neuropathology and Experimental Neurology. 65 (12), 1137-1142 (2006).
- Ludwin, S. K. Central nervous system demyelination and remyelination in the mouse: an ultrastructural study of cuprizone toxicity. Laboratory Investigation. 39 (6), 597-612 (1978).
- Skripuletz, T., et al. Cortical demyelination is prominent in the murine cuprizone model and is strain-dependent. The American Journal of Pathology. 172 (4), 1053-1061 (2008).
- Norkute, A., et al. Cuprizone treatment induces demyelination and astrocytosis in the mouse hippocampus. Journal of Neuroscience Research. 87 (6), 1343-1355 (2009).
- Acs, P., et al. 17beta-estradiol and progesterone prevent cuprizone provoked demyelination of corpus callosum in male mice. Glia. 57 (8), 807-814 (2009).
- Pott, F., et al. Cuprizone effect on myelination, astrogliosis and microglia attraction in the mouse basal ganglia. Brain Research. 1305, 137-149 (2009).
- Jeffery, N. D., Blakemore, W. F. Remyelination of mouse spinal cord axons demyelinated by local injection of lysolecithin. Journal of Neurocytology. 24 (10), 775-781 (1995).
- Blakemore, W. F. Ethidium bromide induced demyelination in the spinal cord of the cat. Neuropathology and Applied Neurobiology. 8 (5), 365-375 (1982).
- Mason, J. L., et al. Oligodendrocytes and progenitors become progressively depleted within chronically demyelinated lesions. The American Journal of Pathology. 164 (5), 1673-1682 (2004).
- Franco, P. G., Silvestroff, L., Soto, E. F., Pasquini, J. M. Thyroid hormones promote differentiation of oligodendrocyte progenitor cells and improve remyelination after cuprizone-induced demyelination. Experimental Neurology. 212 (2), 458-467 (2008).
- Lassmann, H., Bradl, M. Multiple sclerosis: experimental models and reality. Acta Neuropathologica. 133 (2), 223-244 (2017).
- Kerschensteiner, M., et al. Targeting experimental autoimmune encephalomyelitis lesions to a predetermined axonal tract system allows for refined behavioral testing in an animal model of multiple sclerosis. The American Journal of Pathology. 164 (4), 1455-1469 (2004).
- Merkler, D., Ernsting, T., Kerschensteiner, M., Bruck, W., Stadelmann, C. A new focal EAE model of cortical demyelination: multiple sclerosis-like lesions with rapid resolution of inflammation and extensive remyelination. Brain. 129, Pt 8 1972-1983 (2006).
- Ucal, M., et al. Widespread cortical demyelination of both hemispheres can be induced by injection of pro-inflammatory cytokines via an implanted catheter in the cortex of MOG-immunized rats. Experimental Neurology. 294, 32-44 (2017).
- Gardner, C., et al. Cortical grey matter demyelination can be induced by elevated pro-inflammatory cytokines in the subarachnoid space of MOG-immunized rats. Brain. 136, Pt 12 3596-3608 (2013).
- Minagar, A., et al. The thalamus and multiple sclerosis: modern views on pathologic, imaging, and clinical aspects. Neurology. 80 (2), 210-219 (2013).
- Tsunoda, I., Kuang, L. Q., Theil, D. J., Fujinami, R. S. Antibody association with a novel model for primary progressive multiple sclerosis: induction of relapsing-remitting and progressive forms of EAE in H2s mouse strains. Brain Pathology. 10 (3), 402-418 (2000).
- Lifshitz, J., Witgen, B. M., Grady, M. S. Acute cognitive impairment after lateral fluid percussion brain injury recovers by 1 month: evaluation by conditioned fear response. Behavioural Brain Research. 177 (2), 347-357 (2007).
- Kabadi, S. V., Hilton, G. D., Stoica, B. A., Zapple, D. N., Faden, A. I. Fluid-percussion-induced traumatic brain injury model in rats. Nature Protocols. 5 (9), 1552-1563 (2010).
- Leonard, J. R., Grady, M. S., Lee, M. E., Paz, J. C., Westrum, L. E. Fluid percussion injury causes disruption of the septohippocampal pathway in the rat. Experimental Neurology. 143 (2), 177-187 (1997).
- Hare, G. M., et al. Severe hemodilutional anemia increases cerebral tissue injury following acute neurotrauma. Journal of Applied Physiology. 103 (3), 1021-1029 (2007).
- Abbott, N. J. Evidence for bulk flow of brain interstitial fluid: significance for physiology and pathology. Neurochemistry International. 45 (4), 545-552 (2004).
- Amor, S., et al. Identification of epitopes of myelin oligodendrocyte glycoprotein for the induction of experimental allergic encephalomyelitis in SJL and Biozzi AB/H mice. The Journal of Immunology. 153 (10), 4349-4356 (1994).
- Adzemovic, M. Z., Zeitelhofer, M., Hochmeister, S., Gustafsson, S. A., Jagodic, M. Efficacy of vitamin D in treating multiple sclerosis-like neuroinflammation depends on developmental stage. Experimental Neurology. , 39-48 (2013).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request Permission