Användning av Autometallography att lokalisera och semi kvantifiera Silver i valarnas vävnader
Summary
Ett protokoll presenteras för att lokalisera Ag i valarnas lever och njure vävnader av autometallography. Dessutom är en ny analys, heter den cetacean histologiska Ag assay (CHAA) utvecklat för att uppskatta Ag halterna i dessa vävnader.
Abstract
Silvernanopartiklar (AgNPs) har i stor utsträckning används i kommersiella produkter, inklusive textil, kosmetika och vård poster, på grund av deras starka antimikrobiella effekter. De också kan släppas ut i miljön och ackumuleras i havet. Därför AgNPs är den huvudsakliga källan av Ag kontaminering, och allmänhetens medvetenhet om miljötoxicitet AG ökar. Tidigare studier har visat bioackumulering (i producenter) och förstoring (i konsumenter/rovdjur) AG. Valar, kan som toppkonsumenterna över oceanen, ha påverkats negativt av föreningarna som Ag/Ag. Även om koncentrationerna av Ag/Ag föreningar i valarnas vävnader kan mätas med induktivt kopplad plasma mass spektroskopi (ICP-MS), är användning av ICP-MS begränsat av dess höga kapitalkostnader och kravet på vävnad lagring/beredning. Därför, en autometallography (AMG) metod med en kvantitativ bildanalys med hjälp av formalin-fast, paraffin-inbäddat (FFPE) vävnad kan vara en adjuvant metod för att lokalisera Ag distribution på suborgan och uppskatta koncentrationen av Ag i valar vävnaderna. De positiva signalerna som AMG är främst bruna till svarta granulat i olika storlekar i cytoplasman i proximal renal tubulär epitel, hepatocyter och Kupffers celler. Ibland, vissa amorft gyllene gul till brun AMG positiva signaler är anges i lumen och basalmembranet av vissa proximala njurtubuli. Analysen för att uppskatta koncentrationen Ag heter den Cetacean histologiska Ag Assay (CHAA), som är en regressionsmodell som fastställts av data från kvantitativ bildanalys av AMG metod och ICP-MS. Användningen av AMG med CHAA att lokalisera och semi beräkna tungmetaller ger en bekväm metod för studier av plats och tid och mellan djurarter.
Introduction
Silvernanopartiklar (AgNPs) har i stor utsträckning används i kommersiella produkter, inklusive textil, kosmetika och vård poster, på grund av deras stora antimikrobiella effekter1,2. Produktionen av AgNPs och antalet AgNP-innehållande produkter är därför ökade över tid3,4. Dock AgNPs kan släppas ut i miljön och ackumuleras i ocean5,6. De har blivit den största källan till Ag kontaminering, och allmänhetens medvetenhet om miljötoxicitet AG ökar.
Status för AgNPs och Ag i den marina miljön är komplicerad och föränderlig. Tidigare studier har visat att AgNPs kan förbli som partiklar, aggregera, lös, reagerar med olika kemiska arter eller återskapas från Ag+ joner7,8. Flera typer av Ag föreningar, såsom Granulatfyllda, har hittats i Marina sediment, där de kan intas av bentiska organismer och ange de livsmedelskedja9,10. Enligt en tidigare studie på Chi-ku Lagoon området längs den sydvästra kusten i Taiwan, Ag koncentrationerna av Marina sediment är extremt låg och liknande till jordskorpans överflödet, och de fisk lever vävnad är oftast nedanför detektion begränsa (< 0,025 µg/g wet våt)11. Tidigare studier som utförts i olika länder har emellertid visat relativt höga Ag koncentrationer i levern av valar12,13. Ag koncentrationen i levern av valar är åldersberoende, tyder på att källan till Ag i sina kroppar är troligen deras byte12. Dessa rön ytterligare tyder biomagnifieringen av Ag i djur på högre trofiska nivåer. Valar, kan som havet, toppkonsumenterna ha drabbats av negativa hälsoeffekter orsakade av Ag/Ag föreningar12,13,14. Viktigast av allt, som valar är människor däggdjur och den negativa hälsomässiga konsekvenser som orsakas av Ag/Ag föreningar i valar kan också förekomma hos människor. Med andra ord, kunde valar vara sentinel djur för havsmiljön och människor hälsa. Hälsoeffekter, vävnadsdistribution och koncentrationen av Ag i valar är därför av stor oro.
Även om koncentrationerna av Ag/Ag föreningar i valarnas vävnader kan mätas med induktivt kopplad plasma mass spektroskopi (ICP-MS), begränsas användning av ICP-MS av dess höga kapitalkostnader (instrument och underhåll) och kraven för vävnad lagring /Preparation12,15. Dessutom är det oftast svårt att samla in omfattande vävnadsprover i alla utredningar av strandade valar fall på grund av logistiska problem, brist på arbetskraft och brist relaterade resurser12. De frysta vävnadsproverna för ICP-MS analys lagras inte lätt på grund av begränsad kyl utrymme och djupfrysta vävnadsprover kan kasseras på grund av trasig kyl utrustning12. Dessa ovan nämnda hinder hämmar utredningar av kontamineringen i valarnas vävnader av ICP-MS analys med frysta vävnadsprover. Däremot formalinbeständiga vävnadsprover är relativt enkelt att samla under obduktion av döda-strängat valar. Det är därför nödvändigt att utveckla en lättanvänd och billig metod för att upptäcka/åtgärd tungmetallerna i valarnas vävnader med hjälp av formalinbeständiga vävnadsprover.
Även om den suborgan distributioner och halterna av alkalimetaller och alkaliska jord metaller ändras under det formalin-fast, paraffin-inbäddat (FFPE), endast mindre effekter på övergången metaller, såsom Ag, har varit noterade16. FFPE-vävnad har därför ansetts som en idealisk prov resurs för metall lokalisering och mätningar16,17. Autometallography (AMG), en histochemical process, kan förstärka tungmetaller som steglöst storlek gyllene gul till svart AMG positiva signaler på FFPE vävnadssnitt och dessa förstärkta tungmetaller kan visualiseras under ljusmikroskop18, 19 , 20 , 21. därför metoden AMG ger information om de suborgan distributionerna av tungmetaller. Det kan ge ytterligare viktig information för att studera de metaboliska vägarna av tungmetaller i biologiska system eftersom ICP-MS kan endast mäta koncentrationen av tungmetaller på orgel nivå18. Dessutom har digital bild analys programvara, såsom ImageJ, tillämpats på kvantitativ analys av histologiska vävnad avsnitt22,23. Den steglöst medelstora gyllene gul till svart AMG positiva signaler av FFPE vävnadssnitt kan kvantifieras och används för att uppskatta koncentrationerna av tungmetaller. Även om den absoluta Ag koncentrationen inte kan fastställas direkt av AMG metod med kvantitativ bildanalys, kan det beräknas genom en regressionsmodell baserad på uppgifter som erhållits från kvantitativ bildanalys och ICP-MS, som heter valprodukter histologiska Ag assay (CHAA). Med tanke på svårigheterna att mäta Ag koncentrationer av ICP-MS analys i mest strandade valar, CHAA är ett värdefullt adjuvant metod för att uppskatta Ag koncentrationer i valarnas vävnader, som inte kan fastställas med ICP-MS analys på grund av fryst vävnadsprover. Detta dokument beskriver protokollet av en histochemical teknik (AMG-metoden) för att lokalisera Ag på nivån suborgan och ett test som heter CHAA att uppskatta Ag koncentrationerna i lever och njure vävnader av valar.
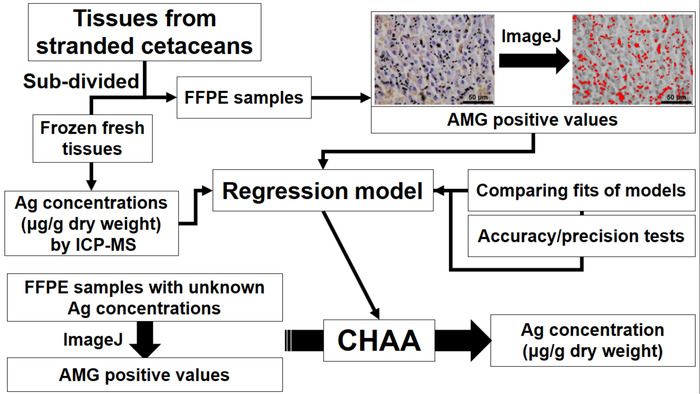
Figur 1: flödesschema som skildrar den inrättandet och tillämpningen av småvalar histologiska Ag assay (CHAA) för att uppskatta Ag koncentrationer. CHAA = småvalar histologiska Ag assay, FFPE = Formalin-fast, paraffin-inbäddat, ICP-MS = induktivt kopplad plasma mass spektroskopi. Klicka här för att se en större version av denna siffra.
Protocol
Representative Results
Discussion
Syftet med artikel studien är att upprätta en adjuvant metod att utvärdera Ag fördelningen på suborgan nivåer och uppskatta Ag koncentrationer i valarnas vävnader. De aktuella protokollen inkludera 1) bestämning av Ag koncentrationer i valarnas vävnader av ICP-MS, 2) AMG analys av par-matchade vävnadsprover med kända Ag koncentrationer, 3) inrättandet av regressionsmodellen (CHAA) för att uppskatta koncentrationerna som Ag av AMG positiva värden, 4) utvärdering av noggrannhet och precision av CHAA, och 5) …
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi tackar Taiwan Cetacean strandning nätverket för provtagning och förvaring, inklusive Taiwan Cetacean Society, Taipei; Valarnas forskningslaboratoriet (Prof. Lien-Siang Chou), Institutet för ekologi och evolutionsbiologi, National Taiwan University, Taipei; National Museum of Natural Science (Dr. Chiou-Ju Yao), Taichung; och marinbiologi & Cetacean Research Center, National Cheng-Kung University. Vi tackar även de skogsbruk Bureau, rådet för jordbruk, Executive Yuan för deras tillstånd.
Materials
| HQ Silver enhancement kit | Nanoprobes | #2012 | |
| Surgipath Paraplast | Leica Biosystems | 39601006 | Paraffin |
| 100% Ethanol | Muto Pure Chemical Co., Ltd | 4026 | |
| Non-Xylene | Muto Pure Chemical Co., Ltd | 4328 | |
| Silane coated slide | Muto Pure Chemical Co., Ltd | 511614 | |
| Cover glass (25 x 50 mm) | Muto Pure Chemical Co., Ltd | 24501 | |
| Malinol | Muto Pure Chemical Co., Ltd | 20092 | |
| GM Haematoxylin Staining | Muto Pure Chemical Co., Ltd | 3008-1 | |
| 10% neutral buffered formalin solution | Chin I Pao Co., Ltd | — | |
| Tip (1000 μL) | MDBio, Inc. | 1000 | |
| PIPETMAN Classic P1000 | Gilson, Inc. | F123602 | |
| 15 ml Centrifuge Tube | GeneDireX, Inc. | PC115-0500 | |
| Dogfish liver | National Research Council of Canada | DOLT-2 | |
| Dogfish muscle | National Research Council of Canada | DORM-2 | |
| Inductively coupled plasma mass spectrometry (ICP-MS) | PerkinElmer Inc. | PE-SCIEX ELAN 6100 DRC | |
| FreeZone 6 liter freeze dry system | Labconco | 7752030 | For freeze drying |
| BRAND® SILBERBRAND volumetric flask | Merck | Z326283 | |
| 30 mL standard vial, flat interior with 33 mm closure | Savillex Corporation | 200-030-12 | For diagestion |
| Nitric acid, superpur®, 65.0% | Merck | 1.00441 | For diagestion |
| Hot Plate/Stirrers | Corning® | PC-220 | For diagestion |
| High Shear lab mixer | Silverson | SL2T | For homogenization |
| Sterile polypropylene sample jar (250mL) | Thermo Scientific™ | 6186L05 | For homogenization |
| Digital camera | Nikon Corporation | DS-Fi2 | |
| Light microscope | Nikon Corporation | ECLIPSE Ni-U | |
| Shandon™ Finesse™ 325 manual microtome | Thermo Scientific™ | A78100001H | |
| Accu-Cut® SRM™ 200 rotary microtome | Sakura | 1429 | |
| Microtome blade S35 | FEATHER® | 207500000 | |
| Slide staining dish and cover | Brain Research Laboratories | #3215 | |
| Steel staining rack | Brain Research Laboratories | #3003 | |
| Shandon embedding center | Thermo Scientific™ | S-EC | |
| Shandon Citadel® tissue processor | Thermo Scientific™ | 69800003 | |
| Slide warmer | Lab-Line Instruments | 26005 | |
| Water bath | Shandon Capshaw | 3964 | |
| Filter paper | Merck | 1541-070 | |
| Prism 6.01 for windows | GraphPad Software | Statistic software | |
| ImageJ | National Institutes of Health | ||
| Stainless steel tissue embedding mould | Shenyang Roundfin Trade Co., Ltd | RD-TBM003 | For paraffin emedding |
References
- McGillicuddy, E., et al. Silver nanoparticles in the environment: Sources, detection and ecotoxicology. Science Total Environment. 575, 231-246 (2017).
- Yu, S. J., Yin, Y. G., Liu, J. F. Silver nanoparticles in the environment. Environmental Science: Processes and Impacts. 15 (1), 78-92 (2013).
- Hansen, S. F., et al. Nanoproducts- what is actually available to European consumers?. Environmental Science: Nano. 3 (1), 169-180 (2016).
- Vance, M. E., et al. Nanotechnology in the real world: Redeveloping the nanomaterial consumer products inventory. Beilstein Journal of Nanotechnology. 6, 1769-1780 (2015).
- Farre, M., Gajda-Schrantz, K., Kantiani, L., Barcelo, D. Ecotoxicity and analysis of nanomaterials in the aquatic environment. Analytical and Bioanalytical Chemistry. 393 (1), 81-95 (2009).
- Walters, C. R., Pool, E. J., Somerset, V. S. Ecotoxicity of silver nanomaterials in the aquatic environment: a review of literature and gaps in nano-toxicological research. Journal of Environmental Science and Health. Part A, Toxic/hazardous Substances & Environmental Engineering. 49 (13), 1588-1601 (2014).
- Levard, C., Hotze, E. M., Lowry, G. V., Brown, G. E. Environmental transformations of silver nanoparticles: impact on stability and toxicity. Environmental Science & Technology. 46 (13), 6900-6914 (2012).
- Massarsky, A., Trudeau, V. L., Moon, T. W. Predicting the environmental impact of nanosilver. Environmental Toxicology and Pharmacology. 38 (3), 861-873 (2014).
- Wang, H., et al. Toxicity, bioaccumulation, and biotransformation of silver nanoparticles in marine organisms. Environmental Science and Technology. 48 (23), 13711-13717 (2014).
- Buffet, P. E., et al. A marine mesocosm study on the environmental fate of silver nanoparticles and toxicity effects on two endobenthic species: the ragworm Hediste diversicolor and the bivalve mollusc Scrobicularia plana. Science of the Total Environment. 470, 1151-1159 (2014).
- Chen, M. H. Baseline metal concentrations in sediments and fish, and the determination of bioindicators in the subtropical Chi-ku Lagoon, S W Taiwan. Marine Pollution Bulletin. 44 (7), 703-714 (2002).
- Li, W. T., et al. Investigation of silver (Ag) deposition in tissues from stranded cetaceans by autometallography (AMG). Environmental Pollution. , 534-545 (2018).
- Chen, M. H., et al. Tissue concentrations of four Taiwanese toothed cetaceans indicating the silver and cadmium pollution in the western Pacific Ocean. Marine Pollution Bulletin. 124 (2), 993-1000 (2017).
- Li, W. T., et al. Immunotoxicity of silver nanoparticles (AgNPs) on the leukocytes of common bottlenose dolphins (Tursiops truncatus). Scientific Reports. , (2018).
- Bornhorst, J. A., Hunt, J. W., Urry, F. M., McMillin, G. A. Comparison of sample preservation methods for clinical trace element analysis by inductively coupled plasma mass spectrometry. American Journal of Clinical Pathology. 123 (4), 578-583 (2005).
- Bonta, M., Torok, S., Hegedus, B., Dome, B., Limbeck, A. A comparison of sample preparation strategies for biological tissues and subsequent trace element analysis using LA-ICP-MS. Analytical and Bioanalytical Chemistry. 409 (7), 1805-1814 (2017).
- Bischoff, K., Lamm, C., Erb, H. N., Hillebrandt, J. R. The effects of formalin fixation and tissue embedding of bovine liver on copper, iron, and zinc analysis. Journal of Veterinary Diagnostic Investigation. 20 (2), 220-224 (2008).
- Miller, D. L., Yu, I. J., Genter, M. B. Use of Autometallography in Studies of Nanosilver Distribution and Toxicity. International Journal of Toxicology. 35 (1), 47-51 (2016).
- Anderson, D. S., et al. Influence of particle size on persistence and clearance of aerosolized silver nanoparticles in the rat lung. Toxicological Sciences. 144 (2), 366-381 (2015).
- Kim, W. Y., Kim, J., Park, J. D., Ryu, H. Y., Yu, I. J. Histological study of gender differences in accumulation of silver nanoparticles in kidneys of Fischer 344 rats. Journal of Toxicology and Environmental Health, Part A. 72 (21-22), 1279-1284 (2009).
- Danscher, G. Applications of autometallography to heavy metal toxicology. Pharmacology Toxicology. 68 (6), 414-423 (1991).
- Deroulers, C., et al. Analyzing huge pathology images with open source software. Diagnostic Pathology. 8, 92 (2013).
- Shu, J., Dolman, G. E., Duan, J., Qiu, G., Ilyas, M. Statistical colour models: an automated digital image analysis method for quantification of histological biomarkers. BioMedical Engineering Online. 15, 46 (2016).
- Geraci, J. R., Lounsbury, V. J. Specimen and data collection. Marine mammals ashore: a field guide for strandings. , 167-230 (2005).
- Shih, C. -. C., Liu, L. -. L., Chen, M. -. H., Wang, W. -. H. . Investigation of heavy metal bioaccumulation in dolphins from the coastal waters off Taiwan. , (2001).
- Liang, C. S., et al. The relationship between the striatal dopamine transporter and novelty seeking and cognitive flexibility in opioid dependence. Progress in Neuro-Psychopharmacology and Biological Psychiatry. 74, 36-42 (2017).
- Spiess, A. N., Neumeyer, N. An evaluation of R2 as an inadequate measure for nonlinear models in pharmacological and biochemical research: a Monte Carlo approach. BMC Pharmacology. 10, 6 (2010).
- Stoltenberg, M., Danscher, G. Histochemical differentiation of autometallographically traceable metals (Au, Ag, Hg, Bi, Zn): protocols for chemical removal of separate autometallographic metal clusters in Epon sections. Histochemical Journal. 32 (11), 645-652 (2000).
- Dimitriadis, V. K., Domouhtsidou, G. P., Raftopoulou, E. Localization of Hg and Pb in the palps, the digestive gland and the gills in Mytilus galloprovincialis (L.) using autometallography and X-ray microanalysis. Environmental Pollution. 125 (3), 345-353 (2003).
- Loumbourdis, N. S., Danscher, G. Autometallographic tracing of mercury in frog liver. Environmental Pollution. 129 (2), 299-304 (2004).
- Stoltenberg, M., Larsen, A., Kemp, K., Bloch, D., Weihe, P. Autometallographic tracing of mercury in pilot whale tissues in the Faroe Islands. International Journal of Circumpolar Health. 62 (2), 182-189 (2003).

