Optimalisert Interferon-gamma ELISpot analysen mål T celle tiltak i Guinea Gris modellen etter vaksinering
Summary
Utviklingen av interferon-gamma ELISpot analysen for guinea gris PBMCs tillater karakterisering av T-celle svar i denne svært relevante modellen studere smittsomme sykdommer. Vi har brukt analysen for å måle T celle svar knyttet intradermal levering av DNA vaksiner.
Abstract
Marsvin har spilt en sentral rolle som relevante liten dyr modell i utviklingen av vaksiner for smittsomme sykdommer som tuberkulose, influensa, difteri og viral hemoragisk feber. Vi har vist at plasmider-DNA (pDNA) vaksine levering i huden utløser robust humoral svar i marsvin. Men var bruk av dette dyret til modell immunreaksjoner noe begrenset tidligere skyldes mangel på tilgjengelig reagenser og protokoller for å studere T celle svar. T celler spille en sentral rolle i både immunoprophylactic og immunterapeutisk mekanismer. Forstå T celle svar er avgjørende for utviklingen av smittsomme sykdommer, og onkologi vaksiner og imøtekommende levering enheter. Her beskriver vi en interferon-gamma (IFN-γ) enzymet knyttet immunospot (ELISpot) analysen for marsvin perifert blod mononukleære celler (PBMCs). Analysen kan forskere å karakterisere vaksine-spesifikke T-celle svar i denne viktige gnager modellen. Muligheten til å analysen celler isolert fra perifert blod gir mulighet til å spore immunogenisitet i enkelte dyr.
Introduction
Protokollen beskrevet her tillater påvisning av interferon-gamma (IFN-γ) sekresjon celler etter antigen tilbakekalling i perifert blod mononukleære celle (PBMC) innbyggere høstet fra Hartley marsvin. Vi har brukt analysen betegner kinetics og størrelsen av antigen-spesifikke T celle Svar å en influensa vaksinering-diett i marsvin. Vi tror denne protokollen vil betydelig drive pre-klinisk utvikling av vaksinasjonsprogrammer i denne svært relevante dyremodell.
T-celler elicited av vaksiner spille en viktig rolle i beskyttelse mot smittestoffer og immunterapeutisk trasé forbundet med andre sykdommer. Betydningen av T-celler har blitt fremhevet i flere vaksine studier. Immunisering oppspore og mus med en plasmider DNA (pDNA)-koding for H5 hemagglutinin og N1 neuraminidase gitt beskyttelse fra sykelighet og dødelighet i en influensa virus utfordring i fravær av nøytralisere antistoffer, indikerer viktigheten av T celle immunitet1. I tillegg til sterk nøytralisere humoral respons, spille T-celler en avgjørende rolle for ikke bare viral klaring2 , men også beskyttelse mot infeksjon med respiratorisk syncytial virus (RSV) i mus3. Hos mennesker var eksisterende CD8 + T celler assosiert med redusert sykdommens alvorlighetsgrad i H1N1 pandemi i 20094. CD4 + T celletall sammen med visse cytokin plasma konsentrasjon er korrelert med sykdommens alvorlighetsgrad i RSV-smittede barn5.
Marsvin har fått kjent som laboratorium modell for forskning og utvikling i ulike områder av medisin som hud allergi, næringsinnhold forskning, studier av hørselen og, mest relevant for dette arbeidet, infeksjonssykdommer. Det var avgjørende for oppdagelsen av vaksiner mot tuberkulose og difteri. Nylig brukes marsvin som modell for influensa6 og Ebola7. Videre tilbyr har fysiologiske likheter til menneskelig hud8, marsvin en tilgjengelig liten dyr modell for dermal narkotika leveringsmåter. I motsetning til sin betydning som laboratorium modell fortsatt tilgjengeligheten av marsvin bestemt analyser og sonder som karakteriserer immunreaksjoner begrenset9. Grunnleggende mobilnettet analyser som den IFN-γ enzym-koblede immunospot (ELISpot-analysen) som rutinemessig brukes i pre-klinisk og klinisk forskning nummerere T celle svar er ikke tilgjengelig.
De første solid-fase enzym knyttet immunospot analyser ble brukt for å bestemme antall spesifikke antistoffer-sekresjon celler i en mangfoldig B celle-befolkning10,11. Formatet har avansert for å oppdage celler sekresjon cytokiner inkludert IL-1, IL-2, IL-4, IL-5, IL-6, IL-10, GM-CSF, TNF-alfa, TNF-beta, granzyme B og IFN-γ. ELISpot analysen besitter høy følsomhet; hver produksjon av cytokin celle kan oppdages. Grensen for påvisning ELISpot analyser er rapportert å være lavere enn 10 plasser per 100.000 PBMCs12. Nylig et marsvin IFN-γ spesifikt antistoff par ble gjort tilgjengelig13, og dette har åpnet opp muligheten til å håndtere denne mangel i feltet.
IFN-γ er ansett som en viktig effektor molekyl i adaptive immunforsvaret; Det kan være produsert og skilles ut av både CD4 og CD8 T celler ved aktivering. IFN-γ har et bredt spekter av biologiske funksjoner i forbindelse med en immunrespons på en virusinfeksjon, som aktivering av makrofager og opp regulering av store histocompatibility kompleks (MHC) jeg og MHCII uttrykk. Det også fremmer B-cellen differensiering, hemmer T-helper-2 cellevekst og aktiverer naturlige drepe celler. IFN-γ blokkerer viral replikasjon i infiserte somatiske celler og upregulates uttrykk for MHC molekyler. Dermed er produksjon av IFN-γ en svært viktig indikasjon på kvaliteten av T celle respons til en vaksine eller patogen.
En viktig del av den her presenteres IFN-γ ELISpot er bruk av PBMCs i stedet for splenocytes13. PBMCs kan fås ved å behandle en ikke-terminal samlet blodprøve, mens innsamling av splenocytes krever dyr euthanization før høsting av milten. Bruk av PBMCs kan IFN-γ T-celle Svar å bli overvåket over en periode og evaluering av virkningene på T-celle svarene som prime-boost regimer14.
For forskere som bruker marsvin som en dyremodell, vil IFN-γ ELISpot metoden utvide omfanget av vitenskapelige data de kan få. Parkeringsmulighetene nå redusere nødvendigheten av å gjennomføre studier med mindre relevant dyr modeller for målet sykdommen, som tidligere ble valgt på grunn av reagens tilgjengeligheten for undersøkelse av mobilnettet svar. Bruk av PBMCs stedet milt eller lymfeknuter gir ikke-terminal eksperimenter og kontinuerlig overvåking av enkelte dyr.
Nedenfor gir vi en detaljert beskrivelse av trinnene involvert i oppdagelsen av en IFN-γ cellulær respons i marsvin pDNA vaksine. Vi viser vår bestemte levering prosedyre og beskriver de generelle ELISpot analysen omfatter blodprøve blod behandling, PBMC innhøsting, analysen prosedyre og dataanalyse. En skjematisk av ELISpot analysen er avbildet i figur 1.
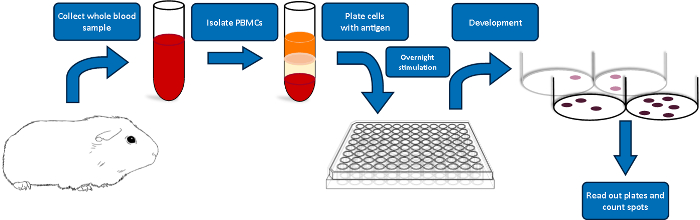
Figur 1 : Skjematisk oversikt over marsvin ELISpot protokollen. Klikk her for å se en større versjon av dette tallet.
Protocol
Representative Results
Discussion
Marsvin er en verdifull dyr modell for pre-klinisk utvikling av vaksiner og intradermal levering strategier. Over protokollen beskriver metodene for å måle antigen-spesifikke T celle svar i denne svært relevante modellen. Analysen gir et klart opplisting av eksterne T-celler produserer Interferon-gamma ved stimulering med antigen-spesifikke peptider. The kinetics av immunrespons kan overvåkes av ikke-terminal blodprøve.
Vi optimalisert protokollen og identifisert viktige aspekter for å oppnå optimale resultater ved hjelp av denne analysen. For eksempel vil dannelse av blodpropp i samlingen røret resultere i suboptimal PBMC utvinning og levedyktighet. Marsvin blodet clots raskt18. Det er avgjørende å utføre blod trekningen raskt. Au-Birck et al. gir en omfattende guide for blødning teknikker i marsvin modell16. Siden samlingen blod krever narkose, anbefales det å vurdere gjeldende standard operasjonsprosedyrer av dette aspektet av prosedyren19. Utilstrekkelig anaesthetized marsvin reagere ved å flytte beina eller vocalization etter en kort klype vevet mellom tærne med neglene eller ved flinching ørene og flytte sine værhår frem etter knipe deres øret. Umiddelbar overføring av blod inn i et rør med antikoagulerende og bland grundig av rulle eller invertere røret flere ganger er et viktig skritt i denne protokollen. For her beskrevet protokollen EDTA-rør ble brukt, og ingen andre antikoagulantia ble testet. Merk at EDTA er hypertonic, rør ideelt fylles mer enn halvfull, og derfor passer røret størrelse for eksempel volumet må brukes.
Når utført korrekt, gir tetthet gradert sentrifugering konsekvent ren PBMC forberedelse. Tetthet-gradient mediet må være ved romtemperatur når lagdeling graderingen før sentrifugering, og bremser bør ikke brukes for å stoppe sentrifuge ved vanlig rør. En betydelig forbedring i forhold til praktisk bruk av PBMC-behandlingen var kombinasjonen av tetthet gradert sentrifugering med PBMC-isolasjon enheter. Dette gir en reduksjon i sentrifugering tid. Tetthet gradert sentrifugering i PBMC-isolasjon enheter og vanlige rør resultater i lignende levedyktighet, teller levende celle behandlet PBMCs og spot formasjon. Uavhengig av type og elueringsrøret for separasjon, buffy pels innhøstingen bør følge umiddelbart. Over en lengre periode er kontakt med tetthet gradert mediet cytotoksisk til PBMCs.
Nøyaktig telling av levedyktig PBMCs er viktig å frø konsekvent lik antall celler i analysen-plate brønnene. Noen metode for live/dead diskriminering bør brukes. I vår lab bruker vi trypan-blå utelukkelse analysen og en automatisert celle-teller.
Spot kvalitet, definert som skarpe og høy kontrast flekker, vil resultere i bedre nøyaktighet og konsekvent spot teller, spesielt når du bruker et automatisk telling system. I tråd med anbefalingene fra produsenten observerte vi etanol pre behandlinger av ELISpot platene skal et avgjørende skritt for å redusere antall bakgrunn flekker og forbedre definisjonen av flekker. Bruk av en plate leser å image ELISpot analysen-platene på slutten av protokollen anbefales. Opprinnelige bilder av hver brønn kan enkelt og effektivt innhentet og lagret. Bruker en analyseprogramvare digitale bilder også tillate objektiv analyse og spot teller forhold til manuell telling av enkelte operatører.
En absolutt nødvendighet for utvikling av analysen beskrevet her var generering av et egnet anti-marsvin Interferon-gamma antistoff par. Musen monoklonale antistoffer V-E4 og N-G3 ble utviklet av hybridoma-teknikken med B-cellen kloner fra mus som ble vaksinert med rekombinant marsvin interferon gamma20. V-E4, som er IgG1 isotype, og N-G3, som er IgG2a, rapporteres å binde både rekombinant og native antigen. Tilordne V-E4 fange antistoff og biotinylated N-G3 som gjenkjenning antistoffer resulterte i høy følsomhet for både rekombinant og innfødt protein samtidig beholde lav bakgrunn signal i en sandwich-ELISA format. Begge antistoffer finnes det vitenskapelige samfunnet gjennom en produksjon avtale ledet av laboratoriet av Dr. Hubert Schaefer, som medforfatter av denne publikasjonen. Forespørsler mottas av Dr. Schaefer lab og deretter produsert av en kommersiell partner.
Plasma interferon-gamma rapporteres å være ustabile i vanlig buffere eller media21. Schaefer et al.20 rapportert bare en moderat nedgang på utvinningsgrad når bruker dårligere IFN-y, som hadde mistet biologiske funksjonalitet, i ELISA format ved hjelp av antistoffer V-E4 og N-G3. Men bør økende inkubasjon tid peptid stimulering av PBMCs over 18 h nøye testes.
Har vært diskutert fordelene ved å bruke PBMCs. Men gjenspeiler her beskrevet analysen bare antigen-spesifikke tiltak av sirkulerende T-celler i periferien. Vev-infiltrere T-celler eller celler isolert fra lymfekar organer, som milten og lymfeknutene, kan ha ulike egenskaper22,23,24. Ingen betydelige forskjeller i mobilnettet svar ble observert ved sammenligning av interferon-gamma flekker fra PBMCs og splenocytes fra marsvin som ble vaksinert med de samme pNP influensa vaksine14.
I denne protokollen beskrev vi en intradermal vaksinasjon prosedyre. En rektor begrunnelse for ID immunisering rettet mot av dendrittiske celler i huden25. Vi og andre har vist at disse cellene kan være spesielt målrettet ved å tilpasse leveringsmetode26, formulering27eller narkotika-design28. Aktivert profesjonell antigen presentere celler kan overføre til en drenering lymfeknute og aktivere den adaptive immunsystem29,30,31,32. Dendrittiske celler er viktig antigen presentasjon celle-typen for grunning produktiv cellular immunreaksjoner.
For denne studien dyr ble vaksinert med plasmider DNA koding nucleoprotein av influensa H1N1 belastning A/PuertoRico/8. Huden levering av denne pDNA vaksine (pNP) i kombinasjon med electroporation hadde blitt vist å framprovosere antigen-spesifikke humoral reaksjoner i marsvin33, oppspore og ikke-menneskelige primater (NHPs)1,34. I tillegg skapte denne vaksinen robust T-celle svar i mus etter levering inn i epidermis35, som kunne tilskrives CD4 og CD8 T-celler ved å stimulere med peptider som representerer bestemte epitopes for disse celle populasjoner. PNP vaksinen var også immunogenic etter mucosal levering som demonstrert av generasjon av humoral svar i kaniner og marsvin, samt cellulære og humorale svar i mus36. Sist kunne vår gruppe demonstrere generasjonen av IFN-γT-celle svar i kaninen etter intra-muskuløse levering (upubliserte data).
Foreløpig kan ikke de observerte Interferon-gamma stedene i marsvin ELISpot tilordnes til et CD4 + eller CD8 + T-celle delsett. Spesielt for design og utvikling av immun terapi rettet mot huden, ville det være svært nyttig for å fastslå om observerte interferon-gamma spot frekvenser er forårsaket av utvidelse av en eller en balansert respons av begge for å evaluere effektiviteten av vaksinasjon utløse kryss-presentasjon. Denne begrensningen kan overvinnes ved negativ celle-sortering for CD4 eller CD8 før såing cellene på tallerkenen eller identifikasjon av MHC, klasse II (for CD4 svar) eller MHC, klasse jeg (for CD8 svar) begrenset epitopes.
Her beskrives Interferon-gamma ELISpot analysen med marsvin PBMCs løser måtte vurdere løpet av mobilnettet svar i guinea gris laboratorium modellen. Dette vil forbedre utvikling av vaksiner og huden levering protokoller. Vi tror at det gir bruken av denne aktuelle dyremodell å studere sykdommer med viktige T-celle komponenter som TB37, Ebola38, HSV39og andre. Det vil redusere bruken av mindre relevant dyremodeller.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi vil gjerne takke medlemmer av Inovio Pharmaceuticals R & D avdelingen for teknisk brukerstøtte og ansatte i Acculab for å gi fremragende dyrehold service. Spesielt ønsker vi å takke Alysha Vu og Joe Agnes for korrekturlesing av manuskriptet. Dette arbeidet var ikke finansiert av noen bestemt stipend fra virkemiddelaktører innen offentlig, kommersielle eller ikke-for-profit.
Materials
| Cellectra-3P | Inovio Pharmaceuticals | ID-Electroporatio device/ non-commercial, R&D-only | |
| K2EDTA blood collection tube | BD | 367844 | |
| Hank’s Balanced Salt Solution | Gibco | 14175-079 | |
| Ficoll-Paque Plus | GE Healthacre | 17144003 | density gradient medium |
| SepMate tube | STEMCELL Technologies | 85415 | PBMC-isolation device |
| RPMI | Thermo Fisher | 11875-135 | |
| heat-deactivated FBS | VWR | 97068-085 | |
| Pen/Strep | Gibco | 15140-122 | |
| β-Mercaptoethanol | Gibco | 21985-023 | |
| 96-well ELISpot PVDF-membrane | Millipore | MSIPS4W10 | ELISpot assay plate |
| Ethanol | Sigma | 459844-1L | |
| UPDI | Invitrogen | 10977-015 | Ultra-Pure DI water |
| Sucrose | Sigma | S7903 | |
| Bovine Serum Albumin | Sigma | A7906 | |
| 10x PBS | HyClone | SH30378.03 | |
| Concanavalin A (ConA) | Sigma | C5275-5MG | |
| alkaline phosphatase (ALP)-conjugated streptavidin | R&D Systems Inc. | SEL002 | |
| BCIP/NBT | R&D Systems Inc. | SEL002 | |
| capture anti-guinea pig IFN-γ antibody V-E4 | GenScript | Order #:U5472CE080-3 | LOT # A217071153 |
| biotinylated detection anti-guinea pig IFN-γ antibody N-G3 | GenScript | Order #:U5472CE080-1 | LOT # A21700598 |
| CTL S6 Micro Analyzer | ImmunoSpot | #S6MIC12 | automated ELISpot plate reader |
| Vi-CELL XR | Beckman-Coulter | 731050 | automated cell counter |
| ImmunoSpot 5.1 | ImmunoSpot | assay analysis software | |
| ESCO Class II Type A2 | ESCO | Biosafety cabinet | |
| Falcon cell strainer | Corning, Inc. | VWR cat# 21008-952 | |
| Exel Comfort Point Insulin syringe | MedLab Supply | 26028 | |
| Rotanta 460R | Hettich | centrifuge | |
| Vi-CELL XR Quad Pak Reagent Kit | Beckman Coulter | 383722 | |
| Incu Safe | Panasonic-Healthcare | incubator | |
| 22µm Filter | ThermoScientific | VWR act# 597-4520 | 22µm Filter |
| KimWipes | Kimberly-Clark Professional | VWR cat# 21903-005 | paper towels |
References
- Laddy, D. J., et al. Heterosubtypic protection against pathogenic human and avian influenza viruses via in vivo electroporation of synthetic consensus DNA antigens. PloS One. 3 (6), 2517 (2008).
- Lee, J. Y., Chang, J. Recombinant baculovirus-based vaccine expressing M2 protein induces protective CD8+ T-cell immunity against respiratory syncytial virus infection. Journal of Microbiology. 55 (11), 900-908 (2017).
- Kinnear, E., et al. Airway T cells protect against RSV infection in the absence of antibody. Mucosal Immunology. , (2017).
- Sridhar, S., et al. Cellular immune correlates of protection against symptomatic pandemic influenza. Nature Medicine. 19 (10), 1305-1312 (2013).
- Brand, H. K., et al. CD4+ T-cell counts and interleukin-8 and CCL-5 plasma concentrations discriminate disease severity in children with RSV infection. Pediatric Research. 73 (2), 187-193 (2013).
- Bouvier, N. M. Animal models for influenza virus transmission studies: a historical perspective. Current Opinion in Virology. 13, 101-108 (2015).
- St Claire, M. C., Ragland, D. R., Bollinger, L., Jahrling, P. B. Animal Models of Ebolavirus Infection. Comparative Medicine. 67 (3), 253-262 (2017).
- Todo, H. Transdermal Permeation of Drugs in Various Animal Species. Pharmaceutics. 9 (3), 33 (2017).
- Schafer, H., Burger, R. Tools for cellular immunology and vaccine research the in the guinea pig: monoclonal antibodies to cell surface antigens and cell lines. Vaccine. 30 (40), 5804-5811 (2012).
- Czerkinsky, C. C., Nilsson, L. A., Nygren, H., Ouchterlony, O., Tarkowski, A. A solid-phase enzyme-linked immunospot (ELISPOT) assay for enumeration of specific antibody-secreting cells. Journal of Immunological Methods. 65 (1-2), 109-121 (1983).
- Sedgwick, J. D., Holt, P. G. A solid-phase immunoenzymatic technique for the enumeration of specific antibody-secreting cells. Journal of Immunological Methods. 57 (1-3), 301-309 (1983).
- Moodie, Z., et al. Response definition criteria for ELISPOT assays revisited. Cancer Immunology, Immunotherapy. 59 (10), 1489-1501 (2010).
- Gillis, P. A., et al. Development of a novel, guinea pig-specific IFN-gamma ELISPOT assay and characterization of guinea pig cytomegalovirus GP83-specific cellular immune responses following immunization with a modified vaccinia virus Ankara (MVA)-vectored GP83 vaccine. Vaccine. 32 (31), 3963-3970 (2014).
- Schultheis, K., et al. Characterization of guinea pig T cell responses elicited after EP-assisted delivery of DNA vaccines to the skin. Vaccine. 35 (1), 61-70 (2017).
- . Mantoux Tuberculin Skin Test DVD Facilitator Guide – CDC (Part One) Available from: https://www.cdc.gov/tb/education/Mantoux/images/mantoux.pdf (2013)
- Birck, M. M., Tveden-Nyborg, P., Lindblad, M. M., Lykkesfeldt, J. Non-Terminal Blood Sampling Techniques in Guinea Pigs. Journal of Visualized Experiments. (92), e51982 (2014).
- Strober, W. Trypan Blue Exclusion Test of Cell Viability. Current Protocols in Immunology. 111, 1-3 (2014).
- Lewis, J. H. Comparative hematology: studies on guinea-pigs (Cavia porcellus). Comparative Biochemistry and Physiology: Comparative Physiology. 102 (3), 507-512 (1992).
- Flecknell, P., Flecknell, P. . Laboratory Animal Anaesthesia (Fourth Edition). , 77-108 (2016).
- Schaefer, H., Kliem, G., Kropp, B., Burger, R. Monoclonal antibodies to guinea pig interferon-gamma: tools for cytokine detection and neutralization. Journal of Immunological Methods. 328 (1-2), 106-117 (2007).
- Lipiainen, T., et al. Formulation and stability of cytokine therapeutics. Journal of Pharmaceutical Sciences. 104 (2), 307-326 (2015).
- Wang, X. Z., et al. Virus-Specific CD8 T Cells in Peripheral Tissues Are More Resistant to Apoptosis Than Those in Lymphoid Organs. Immunity. 18 (5), 631-642 (2003).
- Veron, P., et al. Deep Sequencing of T Cell Receptor in Peripheral Blood and Muscle from Adeno-Associated Virus Vector-Injected Subjects Reveals Differences in T Cell Clonality Between the Two Compartments. Molecular Therapy. 23, 210 (2015).
- Sckisel, G. D., et al. Differential phenotypes of memory CD4 and CD8 T cells in the spleen and peripheral tissues following immunostimulatory therapy. Journal for ImmunoTherapy of Cancer. 5 (1), 33 (2017).
- Yanofsky, V. R., Mitsui, H., Felsen, D., Carucci, J. A. Understanding Dendritic Cells and Their Role in Cutaneous Carcinoma and Cancer Immunotherapy. Clinical and Developmental Immunology. 2013, 624123 (2013).
- Amante, D. H., et al. Direct Transfection of Dendritic Cells in the Epidermis After Plasmid Delivery Enhanced by Surface Electroporation. Human Gene Therapy Methods. 25 (6), 315-316 (2014).
- Mahe, B., et al. Nanoparticle-based targeting of vaccine compounds to skin antigen-presenting cells by hair follicles and their transport in mice. Journal of Investigative Dermatology. 129 (5), 1156-1164 (2009).
- Vandermeulen, G., et al. Skin-specific promoters for genetic immunisation by DNA electroporation. Vaccine. 27 (32), 4272-4277 (2009).
- Brave, A., Nystrom, S., Roos, A. K., Applequist, S. E. Plasmid DNA vaccination using skin electroporation promotes poly-functional CD4 T-cell responses. Immunology and Cell Biology. 89 (3), 492-496 (2011).
- Romani, N., et al. Targeting skin dendritic cells to improve intradermal vaccination. Current Topics in Microbiology and Immunology. 351, 113-138 (2012).
- Smith, T. R., et al. DNA vaccination strategy targets epidermal dendritic cells, initiating their migration and induction of a host immune response. Molecular Therapy Methods & Clinical Development. 1, 14054 (2014).
- Teunissen, M. B., Haniffa, M., Collin, M. P. Insight into the immunobiology of human skin and functional specialization of skin dendritic cell subsets to innovate intradermal vaccination design. Current Topics in Microbiology and Immunology. 351, 25-76 (2012).
- Lin, F., et al. A novel prototype device for electroporation-enhanced DNA vaccine delivery simultaneously to both skin and muscle. Vaccine. 29 (39), 6771-6780 (2011).
- Laddy, D. J., et al. Electroporation of synthetic DNA antigens offers protection in nonhuman primates challenged with highly pathogenic avian influenza virus. Journal of Virology. 83 (9), 4624-4630 (2009).
- Lin, F., et al. Optimization of Electroporation-Enhanced Intradermal Delivery of DNA Vaccine Using a Minimally Invasive Surface Device. Human Gene Therapy Methods. 23 (3), 157-168 (2012).
- Kichaev, G., et al. Electroporation mediated DNA vaccination directly to a mucosal surface results in improved immune responses. Human Vaccines & Immunotherapeutics. 9 (10), 2041-2048 (2013).
- Klunner, T., Bartels, T., Vordermeier, M., Burger, R., Schafer, H. Immune reactions of CD4- and CD8-positive T cell subpopulations in spleen and lymph nodes of guinea pigs after vaccination with Bacillus Calmette Guerin. Vaccine. 19 (15-16), 1968-1977 (2001).
- Shedlock, D. J., et al. Induction of Broad Cytotoxic T Cells by Protective DNA Vaccination Against Marburg and Ebola. Molecular Therapy. 21 (7), 1432-1444 (2013).
- Hensel, M. T., et al. Prophylactic Herpes Simplex Virus 2 (HSV-2) Vaccines Adjuvanted with Stable Emulsion and Toll-Like Receptor 9 Agonist Induce a Robust HSV-2-Specific Cell-Mediated Immune Response, Protect against Symptomatic Disease, and Reduce the Latent Viral Reservoir. Journal of Virology. 91 (9), 02257 (2017).

