Fabrication de microbilles d'amyloïde-Sécrétion d'alginate pour l'utilisation dans la modélisation de la maladie d'Alzheimer
Summary
Ce protocole illustre une méthode d’encapsulation cellulaire par la gélation physique rapide de l’alginate pour immobiliser des cellules. Les microbilles obtenues permettent une sécrétion contrôlée et soutenue de l’amyloïde au fil du temps et peuvent être utilisées pour étudier les effets de l’amyloïde sécrété dans les modèles in vitro et in vivo.
Abstract
Selon l’hypothèse de la cascade amyloïde, le premier déclencheur dans le développement de la maladie d’Alzheimer (MA) est l’accumulation de fragments toxiques d’amyloïde,mD(A), conduisant éventuellement aux caractéristiques classiques de la maladie : plaques amyloïdes, neurofibrillaires et perte synaptique et neuronale. L’absence de modèles précliniques non transgéniques pertinents reflétant la progression de la maladie est l’un des principaux facteurs qui entravent la découverte de traitements médicamenteux efficaces. À cette fin, nous avons développé un protocole pour la fabrication de microbilles d’alginate contenant des cellules sécrétrices d’amyloïdes utiles pour l’étude des effets de la production chronique de l’A.
Des cellules d’ovaire de hamster chinois précédemment transfectées avec un gène humain d’APP, sécrétant des cellules de 7PA2 de A(c.-à-d.), ont été employées dans cette étude. Un modèle in vitro tridimensionnel (3D) pour la libération soutenue de A a été fabriqué par encapsulation des cellules 7PA2 dans l’alginate. Le processus a été optimisé pour cibler un diamètre de perle de 500-600 m pour d’autres études in vivo. L’optimisation de l’encapsulation de cellules 7PA2 dans l’alginate a été exécutée altérant des paramètres de fabrication, par exemple, concentration d’alginate, taux de flux de gel, potentiel électrostatique, fréquence de vibration de tête, solution de gélification. Les niveaux de Sécrétés A ont été analysés au fil du temps et comparés entre les perles d’alginate et les méthodes standard de culture cellulaire (jusqu’à 96 h).
Une concentration de 1,5 x 106 cellules 7PA2/mL et une concentration d’alginate de 2% (w/v) tamponnées avec HEPES et la gélification subséquente dans le chlorure de calcium de 0,5 M pendant 5 min se sont avérées pour fabriquer les microbilles les plus stables. Les microbilles fabriquées étaient 1) de taille uniforme, 2) avec un diamètre moyen de 550 m, 3) contenant environ 100-150 cellules par microbille et 4) capables de sécrétiser A.
En conclusion, notre méthode optimisée pour la production de microbilles d’alginate stables contenant des cellules 7PA2 amyloïdes pourrait permettre la modélisation d’aspects importants de la MA in vitro et in vivo.
Introduction
La modélisation des maladies neurodégénératives est difficile en raison de la nature complexe et complexe du cerveau. Dans la maladie d’Alzheimer (MA), la perte progressive de la fonction synaptique et la mort des neurones est considéré comme un effet en aval de la surproduction soutenue et l’accumulation de bêta-amyloïde (A) peptides suite à un traitement anormal du précurseur amyloïde protéine (APP) selon l’hypothèse de cascade amyloïde1.
Afin de comprendre les mécanismes de cette pathologie induite par l’amyloïde et d’aider à l’identification de nouvelles cibles de traitement, les scientifiques ont développé divers modèles précliniques in vivo. Une catégorie de modèles utilise une injection de bolus d’un peptide synthétique de L’A dans le cerveau du rat2,3,4. La principale limitation de ces modèles est qu’ils s’appuient sur un seul point ou des traitements répétés avec des peptides A en concentrations élevées déposées en une seule fois. Cela est incompatible avec la nature chronique et soutenue de la libération de a dans la maladie5. Une autre catégorie de modèles in vivo est des modèles animaux transgéniques exprimant une ou plusieurs mutations génétiques liées aux variations familiales de la maladie6,7,8,9, 10. Cependant, puisque la MA familiale ne représente que moins de 5 % de tous les cas d’Alzheimer11, la pertinence de ces modèles dans la traduction de la MA sporadique chez l’homme est discutable12. Un autre inconvénient de l’approche transgénique est la formation accélérée de A dès la naissance, qui se traduit par des déficits dans la fonction cognitive et des changements pathologiques trop rapidement et agressivement pour ressembler à la progression de la maladie dans la MA sporadique chez les patients12 . Par exemple, le modèle 5x FAD produit des plaques en aussi peu que 1,5 mois13.
Fait intéressant, ces deux catégories se traduisent par des changements dans la fonction cognitive de pertinence à la recherche AD2,3,4,5,6, et parfois ils sont accompagnés par le l’apparition des caractéristiques pathologiques de la maladie telles que les plaques amyloïdes6,8, phosphorylation tau6,7 et/ou perte synaptique et neuronale7,9, 14. Mais si ces types de modèles peuvent nous donner un aperçu des effets des niveaux élevés d’amyloïde dans le cerveau, qui sont souvent associés à des stades ultérieurs de la MA, ils ne reflètent pas les changements antérieurs exposés en réponse à l’exposition chronique et soutenue à l’A peptide12, comme l’expression altérée des marqueurs synaptiques15 et des composants de la matrice extracellulaire16. Par conséquent, il reste encore un besoin pour créer un modèle chronique qui illustre plus précisément les effets de la sécrétion soutenue de A sur la cognition in vivo et illustre des changements dans la pathologie.
À cette fin, nous avons développé un système qui permet la sécrétion constante et soutenue de aded d’une manière contrôlée en immobilisant les cellules amyloïdes-sécrétrices dans les microbilles d’hydrogel, qui peuvent être ensuite implantées dans le cerveau adulte de rat pour modéliser des aspects sporadiques.
L’alginate était le biomatériau sélectionné car il est biocompatible et n’induit aucune réponse défavorable lorsqu’il est implanté in vivo17. L’encapsulation cellulaire dans les hydrogels d’alginate a été bien établie au cours des quatre dernières décennies. Le premier exemple de sa traduction à la clinique a été rapporté pour le traitement du diabète de type 1 mellitus17. Le premier rapport de l’encapsulation réussie des îlots de Langerhans remonte à 1980. La transplantation de microbilles contenant des cellules sécrétrices d’insuline a révolutionné les options de traitement pour les patients diabétiques car elle a restauré la fonction pancréatique, éliminant le besoin de thérapie par injection d’insuline18. Ces travaux rendent compte de la façon dont l’encapsulation cellulaire peut les protéger contre les contraintes externes, qu’elles soient mécaniques ou chimiques. En fait, les perles d’alginate agissent comme une barrière et isolent les cellules de l’environnement environnant préservant leur phénotype, tout en permettant un accès suffisant aux médias environnants pour les nutriments et le dégagement des sous-produits cellulaires19. En outre, l’utilisation de l’alginate permet l’appariement des propriétés mécaniques des tissus mous20. Les hydrogels d’alginate peuvent être accordés pour avoir une rigidité de 1-30 kPa, en variant simplement la concentration d’alginate et la densité de liaison croisée20,21. Il s’agit d’un aspect essentiel, non seulement pour maintenir l’expression phénotypique des cellules encapsulées in vitro, mais aussi pour éviter tout effet inflammatoire après l’engraftment in vivo22.
Dans ce protocole, des cellules 7PA2 – une lignée de cellules d’ovaire de hamster chinois qui est transfectée de façon stable avec un gène muté APP V717F humain23 – sont utilisées. Ces cellules produisent continuellement des produits catalytiques de l’APP, y compris A1-4224,25, et ont été utilisés pour générer a comme une alternative à la production synthétique dans les études précliniques, aigus in vivo26. Nous décrivons une méthode de fabrication pour immobiliser les cellules 7PA2 dans les microbilles d’alginate « molles », conçues pour permettre la sécrétion soutenue de biomolécules. Comme preuve de concept, nous rendons compte de la libération du peptideA-1-42 au fil du temps. L’alginate qui est utilisé est un alginate à faible viscosité avec un poids moléculaire de 120 000 à 190 000 g/mol et un rapport mannuronique à guluronique de 1,56 (M/G).
Dans d’autres études, ces microbilles peuvent être transplantées en toute sécurité dans les régions du cerveau de rat d’intérêt pour la MA (par exemple, l’hippocampe) pour étudier les effets de la sécrétion chronique de l’A sur le comportement in vivo et la pathologie exvivo. En outre, ce système peut être utilisé pour étudier les effets de la libération chronique de la maladie de La DmD dans les applications in vitro et ex vivo. Par exemple, les microbilles d’alginate contenant 7PA2 peuvent être co-cultivées in vitro avec des cultures neuronales ou astrocytiques afin d’évaluer les effets de l’exposition chronique à l’A sur les mécanismes cellulaires associés à la MA. En outre, cette méthode peut être utilisée pour examiner la relation entre la production chronique de a et la potentialisation à long terme dans l’électrophysiologie ex vivo.
Le point culminant de ce protocole est la modularité et la flexibilité de la méthode de fabrication, qui permet la fabrication de perles d’alginate avec une dimension cible par des paramètres de fabrication de réglage fin. Selon l’application, le protocole peut être ajusté pour obtenir des cibles sur mesure en ce qui concerne la taille des microbilles, la densité des cellules encapsulées et la rigidité des microbilles. Ce protocole peut être utilisé pour l’encapsulation d’une variété de types de cellules, en développant des modèles in vitro tridimensionnels (3D) plus pertinents pour étudier différentes pathologies. Nous avons récemment rapporté sur la façon dont les cellules encapsulées d’alginate peuvent être employées pour modéliser les premiers stades de la progression de cancer20.
Le concept du processus d’encapsulation est basé sur l’extrusion d’un jet laminaire de cellules suspendues dans une solution d’alginate par une buse. Une tête vibrante perturbe le jet avec une fréquence contrôlée résultant en gouttelettes à base d’alginate de taille égale. Un champ électrique externe permet la séparation des gouttelettes formées à base d’alginate, qui, au contact d’une solution enrichie en ions divalents, tels que les ions de calcium, peuvent rapidement se croiser, préservant leur forme sphérique. L’incubation dans la solution de gélation permet la formation de microbilles sphériques contenant des cellules dans un hydrogel physique homogène27. La taille cible des microbilles et des hydrogels d’alginate permet l’échange d’éléments nutritifs et d’oxygène avec les supports de culture cellulaire pendant de longues périodes (semaines). Figure 1 Un spectacle une représentation schématique de l’appareil d’encapsulation utilisé (Figure 1B).
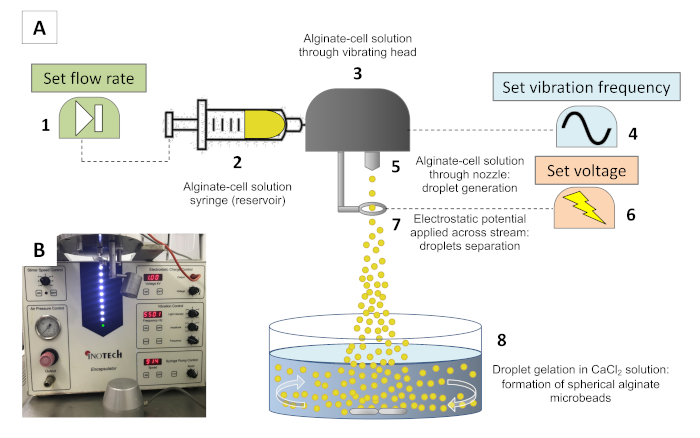
Figure 1 : Le système d’encapsulation. (A) Représentation schématique du système d’encapsulation. Une suspension à cellules d’alginate est chargée dans une seringue (2) et alimentée à travers un réservoir à une vitesse d’extrusion fixée à la pompe à seringue (1). Dans le réservoir, un chapeau de vibration (3) vibre à une fréquence fixée par un générateur de forme d’onde (4) pour perturber le flux à intervalles égaux, formant des gouttelettes de taille égale. Lorsque la solution est alimentée par une buse (5) et que des gouttelettes sont formées, un potentiel électrostatique est appliqué sur une électrode (7) fixée par un générateur de tension (6), qui charge légèrement la surface des gouttelettes, ce qui permet au flux de se propager à la suite de la répulsion forces électrostatiques. Pendant que les gouttelettes s’engagent avec le bain de gel (8), Ca2-conduit le croisement de l’alginate entraîne la formation de microbilles sphériques. (B) Photographie de l’encapsulateur avant la fabrication de microbilles d’alginate. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
La taille des microbilles peut être modifiée en fonction de l’utilisation prévue. Afin de contrôler la taille de la microbille, les différents paramètres décrits à la figure 1A et dans le protocole sont ajustés en conséquence. Le diamètre interne de la buse utilisée a un impact substantiel sur la taille des gouttelettes; l’ajustement des paramètres d’encapsulation, à savoir la vitesse d’extrusion, la fréquence des vibrations et la tension, est essentiel pour parvenir à une distribution de taille cohérente. Tableau 1 décrit comment les différents paramètres peuvent modifier la taille des microbilles obtenues avec ce système.
| paramètre | Taille de la buse | Fréquence des vibrations | Débit | Tension d’électrode |
 |
 |
 |
 |
|
| Taille de perle |
 
|
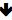 |
 |
– |
Tableau 1 : Paramètres de fabrication et leur influence sur la taille des microbilles. Le tableau illustre comment chaque paramètre peut influencer la taille résultante des microbilles fabriquées, indépendamment de la buse et de la viscosité de la solution utilisée.
Protocol
Representative Results
Discussion
La méthode décrite dans cet article est utile pour encapsuler les cellules réalisant une distribution de taille étroite des microbilles d’alginate27. Il offre également l’avantage de cultiver des cellules dans un environnement immuno-isolé17,19, les protégeant du stress externe. En outre, l’encapsulation des cellules dans l’alginate imite plus étroitement les conditions physiologiques, en particulier en ce qui concerne les interactions cellule-cellule et la rigidité de matrice20. Ces facteurs sont tous particulièrement cruciaux pour une utilisation ultérieure dans les applications pertinentes, telles que l’engraftment in vivo, empêchant les réactions immunitaires potentielles dans le tissu environnant17. En outre, un avantage majeur de ce protocole est la facilité d’aétibilité en fonction de l’application de l’intérêt: il est possible de modifier le protocole et d’optimiser les paramètres pour la fabrication de perles plus grandes ou plus petites, et plus doux ou plus rigides. La méthode décrite est utilisée pour fabriquer des perles assez petites pour être injectées avec des méthodes mini-invasives, et suffisamment grandes pour accueillir un certain nombre de cellules et fournir une libération suffisante de A pour avoir des effets comportementaux et pathologiques observables lors de l’injection dans les modèles animaux.
Le succès de ce protocole dépend d’un certain nombre d’étapes critiques. La manipulation soigneuse des cellules et les techniques optimales de culture cellulaire sont importantes pour maintenir la viabilité et la fonction cellulaires20,28. L’utilisation de conditions de culture standard assure la conservation du fonctionnement normal des cellules 7PA2, comme on l’observe. Cela permet un profil de libération similaire pour A1-42 à partir de cellules encapsulées par rapport aux cultures 2D. En outre, pour que le protocole fonctionne de manière optimale, une solution d’alginate à faible viscosité garantit de meilleurs résultats par rapport à une solution alginate à haute viscosité. Cela garantit qu’un jet laminaire homogène est extrudé par la buse et une distribution uniforme des cellules dans la matrice des perles fabriquées27. Les matériaux utilisés pour encapsuler les cellules doivent avoir un mécanisme de gélification très rapide, permettant la rétention de la forme.
Une autre étape critique dans ce protocole est la manipulation des microbilles fabriquées après la gélification. Ici, nous montrons la récupération des microbilles en utilisant une grande pipette en plastique d’ouverture pour transférer les perles. Alternativement, verser la solution de chlorure de calcium contenant les microbilles dans un filtre à mailles peut être utilisé pour la récupération de perles. Une grande pipette sérologique (5, 10 ou 25 ml) peut être utilisée pour dessiner les microbilles, puis lavée à travers le filtre à mailles au lieu de verser. L’avantage de ceci est une plus grande confiance dans la stérilité de la procédure comparée à verser. Cependant, les limites sont que certaines perles peuvent être déformées si elles sont comprimées par la pipette, en plus de risquer un rendement plus faible si une grande proportion de microbilles ne sont pas sauvés.
Cette approche a été utilisée pour encapsuler différentes lignées cellulaires afin de modéliser et d’étudier différentes maladies (p. ex., la libération d’insuline provenant d’îns pancréatiques encapsulés). La nouveauté de notre approche est l’engraftment des microbilles générées en utilisant ce protocole comme méthode utile dans la modélisation des aspects importants de la maladie d’Alzheimer in vivo. En comparant le profil de libération des cellules encapsulées (Figure 4) aux niveaux de A ‘ générés par une injection de bolus (comme celle rapportée dans d’autres études3,26), une libération plus chronique et soutenue de A peut être Attendu. La figure 6 illustre la tendance prévue qui peut être atteinte. L’utilisation de ce système pour la modélisation in vivo est plus pertinente pour la façon dont la maladie progresse et peut être plus utile dans la découverte et le développement de médicaments.
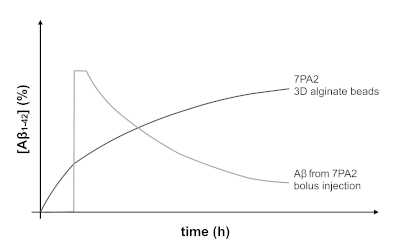
Figure 6 : Profil de libération prévu de a 1-42 à partir de cellules 7PA2 encapsulées par rapport à une injection de bolus. Le profil de la libération de l’A mD provenant de microbilles contenant 7PA2 greffées permet de tester les effets de l’A chronique et de l’A soutenue dans un modèle animal de pertinence pour la MA. Inversement, une injection de bolus créerait un pic dans les niveaux de A sur une courte période de temps, suivie d’un dégagement rapide de A du cerveau. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Les auteurs tient à remercier M. Kajen Suresparan, le Dr Jonathan Wubetu, M. Dominik Grudzinski, Mlle Chen Zhao et le Dr Thierry Pilot pour leur aide dans l’optimisation de la fabrication de microbilles d’alginate, de la culture cellulaire et de la détection a Discussions.
Materials
| µManager software | Vale Lab, UCSF, USA | v.1.46 | |
| 0.22 um PES filter | Merck, UK | SLGP033RS | |
| 15mm Netwell insert 74 um mesh filter | Constar, usa | #3477 | |
| Alginic acid sodium salt from brown algae | Sigma-Aldrich,uk | A0682 | |
| Calcium chloride | Sigma-Aldrich,uk | C1016 | |
| CellTiter96 AQueous One Solution cell proliferation assay | Promega, USA | G3580 | |
| Encapsulator | Inotech | IE-50 | serial no. 05.002.01-2005 |
| HEPES | Sigma-Aldrich,uk | H4024 | |
| Hu Aβ 1-42 ELISA | ThermoFisher, UK | KHB3441 | |
| ImageJ software | ImageJ | v1.49p | |
| Inverted light microscope | Olympus | CKX41 | |
| Leica microscope | Leica microsystems, UK | DMI6000B | |
| Neo sCMOS Camera | Ander, UK | 5.5 | |
| Phosphate buffered saline | Sigma-Aldrich,uk | D1408 | |
| Sodium chloride | Sigma-Aldrich,uk | 433209 | |
| Trispdium citrate dihydrate | Sigma-Aldrich,uk | W302600-K | |
| Trypsin-EDTA solution | Sigma-Aldrich,uk | T4049 |
References
- Hardy, J. A., Higgins, G. A. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 256, 184-185 (1992).
- Karthick, C., et al. Time-dependent effect of oligomeric amyloid-β (1-42)-induced hippocampal neurodegeneration in rat model of Alzheimer’s disease. Neurological Research. 41 (2), 139-150 (2018).
- Watremez, W., et al. Stabilized Low-n Amyloid-β Oligomers Induce Robust Novel Object Recognition Deficits Associated with Inflammatory, Synaptic, and GABAergic Dysfunction in the Rat. Journal of Alzheimer’s Disease. 62 (1), 213-226 (2018).
- Brouillette, J., et al. Neurotoxicity and memory deficits induced by soluble low-molecular-weight amyloid-β1-42 oligomers are revealed in vivo by using a novel animal model. Journal of Neurosciences. 32 (23), 7852-7861 (2012).
- Solana, C., Tarazona, R., Solana, R. Immunosenescence of Natural Killer Cells, Inflammation, and Alzheimer’s Disease. International Journal of Alzheimer’s Disease. , 3128758 (2018).
- Sturchler-Pierrat, C., et al. Two amyloid precursor protein transgenic mouse models with Alzheimer disease-like pathology. Proceedings of the National Academy of Sciences of the United States of America. 94 (24), 13287-13292 (1997).
- Tomiyama, T., et al. A mouse model of amyloid beta oligomers: their contribution to synaptic alteration, abnormal tau phosphorylation, glial activation, and neuronal loss in vivo. Journal of Neurosciences. 30 (14), 4845-4856 (2010).
- Saito, T., et al. Single App knock-in mouse models of Alzheimer’s disease. Nature Neurosciences. 17 (5), 661-663 (2014).
- Oddo, S., et al. Triple-Transgenic Model of Alzheimer’s Disease with Plaques and Tangles: Intracellular A and Synaptic Dysfunction. Neuron. 39 (3), 409-421 (2003).
- Leon, W. C., et al. A Novel Transgenic Rat Model with a Full Alzheimer’s-Like Amyloid Pathology Displays Pre-Plaque Intracellular Amyloid-β-Associated Cognitive Impairment. Journal of Alzheimer’s Disease. 20 (1), 113-126 (2010).
- Prince, M., et al. Dementia UK: Second Edition – Overview. Alzheimer’s Society. , 61 (2007).
- Cavanaugh, S. E., Pippin, J. J., Barnard, N. D. Animal models of Alzheimer disease: historical pitfalls and a path forward. Alternatives to animal experimentation. 31 (3), 279-302 (2014).
- Oakley, H., et al. Intraneuronal β-Amyloid Aggregates, Neurodegeneration, and Neuron Loss in Transgenic Mice with Five Familial Alzheimer’s Disease Mutations: Potential Factors in Amyloid Plaque Formation. The Journal of Neuroscience. 26 (40), 10129-10140 (2006).
- Forny-Germano, L., et al. Alzheimer’s Disease-Like Pathology Induced by Amyloid-β Oligomers in Nonhuman Primates. Journal of Neuroscience. 34 (41), 13629-13643 (2014).
- Masliah, E., et al. Altered expression of synaptic proteins occurs early during progression of Alzheimer’s disease. Neurology. 56 (1), 127-129 (2001).
- Lepelletier, F. X., Mann, D. M. A., Robinson, A. C., Pinteaux, E., Boutin, H. Early changes in extracellular matrix in Alzheimer’s disease. Neuropathology and Applied Neurobiology. 43 (2), 167-182 (2017).
- Calafiore, R., Basta, G. Clinical application of microencapsulated islets: Actual prospectives on progress and challenges. Advanced Drug Delivery Reviews. 67-68, 84-92 (2014).
- Lim, F., Sun, A. M. Microencapsulated islets as bioartificial endocrine pancreas. Science. 210 (4472), 908-910 (1980).
- Tran, N. M., et al. Alginate hydrogel protects encapsulated hepatic HuH-7 cells against hepatitis C virus and other viral infections. PLoS One. 9 (10), 109969 (2014).
- Rios de la Rosa, J. M., Wubetu, J., Tirelli, N., Tirella, A. Colorectal tumor 3D in vitro models: advantages of biofabrication for the recapitulation of early stages of tumour development. Biomedical Physics & Engineering Express. 4 (4), 045010 (2018).
- Tirella, A., Orsini, A., Vozzi, G., Ahluwalia, A. A phase diagram for microfabrication of geometrically controlled hydrogel scaffolds. Biofabrication. 1 (4), 045002 (2009).
- Smalley, K. S. M., Lioni, M., Herlyn, M. Life ins’t flat: Taking cancer biology to the next dimension. In Vitro Cellular & Developmental Biology – Animal. 42 (8-9), 242-247 (2006).
- Podlisny, M. B., et al. Aggregation of secreted amyloid beta-protein into sodium dodecyl sulfate-stable oligomers in cell culture. Journal of Biological Chemistry. 270 (16), 9564-9570 (1995).
- Portelius, E., et al. Mass spectrometric characterization of amyloid-β species in the 7PA2 cell model of Alzheimer’s disease. Journal of Alzheimer’s Disease. 33 (1), 85-93 (2013).
- Welzel, A. T., et al. Secreted amyloid β-proteins in a cell culture model include N-terminally extended peptides that impair synaptic plasticity. Biochimie. 53 (24), 3908-3921 (2014).
- O’Hare, E., et al. Orally bioavailable small molecule drug protects memory in Alzheimer’s disease models. Neurobiology of Aging. 34 (4), 1116-1125 (2013).
- Nedović, V., Willaert, R. Fundamentals of Cell Immobilisation Biotechnology. Methods and Technologies for Cell Immobilisation/Encapsulation. , 185-204 (2004).
- Omer, A., et al. Long-term Normoglycemia in Rats Receiving Transplants with Encapsulated Islets. Transplantation. 79 (1), 52-58 (2005).

