단백질 흡착 및 폴리머 역학의 석영 결정 미세 균형 측정시 시료 준비
Summary
석영 크리스탈 마이크로 저울은 생물 의학 및 환경 감지, 코팅 및 폴리머 과학의 조사와 관련된 미크론 또는 서브미크론 범위의 필름에 대한 정확한 질량 및 점탄성 특성을 제공할 수 있습니다. 샘플 두께는 센서와 접촉하는 재료로부터 정보를 얻을 수 있는 영향을 미칩니다.
Abstract
이 연구에서는 석영 결정 미세 균형 실험에 대한 박막 준비가 데이터의 적절한 모델링을 알리고 필름의 특성을 정량화할 수 있는 방법을 결정하는 다양한 예제를 제시합니다. 석영 크리스탈 마이크로밸런스는 고주파로 진동하는 석영 결정의 기계적 공명 변화를 관찰하여 적용된 필름의 질량 및/또는 기계적 특성의 미세한 변화를 측정하기 위한 독특하고 민감한 플랫폼을 제공합니다. 이 방법의 장점은 실험적 다양성, 광범위한 실험 시간 길이에 대한 특성 의 변화를 연구할 수 있는 능력, 작은 샘플 크기의 사용 등이 있습니다. 센서에 증착된 층의 두께와 전단 계수를 기반으로 재료와 다른 정보를 얻을 수 있음을 입증합니다. 여기서, 이 개념은 특히 염 농도의 함수로서 팽창 시 금 및 다연산염 복합체에 흡착된 콜라겐의 질량 및 점탄성 계산을 초래하는 실험 파라미터를 표시하기 위해 이용된다.
Introduction
석영 크리스탈 마이크로 밸런스 (QCM)는 표면에 부착 된 질량에 의존하는 공진 주파수를 모니터링하기 위해 석영 결정의 압전 효과를 활용합니다. 이 기술은 AT 컷 석영 결정 센서의 공진 주파수 및 대역폭(전형적으로 5MHz범위)의 공기 또는 유체를 필름증착 후 센서의 주파수 및 대역폭과 비교합니다. QCM을 사용하여 질량에 대한 높은 감도 및 점탄성 특성 변화(샘플 균일도 및 두께에 따라 다름), situ2에서연구를 수행할 수 있는 능력 및 기존 전단 유변학 또는 동적 기계적 분석(DMA)보다 훨씬 짧은 유변학 적 시량을 조사하는 기능을 포함하여 박막 특성 및 인터페이스를 연구하는 데는 몇 가지 이점이 있습니다. 짧은 유변학적 시간 척도를 조사하면 이 시점의 응답이 매우 짧은 (ms)3 및 긴(년) 기간 동안 어떻게 변경되는지 관찰할 수 있습니다4. 이 기능은 다양한 운동 과정의 연구에 유익하며 또한 전통적인 유변학 기술5,6의유용한 확장이다.
QCM의 높은 감도는 또한 극히 작은 생체 분자의 근본적인 상호 작용을 연구하는 생물학 응용에 있는 그것의 무거운 사용으로 이끌어 냈습니다. 코팅되지 않았거나 기능화된 센서 표면은 단백질 흡착을 조사하는 데 사용될 수 있습니다. 더욱이, 효소, 항체 및 압타머 사이의 복잡한 결합 이벤트를 통한 바이오센싱은 질량7,8,9의변화에 기초하여 조사될 수 있다. 예를 들어, 이 기술은 주파수 및점탄성(10)의상관관계를 관찰함으로써 유체-함유 소포를 경질 구조로 흡착하는 2상 과정으로서 평면 지질 이중층으로 소포의 변형을 이해하는 데 사용되어 왔다. 최근 몇 년 동안, QCM은 소포 또는 나노 입자(11)에의한 약물 전달을 모니터링할 수있는 강력한 플랫폼을 추가로 제공했다. 재료 공학 및 분자 및 세포 생물학의 교차점에서, 우리는 단백질, 핵산, 리포솜 및 세포와 같은 물질과 생리 활성 성분 사이의 주요 상호 작용을 해명하기 위해 QCM을 사용할 수 있습니다. 예를 들어, 생체물질에 대한 단백질 흡착은 염증과 같은 하류 세포 반응을 중재하고 생체 적합성의 긍정적인 지표로 자주 사용되며, 다른 경우에는 혈액과 접촉하는 코팅에 세포외 단백질 부착이 혈관12,13에서위험한 응고를 유도할 수 있다. 따라서 QCM은 다양한 요구에 적합한 후보를 선택하는 도구로 사용할 수 있습니다.
QCM 실험을 수행하기 위한 두 가지 일반적인 접근법은 실험으로부터 유사한 데이터를 수집합니다: 제1 접근법은 전도도 피크의 주파수 시프트 및 반대역폭(Γ)을기록합니다. 두 번째 접근법인 QCM(D)은 주파수 시프트와 발산 계수를 기록하며, 이는 방정식 1,14를 통해 Γ에 정비례합니다.
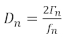 (1)
(1)
여기서 D는 소멸 계수이고 θ는 주파수입니다. D와 Γ 는 필름이 센서에 미치는 감쇠 효과와 관련이 있으며, 이는 필름의 강성을 나타냅니다. 서브스크립트 n은 쿼츠 센서의 홀수 공진 주파수인 주파수 배음 또는 고조파를 나타냅니다(n = 1, 3, 5, 7…). 필름의 질량 및 점탄성 특성을 얻기 위해 다중 고조파를 사용하는 모델에 대한 추가 논의는 요한스만14 및 Shull 그룹15,16,17,18의이전 논문에 의한 검토에서 찾을 수 있다.
QCM 샘플을 준비하기 위한 한 가지 주요 고려 사항은 센서 표면에 박막을 적용하는 방법입니다. 몇 가지 일반적인 방법은 실험19,20동안 센서 표면에 필름의 스핀 코팅, 딥 코팅, 드롭 코팅, 또는 흡착을 포함한다. QCM 샘플에는 사우어브레이 한계, 점탄성 정권, 벌크 정권 및 과다 댐프드 정권의 네 가지 영역이 있습니다. 충분히 얇은 필름의 경우, 사우어브레이 한계가 적용되며, 여기서 주파수시프트(Δδ)는 필름의 표면 질량 밀도를 제공한다. Sauerbrey 한계 내에서 주파수 시프트는 공진 고조파, n 및 감쇠 계수(D 또는 Γ)의변화에 따라 선형으로 스케일링됩니다. 이 정권에서 충분한 정보는 추가 가정을하지 않고 계층의 유변학적 특성을 고유하게 결정할 수 없다. 이 정권의 데이터는 필름의 표면 질량 밀도(또는 밀도가 선험적이라고알려진 경우 두께)를 계산하는 데 사용됩니다. 결정과 접촉하는 매체가 충분히 두꺼운 벌크 정권에서, 전단 전단 파는 완전히 완충되기 전에 매체로 전파됩니다. 여기서, Δ를 사용하여 질량 정보를 얻을 수 없다. 그러나, 이 지역에서, 점탄성 특성은 Δδ 및 ΔΓ 15,18의조합을 사용하여 안정적으로 결정된다. 벌크 정권에서 매체가 너무 단단하면 필름이 센서의 공명을 축축하게하여 QCM에서 신뢰할 수있는 데이터의 수집을 방지합니다. 점탄성 정권은 필름이 필름을 통해 완전히 전파될 수 있을 만큼 필름이 충분히 얇을 뿐만 아니라 감쇠 계수에 대한 신뢰할 수 있는 값을 가지는 중간 정권입니다. 감쇠 계수 와 Δδ는 필름의 점탄성 특성뿐만 아니라 질량을 결정하는 데 사용할 수 있습니다. 여기서, 점탄성 특성은 복합 전단 계수의 밀도 및 크기의 생성에 의해 주어진 | G*| p 및 Φ = 아크탄(G”/ G’)에의해 주어진 위상 각도. 필름이 사우어브레이 한계에서 제조될 때, 단위 면적당 질량은21이하의 Sauerbrey 방정식에 따라 직접 계산될 수 있습니다.
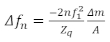 (2)
(2)
여기서 Δ는공진 주파수의 변화, n은 관심의 배음이고, θ1은 센서의 공진 주파수이고, Δ m/A는 필름의 면적당 질량이고, Z q는 쿼츠의 음향 임피던스이며, AT 컷 쿼츠는 Zq = 8.84 x 106 kg/m2s이다. 점탄성 정권은 중합체 막의 연구에 가장 적합하며, 벌크 한계는 점성 중합체22 또는 단백질용액(16)을연구하는데 유용하다. 다른 정권은 관심있는 재료의 특성에 따라 달라지며, 전체 점탄성 및 질량 특성화를위한 최적의 두께는 일반적으로 필름 강성에 따라 증가합니다. 도 1은 필름의 아리얼 밀도, 복잡한 전단 계수 및 위상 각도에 대하여 4개의 영역을 설명하며, 여기서 우리는 위상 각도와 이러한 유형의 재료와 관련이 있는 것으로 나타난 필름 강성 사이의 특정 관계를 가정했습니다. 실용적인 관심의 많은 필름은 두께가 수십 에서 수백 미크론23의순서에있는 특정 생물 막과 같은 QCM을 사용하여 점탄성 특성을 연구하기에 너무 두껍습니다. 이러한 두꺼운 필름은 일반적으로 QCM을 사용하여 연구하기에 적합하지 않지만 훨씬 낮은 주파수 공진기(예:비틀림 공진기)(예: 비틀림 공진기)를 사용하여 측정될 수 있으며, 전단파가 필름 내로 더 전파될 수 있도록 한다.
주어진 QCM 샘플과 어떤 식이 관련이 있는지 를 결정하기 위해, 액영 결정 센서의 기계적 진동에 대한 필름두께(d)의비율인 d/λ n 파라미터를 이해하는 것이 중요하다(λn)15,16, 18. 이상적인 점탄성 정권은 d /λn = 0.05 – 0.218이며,여기서 0.05 미만의 값은 Sauerbrey 한계 내에 있고 0.2 이상의 값은 벌크 정권에 접근합니다. d/λ n에 대한 보다 엄격한 설명은 다른곳에서 15,18,제공되지만, 사우어브레이 한계 및 점탄성 한계를 delineating 하는 정량적 파라미터이다. 아래 에서 사용되는 분석 프로그램은 이 매개 변수를 직접 제공합니다.
QCM으로 박막을 분석하는 데는 몇 가지 추가 제한사항이 있습니다. Sauerbrey 및 점탄성 계산은 필름 두께 전체와 QCM의 전극 표면을 가로질러 필름이 균일하다고 가정합니다. 이 가정은 공극이나 필러가 존재하는 필름을 연구하는 것을 어렵게 만드는 동안, 접목 된 나노 입자6로구성된 필름에 대한 몇 가지 QCM 조사가 있었습니다. 전체 막 두께에 비해 이질성이 작으면 복합 시스템의 신뢰할 수 있는 점탄성 특성을 여전히 얻을 수 있습니다. 보다 이질적인 시스템의 경우 점탄성 분석에서 얻은 값은 항상 신중하게 보아야 합니다. 이상적으로는 알 수 없는 이질성이 있는 시스템에서 얻은 결과를 균질한 것으로 알려진 시스템에 대해 검증해야 합니다. 이 문서에서 설명하는 예제 시스템에서 수행한 접근 방식입니다.
이 백서에서 설명하는 중요한 점은 주파수 도메인(Γ가 보고되는 위치)에서 수행된 QCM 측정과 시간 도메인 실험(D가 보고되는 위치) 간의 정확한 대응입니다. 두 개의 서로 다른 QCM 실험( 일회성 도메인 및 하나의 주파수 도메인)의 결과가 각각 다르지만 개념적으로 관련된 모델 시스템을 수반하는 것으로 설명되어 있습니다. 첫 번째 시스템은 시간 영역(QCM-D) 측정 동안 시간에 걸친 대표적인 결합 역학 및 흡착의 평형을 설명하기 위해 센서에 콜라겐 부착의 간단한 예입니다. 콜라겐은 신체에서 가장 풍부한 단백질로, 결합 행동과 형태학의 다양성으로 알려져 있습니다. 여기서 사용되는 콜라겐 용액은 흡착을 유도하기 위해 센서의 금 표면의 추가적인 기능화를 필요로 하지 않는다9. 상기 제2 실험 시스템은 음이온성 폴리스티렌 설포네이트(PSS) 및 양이온폴리(diallyldimethylammonium)(PDADMA)로 구성된 다연화 복합체(PEC)가 사드만 등22와동일한 방식으로 제조된다. 이러한 재료는 팽창하고 염 (이 경우 KBr) 솔루션에 부드러운된다, 주파수 도메인 접근 방식을 사용하여 폴리머 역학을 공부하기위한 간단한 플랫폼을 제공 (QCM-Z). 각 프로토콜에 대해 측정을 준비, 복용 및 분석하는 프로세스는 그림 2에나와 있습니다. 회로도는 QCM-Z와 QCM-D 접근법간의 주요 차이점이 실험에 사용된 데이터 수집 단계와 계측에 있음을 보여줍니다. 언급된 모든 샘플 전처리 기법은 두 가지 접근법과 호환되며, 각 접근법은 도 1에도시된 세 가지 영역에서 샘플을 분석할 수 있다.
우리의 데이터는 측정 전이나 측정 중에 센서 코팅에 의한 시료의 제조가 시스템의 점탄성 특성을 추출하는 능력을 지시한다는 것을 보여줍니다. 실험의 초기 단계를 적절하게 설계하여 분석 단계에서 정확하게 수집할 수 있는 정보를 결정할 수 있습니다.
Protocol
Representative Results
Discussion
콜라겐 흡착 결과는 사우어브레이 및 점탄성 정권에 걸쳐 있습니다. 해당 고조파 수로 정규화된 주파수 시프트를 플로팅함으로써 Sauerbrey 한계가 측정의 처음 2시간 동안 유효합니다. 그러나 센서에 대한 질량 준수량이 증가함에 따라 세 번째 및 다섯 번째 고조파에 대한 정규화된 주파수 이동이 서로 이탈하기시작합니다(t > 2 h)는 흡착 필름의 점탄성 특성을 결정하는 능력을 나타냅니다.</p…
Divulgations
The authors have nothing to disclose.
Acknowledgements
이 작업은 NSF (DMR-1710491, OISE-1743748)에 의해 지원되었다. J.R. 및 E.S.는 NSF(DMR-1751308)의 지원을 인정합니다.
Materials
| Acetic acid | Sigma-Aldrich | A6283 | For collagen adsorption |
| Ammonium hydroxide solution | Sigma-Aldrich | 221228 | For collagen adsorption |
| Aqueous QCM probe | AWSensors | CLS 00050 A | For polyelectrolyte swelling |
| Collagen I Rat Protein, Tail | Thermo Fisher Scientific | A1048301 | For collagen adsorption |
| Distilled water | Sigma-Aldrich | EM3234 | For polyelectrolyte swelling; generally easy to acquire in research labs, but there is a catalog number in case it is not accessible |
| Ethanol | Sigma-Aldrich | 793175-1GA-PB | For polyelectrolyte swelling |
| Gibco Phosphate Buffered Saline | Thermo Fisher Scientific | 20012-027 | For collagen adsorption |
| Hellmanex III | Sigma-Aldrich | Z805939 | For collagen adsorption |
| Hydrogen peroxide solution | Sigma-Aldrich | 216763 | For collagen adsorption |
| Kimberly-Clark Professional Kimtech Science Kimwipes Delicate Task Wipers, 1-Ply | Fisher Scientific | 06-666A | For polyelectrolyte swelling |
| NP2K VNA | Makarov Instruments | For polyelectrolyte swelling | |
| Poly(diallyldimethylammonium chloride), MW 200,000 | Sigma-Aldrich | 409022 | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Poly(styrene-sulfonate) sodium salt 30% weight in water | Sigma-Aldrich | 561967-500G | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Potassium Bromide | Sigma-Aldrich | 793604-1KG | For polyelectrolyte swelling |
| QSense QCM Explorer System | Biolin Scientific | For collagen adsorption | |
| Sodium acetate, anhydrous | Sigma-Aldrich | S2889 | For collagen adsorption |
| Spin coater, Model WS-650MZ-23NPP | Laurell technologies | For polyelectrolyte swelling |
References
- Marx, K. A. Quartz crystal microbalance: A useful tool for studying thin polymer films and complex biomolecular systems at the solution – Surface interface. Biomacromolecules. 4 (5), 1099-1120 (2003).
- Kleber, C., Hilfrich, U., Schreiner, M. In situ QCM and TM-AFM investigations of the early stages of degradation of silver and copper surfaces. Applied Surface Science. 253 (7), 3712-3721 (2007).
- Yeh, C. J., Hu, M., Shull, K. R. Oxygen Inhibition of Radical Polymerizations Investigated with the Rheometric Quartz Crystal Microbalance. Macromolecules. 51 (15), 5511-5518 (2018).
- Sturdy, L. F., Yee, A., Casadio, F., Shull, K. R. Quantitative characterization of alkyd cure kinetics with the quartz crystal microbalance. Polymer. 103, 387-396 (2016).
- Delgado, D. E., Sturdy, L. F., Burkhart, C. W., Shull, K. R. Validation of quartz crystal rheometry in the megahertz frequency regime. Journal of Polymer Science, Part B: Polymer Physics. , 1-9 (2019).
- Bilchak, C. R., Huang, Y., Benicewicz, B. C., Durning, C. J., Kumar, S. K. High-Frequency Mechanical Behavior of Pure Polymer-Grafted Nanoparticle Constructs. ACS Macro Letters. 8 (3), 294-298 (2019).
- Hook, F., Rodahl, M., Brzezinski, P., Kasemo, B. Energy dissipation kinetics for protein and antibody-antigen adsorption under shear oscillation on a quartz crystal microbalance. Langmuir. 14, 729-734 (1998).
- Liss, M., Petersen, B., Wolf, H., Prohaska, E. An aptamer-based quartz crystal protein biosensor. Analytical Chemistry. 74 (17), 4488-4495 (2002).
- Felgueiras, H. P., Murthy, N. S., Sommerfeld, S. D., Brás, M. M., Migonney, V., Kohn, J. Competitive Adsorption of Plasma Proteins Using a Quartz Crystal Microbalance. ACS Applied Materials and Interfaces. 8 (21), 13207-13217 (2016).
- Keller, C. A., Kasemo, B. Surface specific kinetics of lipid vesicle adsorption measured with a quartz crystal microbalance. Biophysical Journal. 75, 1397-1402 (1998).
- Olsson, A. L. J., Quevedo, I. R., He, D., Basnet, M., Tufenkji, N. Using the quartz crystal microbalance with dissipation monitoring to evaluate the size of nanoparticles deposited on surfaces. ACS Nano. 7 (9), 7833-7843 (2013).
- Xu, X., Zhang, C., Zhou, Y., Cheng, Q. L. J., Yao, K., Chen, Q. Quartz crystal microbalance study of protein adsorption on chitosan, chitosan/poly(vinyl pyrrolidone) blends and chitosan-graft-poly(vinyl pyrrolidone) surfaces. Journal of Bioactive and Compatible Polymers. 22, 195-206 (2007).
- Weber, N., Pesnell, A., Bolikal, D., Zeltinger, J., Kohn, J. Viscoelastic properties of fibrinogen adsorbed to the surface of biomaterials used in blood-contacting medical devices. Langmuir. 23, 3298-3304 (2007).
- Johannsmann, D. Viscoelastic, mechanical, and dielectric measurements on complex samples with the quartz crystal microbalance. Physical Chemistry Chemical Physics. 10 (31), 4516-4534 (2008).
- Denolf, G. C., Sturdy, L. F., Shull, K. R. High-frequency rheological characterization of homogeneous polymer films with the quartz crystal microbalance. Langmuir. 30 (32), 9731-9740 (2014).
- Martin, E. J., Mathew, M. T., Shull, K. R. Viscoelastic properties of electrochemically deposited protein/metal complexes. Langmuir. 31 (13), 4008-4017 (2015).
- Sturdy, L., Casadio, F., Kokkori, M., Muir, K., Shull, K. R. Quartz crystal rheometry: A quantitative technique for studying curing and aging in artists’ paints. Polymer Degradation and Stability. 107, 348-355 (2014).
- Sadman, K., Wiener, C. G., Weiss, R. A., White, C. C., Shull, K. R., Vogt, B. D. Quantitative Rheometry of Thin Soft Materials Using the Quartz Crystal Microbalance with Dissipation. Analytical Chemistry. 90 (6), 4079-4088 (2018).
- Wasilewski, T., Szulczyński, B., Kamysz, W., Gębicki, J., Namieśnik, J. Evaluation of three peptide immobilization techniques on a qcm surface related to acetaldehyde responses in the gas phase. Sensors (Switzerland). 18 (11), 1-15 (2018).
- Lvov, Y., Ariga, K., Kunitake, T., Ichinose, I. Assembly of Multicomponent Protein Films by Means of Electrostatic Layer-by-Layer Adsorption. Journal of the American Chemical Society. 117 (22), 6117-6123 (1995).
- Sauerbrey, G. Verwendung von Schwingquarzen zur Wägung dünner Schichten und zur Mikrowägung. Zeitschrift für Physik. 155 (2), 206-222 (1959).
- Sadman, K., Wang, Q., Chen, Y., Keshavarz, B., Jiang, Z., Shull, K. R. Influence of Hydrophobicity on Polyelectrolyte Complexation. Macromolecules. 50 (23), 9417-9426 (2017).
- Sievers, P., Moß, C., Schröder, U., Johannsmann, D. Use of torsional resonators to monitor electroactive biofilms. Biosensors and Bioelectronics. 110, 225-232 (2018).
- Ringberg, J. Q-Sense Explorer Operator Manual. Biolin Scientific. , (2017).
- Ringberg, J. Q-Sense User Guide: Instrument care and sensor pre-cleaning. Biolin Scientific. , (2015).
- Kern, W. The Evolution of Silicon Wafer Cleaning Technology. Journal of The Electrochemical Society. 137 (6), 1887 (1990).
- Sadman, K. . sadmankazi/QCM-D-Analysis-GUI: QCMD-Analyze. , (2018).

