Optimering af væksten af endothiapepsinkrystaller til serielle krystallografieksperimenter
Summary
Formålet med denne artikel er at give seeren en solid forståelse af, hvordan man omdanner deres lille volumen, dampdiffusionsprotokol til dyrkning af store, enkeltproteinkrystaller til en storvolumenbatchmikrokrystallisationsmetode til seriel krystallografi.
Abstract
Her præsenteres en protokol for at lette dannelsen af store mængder (> 100 μL) mikrokrystallinske opslæmninger, der er egnede til serielle krystallografieksperimenter ved både synkrotroner og XFEL’er. Metoden er baseret på en forståelse af proteinkrystalfasediagrammet, og hvordan denne viden kan udnyttes. Metoden er opdelt i tre faser: (1) optimering af krystalmorfologi, (2) overgang til batch og (3) skalering. Trin 1 indebærer at finde godt diffrakterende, enkelte krystaller, forhåbentlig men ikke nødvendigvis, der præsenterer i en terninglignende morfologi. I trin 2 optimeres trin 1-tilstanden efter krystalvæksttid. Denne strategi kan omdanne krystaller dyrket ved dampdiffusion til batch. Når krystalvækst kan forekomme inden for ca. 24 timer, kan et morfogram af protein- og bundfældningsblandingen plottes og anvendes som grundlag for en skaleringsstrategi (trin 3). Når krystaller kan dyrkes i batch, kan skalering forsøges, og krystalstørrelsen og koncentrationen optimeres, når volumenet øges. Endothiapepsin er blevet anvendt som demonstrationsprotein til denne protokol. Nogle af de præsenterede beslutninger er specifikke for endothiapepsin. Det er dog håbet, at den måde, de er blevet anvendt på, vil inspirere til en måde at tænke på denne procedure, som andre kan tilpasse til deres egne projekter.
Introduction
Rumtemperatur (RT) makromolekylær krystallografi er populær igen inden for strukturbiologi samfund. Udviklingen af røntgenfri elektronlaser (XFEL) lyskilder har ansporet udviklingen af RT-prøveleveringsmetoder 1,2,3,4, og disse metoder er nu blevet anvendt på synkrotroner 5,6,7,8. RT-metoder åbner ikke kun muligheden for pumpesondeeksperimentelle strageties 9,10,11,12, men der er også stigende beviser for, at de fremmer alternative konformationstilstande inden for proteiner 13,14,15,16,17.
Hovedårsagen til, at kryo-metoder fik trækkraft over RT-tilgange i slutningen af 1990’erne, var imidlertid opbremsningen af strålingsskader ved krystaltemperaturerunder nul 18. Kryo-metoder19 begyndte at muliggøre indsamling af et komplet datasæt fra en enkelt proteinkrystal. Moderne RT-metoder ved XFELs og synkrotroner løste problemet med enkeltkrystalstrålingsskader ved udvikling af hurtige (> 100 Hz) krystalleveringsstrategier 1,2,3,4. Disse metoder giver mulighed for indsamling af et komplet datasæt fra tusindvis af individuelt eksponerede krystaller. Disse RT-leveringsmetoder kræver derfor produktion af store mængder opløsninger indeholdende homogene mikrokrystaller (> 100 μL < 50 μm krystaller). Men da kryometoder har tendens til kun at kræve enkeltkrystaller, er metoder til at skabe sådanne mikrokrystallinske opslæmninger i øjeblikket ikke allestedsnærværende på tværs af proteinkrystallografilaboratorier.
Der er eksempler i litteraturen på, hvordan man gør dele af mikrokrystallisationsoptimeringsproceduren for serielle krystallografiprøver. Her skal der skelnes mellem membran og opløselige proteiner. Protokoller til optimering af væksten af mikromembranproteinkrystaller dyrket i monoolein (eller et andet lipid) til lipidisk kubisk fase (LCP) er blevet godt beskrevet20,21,22. Imidlertid mangler der generelt metoder til mikrokrystallisation af opløselige proteiner, herunder membranproteiner dyrket under ikke-LCP-betingelser. Tidligere undersøgelser har fokuseret på specifikke dele af processen, såsom mikrokrystalscreening 23,24, forbedring af kimdannelse24 og skalering ved hjælp af fri grænsefladediffusion 25, men ikke en komplet metode.
Imidlertid blev der for nylig beskreveten metode 26 , der forsøger at tilbyde en komplet protokol. Ligesom mange aspekter af proteinkrystallografi er det ikke nyt. Mange af de foreslåede ideer blev allerede beskrevet af Rayment (2002)27. Metoden har til formål at vise krystallografer, hvordan man udfører konverteringen fra en enkelt krystal dyrket ved hjælp af dampdiffusion til en batchmetode til dyrkning af tusindvis af mikrokrystaller. Metoden fokuserer på dampdiffusion som et fælles udgangspunkt, da 95% af alle Protein Data Bank (PDB) aflejringer kommer fra krystaller dyrket i dampdiffusionsplader26. Dampdiffusion er imidlertid ikke den ideelle metode til mikrokrystallisation26, så der beskrives en metode til at konvertere dampdiffusion til batchkrystallisation. Når krystaller kan dyrkes i batch, bliver skaleringsruter til større mængder mere praktiske. I betragtning af proteinkrystalliseringens luner vil forfatterne understrege, at denne metode ikke er fejlsikker. Protokollen skal dog i det mindste give et indblik i et proteins ‘krystalliseringsrum’.
Denne metode er afhængig af proteinkrystalliseringsfasediagrammet, og hvordan en forståelse af dette diagram kan fungere som vejledning under mikrokrystallisationsoptimering. Et proteinfasediagram er almindeligvis afbildet som et x/y-plot med udfældnings- og proteinkoncentrationer på henholdsvis x- og y-akserne (figur 1A). Fra punktet rent vand (nederste venstre hjørne – figur 1A) øges koncentrationen af både protein og bundfald, indtil opløselighedslinjen er nået. Opløselighedslinjen markerer overmætningspunktet (lilla linje – figur 1A). Når et protein er overmættet, bliver opløsningen termodynamisk ustabil og begynder at adskille sig i to faser: ‘proteinrig’ og en stabil mættet opløsning. Denne adskillelse kan forekomme hvor som helst uden for opløselighedslinjen, og dens kinetik afhænger af proteinets egenskaber og opløsningens komponenter.
Når protein- og bundfaldkoncentrationerne er for store, nedbrydes proteinet ustabilt ud af opløsningen og resulterer i amorft bundfald (lyserødt område – figur 1A). Imidlertid kan ordnet faseadskillelse forekomme i kimdannelsesområdet [se Garcia-Ruiz (2003) 28 for detaljeret beskrivelse], og krystalnukleanter har tilbøjelighed til at danne (grøn region – figur 1A). Nukleation og vækst fjerner protein fra opløsningen og flytter dråben ind i det metastabile område, hvor væksten kan fortsætte, indtil opløselighedslinjen er nået [se McPherson og Kuznetsov (2014) 29 for detaljeret diskussion]. Diagrammet er for langt de fleste krystalliseringsbetingelser en grov oversimplificering30. Uanset dette er diagrammet dog stadig af stor nytte for mikrokrystallografer, da kortlægningen af diagrammet gør det muligt at bestemme opløselighedslinjen og kinetikken for kimdannelse.
Med hensyn til at skabe mikrokrystaller er de to faktorer under krystallisering, der skal optimeres, antallet af krystaller (Xn) og deres gennemsnitlige, længste dimension (Xs). X n vil være proportional med antallet af kimdannelseshændelser (n ) (Eq. 1).
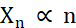 Eq. 1
Eq. 1
X s er proportional med koncentrationen af frit protein over opløselighedslinjen (Ps) divideret med Xn (Eq. 2).
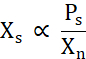 Eq. 2
Eq. 2
I en perfekt situation ville enhver kimdannelsesbegivenhed give en mulig krystal, og hver eneste af disse krystaller ville have lige adgang til det tilgængelige protein i opløsning. Figur 2 er en grafisk repræsentation fra et ideelt scenario af forholdet mellem Xn og Xs. I praksis er den vigtigste kontrol, en krystallograf har over Xn og Xs , ved at påvirke mængden af kimdannelse eller ved tilsætning af frøkrystaller. Mikrokrystallografen skal bedømme, hvordan man øger Xn , således at der både kan skabes en passende krystalkoncentration og krystalstørrelse.
De fleste krystalliseringsteknikker kræver en “overgangsperiode” (figur 1B). For eksempel i et dampdiffusionseksperiment, ved blanding af protein- og bundfældningsopløsningerne, vil koncentrationerne af hver ændre sig, når dråben udligner sig med brøndopløsningen. Man håber, at disse ændringer gradvist vil overføre faldet til kimdannelseszonen, hvor tilbøjeligheden til krystallisation vil stige. Når krystaller begynder at nukleere og vokse, vil mængden af protein i opløsning begynde at falde, hvilket reducerer sandsynligheden for yderligere kimdannelse. Den ultimative mængde kimdannelse vil være protein- og tilstandsspecifik og også afhængig af dybden af penetration af i nukleationszonen. I betragtning af den begrænsede kimdannelseszonepenetration af metoder, der kræver et overgangstrin, vil kimdannelsesniveauet i sidste ende være begrænset til kimdannelseshastigheden ved metastabil-nukleationsregionsgrænsen.
På grund af vigtigheden af at kunne forbedre kimdannelsesniveauet for en mikrokrystallograf er det vigtigt at flytte til en batchkrystallisationsmetode. Batch kan drage større fordel af hele nukleationsområdet (figur 1C). I batchmetoder er ideen at blande proteinet og bundfaldet sammen, således at der skabes en overmættet opløsning uden behov for ændringer i komponentkoncentrationer. Nukleation bør være mulig umiddelbart efter blanding. Batchmetoder tillader derfor, at hele kimdannelseszonen teoretisk nås. Enhver stigning i kimdannelseskinetik ud over metastabil-nukleationsgrænsen kan derefter udnyttes.
Hvis det basale niveau af krystalkimdannelse ikke er nok til at generere et stort Xn, kan mikrosåningsmetoder anvendes. Ved mikrosåning brydes forvoksede krystaller op for at skabe en opslæmning af krystallinske fragmenter, der kan fungere som et stillads for frisk krystalvækst31,32. Mikrosåning har været meget udbredt i seriel krystallografisk prøveforberedelse som en måde at øge Xn uden behov for at øge krystalkimdannelsen (figur 1C).
Overgangen fra dampdiffusion til batch kan visualiseres på et fasediagram som at flytte det eksperimentelle udgangspunkt fra enten de ikke-overmættede eller metastabile regioner til kimdannelseszonen. Dette kan gøres ved at øge protein- og/eller udfældningskoncentrationerne og/eller forholdet mellem de to inden for faldet (figur 1D) og observere, hvilke betingelser der giver krystaller, der viser sig hurtigt (< 24 timer)26. Fuldstændig dampdiffusionsdråbeligevægt kan tage dage eller uger33. Derfor, ved at lede efter betingelser, der viser hurtigt fremkomne krystaller, kan batchbetingelser findes uden at skulle flytte til alternative krystalliseringsscreeningsformater såsom mikrobatch34,35,36,37.
Når kimdannelseszonen er fundet, er der fundet en batchtilstand, og der kan oprettes et morfogram – her et groft fasediagram. Morfogrammet er af stor nytte, når man overvejer, om man skal bruge en podet batch eller lige batchprotokol. Ved at plotte Xn som funktion af protein- og bundfældningskoncentrationen kan der foretages en vurdering af kimdannelseskinetikken26. Hvis X n forbliver lav over hele kimdannelsesområdet, kan det være nødvendigt med frøbatch for at gøre Xn stor nok til at begrænse krystalvækst. Denne vurdering er det første skridt i processen med at skalere til større mængder (> 100 μL).
Denne metode blev designet således, at den kunne udføres i de fleste krystallisationslaboratorier ved hjælp af standard dampdiffusionskrystallisationsudstyr. Der er også udført mange undersøgelser, som beskriver teknikker til at lette mange dele af denne proces, hvis udstyret er tilgængeligt. Disse omfatter, men er ikke begrænset til, dynamisk lysspredning (DLS) 25,27, ikke-lineær billeddannelse 20,24,25, pulverdiffraktion 20,24,27 og elektronmikroskopi 26 [se Cheng et al. (2020) 40 for en god gennemgang].
Formålet med dette arbejde er at give en visuel demonstration af metoden til overgang fra lille volumen ( 100 μL) batchkrystallisering. Endothiapepsin fra Cryphonectria parasitica er blevet brugt som et eksempelsystem til demonstration af denne oversættelse. Den type eksperiment og prøveleveringsmetode, som mikrokrystallerne er nødvendige for, vil påvirke det ideelleX-s output26. For blandingsforsøg, der kræver en millisekundtidsopløsning41 eller gasdynamiske virtuelle dyser42, kan en endelig Xs på < 5 μm være ønskelig. I dette tilfælde var målet at producere proteinkrystaller, der diffrakterer til ca. 1,5 Å, til et fotonaktiveret pumpesondeeksperiment og ved hjælp af en leveringsmetode med fast mål.
For at give en illustration af prøvekravene til et sådant serielt krystallografieksperiment ved anvendelse af endothiapepsin viser tabel 1 de eksperimentelle parametre for et hypotetisk eksperiment. Eksempeloplysningerne var baseret på den protokol, der er beskrevet nedenfor. I betragtning af nogle konservative skøn over hitrater og dataindsamlingskrav er 50 mg det samlede prøveforbrugsestimat for hele eksperimentet.
Figur 3 viser et rutediagram over den komplette optimeringsproces fra indledende dampdiffusionskrystallisation i lille volumen til storskalabatch. For de fleste serielle krystallografiprojekter begynder denne protokol på trin 2: ‘overgang til batch’, da målproteinet allerede vil være krystalliseret. Trin 1 er dog medtaget for fuldstændighed og for at minde læserne om dens betydning. At finde en tilstand, der giver anledning til en godt diffrakterende, enkelt, stor krystal, er det bedste udgangspunkt for mikrokrystaloptimering. I trin 2 kan denne tilstand derefter optimeres fra dampdiffusion til batch, og et morfogram af nukleations- og metastabile regioner kan plottes. Når dette er gjort, kan batchbetingelsen skaleres til større mængder i trin 3. Ved afslutningen af rutediagrammet vil en krystallograf have skabt en gentagelig, stor volumen (> 100 μL), mikrokrystallisation, batchprotokol for endothiapepsin. Denne metode kan derefter anvendes på deres særlige protein af interesse.
Protocol
Representative Results
Discussion
Den præsenterede metode viser, hvordan man optimerer krystalliseringen af endothiapepsin fra store krystaller (≥ 100 μm længste dimension), dyrket i sparsomme matrix 96-brøndskærme, til mikrokrystaller, dyrket i centrifugerør (300 μL volumen) via batch. Ideen bag protokollen er, at de skridt, der er taget for at optimere endothiapepsin, også kan bruges til andre proteiner. I sidste ende besvarer problemet med at skabe store mængder (>100 μL) mikrokrystaller (10-20 μm) til serielle krystallografieksperimenter ved XFEL’er og synkrotroner.
Protokollen opdeler opgaven med mikrokrystallisation i store mængder i tre trin: (1) Optimering af krystalmorfologi, (2) Overgang til batch og (3) Skalering. I trin 1 skal rækkevidden af krystalformer, som et protein kan skabe, undersøges i dampdiffusionsplader. Betingelser, der giver anledning til enkelte, kasselignende krystaller, der diffrakterer til den krævede opløsning, bør være målet. I trin 2 kan udvalgte betingelser derefter omdannes fra dampdiffusion til batch. Her er optimeringskriteriet krystalvæksttid og at finde forhold, der giver anledning til proteinkrystaller inden for 24 timer. Et morfogram kan også plottes, hvilket giver eksperimentatoren en ide om placeringen af opløselighedslinjen og nukleationszonegrænserne. Dette morfogram er af stor nytte i trin 3, skalering. Morfogrammet vil give en indikation af, om kimdannelse alene kan øge Xn og drive Xs ned. Efterhånden som eksperimentets volumen øges, kanXn og Xs løbende vurderes som nøglekriterierne for skaleringssucces.
I tilfælde af endothiapepsin opdagede trin 1, hvad der potentielt var en tidligere ukendt krystalmorfologi for endothiapepsin. Denne morfologi havde den samme rumgruppe som de tidligere rapporterede, men vigtigere for seriel krystallografi, en mere kasselignende form. Enkeltkrystaller syntes også at vokse fra enkeltnukleationspunkter, i modsætning til ventilatorerne skabt af andre forhold (figur 4). For den valgte tilstand var trin 2 allerede delvist tilfreds, da krystalvækst fandt sted i < 24 timer. Morfogrammet indikerede, at både en ren eller seed-batch-protokol kan være vellykket ved skalering i trin 3. Indledende skalering i lige batch skabte en tilstand, der producerede krystaller med et X,n og Xs område på henholdsvis 3,6 ± 1,2 x 106 krystaller · ml-1 og 42 ± 4,1 μm. Disse krystaller, selvom de var acceptable for nogle serielle krystallografieksperimenter, blev anset for at være for store. Så yderligere optimeringer blev udført. Den endelige protokol producerede krystaller med en koncentration og størrelsesområde på henholdsvis 3,1 x 106 krystaller · ml-1 og 15 ± 3,9 μm. Dette var mere end ideelt til de planlagte eksperimenter.
Metoden fokuserer på transformation af ‘opløselige’ proteinkrystaller dyrket i dampdiffusionsplader til batch. Årsagen til dette fokus er, at langt størstedelen af opløselige proteinkrystaller dyrkes via dampdiffusion26. Imidlertid kunne de præsenterede koncepter også anvendes på opløselige proteinkrystaller dyrket ved hjælp af andre metoder, såsom mikrobatch. Begreberne kan også anvendes på membranproteinkrystaller dyrket i LCP; da dette også er en batchkrystallisationsproces.
Et centralt aspekt af protokollen er processen med at transformere betingelserne for krystaller dyrket i dampdiffusionsplader, så de kan dyrkes i batch. Til denne transformation anvender metoden det kriterium, der er foreslået af Beale et al. (2019)26. Krystaller dyrket via en batchproces, selv i dampdiffusionsplader, dannes hurtigt (< 24 timer). Dette kriterium er en tilnærmelse baseret på hastigheden af dampdiffusionsfaldsligevægt og gælder mest for PEG-baserede bundfældningsbetingelser. Imidlertid vil krystallisationsbetingelser indeholde en lang række forbindelser, som vil påvirke ligevægtstiden. Ligevægten af saltbaserede krystallisationsbetingelser, f.eks. stærkt koncentreret ammoniumchlorid, kan ske på 1-2 dage. Derfor er 24 timer-kriteriet muligvis ikke sandt for saltbaserede forhold. Saltbaserede forhold kan også have mere komplekse fasediagrammer26,30, der muligvis ikke er i overensstemmelse med arketypen præsenteret i denne protokol. Det kan være nødvendigt at reducere tidskriteriet for saltbaserede forhold til 12 eller 6 timer, hvis det viser sig umuligt at skalere til større mængder.
En anden begrænsning af denne metode er dens tilsyneladende kompleksitet. Protokollen, der blev fulgt for at optimere mikrokrystallisationen af endothiapepsin, ændrede faktisk den oprindelige tilstand fra den sparsomme matrixskærm relativt lidt. Det første hit, der blev observeret på PACT-skærmen, var 0,1 HEPES pH 7,0, 0,2 MMgCl2 og 20% (w/v) PEG 6.000. Den endelige skalerede krystallisationsbuffer var 0,1 Tris-HCl pH 7,0, 0,15 MMgCl2 og 40% (w/v) PEG 6.000. Det er også meget muligt, at ændringen i buffer fra HEPES til Tris-HCI ogMgCl2-koncentration bidrog lidt til processens succes. At lade stigningen i PEG 6.000-koncentrationen være den eneste optimering, og en, der kunne have været opnået ganske enkelt.
Denne vurdering er imidlertid også for forenklet. Det diskonterer ikke kun de problemer, der opstår under skalering (dvs. brugen af frø og slukning), men også det faktum, at bare fordi dette protein viste sig ligetil, er der ingen garanti for, at det næste også vil vise sig at være. De trin, der anbefales i protokollen, blev udtænkt, fordi optimering af skalering af proteinkrystalliseringsvolumener kan være meget proteindyrt. I løbet af de syv endothiapepsinskaleringsforsøg, der vises, blev 100 mg protein forbrugt. Nogle af disse skridt blev ganske vist udført for at vise deres konsekvenser i lyset af denne protokol. Alligevel kan 100 mg af et protein plus potentielt yderligere 50 mg for protein, der indtages under et eksperiment (tabel 1), være en betydelig investering i enten tid eller penge.
Heldigvis er det ikke klart, at denne masse af krævet prøve er allestedsnærværende på tværs af alle proteiner. Endothiapepsin var meget opløseligt og krævede derfor en stor proteinkoncentration for at nå overmætning. I andre (i øjeblikket under optimering) kan overmætning nås ved 10 eller endda 5 mg / ml. Sådanne variabler er proteinspecifikke og skal omfavnes, når de vises.
Andre begrænsninger ved metoden inkluderer dens afhængighed af komplekst udstyr såsom væskehåndteringsrobotter til skærm- og pladeoprettelse og billeddannere til automatisk billedplader, når det er nødvendigt. Alternative rutiner er blevet tilbudt for at begrænse behovet for nogle af disse stykker udstyr, men protokollen vil være mere tidskrævende at følge uden dem. Protokollen foreslår også at teste diffraktionen af optimerede krystaller. For krystallografer uden regelmæssig adgang til en synkrotron kan disse tests vise sig udfordrende. Kontrol på hvert trin er muligvis ikke nødvendig, men disse tests anbefales kraftigt, når et hit er blevet identificeret, og før og efter skalering. Ikke-diffrakterende krystaller ved en XFEL er desværre ikke en ualmindelig forekomst. I betragtning af dette er det bedre at fejle på forsigtighedssiden med hensyn til antagelser om krystaldiffraktion.
I sidste ende vil denne protokol og resultater, der præsenteres her, tilbyde en guide, ideer og et eksempel til dem, der kæmper med at producere prøver til serielle krystallografieksperimenter. Forhåbentlig, efterhånden som seriel krystallografi videreudvikles, vil prøvekravene til teknikken blive reduceret, således at behovet for protokoller som dette vil blive reduceret. Men selv i dette tilfælde vil de strategier, der præsenteres her, stadig være nyttige for dem, der ønsker at udforske krystalliseringsrummet for deres protein.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dette projekt har modtaget støtte fra EU’s Horizon 2020 forsknings- og innovationsprogram under Marie Skłodowska-Curie-tilskudsaftale nr. 701647. Mange tak for hjælp og støtte fra beamline-forskere ved Swiss Light Source beamline X10SA-PXII.
Materials
| Swissci 96-well 2-Drop plates | Molecular Dimensions | MD11-002 | 96-well 2-drop crystallisation plate |
| Swissci 96-well 3-Drop plates | Molecular Dimensions | MD11-003 | 96-well 3-drop crystallisation plate |
| mosquito LCP liquid handling robot | sptlabtech | mosquito LCP | Crystallisation robot |
| ClearVue Sheets | Molecular Dimensions | MD6-015 | 96-well crystallization plate seals |
| Safe-Tube 1.5 mL | Eppendorf | 30120086 | 1.5 mL centrifuge tubes |
| Scaple | Swan and Morton | No. 3 scalple and No. 3 handle | Scalple for cutting open plate seals |
| MS 3 Vortex | IKA | 3319000 | Vortex for mixing solution and making seed stocks |
| 24-well XRL Plate | Molecular Dimensions | MD3-11 | 24-well hanging-drop plates |
| Tube revolver/rotator | Thermo Fischer Scientific | 88881001 | Tube revolver for mixing solution during scaling |
| Eppendorf Research plus pipettes | Eppendorf | Range of manual pipettes, 0.5-10, 1-20, 10-100, 100-1000 µL | |
| Eppendorf pipette tips | Eppendorf | Range of tip sizes for manual pipettes | |
| Suparen 600 | Prochem AG | Suparen 600 | Endothiapepsin solution |
| Sodium Acetate | Sigma-Aldrich | 241245-1KG | Sodium Acetate |
| Tris | Merck | 8382T014 | Tris |
| Magnesium Chloride | Sigma-Aldrich | M2670-1kg | Magnesium Chloride |
| PEG 6,000 | Sigma-Aldrich | 81255-1kg | PEG 6,000 |
| Ethelyene glycol | Sigma-Aldrich | 324558-1L | Ethelyene glycol for cyro-protecting the crystals |
| PACT Premier HT screen | Molecular Dimensions | MD1-36 | PACT Premier 96-well crystal screen |
| DOW CORNING high vacuum grease | Molecular Dimensions | MD6-02 | Grease for sealing 24-well plates |
| Hirschmann 22 x 22 mm glaser cover slides | Hirschmann | 8000104 | Cover slides for sealing 24-well sitting drop plates |
| Crystal pins | PSI | Manufactured inhouse | Thin-film supports for micro-crystals. |
| 1-1.3 mm SiLibeads Type S | Faust | 6239547 | Glass beads for making mico-seed stocks |
| Macbook Pro | Apple | Macbook Pro | Computer for performing data analysis |
| CCP4 software suite | CCP4 | Diffraction pattern data processing software | |
| Excel | Microsoft | Microsoft Office | Plotting tool for phase diagram |
| Hausser Scientific Bright-Line counting chamber | Thermo Fischer Scientific | 02-671-51B | Tool to calculate crystal concentration |
| PACT Premier | Molecular Dimensions | MD1-29-ECO | Sparse-matrix crystallization screen |
| Rock Imager | Formulatrix | Rock Imager | Temperature controlled crystal plate storage and imager |
| Rock MakerWeb | Formulatrix | Rock MakerWeb | Crystal plate creation and image storage stoftware |
| Formulator | Formulatrix | Formulator | 96-well crystal screen creation liquid handling robot |
| Leica MZ16 Microscope | Leica | Leica MZ16 | Light microscope |
| LAS V4.6 | Leica | LAS V4.6 | Software for Leica microscopes |
| Spectra/Por 3.5 kDa dialysis tubing | Spectrumlabs | Spectra/Por 3 Dialysis Membrane | 3.5 kDa dialysis membrane |
| Dialysis tubing closures | Spectrumlabs | Spectra/Por 3 Duniversal Closures | Clips to seal the dialysis tubing ends |
| Amicon 10 kDa centrifugal concentrator | Merck-Millipore | Amicon Ultra-15 10 kDa centrifugal concentrator | 10 kDa centrifugal filter |
| 5810 R swing bucket centrifuge | Eppendorf | 5810 R Centrifuge | Swing bucket centrifuge |
References
- DePonte, D. P., et al. Gas dynamic virtual nozzle for generation of microscopic droplet streams. Journal of Physics D: Applied Physics. 41 (19), 195505 (2008).
- Hunter, M. S., et al. Fixed-target protein serial microcrystallography with an x-ray free electron laser. Scientific Reports. 4 (1), 6026 (2014).
- Weierstall, U., et al. Lipidic cubic phase injector facilitates membrane protein serial femtosecond crystallography. Nature Communications. 5 (1), 1-6 (2014).
- Roessler, C. G. G., et al. Acoustic Injectors for Drop-On-Demand Serial Femtosecond Crystallography. Structure. 24 (4), 631-640 (2016).
- Sherrell, D. A., et al. A modular and compact portable mini-endstation for high-precision, high-speed fixed target serial crystallography at FEL and synchrotron sources. Journal of Synchrotron Radiation. 22 (6), 1372-1378 (2015).
- Roedig, P., et al. A micro-patterned silicon chip as sample holder for macromolecular crystallography experiments with minimal background scattering. Scientific Reports. 5 (1), 1-11 (2015).
- Botha, S., et al. Room-temperature serial crystallography at synchrotron X-ray sources using slowly flowing free-standing high-viscosity microstreams. Acta Crystallographica Section D Biological Crystallography. 71 (2), 387-397 (2015).
- Weinert, T., et al. Serial millisecond crystallography for routine room-temperature structure determination at synchrotrons. Nature Communications. 8 (1), 542 (2017).
- Tenboer, J., et al. Time-resolved serial crystallography captures high-resolution intermediates of photoactive yellow protein. Science. 346 (6214), 1242-1246 (2014).
- Nango, E., et al. A three-dimensionalmovie of structural changes in bacteriorhodopsin. Science. 354 (6319), 1552-1557 (2016).
- Suga, M., et al. Light-induced structural changes and the site of O=O bond formation in PSII caught by XFEL. Nature. 543 (7643), 131-135 (2017).
- Mehrabi, P., et al. Liquid application method for time-resolved analyses by serial synchrotron crystallography. Nature Methods. 16 (10), 979-982 (2019).
- Halle, B. Biomolecular cryocrystallography: structural changes during flash-cooling. Proceedings of the National Academy of Sciences of the United States of America. 101 (14), 4793-4798 (2004).
- Fraser, J. S., et al. Hidden alternative structures of proline isomerase essential for catalysis. Nature. 462 (7273), 669-673 (2009).
- Fenwick, R. B., van den Bedem, H., Fraser, J. S., Wright, P. E. Integrated description of protein dynamics from room-temperature X-ray crystallography and NMR. Proceedings of the National Academy of Sciences of the United States of America. 111 (4), 445-454 (2014).
- Keedy, D. A., et al. Mapping the conformational landscape of a dynamic enzyme by multitemperature and XFEL crystallography. Elife. 4, (2015).
- Thomaston, J. L., et al. XFEL structures of the influenza M2 proton channel: Room temperature water networks and insights into proton conduction. Proceedings of the National Academy of Sciences of the United States of America. 114 (51), 13357-13362 (2017).
- Haas, D. J., Rossmann, M. G. Crystallographic studies on lactate dehydrogenase at -75 °C. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 26 (7), 998-1004 (1970).
- Hope, H. Cryocrystallography of biological macromolecules: a generally applicable method. Acta Crystallographica Section B Structural Science. 44 (1), 22-26 (1988).
- Wu, W., et al. Batch crystallization of rhodopsin for structural dynamics using an X-ray free-electron laser. Acta Crystallographica Section:F Structural Biology Communications. 71 (7), 856-860 (2015).
- Ishchenko, A., Cherezov, V., Liu, W. Preparation and delivery of protein microcrystals in lipidic cubic phase for serial femtosecond crystallography. Journal of Visualized Experiments. (115), e54463 (2016).
- Andersson, R., et al. Well-based crystallization of lipidic cubic phase microcrystals for serial X-ray crystallography experiments. Acta Crystallographica Section D: Structural Biology. 75 (10), 937-946 (2019).
- Luft, J. R., et al. The detection and subsequent volume optimization of biological nanocrystals. Structural Dynamics. 2 (4), 041710 (2015).
- Lee, D. B., et al. Supersaturation-controlled microcrystallization and visualization analysis for serial femtosecond crystallography. Scientific Reports. 8 (1), 1-10 (2018).
- Kupitz, C., et al. Microcrystallization techniques for serial femtosecond crystallography using photosystem II from Thermosynechococcus elongatus as a model system. Philosophical transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1647), 20130316 (2014).
- Beale, J. H., et al. Successful sample preparation for serial crystallography experiments. Journal of Applied Crystallography. 52, 1385-1396 (2019).
- Rayment, I. Small-scale batch crystallization of proteins revisited: An underutilized way to grow large protein crystals. Structure. 10 (2), 147-151 (2002).
- García-Ruiz, J. M. Nucleation of protein crystals. Journal of Structural Biology. 142 (1), 22-31 (2003).
- McPherson, A., Kuznetsov, Y. G. Mechanisms, kinetics, impurities and defects: Consequences in macromolecular crystallization. Acta Crystallographica Section F:Structural Biology Communications. 70 (4), 384-403 (2014).
- Rupp, B. Origin and use of crystallization phase diagrams. Acta crystallographica. Section F, Structural biology communications. 71, 247-260 (2015).
- Luft, J. R., DeTitta, G. T. A method to produce microseed stock for use in the crystallization of biological macromolecules. Acta Crystallographica Section D Biological Crystallography. 55 (5), 988-993 (1999).
- Ireton, G. C., Stoddard, B. L. Microseed matrix screening to improve crystals of yeast cytosine deaminase. Acta crystallographica. Section D, Biological crystallography. 60 (3), 601-605 (2004).
- Forsythe, E. L., Maxwell, D. L., Pusey, M. Vapor diffusion, nucleation rates and the reservoir to crystallization volume ratio. Acta Crystallographica Section D Biological Crystallography. 58 (10), 1601-1605 (2002).
- Chayen, N. E., Shaw Stewart, P. D., Maeder, D. L., Blow, D. M. IUCr An automated system for micro-batch protein crystallization and screening. Journal of Applied Crystallography. 23 (4), 297-302 (1990).
- Chayen, N. E., Shaw Stewart, P. D., Blow, D. M. Microbatch crystallization under oil – a new technique allowing many small-volume crystallization trials. Journal of Crystal Growth. 122 (1-4), 176-180 (1992).
- Chayen, N. E. Comparative studies of protein crystallization by vapour-diffusion and microbatch techniques. Acta Crystallographica Section D: Biological Crystallography. 54 (1), 8-15 (1998).
- D’Arcy, A., Mac Sweeney, A., Stihle, M., Haber, A. The advantages of using a modified microbatch method for rapid screening of protein crystallization conditions. Acta Crystallographica – Section D Biological Crystallography. 59 (2), 396-399 (2003).
- Darmanin, C., et al. Protein crystal screening and characterization for serial femtosecond nanocrystallography. Scientific Reports. 6, 25345 (2016).
- Gati, C., et al. Atomic structure of granulin determined from native nanocrystalline granulovirus using an X-ray free-electron laser. Proceedings of the National Academy of Sciences of the United States of America. 114 (9), 2247-2252 (2017).
- Cheng, R. K. Y. Towards an optimal sample delivery method for serial crystallography at XFEL. Crystals. 10 (3), 215 (2020).
- Schmidt, M. Mix and Inject: Reaction Initiation by Diffusion for Time-Resolved Macromolecular Crystallography. Advances in Condensed Matter Physics. 2013, 1-10 (2013).
- Oberthuer, D., et al. Double-flow focused liquid injector for efficient serial femtosecond crystallography. Scientific Reports. 7 (1), 44628 (2017).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta crystallographica. Section F, Structural biology communications. 70, 2-20 (2014).
- Yaoi, M., et al. Effect of stirring method on protein crystallization. Japanese Journal of Applied Physics, Part 2: Letters. 43 (10), 1318 (2004).
- Castro, F., Ferreira, A., Teixeira, J. J., Rocha, F. Influence of Mixing Intensity on Lysozyme Crystallization in a Meso Oscillatory Flow Reactor. Crystal Growth & Design. 18 (10), 5940-5946 (2018).
- Moews, P. C., Bunn, C. W. An X-ray crystallographic study of the rennin-like enzyme of Endothia parasitica. Journal of Molecular Biology. 54 (2), 395-397 (1970).
- Newman, J., et al. Towards rationalization of crystallization screening for small- to medium-sized academic laboratories: the PACT/JCSG+ strategy. Acta crystallographica. Section D, Biological. 61, 1426-1431 (2005).
- Ebrahim, A., et al. Resolving polymorphs and radiation-driven effects in microcrystals using fixed-target serial synchrotron crystallography. Acta Crystallographica Section D Structural Biology. 75, 151-159 (2019).
- Davy, B., et al. Reducing sample consumption for serial crystallography using acoustic drop ejection. Journal of Synchrotron Radiation. 26 (5), (2019).

