En 3D-kartografisk beskrivning av cellen genom Cryo Soft X-ray Tomography
Summary
Här presenteras ett protokoll som beskriver provberedningen och datainsamlingsstegen som krävs i kryo mjuk röntgentomografi (SXT) för att avbilda ultrastrukturen hos hela kryobevarade celler med en upplösning av 25 nm halv tonhöjd.
Abstract
Avbildningstekniker är grundläggande för att förstå cellorganisation och maskiner inom biologisk forskning och relaterade områden. Bland dessa tekniker tillåter kryo mjuk röntgentomografi (SXT) avbildning av hela kryokonserverade celler i vattenfönstrets röntgenenergiområde (284-543 eV), där kolstrukturer i sig har högre absorption än vatten, vilket möjliggör 3D-rekonstruktion av den linjära absorptionskoefficienten för materialet i varje voxel. Kvantitativ strukturell information på nivån av hela celler upp till 10 μm tjock kan sedan uppnås på detta sätt, med hög genomströmning och rumslig upplösning ner till 25-30 nm halvhöjd. Cryo-SXT har visat sig vara relevant för aktuell biomedicinsk forskning, vilket ger 3D-information om cellulära infektionsprocesser (virus, bakterier eller parasiter), morfologiska förändringar på grund av sjukdomar (såsom recessiva genetiska sjukdomar) och hjälper oss att förstå läkemedelsverkan på cellulär nivå eller lokalisera specifika strukturer i 3D-cellulär miljö. Dessutom, genom att dra nytta av den avstämbara våglängden vid synkrotronanläggningar, kan spektromikroskopi eller dess 3D-motsvarighet, spektrotomografi, också användas för att avbilda och kvantifiera specifika element i cellen, såsom kalcium i biomineraliseringsprocesser. Cryo-SXT ger kompletterande information till andra biologiska avbildningstekniker såsom elektronmikroskopi, röntgenfluorescens eller synligt ljusfluorescens och används vanligtvis som en partnermetod för 2D- eller 3D-korrelativ avbildning vid kryogena förhållanden för att länka funktion, plats och morfologi.
Introduction
Cryo-SXT kan spela en central roll i biologisk bildforskning eftersom det ger 3D-medelupplösning (25-30 nm halv tonhöjd) volymer av hydratiserade hela celler 1,2,3,4,5,6. I vattenfönstrets energiområde, mellan kol- och syreabsorptionen k-kanter (4,4-2,3 nm), absorberar kolrika cellulära strukturer 10 gånger mer än det syrerika mediet som genomtränger och omger dem. I detta energiområde kan förglasade celler upp till 10 μm tjocklek avbildas utan behov av sektionering eller färgning, vilket leder till kvantitativa kontrastprojektioner med hög absorption, vilket i kombination med provrotationsförmåga möjliggör tomografisk rekonstruktion av den cellulära strukturen. Cryo-SXT fyller en nisch när det gäller provdimensioner och rumslig upplösning som inte är lättillgänglig med någon annan bildteknik.
I korthet är absorptionskontrasten för kryo-SXT kvantitativ, eftersom dämpningen av fotonerna genom provet av tjocklek t följer Beer-Lambert-lagen enligt följande: 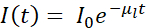 , där I0 representerar infallande intensitet och μl den linjära absorptionskoefficienten, som beror på våglängden λ och den imaginära delen β av provets brytningsindex (
, där I0 representerar infallande intensitet och μl den linjära absorptionskoefficienten, som beror på våglängden λ och den imaginära delen β av provets brytningsindex (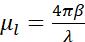 ). Dämpningen är en funktion av den biokemiska sammansättningen och tjockleken på strukturerna som avbildas, där varje biokemisk komponent har en specifik röntgenlinjär absorptionskoefficient μl (LAC). Detta innebär att varje tomografi voxelvärde beror på de kemiska elementen och deras koncentration i den voxel7. Detta möjliggör naturlig diskriminering av olika organeller såsom kärnor, nukleoler, lipidkroppar eller mitokondrier, eller olika komprimeringstillstånd av kromatin enbart baserat på deras inneboende LAC-värden rekonstruerade 2,8,9.
). Dämpningen är en funktion av den biokemiska sammansättningen och tjockleken på strukturerna som avbildas, där varje biokemisk komponent har en specifik röntgenlinjär absorptionskoefficient μl (LAC). Detta innebär att varje tomografi voxelvärde beror på de kemiska elementen och deras koncentration i den voxel7. Detta möjliggör naturlig diskriminering av olika organeller såsom kärnor, nukleoler, lipidkroppar eller mitokondrier, eller olika komprimeringstillstånd av kromatin enbart baserat på deras inneboende LAC-värden rekonstruerade 2,8,9.
Dessutom är kryo-SXT en teknik med hög genomströmning med tomogram som samlas in på några minuter. Detta möjliggör specifikt mesoskala avbildning av cellpopulationer som kan fångas vid viktiga tidpunkter som delning, differentiering och apoptos, men också vid olika svarstillstånd som de som induceras av kemisk exponering för specifika läkemedelsterapier eller patogena infektioner. Data som samlas in vid dessa nyckelpunkter kommer att leverera 3D-beskrivning av systemet med en trogen registrering av den rumsliga organisationen av de olika cellulära organellerna vid dessa specifika ögonblick.
Vanligtvis används kryo-SXT i kombination med andra tekniker som följer korrelativa tillvägagångssätt som gör det möjligt att lokalisera specifika egenskaper, händelser eller makromolekyler inom 3D-cellulär miljö 4,10,11,12,13,14,15,16 eller hårda röntgenfluorescensdata 17,18 . Korrelativa tillvägagångssätt vid kryogena förhållanden är av största vikt för att få den mest kompletta och värdefulla bilden av det intressanta systemet. En kortfattad sammanfattning av det typiska arbetsflödet vid Kryo-SXT-strållinjerna Mistral (Alba) och B24 (Diamond) skisseras i figur 1.
Genom att utnyttja våglängdsinställningsförmågan vid synkrotronanläggningar kan spektroskopisk information erhållas utöver den strukturella med användning av den specifika differentiella absorptionen av specifika element som ingår i provet. Ett exempel på detta skulle vara placeringen av kalcium i studien av biomineraliseringsprocesser i celler 19,20,21. Genom att ta 2D-bilder vid olika fotonenergier (spektra) eller tomogram nedanför och vid röntgenabsorptionskanten av intresse kan pixlarna eller voxlarna som innehåller det valda elementet identifieras. Spektra tillåter också differentiering av kemiska tillstånd (dvs utvecklingen av amorft kalcium till hydroxiapatit som i föregående biomineraliseringsexempel20). Kvantifiering av olika element är möjlig i 2D och 3D. Spektroskopisk avbildning av förglasade celler görs vanligtvis i vattenfönstret, men är också möjlig vid andra energiområden om vattenhalten är tillräckligt låg eller om andra provberedningsprotokoll, inklusive uttorkning, används22. Ett detaljerat spektroskopi steg-för-steg-protokoll ligger utanför protokollets fokus häri.
I det följande fokuserar protokollet på att kortfattat sammanfatta de viktigaste provberedningsstegen, även om varje system kan behöva individuell förfining, följt av en detaljerad steg-för-steg-datainsamlingsprocedur för kryo mjuk röntgentomografi.
Protocol
Representative Results
Discussion
Provberedning är ett kritiskt steg för att erhålla högkvalitativa mjuka röntgentomogram, eftersom deras kvalitet direkt beror på kvaliteten på provförglasningen och isskiktets tjocklek i vilken cellen är inbäddad. Projektioner med högt signal-brusförhållande kommer att samlas in i områden med tunt islager, vilket gör det möjligt att minimera den stråldos som krävs för att uppnå högsta möjliga upplösning. Dessutom kommer cellkonfluensen också att påverka den slutliga tomogramkvaliteten, eftersom man bör undvika att angränsande celler kommer in i FoV vid rotation. Slutligen kommer den rätta dispersionen av Au fiducialmarkörer att bestämma noggrannheten för projektionsinriktningen och sedan slutligen bestämma kvaliteten på den slutliga 3D-rekonstruerade volymen. Observera att en korrekt spridning av Au fiducials på nätet möjliggör automatisering av projektionsjusteringssteget, utan vilket en hög expertis behövs för ett sådant kritiskt steg.
Protokollet här visar bara en möjlig provberedningsstrategi, som har likheter med de som används i kryoelektrontomografi (kryo-ET). I båda fallen kommer protokoll som förbättrar den krävande provberedningen för bättre reproducerbarhet att vara grundläggande för framgången för dessa tekniker, och ansträngningar görs mot detta mål29. Det är värt att nämna att förutom att avbilda isolerade celler kan delar av vävnad också visualiseras förutsatt att överföringssignalen genom sektionen räcker vid höga lutningsvinklar. Vanligtvis kommer detta att innebära sektioner av få mikron (under 10 μm).
För att avbilda en specifik struktur eller händelse inuti en cell måste man se till att den här funktionen är inne i FoV i tilt-serien. Eftersom FoV i kryo-SXT är begränsad till 10 x 10 μm2 till 15 x 15 μm2 beroende på linsen och står för en pixelöversampling av upplösningen till minst en faktor 2, är den ofta mindre än hela cellförlängningen (se de röda rutorna som anges i figur 5). Därför måste avkastningen hittas och märkas korrekt. Detta görs vanligtvis med hjälp av fluorescerande taggar och korrelativa tillvägagångssätt för synligt ljus. 2D-strategier som kombinerar epifluorescens är enkla eftersom det mjuka röntgenöverföringsmikroskopet har ett integrerat on-line synligt ljusfluorescensmikroskop, men andra metoder för högupplöst 2D- eller 3D-fluorescenssignal finns ocksåtillgängliga 4,12,13,15,16 . I dessa fall måste rutnätet avbildas först i specifika instrument som superupplösningsmikroskop. Observera att de mest effektiva korrelativa metoderna är de som involverar datainsamling vid kryogena förhållanden. Detta beror på att tidsfördröjningen mellan rumstemperatur (RT), synligt ljusfluorescensavbildning och provförglasning, till exempel, kommer att hindra att fånga rätt cellulär händelse i tid; Dessutom kan förglasningsförfarandet lossa den intressanta cellen som har avbildats vid RT från rutnätet. Även om de flesta korrelativa avbildningsmetoder kan innebära att provnäten måste manipuleras och transporteras från ett instrument till ett annat, och trots den ökade risken för nätförorening eller skada som detta medför, är belöningen tydlig: att kunna identifiera specifika händelser eller molekyler inom det cellulära landskapet.
När helcellsavbildning krävs är det möjligt att sy olika tomogram förutsatt att den totala dosen som appliceras inte överskrider gränsen för strålskador. Vanligtvis är den deponerade dosen för att samla in få tomogram på samma cell långt under gränsen vid den uppnåeliga upplösningen (109 Gy) och därför krävs ingen specifik strategi för att sänka dosen, även om detta är prov- och experimentberoende. Vid intensiv datainsamling, t.ex. spektrotomografi, skulle det verkligen krävas en minimering av dosen och en bekväm datainsamling och specifika behandlingsstrategier.
Cryo-SXT har flera begränsningar, vilket bör nämnas här. Den första är den välkända saknade kilen, som är inneboende för att använda platta provstöd. Kapillärprovstöd som tillåter 180-graders rotation har använts tidigare och används fortfarande vid vissa anläggningar, men de uppvisar också nackdelar som en fattig kontrast på grund av glasabsorptionen och begränsningen av att använda celler i suspension. Ett sätt att minska effekten av den saknade kilen är att utföra dubbel lutningstomografi. Detta är verkligen möjligt vid Mistral strålrör nuförtiden. Den andra begränsningen fastställs av Fresnel-zonplattlinsen som används i sådana mikroskop. Detta objektiv ställer in den ultimata upplösningen som kan uppnås och skärpedjupet (DoF), båda är tätt relaterade. Detta innebär att ökad upplösning kommer att minska DoF medan cellens tjocklek ofta blir större. Till exempel kommer en 40 nm-lins i teorin att ha en DoF på 3 μm och en upplösning på 24,4 nm halv tonhöjd. Kompromissen mellan upplösning och DoF är därför strategisk och valet av lins beror på typen av cell30,31. Slutligen är operativa TXM över hela världen långt ifrån idealiska mikroskop och ansträngningar görs för att förbättra de optiska systemen för att nå de teoretiska förväntningarna. Slutligen kan visualiseringen och segmenteringen av de rekonstruerade volymerna utföras med specifika programvaruverktyg 25,32,33,34.
Sammanfattningsvis tillåter kryo-SXT avbildning av celler kvantitativt vid medelhög upplösning (25-30 nm halv tonhöjd) och i statistiska tal (få tiotals tomogram per dag). Detta gör det möjligt att erhålla organellernas organisation, distribution och dimension vid specifika förhållanden, till exempel under patogeninfektion eller sjukdomar, vid exakta tidpunkter eller efter särskilda behandlingar. Det är därför en användbar kompletterande biologisk avbildningsteknik till de vanligare elektron- och synliga ljusmikroskopierna, var och en av dem hanterar ett specifikt spektrum av provdimensioner och upplösning. Cryo-SXT används ofta i korrelativa tillvägagångssätt som involverar synlig ljusfluorescens, men andra kryokorrelativa strategier är också möjliga.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Projektet har fått finansiering från Europeiska kommissionens Horizon 2020 iNEXT-Discovery-projekt och Eus forsknings- och innovationsprogram Horizon 2020 inom ramen för Marie Skłodowska-Curie-bidragsavtalet nr 75439.
Materials
| Amira | Thermo Fisher | Software for segmentation | |
| Au Holey Carbon Films finder grids | (Quantifoil Micro Tools Gmb | R 2/2 Au G200F1 | Au Holey Carbon Films finder grids |
| Au nanoparticles | BBI Group, Cardiff, UK | Au nanoparticles 100nm | 100 nm Au nanoparticles (NPs) at Mistral (Alba) |
| Au nanoparticles | BBI Group, Cardiff, UK | Au nanoparticles 250nm | 250 nm Au nanoparticles (NPs) at B24 (Diamond) |
| Axio Scope A1 | Zeiss | 430035 9060 | Fluorescence microscope |
| Blotting No.1 filter paper | Whatman | WHA10010155 | Blotting filter |
| Bsoft | Software for projection alignment, reconstruction and visualization (Heymann et al., 2008) | ||
| Chimera | Software for segmentation (Pettersen et al. 2004) | ||
| Cryo-EM Glow Discharge Set | PELCO easiGlow | 91000S | Glow Discharge Cleaning System |
| Cu Holey Carbon Films finder grids | (Quantifoil Micro Tools Gmb | R 2/2Cu G200F1 | Cu Holey Carbon Films finder grids |
| Fetal calf serum | Sigma | F9665 | Heat Inactivated, sterile-filtered, suitable for cell culture |
| ImageJ | Software for image processing and analysis in Java (NIH & LOCI University of Wisconsin) | ||
| IMOD | Software for projection alignment, reconstruction and visualization (Kremer et al., 1996) | ||
| Leica EM GP Grid Plunger | Leica | 16706401 | Automatic Plunge Freezer EM |
| LINKAM cryo-stage | Linkam Scientific Instruments | CMS 196 | Cryo-Correlative Microscopy Stage |
| MIB | Software for segmentation (Belevich et al. 2016) | ||
| P100 Petri dish | Sigma | P6106 | Treated for cell culture and sterile |
| P60 Petri dish | Sigma | D8054 | Treated for cell culture and sterile |
| Polylysin | Sigma | P4707 | Poly-L-lysine solution 0.01%, sterile-filtered |
| Soft X-Ray microscope 0.25-1.2keV | Xradia | NCT-SB | Transmission soft X-Ray microscope |
| SURVOS | Software for segmentation (Luengo et al. 2017) | ||
| Tomo3d | Software for reconstruction (SIRT, WBP) (Agulleiro et al. 2011) | ||
| TomoJ | Software for reconstruction (ART) (Messaoudi et al., 2007) | ||
| XM Data Explorer | Zeiss | TXM software |
References
- Carrascosa, J. L., et al. Cryo X-ray tomography of vaccinia virus membranes and inner compartments. Journal of Structural Biology. 168, 234-239 (2009).
- Uchida, M., et al. Soft X-ray tomography of phenotypic switching and the cellular response to antifungal peptoids in Candida albicans. PNAS. 106, 19375-19380 (2009).
- Schneider, G., et al. Three-dimensional cellular ultrastructure resolved by X-ray microscopy. Nature Methods. 10, 1-3 (2010).
- Chichón, F. J., et al. Cryo nano-tomography of vaccinia virus infected cells. Journal of Structural Biology. 177, 202-211 (2012).
- Groen, J., Conesa, J. J., Valcárcel, R., Pereiro, E. The cellular landscape by soft X-ray tomography. Biophysical Reviews. 11, 611-619 (2019).
- Kepsutlu, B., et al. Cells undergo major changes in the quantity of cytoplasmic organelles after uptake of gold nanoparticles with biologically relevant surface coatings. ACS Nano. 14, 2248-2264 (2020).
- Natterer, F. . The mathematics of computerized tomography. , (1986).
- Weiss, D., et al. Computed tomography of cryogenic biological specimens based on X-ray microscopic images. Ultramicroscopy. 84, 185-197 (2000).
- Clowney, E. J., et al. Nuclear aggregation of olfactory receptor genes governs their monogenic expression. Cell. 151, 724-737 (2012).
- Duke, E. M. H., et al. Imaging endosomes and autophagosomes in whole mammalian cells using correlative cryo-fluorescence and cryo-soft X-ray microscopy (cryo-CLXM). Ultramicroscopy. 143, 77-87 (2014).
- Cinquin, B., et al. Putting molecules in their place. Journal of Cellular Biochemistry. 115, 209-216 (2014).
- Hagen, C., et al. Multimodal nanoparticles as alignment and correlation markers in fluorescence/soft X-ray cryo-microscopy/tomography of nucleoplasmic reticulum and apoptosis in mammalian cells. Ultramicroscopy. 146, 46-54 (2014).
- Pérez-Berná, A. J., et al. Structural changes in cells images by soft X-ray cryo-tomography during Hepatitis C virus infection. ACS Nano. 10, 6597-6611 (2016).
- Chiappi, M., et al. Cryo-soft X-ray tomography as a quantitative three-dimensional tool to model nanoparticle:cell interaction. Journal of Nanobiotechnology. 14, 15 (2016).
- Varsano, N., et al. Development of correlative cryo-soft X-ray tomography and stochastic reconstruction microscopy. A study of cholesterol crystal early formation in cells. Journal of the American Chemical Society. 138, 14931-14940 (2016).
- Kounatidis, I., et al. Correlative cryo-structured illumination fluorescence microscopy and soft X-ray tomography elucidates reovirus intracellular release pathway. Cell. 182, 1-16 (2020).
- Kapishnikov, S., et al. Mode of action of quinoline antimalarial drugs in red blood cells infected by Plasmodium falciparum revealed in vivo. PNAS. 116 (46), 22946-22952 (2019).
- Conesa, J. J., et al. Unambiguous intracellular localization and quantification of a potent iridium anticancer compound by correlative 3D cryo X-ray imaging. Angewandte Chemie International Edition. 59, 1270-1278 (2020).
- Gal, A., et al. Native-state imaging of calcifying and noncalcifying microalgae reveals similarities in their calcium storage organelles. PNAS. 115 (43), 11000-11005 (2018).
- Procopio, A., et al. Chemical fingerprint of Zn-hydroxyapatite in the early stages of osteogenic differentiation. ACS Central Science. 5, 1449-1460 (2019).
- Kahil, K., et al. Cellular pathways of calcium transport and concentration toward mineral formation in sea urchin larvae. PNAS. 117 (49), 30957-30965 (2020).
- Conesa, J. J., et al. Intracellular nanoparticles mass quantification by near-edge absorption soft X-ray nanotomography. Scientific Reports. 6, 22354 (2016).
- Otón, J., Sorzano, C. O. S., Maribini, R., Pereiro, E., Carazo, J. M. Measurement of the modulation transfer function of an X-ray microscope based on multiple Fourier orders analysis of a Siemens star. Optics Express. 23 (8), 9567-9572 (2015).
- Otón, J., et al. Characterization of transfer function, resolution and depth of field of a soft X-ray microscope applied to tomography enhancement by Wiener deconvolution. Biomedical Optics Express. 7, 5092-5103 (2016).
- Kremer, J. R., Mastronarde, D. N., McIntosh, J. R. Computer visualization of three-dimensional image data using IMOD. Journal of Structural Biology. 116, 71-76 (1996).
- Heymann, J. B., Cardone, G., Winkler, D. C., Steven, A. C. Computational resources for cryo-electron tomography in Bsoft. Journal of Structural Biology. 161, 232-242 (2008).
- Messaoudi, C., et al. Three-dimensional chemical mapping by EFTEM-TomoJ including improvement of SNR by PCA and ART reconstruction of volume by noise supression. Microscopy Microanalysis. 19, 1669-1677 (2013).
- Agulleiro, J. I., Fernández, J. J. Fast tomographic reconstruction on multicore computers. Bioinformatics. 27, 582-583 (2011).
- Toro-Nahuelpan, M., et al. Tailoring cryo-electron microscopy grids by photo-micropatterning for in-cell structural studies. Nature Methods. 17, 50-54 (2020).
- Attwood, D. . Soft X-rays and Extreme Ultraviolet Radiation. Principles and Applications. , (2000).
- Howells, M., Jacobsen, C., Warwick, T. . Principles and Applications of Zone Plate X-ray. Microscopes. Science of Microscopy. , (2007).
- Pettersen, E. F., et al. UCSF Chimera–a visualization system for exploratory research and analysis. Journal of Computational Chemistry. 25, 1605-1612 (2004).
- Belevich, I., Joensuu, M., Kumar, D., Vihinen, H., Jokitalo, E. Microscopy image browser: a platform for segmentation and analysis of multidimensional datasets. PLOS Biology. 14 (1), 1002340 (2016).
- Luengo, I., et al. SuRVoS: Super-region volume segmentation workbench. Journal of Structural Biology. 198, 43-53 (2017).

