Tredimensionell in vitro biomimetisk modell av neuroblastom med hjälp av kollagenbaserade strukturer
Summary
Denna artikel listar de steg som krävs för att så neuroblastomcellinjer på tidigare beskrivna tredimensionella kollagenbaserade strukturer, upprätthålla celltillväxt under en förutbestämd tidsram och hämta strukturer för flera celltillväxt- och cellbeteendeanalyser och nedströmsapplikationer, anpassningsbara för att tillfredsställa en rad experimentella mål.
Abstract
Neuroblastom är den vanligaste extrakraniella solida tumören hos barn och står för 15 % av de totala dödsfallen i barncancer. Den naturliga tumörvävnaden är en komplex tredimensionell (3D) mikromiljö som involverar lager av cancerösa och icke-cancerösa celler omgivna av en extracellulär matris (ECM). ECM ger fysiskt och biologiskt stöd och bidrar till sjukdomsprogression, patientprognos och terapeutiskt svar.
Denna artikel beskriver ett protokoll för att sätta ihop ett 3D-ställningsbaserat system för att efterlikna neuroblastommikromiljön med hjälp av neuroblastomcellinjer och kollagenbaserade ställningar. Stödställningarna kompletteras med antingen nanohydroxiapatit (nHA) eller glykosaminoglykaner (GAG), som finns naturligt i höga koncentrationer i ben och benmärg, de vanligaste metastaserna för neuroblastom. Den 3D-porösa strukturen hos dessa strukturer möjliggör neuroblastomcellbindning, proliferation och migration och bildandet av cellkluster. I denna 3D-matris är cellens svar på terapier mer reflekterande av in vivo-situationen .
Det ställningsbaserade odlingssystemet kan upprätthålla högre celldensiteter än konventionell tvådimensionell (2D) cellodling. Därför är optimeringsprotokoll för initiala såddcellantal beroende av de önskade experimentella tidsramarna. Modellen övervakas genom att bedöma celltillväxt via DNA-kvantifiering, cellviabilitet via metaboliska analyser och celldistribution inom ställningarna via histologisk färgning.
Denna modells tillämpningar inkluderar bedömning av gen- och proteinuttrycksprofiler samt cytotoxicitetstestning med konventionella läkemedel och miRNA. 3D-odlingssystemet möjliggör exakt manipulation av cell- och ECM-komponenter, vilket skapar en miljö som är mer fysiologiskt lik naturlig tumörvävnad. Därför kommer denna 3D in vitro-modell att öka förståelsen för sjukdomspatogenesen och förbättra korrelationen mellan resultat som erhållits in vitro, in vivo i djurmodeller och försökspersoner.
Introduction
Neuroblastom är en barncancer i det sympatiska nervsystemet som uppstår under embryonal utveckling eller tidigt postnatalt liv på grund av omvandlingen av neurala toppceller1. Det är den vanligaste solida extrakraniella tumören hos barn, representerar 8 % av de maligniteter som diagnostiseras hos patienter under 15 år och är ansvarig för 15 % av alla dödsfall i barncancer. Sjukdomen uppvisar mycket heterogena kliniska beteenden på grund av specifika kromosomala, genetiska och epigenetiska förändringar och histopatologiska egenskaper.
Dessa förändringar bidrar till aggressiviteten hos neuroblastom och dåliga resultat hos pediatriska patienter. Nuvarande behandlingar visar sig därför vara ineffektiva på lång sikt för nästan 80 % av patienterna med den kliniskt aggressiva sjukdomen2, vilket belyser det faktum att behandlingen för denna patientgrupp fortfarande är utmanande. Detta beror sannolikt på att mekanismerna för neuroblastomheterogenitet och metastaser fortfarande inte är helt klarlagda. Tumörmikromiljön (TME) anses dock nu allmänt spela en roll i utvecklingen av många cancerformer. Ändå är det fortfarande understuderat i neuroblastom 3,4.
Den ursprungliga TME-mikromiljön är en komplex 3D-mikromiljö med cancerceller och icke-cancerceller omgivna av en ECM. ECM hänvisar till den acellulära komponenten i en vävnad som ger strukturellt och biokemiskt stöd till sina cellulära invånare och bidrar till sjukdomsprogression, patientprognos och terapeutiskt svar5. Detta främjande av sjukdomsprogression beror på “dynamisk ömsesidighet” eller pågående dubbelriktad kommunikation mellan celler och ECM 6,7,8. När cancern fortskrider omorganiseras stromalt kollagen ofta i linjära mönster vinkelrätt mot gränsytan mellan stroma och cancer, som cancerceller använder som en migrationsväg till metastasering 9,10,11.
Huvudkomponenterna i denna naturliga funktionella biologiska struktur inkluderar ett fibröst nätverk av kollagener typ I och II och andra proteiner, inklusive elastin, glykoproteiner som laminin, samt en rad proteoglykaner och andra lösliga komponenter12,13. Dessa proteiner i den ursprungliga ECM har nu blivit attraktiva naturliga biomolekyler för utveckling av 3D in vitro-modeller. Användningen av 3D-strukturer för in vitro-cellodling ökar i popularitet på grund av dess större fysiologiska representation av TME jämfört med traditionell 2D-monolagerodling. De tillverkade 3D-ställningarna hjälper cellbindning, proliferation, migration, metabolism och respons på stimuli som ses i in vivo biologiska system.
Huvudkomponenten i dessa 3D-strukturer är kollagen, som är en nyckelspelare i många normala biologiska processer, inklusive vävnadsreparation, angiogenes, vävnadsmorfogenes, cellvidhäftning och migration11. Kollagenbaserade 3D-matriser har visat sin robusta funktionalitet för att modellera ECM, och fungerar som en in vitro biomimetisk mikromiljö samtidigt som de möjliggör cell-ECM-interaktioner samt cellmigration och invasion. Dessa 3D-matriser ger också en mer exakt analys av cellsvar på kemoterapeutiska läkemedel än traditionell 2D- eller “platt” odling i många cancermodeller 14,15,16, inklusive neuroblastom 17,18. Genetisk analys av 3D-cellkulturer har rapporterat en högre korrelation med den mänskliga vävnadsprofilen även jämfört med djurmodeller19. Sammantaget är hörnstenen i dessa 3D-strukturer att ge cellerna en lämplig in vitro-miljö, vilket rekapitulerar den ursprungliga vävnadsarkitekturen och underlättar dubbelriktad molekylär överhörning8.
För att öka komplexiteten hos kollagenbaserade modeller inkorporeras andra vanliga ECM-komponenter i vävnadsteknikprocessen, vilket skapar mer fysiologiskt relevanta modeller för att återspegla nischade TME-metoder i olika vävnader. Till exempel underlättar GAG, negativt laddade polysackarider som finns i alla däggdjursvävnader20, cellbindning, migration, proliferation och differentiering. Kondroitinsulfat är en specifik typ av GAG som finns i ben och brosk, som tidigare har använts i vävnadstekniska applikationer för benreparation 21,22,23,24,25. Nanohydroxiapatit (nHA) är den huvudsakliga oorganiska beståndsdelen i mineralsammansättningen i mänsklig benvävnad och utgör upp till 65 viktprocent av benet26 och används därför i stor utsträckning för benersättning och regenerering27. Således är GAG och nHA attraktiva kompositer för att rekonstruera det primära neuroblastom-ECM:t och modellera de vanligaste metastaserna av neuroblastom, benmärg (70,5 %) och ben (55,7 %)28.
Ställningar som innehåller dessa ECM-komponenter utvecklades ursprungligen för benvävnadstekniska tillämpningar med omfattande analys av deras biokompatibilitet, toxicitet och osteoledande och osteoinduktiva egenskaper29,30. De är porösa, kollagenbaserade matriser som framställs med hjälp av frystorkningstekniker för att kontrollera deras fysikaliska och biologiska egenskaper. Kollagenställningarna kompletterade med antingen nHA (Coll-I-nHA) eller kondroitin-6-sulfat (Coll-I-GAG) visade sig vara framgångsrika i att efterlikna primär TME vid bröstcancer31 och metastasering till skelettet vid prostatacancer15 samt neuroblastom17. Frystorkningstekniken som används för att tillverka dessa kompositställningar ger reproducerbar homogenitet i porstorlek och porositet inom ställningarna22,23,24. Kortfattat tillverkas en kollagenuppslamning (0,5 viktprocent) genom att blanda fibrillärt kollagen med 0,05 M ättiksyra. För Coll-I-GAG tillsätts 0,05 viktprocent chrondoitin-6-sulfat isolerat från hajbrosk till kollagenuppslamningen under blandningen. För de sammansatta Coll-I-nHA-ställningarna syntetiseras hydroxiapatitpartiklarna i nanostorlek enligt tidigare beskrivet27 och tillsätts kollagenuppslamningen i förhållandet 2:1 till kollagenets vikt under blandningsprocessen. Alla ställningar tvärbinds och steriliseras fysiskt med hjälp av en dehydrotermisk behandling vid 105 °C i 24 timmar25. Cylindriska ställningar (6 mm diameter, 4 mm höjd) erhålls med hjälp av en biopsistans och kan kemiskt tvärbindas med 3 mM N-(3-dimetylaminopropyl)-N’-etylkarbodiimidhydroklorid och 5,5 mM N-hydroxisuccinimid (EDAC/NHS) i destillerat vatten (dH2O) för att förbättra konstruktionernas mekaniska egenskaper30. Denna väloptimerade tillverkningsprocess av två kollagenställningar skapar ställningar med reproducerbara mekaniska egenskaper, inklusive porstorlek, porositet och styvhet (kPa). Både Coll-I-GAG- och Coll-I-nHA-ställningar har olika fysiska egenskaper, vilket skapar olika miljöförhållanden. Egenskaperna för varje ställning visas i tabell 1.
| Coll-I-GAG | Coll-I-nHA | |
| Ställningens storlek (diameter [mm] x höjd [mm]) |
6 × 4 17 | 6 × 4 17 |
| Kollagenkoncentration (viktprocent) | 0,5 17 | 0,5 17 |
| Substratkoncentration (viktprocent) [baserat på kollagenets vikt] |
0,05 15,17 | 200 17 Stockholm |
| Genomsnittlig porstorlek (mm) | 96 22 Stockholm | 96 – 120 29 |
| Porositet (%) | 99,5 23 | 98,9 – 99,4 27 |
| Styvhet (kPa) | 1,5 27 Stockholm | 5,5 – 8,63 29 |
Tabell 1: Översikt över de mekaniska egenskaperna hos de två strukturer som används för att studera neuroblastombiologi.
Denna artikel beskriver ett protokoll för att sätta ihop ett 3D-ställningsbaserat system för att bättre efterlikna neuroblastommikromiljön med hjälp av neuroblastomcellinjer och tidigare beskrivna kollagenbaserade strukturer kompletterade med antingen nHA (Coll-I-nHA) eller kondroitin-6-sulfat (Coll-I-GAG). Protokollet inkluderar nedströmsmetoder för att analysera tillväxtmekanismerna hos neuroblastomcellerna i en mer fysiologiskt relevant miljö med hjälp av tidigare optimerade billiga metoder anpassade från 2D-monolagerodling Figur 1.
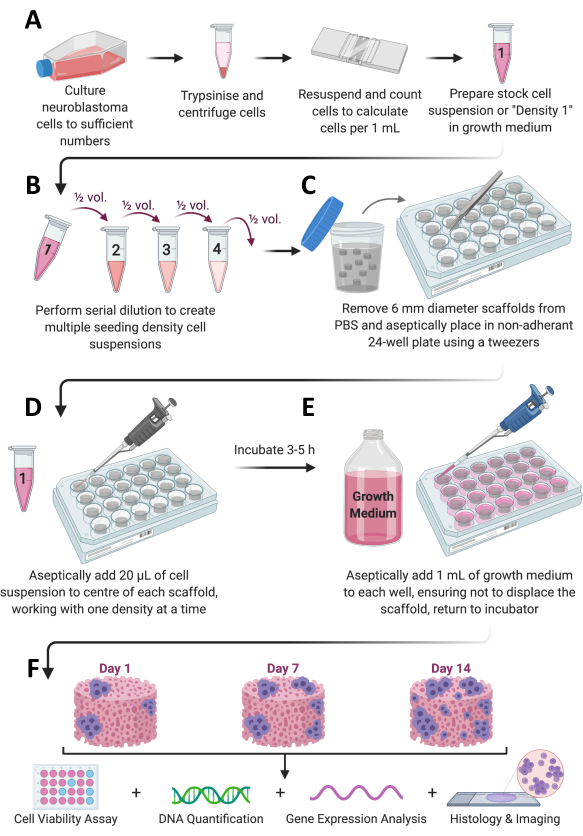
Bild 1: Övergripande protokollarbetsflöde. A) Cellerna odlas till tillräckligt antal, delas, räknas och återsuspenderas i en lämplig volym medium. (B) Detta cellmaterial genomgår sedan seriespädning för att framställa totalt 4 cellsuspensioner med olika densitet. (C) Kollagenbaserade ställningar pläteras sterilt i icke-vidhäftande 24-hålsplattor, och (D) 20 μL cellsuspension tillsätts i mitten av varje ställning och lämnas att inkubera vid 37 °C, 5 % CO2 och 95 % luftfuktighet i 3-5 timmar. (E) Komplett tillväxtmedium (1 ml) tillsätts sedan långsamt till varje ställning och plattorna placeras tillbaka i inkubatorn för att möjliggöra celltillväxt under önskad tidsram. (F) Vid varje förutbestämd tidpunkt hämtas flera strukturer för bedömning av cellviabilitet och tillväxt, analys av genuttryck och histologisk färgning. Klicka här för att se en större version av denna figur.
Protocol
Representative Results
Discussion
3D-modellen av scaffold-cancerceller har visat sig vara ett värdefullt och mångsidigt verktyg för att få mekanistisk insikt i neuroblastomcellers tillväxt, livsduglighet och infiltration av celler i en förenklad TME32. Den 3D-neuroblastommodell som beskrivs här efterliknar den minimala TME-metoden och ger mer fysiologiskt relevanta data än en 2D-monolagerodling. En stor nackdel med 3D-cellodling är ökad experimentell komplexitet och längre tidsramar. Här beskrivs ett optimerat protokoll för sådd, tillväxt och underhåll av neuroblastomceller på kollagenbaserade strukturer följt av nedströmsanalyser och applikationer, vilket ger robust karakterisering av celltillväxt. Vi strävade efter att få insikter om den optimala cellsåddstätheten för strukturerna för att skapa en förutsägbar och kontrollerbar miljö för att utvärdera läkemedelsbehandlingar mot cancer i ett snabbt 14-dagars experimentellt fönster. Kombinationen av alla dessa beskrivna enkla protokoll ger en väl avrundad bedömning av neuroblastomcelltillväxt i det ställningsbaserade de vitro-odlingssystemet.
De kritiska punkterna i protokolluppsättningen har betonats för att göra det möjligt för forskare att snabbt fastställa detsamma i sina laboratorier. Till exempel tillåter de angivna inkubationstiderna för bättre prestanda för den kolorimetriska cellviabilitetsanalysen djupare penetration av reagenset i ställningens porer för att nå alla celler. Dessutom är den fluorescerande dsDNA-färgningstekniken robust och okomplicerad; DNA-frisättning från byggnadsställningarna kräver dock kraftig celllys eftersom cellerna är “fångade” i kollagenfibrerna.
Med hjälp av den enkla DNA-kvantifieringsanalysen som beskrivs kan vi identifiera den logaritmiska tillväxtfasen på kollagenbaserade strukturer för screening av cancerläkemedel med hjälp av denna modell. I den beskrivna experimentella miljön användes 4 initiala cellsåddstätheter med en total 14-dagarsperiod och analystidpunkter på dag 1, 7 och 14. Vi identifierade att KellyLuc-celler sådda vid 4 × 105 celler/byggnadsställning har det mest signifikant aktiva proliferationsfönstret mellan dag 7 och 14. Dessa tillväxtdata i logfasen kommer att möjliggöra en tillförlitlig tolkning av olika cellcytotoxicitetsexperiment. Det eliminerar spekulationer om eventuell nedgång i tillväxt eller celldöd till följd av undertryckt tillväxt på den 3D-porösa plattformen snarare än från läkemedelstoxicitet. Cellviabilitet är också en allmänt använd bedömning av lämpligheten hos 3D-plattformar för att stödja tillväxten av olika celltyper33,34. Även om det finns många analyser för att mäta cellviabilitet, inklusive levande/död färgning, ATP-mätning, proliferationsanalyser, fann vi att användningen av Alamar Blue-kolorimetrisk cellviabilitetsanalys var en enkel och effektiv teknik för att stödja DNA-kvantifieringsdata.
Den kombinerade användningen av DNA-kvantifiering och cellviabilitet gav kompletterande bevis för att den optimala densiteten för fröceller på ställningen i genomsnitt är 2-4 × 105 celler/byggnadsställning. Detta protokoll kan dock enkelt anpassas för att uppfylla olika experimentella tidsramar, analystidpunkter och nedströmsapplikationer. Även om detta protokoll beskriver utvärderingen av monokulturcelltillväxt av neuroblastomceller på byggnadsställningar, är ställningarna lätt att ändra för användning som en plattform för samodling, beskriven av do Amaral et al., som använde kollagen-GAG-ställningar för att samodla keratinocyter och fibroblaster i en undersökning av sårläkning35.
Den beskrivna 3D-modellen möjliggör visualisering av celltillväxt och infiltration med hjälp av olika välkända tekniker, såsom immunofluorescens och standard H&E. Det är viktigt att visualisera cellerna tillsammans med karakteriseringen av tillväxt med hjälp av biokemiska analyser på grund av mångfalden av cellmorfologi och tillväxtmönster på byggnadsställningar. Att förstå tillväxtmönstret kan ge insikter om tillväxtbeteende och framtida respons på cancerläkemedel. Till exempel ger IMR32-tillväxt med hjälp av DNA-kvantifiering liknande mönster som Kelly, även om IMR32 vid visualisering med H&E växer i större kluster än Kelly, som uppvisade mer spridd tillväxt (figur 9). Dessa varierande tillväxtmönster för cellinjer i scaffolds återspeglar det kliniska scenariot för tumörheterogenitet. Att undersöka läkemedelssvar mot cancer med hjälp av en panel av cellinjer med olika morfologier i 3D-strukturer kommer att öka det prediktiva värdet för patientsvar på samma läkemedel.
Detektion av gen- eller proteinuttryck kan också utföras med andra metoder som RT-qPCR eller ELISA om proteinet av intresse utsöndras. En surrogatmarkör för neuroblastomprogression, kromogranin A (CgA)36, användes för att ytterligare karakterisera neuroblastomcelltillväxt i 3D. Som beskrivits i tidigare arbete17 ökade CgA-utsöndringen när cellerna förökade sig (Figur 10). Även om cellodling i monolager inte kunde fånga denna ökning, eftersom proliferation innebar att cellerna nådde fullt sammanflöde i odlingsskålarna, möjliggjorde användningen av 3D-kollagenställningarna långvarig bedömning av CgA-sekretionen.
Denna 3D in vitro-modell kanske inte är lämplig för alla forskningsfrågor för att studera neuroblastombiologi och svar på terapier. En av begränsningarna är ojämn cellpenetration i byggnadsställningar och bildandet av cellkluster av varierande storlek, vilket beror på en given cellinje och kan leda till okontrollerbar diffusion av näringsämnen och testläkemedel. Denna egenskap påverkar robustheten i terapeutisk screening. Men trots denna begränsning är det viktigt att tänka på att inhemska tumörer också är heterogena i storlek och cancercellsfördelning och innehåller många andra celltyper i tumörvävnaden. För att övervinna denna begränsning föreslår vi att man använder varje cellbefolkad struktur som en enda mikrovävnad för vilken följande parametrar kommer att optimeras: (a) inkubationstider för cellviabilitetsreagenset att nå cellerna och cellklustren, och (b) lysering av cellerna i Triton X-100-buffert genom förbehandling av celler på strukturer med en vävnadslysare för att frigöra DNA från cellerna som finns djupt i ställningen.
En annan teknisk begränsning med detta protokoll är bristen på mekanisk testning av varje parti av nytillverkade ställningar för denna modell. Men genom att använda den robusta tillverkningsprocessen för ställningarna, som har karakteriserats utförligt i förhållande till fysikaliska och kemiska egenskaper hos ställningarna, såsom tryck- och dragmodul, porositet och visuell porstruktur och homogenitet, säkerställs att ställningens kvaliteter bibehålls genom batcher 21,24,27,30,37.
Sammanfattningsvis presenterar denna artikel en serie enkla metoder för analys av cellulär tillväxt på kollagenbaserade byggnadsställningar. Både den experimentella tidslinjen och analyspunkterna kan bytas ut beroende på de specifika forskningsfrågorna. Detta protokoll är också anpassningsbart till andra celltyper. Resultaten som visas ovan ger belägg för hur denna sammanställning av metoder gav insikt i den optimala såddtätheten för olika neuroblastomcellinjer för att skapa kontinuerlig tillväxt under 14 dagar. Sammanslagningen av resultat som erhållits från alla metoder i detta protokoll ger en överlägsen förståelse för celltillväxt inom 3D-kollagenmatrisen. Framtida användning av denna modell kommer sannolikt att involvera samodlingssystem som är specifika för neuroblastomet TME och testning av olika nya läkemedel mot cancer.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Detta arbete stöddes av National Children’s Research Centre (NCRC), Irish Research Council (IRC) och Neuroblastoma UK. Illustrationerna är skapade med hjälp av BioRender.
Materials
| Cells | |||
| IMR-32 | ATCC | CCL-127 | |
| Kelly | ECACC | 82110411 | |
| KellyCis83 | Made in lab – derived from Kelly (Piskareva et al., 2015) | – | Increasing exposure to cisplatin. Cross resistance acquired |
| SH-SY5Y | ATCC | CRL-2266 | |
| Disposable | |||
| 0.22 µm syringe filter | Millex | SLHP033RS | |
| 1.5 mL Eppendorf tube | Eppendorf | 0030 120.086 | |
| 100 mL sterile Pot | Starstedt | – | |
| 10 mL plastic pipette | Cellstar | 607 180 | |
| 15 mL Falcon tube | Starstedt | 62.554.502 | |
| 25 mL plastic pipette | Cellstar | 760 180 | |
| 50 mL Falcon tube | Starstedt | 62.547.254 | |
| 5 mL plastic pipette | Cellstar | 606 180 | |
| 6 mm Biopsy punches | Kai Medical | BP-60F | |
| Aluminium foil | – | – | |
| Cover Slip | Menzel-Glaser | – | |
| HYPERflask | Corning | CLS10030 | |
| Microscope slides | Thermo Scientific | J1840AMNT | |
| Opaque black 96-well plate | Costar | 3915 | |
| Sterile P10 tips | Starlab | S1121-3810 | |
| Sterile P1000 tips | Starlab | S1122-1830 | |
| Sterile P20 tips | Starlab | S1123-1810 | |
| Sterile P200 tips | Starlab | S1120-8810 | |
| T-175 (175 cm2 flask) | Sarstedt | 83.3912 | |
| T-75 (75 cm2 flask) | Sarstedt | 83.3911.302 | |
| Translucent clear 96 well plate | Cellstar | 655180 | |
| Translucent non-adherent 24 well plates | Cellstar | 83.3922.500 | |
| Equipment | |||
| Autoclave | Astell | – | |
| Automatic tissue processor | Leica | TP1020 | |
| Centrifuge 5804 | Eppendorf | – | |
| Hemocytometer | Hausser Scientific | – | |
| Incubator | ThermoScientific | – | |
| Microtome | Leica | RM2255 | |
| Oven | Memmert | Calibrated by: Cruinn diagnostics Ltd | |
| P10 pipette | Gilson | ||
| P100 pipette | Gilson | ||
| P1000 pipette | Gilson | ||
| P20 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| P200 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| Paraffin section flotation bath | Electrothermal | MH8517 | Calibrated by: Cruinn diagnostics Ltd |
| Pipette electronic dispenser | Corning | StripipetterUltra | Calibrated by: Cruinn diagnostics Ltd |
| Plate cooler | Leica | EG1140C | Calibrated by: Cruinn diagnostics Ltd |
| Refrigerator -20 °C | Liebherr | – | |
| Refrigerator -80 °C | Liebherr | – | |
| Refrigerator 4 °C | Liebherr | – | |
| Seesaw Rocker | DLAb | SK-D1807-E | |
| Spectrophotometer – Victor3V Platereader | PerkinElmer | 1420 | |
| Tissue culture hood/Laminar flow hood | GMI | 8038-30-1044 | |
| Tissue Lyser | Qiagen | TissueLyser LT | |
| Tweezers | – | – | |
| Water bath | Grant | – | |
| Wax embedder | Leica | EG1140H | |
| Materials | |||
| 1 L Water | Adrona – Biosciences | 568 | |
| 1% Triton-X | Sigma Aldrich | 9002-93-1 | |
| 10x PBS tablets | Sigma Aldrich | P4417-100TAB | |
| 37% paraformaldehyde | Sigma-Aldrich | F8775 | |
| Alamar Blue Cell Viability Reagent | Invitrogen | DAL1100 | |
| Collagen- glycosaminoglycan scaffold | Tissue engineering research group (TERG) | ||
| Collagen-nanohydroxyapatite scaffold | Tissue engineering research group (TERG) | ||
| dH20 | Adrona – Biosciences | 568 | |
| Eosin | Sigma-Aldrich | E4009 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| EtOH | Sigma-Aldrich | 1.00983.2500 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| F12 | Gibco | 21765-029 | |
| FBS | Gibco | 10270-106 | |
| Hemaytoxylin | Sigma-Aldrich | HHS32-1L | |
| L-Glutamine | Gibco | 25030-024 | |
| MEM | Gibco | 21090-022 | |
| miRNA easy Kit | Qiagen | 217004 | |
| MNEAA’s | Gibco | 11140-035 | |
| Penicillin/streptomycin | Gibco | 015140-122 | |
| Qiazol | Qiagen | 79306 | |
| Quant-iT PicoGreen dsDNA Assay Kit | Invitrogen | P11496 | |
| RPMI | Gibco | 21875-034 | |
| Sodium bicarbonate | Sigma Aldrich | S7795-500G | |
| Tissue embedding Medium | Sigma | A6330-4LB | |
| Trypsin-EDTA | Gibco | 25300-054 | |
| Software | |||
| Excel | – | Excel 2016 | |
| ImageJ | – | – | |
| Prism | – | Version 9 | |
References
- Davidoff, A. M. Neuroblastoma. Seminars in Pediatric Surgery. 21 (1), 2-14 (2012).
- Matthay, K. K., et al. Neuroblastoma. Nature Reviews Disease Primers. 2, 16078 (2016).
- Costard, L. S., Hosn, R. R., Ramanayake, H., O’Brien, F. J., Curtin, C. M. Influences of the 3D microenvironment on cancer cell behaviour and treatment responsiveness: a recent update on lung, breast and prostate cancer models. Acta Biomaterialia. , (2021).
- Borriello, L., Seeger, R. C., Asgharzadeh, S., Declerck, Y. A. More than the genes, the tumor microenvironment in neuroblastoma. Cancer Letters. 380 (1), 304-318 (2016).
- Walker, C., Mojares, E., Del Río Hernández, A. Role of extracellular matrix in development and cancer progression. International Journal of Molecular Sciences. 19 (10), 3028 (2018).
- Bissell, M. J., Hall, H. G., Parry, G. How does the extracellular matrix direct gene expression. Journal of Theoretical Biology. 99 (1), 31-68 (1982).
- Schultz, G. S., Davidson, J. M., Kirsner, R. S., Bornstein, P., Herman, I. M. Dynamic reciprocity in the wound microenvironment. Wound Repair and Regeneration. 19 (2), 134-148 (2011).
- Brancato, V., Oliveira, J. M., Correlo, V. M., Reis, R. L., Kundu, S. C. Could 3D models of cancer enhance drug screening. Biomaterials. 232, 119744 (2020).
- Provenzano, P. P., et al. Collagen density promotes mammary tumor initiation and progression. BMC Medicine. 6, 11 (2008).
- Provenzano, P. P., et al. Collagen reorganization at the tumor-stromal interface facilitates local invasion. BMC Medicine. 4, 38 (2006).
- Ouellette, J. N., et al. Navigating the collagen jungle: The biomedical potential of fiber organization in cancer. Bio-ingénierie. 8 (2), 1-19 (2021).
- Kreger, S. T., Voytik-Harbin, S. L. Hyaluronan concentration within a 3D collagen matrix modulates matrix viscoelasticity, but not fibroblast response. Matrix Biology. 28 (6), 336-346 (2009).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. Journal of Cell Science. 123 (24), 4195-4200 (2010).
- Hume, R. D., et al. Tumour cell invasiveness and response to chemotherapeutics in adipocyte invested 3D engineered anisotropic collagen scaffolds. Scientific Reports. 8 (1), 12658 (2018).
- Fitzgerald, K. A., et al. The use of collagen-based scaffolds to simulate prostate cancer bone metastases with potential for evaluating delivery of nanoparticulate gene therapeutics. Biomaterials. 66, 53-66 (2015).
- Sapudom, J., Pompe, T. Biomimetic tumor microenvironments based on collagen matrices. Biomaterials Science. 6 (8), 2009-2024 (2018).
- Curtin, C., et al. A physiologically relevant 3D collagen-based scaffold-neuroblastoma cell system exhibits chemosensitivity similar to orthotopic xenograft models. Acta Biomaterialia. 70, 84-97 (2018).
- Gavin, C., et al. Neuroblastoma invasion strategies are regulated by the extracellular matrix. Cancers. 13 (4), 1-23 (2021).
- Ridky, T. W., Chow, J. M., Wong, D. J., Khavari, P. A. Invasive three-dimensional organotypic neoplasia from multiple normal human epithelia. Nature Medicine. 16 (12), 1450-1456 (2010).
- Casal, e. J., Crane, J. S. . Biochemistry, Glycosaminoglycans. , (2019).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. J. The effect of pore size on cell adhesion in collagen-GAG scaffolds. Biomaterials. 26 (4), 433-441 (2005).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. Influence of freezing rate on pore structure in freeze-dried collagen-GAG scaffolds. Biomaterials. 25 (6), 1077-1086 (2004).
- Haugh, M. G., Murphy, C. M., McKiernan, R. C., Altenbuchner, C., O’Brien, F. J. Crosslinking and mechanical properties significantly influence cell attachment, proliferation, and migration within collagen glycosaminoglycan scaffolds. Tissue Engineering. Part A. 17 (9-10), 1201-1208 (2011).
- Murphy, C. M., Haugh, M. G., O’Brien, F. J. The effect of mean pore size on cell attachment, proliferation and migration in collagen-glycosaminoglycan scaffolds for bone tissue engineering. Biomaterials. 31 (3), 461-466 (2010).
- Haugh, M. G., Jaasma, M. J., O’Brien, F. J. The effect of dehydrothermal treatment on the mechanical and structural properties of collagen-GAG scaffolds. Journal of Biomedical Materials Research – Part A. 89 (2), 363-369 (2009).
- Lowe, B., Hardy, J. G., Walsh, L. J. Optimizing nanohydroxyapatite nanocomposites for bone tissue engineering. ACS Omega. 5 (1), 1-9 (2020).
- Cunniffe, G. M., Dickson, G. R., Partap, S., Stanton, K. T., O’Brien, F. J. Development and characterisation of a collagen nano-hydroxyapatite composite scaffold for bone tissue engineering. Journal of Materials Science. Materials in Medicine. 21 (8), 2293-2298 (2010).
- DuBois, S. G., et al. Metastatic sites in stage IV and IVS neuroblastoma correlate with age, tumor biology, and survival. Journal of Pediatric Hematology/Oncology. 21 (3), 181-189 (1999).
- Ryan, A. J., Gleeson, J. P., Matsiko, A., Thompson, E. M., O’Brien, F. J. Effect of different hydroxyapatite incorporation methods on the structural and biological properties of porous collagen scaffolds for bone repair. Journal of Anatomy. 227 (6), 732-745 (2015).
- Tierney, C. M., et al. The effects of collagen concentration and crosslink density on the biological, structural and mechanical properties of collagen-GAG scaffolds for bone tissue engineering. Journal of the Mechanical Behavior of Biomedical Materials. 2 (2), 202-209 (2009).
- Cox, R. F., Jenkinson, A., Pohl, K., O’Brien, F. J., Morgan, M. P. Osteomimicry of mammary adenocarcinoma cells in vitro; increased expression of bone matrix proteins and proliferation within a 3D collagen environment. PLoS One. 7 (7), 41679 (2012).
- Nolan, J. C., et al. Preclinical models for neuroblastoma: advances and challenges. Cancer Letters. 474, 53-62 (2020).
- Sirivisoot, S., Pareta, R., Harrison, B. S. Protocol and cell responses in threedimensional conductive collagen gel scaffolds with conductive polymer nanofibres for tissue regeneration. Interface Focus. 4 (1), 20130050 (2014).
- Thevenot, P., Nair, A., Dey, J., Yang, J., Tang, L. Method to analyze three-dimensional cell distribution and infiltration in degradable scaffolds. Tissue Engineering. Part C-Methods. 14 (4), 319-331 (2008).
- do Amaral, R. J. F. C., et al. Functionalising collagen-based scaffolds with platelet-rich plasma for enhanced skin wound healing potential. Frontiers in Bioengineering and Biotechnology. 7, 371 (2019).
- Gkolfinopoulos, S., Tsapakidis, K., Papadimitriou, K., Papamichael, D., Kountourakis, P. Chromogranin A as a valid marker in oncology: Clinical application or false hopes. World Journal of Methodology. 7 (1), 9-15 (2017).
- O’Brien, F. J., et al. The effect of pore size on permeability and cell attachment in collagen scaffolds for tissue engineering. Technology and Health Care. 15 (1), 3-17 (2007).

