Tredimensjonal in vitro biomimetisk modell av neuroblastom ved bruk av kollagenbaserte stillas
Summary
Dette papiret viser trinnene som kreves for å frø neuroblastomcellelinjer på tidligere beskrevne tredimensjonale kollagenbaserte stillas, opprettholde cellevekst for en forhåndsbestemt tidsramme og hente stillas for flere cellevekst- og celleadferdsanalyser og nedstrømsapplikasjoner, tilpasningsdyktige for å tilfredsstille en rekke eksperimentelle mål.
Abstract
Neuroblastom er den vanligste ekstrakranielle solide svulsten hos barn, og står for 15% av de totale dødsfallene i barnekreft. Det opprinnelige tumorvevet er et komplekst tredimensjonalt (3D) mikromiljø som involverer lag av kreft- og ikke-kreftceller omgitt av en ekstracellulær matrise (ECM). ECM gir fysisk og biologisk støtte og bidrar til sykdomsprogresjon, pasientprognose og terapeutisk respons.
Dette papiret beskriver en protokoll for montering av et 3D-stillasbasert system for å etterligne neuroblastommikromiljøet ved hjelp av neuroblastomcellelinjer og kollagenbaserte stillas. Stillasene er supplert med enten nanohydroksyapatitt (nHA) eller glykosaminoglykaner (GAGs), naturlig funnet i høye konsentrasjoner i bein og benmarg, de vanligste metastatiske stedene for neuroblastom. Den 3D porøse strukturen til disse stillasene tillater neuroblastomcellefeste, spredning og migrasjon, og dannelsen av celleklynger. I denne 3D-matrisen reflekterer celleresponsen på terapeutika mer in vivo-situasjonen .
Det stillasbaserte kultursystemet kan opprettholde høyere celletetthet enn konvensjonell todimensjonal (2D) cellekultur. Derfor er optimaliseringsprotokoller for innledende såcellenumre avhengig av de ønskede eksperimentelle tidsrammene. Modellen overvåkes ved å vurdere cellevekst via DNA-kvantifisering, cellenes levedyktighet via metabolske analyser og cellefordeling i stillasene via histologisk farging.
Denne modellens applikasjoner inkluderer vurdering av gen- og proteinuttrykksprofiler samt cytotoksisitetstesting ved bruk av konvensjonelle legemidler og miRNA. 3D-kultursystemet muliggjør presis manipulering av celle- og ECM-komponenter, og skaper et miljø som er mer fysiologisk lik naturlig tumorvev. Derfor vil denne 3D in vitro-modellen fremme forståelsen av sykdomspatogenesen og forbedre korrelasjonen mellom resultater oppnådd in vitro, in vivo i dyremodeller og mennesker.
Introduction
Neuroblastom er en pediatrisk kreft i det sympatiske nervesystemet som oppstår under embryonisk utvikling eller tidlig postnatalt liv på grunn av transformasjon av nevrale kamceller1. Det er den vanligste solide ekstrakranielle svulsten hos barn, som representerer 8% av malignitetene diagnostisert hos pasienter under 15 år, og er ansvarlig for 15% av alle dødsfall i barndomskreft. Sykdommen viser svært heterogen klinisk atferd på grunn av spesifikke kromosomale, genetiske og epigenetiske endringer og histopatologiske egenskaper.
Disse endringene bidrar til aggressiviteten til neuroblastom og dårlige resultater hos pediatriske pasienter. Derfor viser dagens behandlinger seg å være ineffektive på lang sikt for nesten 80% av pasientene med den klinisk aggressive sykdommen2, noe som understreker det faktum at behandling for denne gruppen pasienter fortsatt er utfordrende. Dette skyldes sannsynligvis at mekanismene for neuroblastom, heterogenitet og metastaser fortsatt ikke er fullt ut forstått. Imidlertid er tumormikromiljøet (TME) nå allment antatt å spille en rolle i utviklingen av mange kreftformer; Likevel er det fortsatt understudert i neuroblastom 3,4.
Den opprinnelige TME er et komplekst 3D-mikromiljø som involverer kreft- og ikke-kreftceller omgitt av en ECM. ECM refererer til den acellulære komponenten i et vev som gir strukturell og biokjemisk støtte til sine cellulære beboere og bidrar til sykdomsprogresjon, pasientprognose og terapeutisk respons5. Denne fremmelsen av sykdomsprogresjon skyldes “dynamisk gjensidighet” eller pågående toveis kommunikasjon mellom celler og ECM 6,7,8. Etter hvert som kreft utvikler seg, blir stromalkollagen omorganisert ofte i lineære mønstre vinkelrett på stroma-kreftgrensesnittet, som kreftceller bruker som en migrerende rute til metastase 9,10,11.
Hovedkomponentene i dette opprinnelige funksjonelle biologiske stillaset inkluderer et fibrøst nettverk av kollagen type I og II og andre proteiner, inkludert elastin, glykoproteiner som laminin, samt en rekke proteoglykaner og andre løselige komponenter12,13. Disse proteinene fra den opprinnelige ECM har nå blitt attraktive naturlige biomolekyler for å utvikle 3D in vitro-modeller 3. Anvendelsen av 3D-stillas for in vitro cellekultur øker i popularitet på grunn av sin større fysiologiske representasjon av TME sammenlignet med tradisjonell 2D monolagskultur. De produserte 3D-stillasene hjelper cellefeste, spredning, migrasjon, metabolisme og respons på stimuli sett i in vivo biologiske systemer.
Hovedkomponenten i disse 3D-stillasene er kollagen, som er en nøkkelspiller i mange normale biologiske prosesser, inkludert vevsreparasjon, angiogenese, vevsmorfogenese, celleadhesjon og migrasjon11. Kollagenbaserte 3D-matriser har vist sin robuste funksjonalitet for å modellere ECM, og fungerer som et in vitro biomimetisk mikromiljø samtidig som det muliggjør celle-ECM-interaksjoner samt cellemigrasjon og invasjon. Disse 3D-matrisene gir også en mer nøyaktig analyse av cellerespons på kjemoterapeutiske legemidler enn tradisjonell 2D eller “flat” kultur i mange kreftmodeller 14,15,16, inkludert neuroblastom 17,18. Genetisk analyse av 3D-cellekulturer har rapportert en høyere korrelasjon med den menneskelige vevsprofilen selv sammenlignet med dyremodeller19. Samlet sett er hjørnesteinen i disse 3D-stillasene å gi cellene et egnet in vitro-miljø, som rekapitulerer den opprinnelige vevsarkitekturen og muliggjør toveis molekylær crosstalk8.
For å øke kompleksiteten til kollagenbaserte modeller, er andre vanlige ECM-komponenter innlemmet i vevsteknikkprosessen, og skaper dermed mer fysiologisk relevante modeller for å gjenspeile nisje-TME i forskjellige vev. For eksempel letter GAGs, negativt ladede polysakkarider som finnes i alle pattedyrvev20, cellevedlegg, migrasjon, spredning og differensiering. Chondroitinsulfat er en spesifikk type GAG som finnes i bein og brusk, som tidligere har blitt brukt i vevstekniske applikasjoner for beinreparasjon 21,22,23,24,25. Nanohydroksyapatitt (nHA) er den viktigste uorganiske bestanddelen av mineralsammensetningen av humant beinvev, som utgjør opptil 65 vekt% bein26 og brukes derfor mye til beinutskifting og regenerering27. Dermed er GAGs og nHA attraktive kompositter for å rekonstruere det primære neuroblastomet ECM og modellere de vanligste metastatiske stedene for neuroblastom, benmarg (70,5%) og bein (55,7%)28.
Stillas som inneholder disse ECM-komponentene ble opprinnelig utviklet for beinvevstekniske applikasjoner med omfattende analyse av deres biokompatibilitet, toksisitet og osteoledende og osteoinduktive egenskaper29,30. De er porøse, kollagenbaserte matriser produsert ved hjelp av frysetørkingsteknikker for å kontrollere deres fysiske og biologiske egenskaper. Kollagenstillasene supplert med enten nHA (Coll-I-nHA) eller kondroitin-6-sulfat (Coll-I-GAG) viste suksess i å etterligne den primære TME i brystkreft31 og metastase til bein i prostatakreft15 samt neuroblastom17. Frysetørkingsteknikken som brukes til å produsere disse sammensatte stillasene gir reproduserbar homogenitet i porestørrelse og porøsitet i stillasene22,23,24. Kort fortalt fremstilles en kollagenoppslemming (0,5 vekt%) ved å blande fibrillært kollagen med 0,05 M eddiksyre. For Coll-I-GAG tilsettes 0,05 vekt% av krondoitin-6-sulfat isolert fra haibrusk til kollagenoppslemmingen mens den blandes. For de sammensatte Coll-I-nHA-stillasene syntetiseres hydroksyapatitt partikler i nanostørrelse som tidligere beskrevet27 og tilsettes kollagenoppslemmingen i forholdet 2: 1 til vekten av kollagenet under blandingsprosessen. Alle stillas er fysisk tverrbundet og sterilisert ved hjelp av en dehydrotermisk behandling ved 105 °C i 24 timerog 25. Sylindriske stillaser (6 mm diameter, 4 mm høyde) oppnås ved hjelp av en biopsistans og kan kjemisk kryssbindes med 3 mM N-(3-dimetylaminopropyl)-N’-etylkarbodiimidhydroklorid og 5,5 mM N-hydroksysuccinimid (EDAC / NHS) i destillert vann (dH2O) for å forbedre de mekaniske egenskapene til konstruksjonene30. Denne veloptimaliserte produksjonsprosessen av to kollagenstillas skaper stillas med reproduserbare mekaniske egenskaper, inkludert porestørrelse, porøsitet og stivhet (kPa). Både Coll-I-GAG og Coll-I-nHA stillas har varierende fysiske egenskaper, noe som skaper forskjellige miljøforhold. Egenskapene til hvert stillas er vist i tabell 1.
| Coll-I-GAG | Coll-I-nHA | |
| Stillas størrelse (diameter [mm] x høyde [mm]) |
6 x 4 17 | 6 x 4 17 |
| Kollagenkonsentrasjon (vekt%) | 0,5 17 | 0,5 17 |
| Substratkonsentrasjon (vekt%) [Basert på vekten av kollagen] |
0,05 15,17 | 200 17 |
| Gjennomsnittlig porestørrelse (mm) | 96 22 | 96 – 120 29 |
| Porøsitet (%) | 99,5 23 | 98,9 til 99,4 27 |
| Stivhet (kPa) | 1.5 27 | 5,5 til 8,63 29 |
Tabell 1: Oversikt over de mekaniske egenskapene til de to stillasene som er tatt i bruk for å studere nevroblastombiologi.
Dette papiret beskriver en protokoll for montering av et 3D-stillasbasert system for bedre å etterligne neuroblastommikromiljøet ved hjelp av neuroblastomcellelinjer og tidligere beskrevne kollagenbaserte stillaser supplert med enten nHA (Coll-I-nHA) eller kondroitin-6-sulfat (Coll-I-GAG). Protokollen inkluderer nedstrømsmetoder for å analysere vekstmekanismene til neuroblastomcellene i et mer fysiologisk relevant miljø ved hjelp av tidligere optimaliserte billige metoder tilpasset 2D monolagskultur Figur 1.
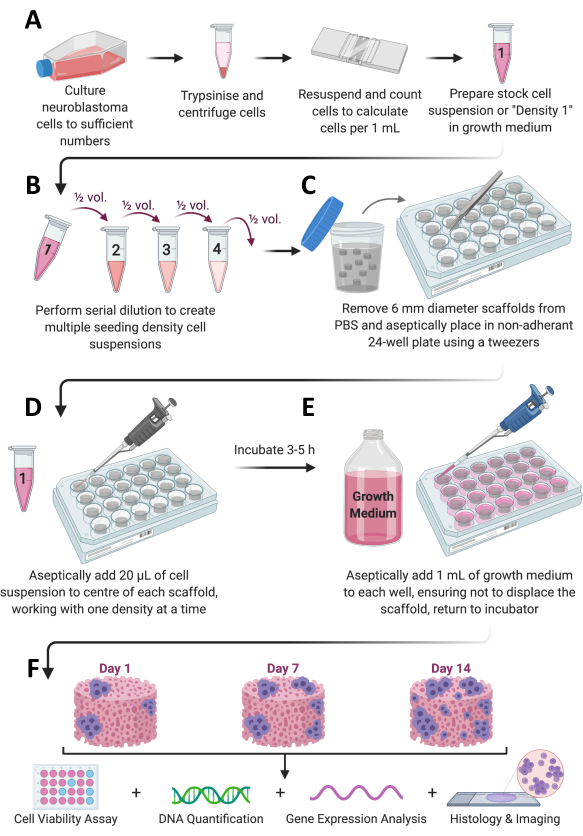
Figur 1: Samlet protokollarbeidsflyt. (A) Celler dyrkes til tilstrekkelig antall, splittes, telles og resuspenderes i et passende volum av medium. (B) Denne cellemassen gjennomgår deretter seriefortynning for å fremstille totalt 4 cellesuspensjoner med forskjellige tettheter. (C) Kollagenbaserte stillaser er sterilt belagt i ikke-klebende 24-brønnsplater, og (D) 20 μL cellesuspensjon tilsettes midten av hvert stillas og får inkubere ved 37 °C, 5% CO2 og 95% fuktighet i 3-5 timer. (E) Komplett vekstmedium (1 ml) tilsettes deretter sakte til hvert stillas, og platene plasseres tilbake i inkubatoren for å tillate cellevekst i ønsket tidsramme. (F) Ved hvert forhåndsbestemt tidspunkt hentes flere stillas for celle levedyktighet og vekstvurdering, genuttrykksanalyse og histologisk farging. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
3D-stillas-kreftcellemodellen har vist seg å være et verdifullt og allsidig verktøy for å få mekanistisk innsikt i nevroblastomcellevekst, levedyktighet og infiltrasjon av celler i en forenklet TME32. 3D-neuroblastommodellen beskrevet her etterligner minimal TME og gir mer fysiologisk relevante data enn en 2D monolagskultur. En stor ulempe med 3D-cellekultur er økt eksperimentell kompleksitet og lengre tidsrammer. Beskrevet her er en optimalisert protokoll for såing, vekst og vedlikehold av neuroblastomceller på kollagenbaserte stillaser etterfulgt av nedstrøms analyser og applikasjoner, noe som gir robust karakterisering av cellevekst. Vi hadde som mål å få innsikt i den optimale cellesåtettheten for stillasene for å skape et forutsigbart og kontrollerbart miljø for å vurdere behandling mot kreft i et raskt 14-dagers eksperimentelt vindu. Kombinasjonen av alle disse beskrevne enkle protokollene gir en godt avrundet vurdering av nevroblastomcellevekst i stillasbasert in vitro-kultursystem .
De kritiske punktene i protokolloppsettet har blitt vektlagt for å tillate forskere å etablere det samme i sine laboratorier raskt. For eksempel tillater de angitte inkubasjonstidene for bedre ytelse av den kolorimetriske cellelevedyktighetsanalysen dypere penetrasjon av reagenset i stillasporene for å nå alle celler. Dessuten er den fluorescerende dsDNA-fargeteknikken robust og grei; DNA-frigjøring fra stillasene krever imidlertid kraftig cellelyse da cellene er “fanget” i kollagenfibre.
Ved hjelp av den enkle DNA-kvantifiseringsanalysen som er beskrevet, kan vi identifisere loggvekstfasen på kollagenbaserte stillaser for screening av kreftmedisiner ved hjelp av denne modellen. I den beskrevne eksperimentelle settingen ble 4 innledende cellesåingstettheter brukt med en samlet 14-dagers periode og analysetidspunkter på dag 1, 7 og 14. Vi identifiserte at KellyLuc-celler sådd ved 4 × 105 celler/stillas har det mest signifikante aktive spredningsvinduet mellom dag 7 og 14. Disse loggfasevekstdataene vil muliggjøre pålitelig tolkning av forskjellige cellecytotoksisitetseksperimenter. Det eliminerer spekulasjoner om enhver nedgang i vekst eller celledød som følge av undertrykt vekst på den porøse 3D-plattformen i stedet for fra legemiddeltoksisitet. Cell levedyktighet er også en mye brukt vurdering for egnetheten til 3D-plattformer for å støtte veksten av forskjellige celletyper33,34. Mens det er mange analyser for å måle cellenes levedyktighet, inkludert levende / død farging, ATP-måling, spredningsanalyser, fant vi bruken av Alamar Blue kolorimetrisk celle levedyktighetsanalyse for å være en enkel og effektiv teknikk for å støtte DNA-kvantifiseringsdata.
Den kombinerte bruken av DNA-kvantifisering og celle levedyktighet ga komplementære bevis på at den optimale tettheten til frøceller på stillaset for å oppnå fortsatt vekst over en 14-dagers periode i gjennomsnitt er 2-4 × 105 celler / stillas. Denne protokollen kan imidlertid enkelt tilpasses for å tilfredsstille forskjellige eksperimentelle tidsrammer, analysetidspunkter og nedstrømsapplikasjoner. Selv om denne protokollen beskriver evalueringen av monokulturcellevekst av neuroblastomceller på stillas, er stillasene lett å endre for bruk som en plattform for samkultur, beskrevet av Amaral et al., som benyttet kollagen-GAG-stillas til å dyrke keratinocytter og fibroblaster i en undersøkelse av sårheling35.
Den beskrevne 3D-modellen muliggjør visualisering av cellevekst og infiltrasjon ved hjelp av forskjellige kjente teknikker, for eksempel immunfluorescens og standard H&E. Det er viktig å visualisere cellene sammen med karakterisering av vekst ved hjelp av biokjemiske analyser på grunn av mangfoldet av cellemorfologi og vekstmønstre på stillas. Å forstå vekstmønsteret kan gi innsikt i vekstatferd og fremtidig respons på kreftmedisiner. For eksempel gir IMR32-vekst ved hjelp av DNA-kvantifisering lignende mønstre som Kelly, men ved visualisering ved hjelp av H&E vokser IMR32 i større klynger enn Kelly, som viste mer spredt vekst (figur 9). Disse varierte vekstmønstrene av cellelinjer i stillas gjenspeiler det kliniske scenariet for tumorheterogenitet. Undersøkelse av legemiddelrespons mot kreft ved hjelp av et panel av cellelinjer med ulik morfologi i 3D-stillas vil øke den prediktive verdien for pasientrespons på de samme legemidlene.
Deteksjon av gen- eller proteinuttrykk kan også utføres ved hjelp av andre tilnærminger som RT-qPCR eller ELISA hvis proteinet av interesse utskilles. En surrogatmarkør for nevroblastomprogresjon, kromogranin A (CgA)36, ble brukt til å i tillegg karakterisere nevroblastomcellevekst i 3D. Som beskrevet i tidligere arbeid17, økte CgA-sekresjonen etter hvert som cellene prolifererte (figur 10). Mens monolags cellekultur ikke kunne fange denne økningen, da spredning betydde at celler nådde full samløp i kulturskålene, tillot bruken av 3D-kollagenstillasene langvarig vurdering av CgA-sekresjon.
Denne 3D in vitro-modellen er kanskje ikke egnet for alle forskningsspørsmål for å studere neuroblastombiologi og respons på terapi. En av begrensningene er ujevn cellepenetrasjon i stillas og dannelse av celleklynger av varierende størrelse, som avhenger av en gitt cellelinje og kan føre til ukontrollerbar diffusjon av næringsstoffer og testmedisiner. Denne funksjonen påvirker robustheten i terapeutisk screening. Til tross for denne begrensningen er det imidlertid viktig å vurdere at innfødte svulster også er heterogene i størrelse og kreftcellefordeling og inneholder mange andre celletyper i tumorvevet. For å overvinne denne begrensningen foreslår vi bruk av hvert cellebefolket stillas som et enkelt mikrovev for hvilket følgende parametere vil bli optimalisert: (a) inkubasjonstider for cellens levedyktighetsreagens for å nå cellene og celleklyngene, og (b) lysering av cellene i Triton X-100-buffer ved forbehandling av celler på stillaser med en vevslyser for å frigjøre DNA fra cellene som finnes dypt i stillaset.
En annen teknisk begrensning av denne protokollen er mangelen på mekanisk testing av hver batch av nyproduserte stillaser for denne modellen. Bruk av stillasets robuste produksjonsprosess, som har blitt omfattende karakterisert i forhold til fysiske og kjemiske egenskaper til stillasene, som kompresjons- og strekkmodul, porøsitet og visuell porestruktur og homogenitet, sikrer imidlertid at stillasegenskapene opprettholdes gjennom partiene 21,24,27,30,37.
Oppsummert presenterer denne artikkelen en rekke enkle metoder for analyse av cellulær vekst på kollagenbaserte stillas. Både den eksperimentelle tidslinjen og analysepunktene kan byttes ut avhengig av de spesifikke forskningsspørsmålene. Denne protokollen kan også tilpasses andre celletyper. Resultatene vist ovenfor gir bevis på hvordan denne sammenstillingen av metoder ga innsikt i den optimale såtettheten for forskjellige neuroblastomcellelinjer for å skape kontinuerlig vekst over 14 dager. Sammenslåingen av resultater oppnådd fra alle metodene i denne protokollen gir en overlegen forståelse av cellevekst i 3D-kollagenmatrisen. Fremtidig utnyttelse av denne modellen vil trolig innebære kokultursystemer som er spesifikke for neuroblastom TME og testing av ulike nye kreftmedisiner.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av National Children’s Research Center (NCRC), Irish Research Council (IRC) og Neuroblastoma UK. Illustrasjonene ble laget ved hjelp av BioRender.
Materials
| Cells | |||
| IMR-32 | ATCC | CCL-127 | |
| Kelly | ECACC | 82110411 | |
| KellyCis83 | Made in lab – derived from Kelly (Piskareva et al., 2015) | – | Increasing exposure to cisplatin. Cross resistance acquired |
| SH-SY5Y | ATCC | CRL-2266 | |
| Disposable | |||
| 0.22 µm syringe filter | Millex | SLHP033RS | |
| 1.5 mL Eppendorf tube | Eppendorf | 0030 120.086 | |
| 100 mL sterile Pot | Starstedt | – | |
| 10 mL plastic pipette | Cellstar | 607 180 | |
| 15 mL Falcon tube | Starstedt | 62.554.502 | |
| 25 mL plastic pipette | Cellstar | 760 180 | |
| 50 mL Falcon tube | Starstedt | 62.547.254 | |
| 5 mL plastic pipette | Cellstar | 606 180 | |
| 6 mm Biopsy punches | Kai Medical | BP-60F | |
| Aluminium foil | – | – | |
| Cover Slip | Menzel-Glaser | – | |
| HYPERflask | Corning | CLS10030 | |
| Microscope slides | Thermo Scientific | J1840AMNT | |
| Opaque black 96-well plate | Costar | 3915 | |
| Sterile P10 tips | Starlab | S1121-3810 | |
| Sterile P1000 tips | Starlab | S1122-1830 | |
| Sterile P20 tips | Starlab | S1123-1810 | |
| Sterile P200 tips | Starlab | S1120-8810 | |
| T-175 (175 cm2 flask) | Sarstedt | 83.3912 | |
| T-75 (75 cm2 flask) | Sarstedt | 83.3911.302 | |
| Translucent clear 96 well plate | Cellstar | 655180 | |
| Translucent non-adherent 24 well plates | Cellstar | 83.3922.500 | |
| Equipment | |||
| Autoclave | Astell | – | |
| Automatic tissue processor | Leica | TP1020 | |
| Centrifuge 5804 | Eppendorf | – | |
| Hemocytometer | Hausser Scientific | – | |
| Incubator | ThermoScientific | – | |
| Microtome | Leica | RM2255 | |
| Oven | Memmert | Calibrated by: Cruinn diagnostics Ltd | |
| P10 pipette | Gilson | ||
| P100 pipette | Gilson | ||
| P1000 pipette | Gilson | ||
| P20 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| P200 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| Paraffin section flotation bath | Electrothermal | MH8517 | Calibrated by: Cruinn diagnostics Ltd |
| Pipette electronic dispenser | Corning | StripipetterUltra | Calibrated by: Cruinn diagnostics Ltd |
| Plate cooler | Leica | EG1140C | Calibrated by: Cruinn diagnostics Ltd |
| Refrigerator -20 °C | Liebherr | – | |
| Refrigerator -80 °C | Liebherr | – | |
| Refrigerator 4 °C | Liebherr | – | |
| Seesaw Rocker | DLAb | SK-D1807-E | |
| Spectrophotometer – Victor3V Platereader | PerkinElmer | 1420 | |
| Tissue culture hood/Laminar flow hood | GMI | 8038-30-1044 | |
| Tissue Lyser | Qiagen | TissueLyser LT | |
| Tweezers | – | – | |
| Water bath | Grant | – | |
| Wax embedder | Leica | EG1140H | |
| Materials | |||
| 1 L Water | Adrona – Biosciences | 568 | |
| 1% Triton-X | Sigma Aldrich | 9002-93-1 | |
| 10x PBS tablets | Sigma Aldrich | P4417-100TAB | |
| 37% paraformaldehyde | Sigma-Aldrich | F8775 | |
| Alamar Blue Cell Viability Reagent | Invitrogen | DAL1100 | |
| Collagen- glycosaminoglycan scaffold | Tissue engineering research group (TERG) | ||
| Collagen-nanohydroxyapatite scaffold | Tissue engineering research group (TERG) | ||
| dH20 | Adrona – Biosciences | 568 | |
| Eosin | Sigma-Aldrich | E4009 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| EtOH | Sigma-Aldrich | 1.00983.2500 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| F12 | Gibco | 21765-029 | |
| FBS | Gibco | 10270-106 | |
| Hemaytoxylin | Sigma-Aldrich | HHS32-1L | |
| L-Glutamine | Gibco | 25030-024 | |
| MEM | Gibco | 21090-022 | |
| miRNA easy Kit | Qiagen | 217004 | |
| MNEAA’s | Gibco | 11140-035 | |
| Penicillin/streptomycin | Gibco | 015140-122 | |
| Qiazol | Qiagen | 79306 | |
| Quant-iT PicoGreen dsDNA Assay Kit | Invitrogen | P11496 | |
| RPMI | Gibco | 21875-034 | |
| Sodium bicarbonate | Sigma Aldrich | S7795-500G | |
| Tissue embedding Medium | Sigma | A6330-4LB | |
| Trypsin-EDTA | Gibco | 25300-054 | |
| Software | |||
| Excel | – | Excel 2016 | |
| ImageJ | – | – | |
| Prism | – | Version 9 | |
References
- Davidoff, A. M. Neuroblastoma. Seminars in Pediatric Surgery. 21 (1), 2-14 (2012).
- Matthay, K. K., et al. Neuroblastoma. Nature Reviews Disease Primers. 2, 16078 (2016).
- Costard, L. S., Hosn, R. R., Ramanayake, H., O’Brien, F. J., Curtin, C. M. Influences of the 3D microenvironment on cancer cell behaviour and treatment responsiveness: a recent update on lung, breast and prostate cancer models. Acta Biomaterialia. , (2021).
- Borriello, L., Seeger, R. C., Asgharzadeh, S., Declerck, Y. A. More than the genes, the tumor microenvironment in neuroblastoma. Cancer Letters. 380 (1), 304-318 (2016).
- Walker, C., Mojares, E., Del Río Hernández, A. Role of extracellular matrix in development and cancer progression. International Journal of Molecular Sciences. 19 (10), 3028 (2018).
- Bissell, M. J., Hall, H. G., Parry, G. How does the extracellular matrix direct gene expression. Journal of Theoretical Biology. 99 (1), 31-68 (1982).
- Schultz, G. S., Davidson, J. M., Kirsner, R. S., Bornstein, P., Herman, I. M. Dynamic reciprocity in the wound microenvironment. Wound Repair and Regeneration. 19 (2), 134-148 (2011).
- Brancato, V., Oliveira, J. M., Correlo, V. M., Reis, R. L., Kundu, S. C. Could 3D models of cancer enhance drug screening. Biomaterials. 232, 119744 (2020).
- Provenzano, P. P., et al. Collagen density promotes mammary tumor initiation and progression. BMC Medicine. 6, 11 (2008).
- Provenzano, P. P., et al. Collagen reorganization at the tumor-stromal interface facilitates local invasion. BMC Medicine. 4, 38 (2006).
- Ouellette, J. N., et al. Navigating the collagen jungle: The biomedical potential of fiber organization in cancer. Bio-ingénierie. 8 (2), 1-19 (2021).
- Kreger, S. T., Voytik-Harbin, S. L. Hyaluronan concentration within a 3D collagen matrix modulates matrix viscoelasticity, but not fibroblast response. Matrix Biology. 28 (6), 336-346 (2009).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. Journal of Cell Science. 123 (24), 4195-4200 (2010).
- Hume, R. D., et al. Tumour cell invasiveness and response to chemotherapeutics in adipocyte invested 3D engineered anisotropic collagen scaffolds. Scientific Reports. 8 (1), 12658 (2018).
- Fitzgerald, K. A., et al. The use of collagen-based scaffolds to simulate prostate cancer bone metastases with potential for evaluating delivery of nanoparticulate gene therapeutics. Biomaterials. 66, 53-66 (2015).
- Sapudom, J., Pompe, T. Biomimetic tumor microenvironments based on collagen matrices. Biomaterials Science. 6 (8), 2009-2024 (2018).
- Curtin, C., et al. A physiologically relevant 3D collagen-based scaffold-neuroblastoma cell system exhibits chemosensitivity similar to orthotopic xenograft models. Acta Biomaterialia. 70, 84-97 (2018).
- Gavin, C., et al. Neuroblastoma invasion strategies are regulated by the extracellular matrix. Cancers. 13 (4), 1-23 (2021).
- Ridky, T. W., Chow, J. M., Wong, D. J., Khavari, P. A. Invasive three-dimensional organotypic neoplasia from multiple normal human epithelia. Nature Medicine. 16 (12), 1450-1456 (2010).
- Casal, e. J., Crane, J. S. . Biochemistry, Glycosaminoglycans. , (2019).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. J. The effect of pore size on cell adhesion in collagen-GAG scaffolds. Biomaterials. 26 (4), 433-441 (2005).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. Influence of freezing rate on pore structure in freeze-dried collagen-GAG scaffolds. Biomaterials. 25 (6), 1077-1086 (2004).
- Haugh, M. G., Murphy, C. M., McKiernan, R. C., Altenbuchner, C., O’Brien, F. J. Crosslinking and mechanical properties significantly influence cell attachment, proliferation, and migration within collagen glycosaminoglycan scaffolds. Tissue Engineering. Part A. 17 (9-10), 1201-1208 (2011).
- Murphy, C. M., Haugh, M. G., O’Brien, F. J. The effect of mean pore size on cell attachment, proliferation and migration in collagen-glycosaminoglycan scaffolds for bone tissue engineering. Biomaterials. 31 (3), 461-466 (2010).
- Haugh, M. G., Jaasma, M. J., O’Brien, F. J. The effect of dehydrothermal treatment on the mechanical and structural properties of collagen-GAG scaffolds. Journal of Biomedical Materials Research – Part A. 89 (2), 363-369 (2009).
- Lowe, B., Hardy, J. G., Walsh, L. J. Optimizing nanohydroxyapatite nanocomposites for bone tissue engineering. ACS Omega. 5 (1), 1-9 (2020).
- Cunniffe, G. M., Dickson, G. R., Partap, S., Stanton, K. T., O’Brien, F. J. Development and characterisation of a collagen nano-hydroxyapatite composite scaffold for bone tissue engineering. Journal of Materials Science. Materials in Medicine. 21 (8), 2293-2298 (2010).
- DuBois, S. G., et al. Metastatic sites in stage IV and IVS neuroblastoma correlate with age, tumor biology, and survival. Journal of Pediatric Hematology/Oncology. 21 (3), 181-189 (1999).
- Ryan, A. J., Gleeson, J. P., Matsiko, A., Thompson, E. M., O’Brien, F. J. Effect of different hydroxyapatite incorporation methods on the structural and biological properties of porous collagen scaffolds for bone repair. Journal of Anatomy. 227 (6), 732-745 (2015).
- Tierney, C. M., et al. The effects of collagen concentration and crosslink density on the biological, structural and mechanical properties of collagen-GAG scaffolds for bone tissue engineering. Journal of the Mechanical Behavior of Biomedical Materials. 2 (2), 202-209 (2009).
- Cox, R. F., Jenkinson, A., Pohl, K., O’Brien, F. J., Morgan, M. P. Osteomimicry of mammary adenocarcinoma cells in vitro; increased expression of bone matrix proteins and proliferation within a 3D collagen environment. PLoS One. 7 (7), 41679 (2012).
- Nolan, J. C., et al. Preclinical models for neuroblastoma: advances and challenges. Cancer Letters. 474, 53-62 (2020).
- Sirivisoot, S., Pareta, R., Harrison, B. S. Protocol and cell responses in threedimensional conductive collagen gel scaffolds with conductive polymer nanofibres for tissue regeneration. Interface Focus. 4 (1), 20130050 (2014).
- Thevenot, P., Nair, A., Dey, J., Yang, J., Tang, L. Method to analyze three-dimensional cell distribution and infiltration in degradable scaffolds. Tissue Engineering. Part C-Methods. 14 (4), 319-331 (2008).
- do Amaral, R. J. F. C., et al. Functionalising collagen-based scaffolds with platelet-rich plasma for enhanced skin wound healing potential. Frontiers in Bioengineering and Biotechnology. 7, 371 (2019).
- Gkolfinopoulos, S., Tsapakidis, K., Papadimitriou, K., Papamichael, D., Kountourakis, P. Chromogranin A as a valid marker in oncology: Clinical application or false hopes. World Journal of Methodology. 7 (1), 9-15 (2017).
- O’Brien, F. J., et al. The effect of pore size on permeability and cell attachment in collagen scaffolds for tissue engineering. Technology and Health Care. 15 (1), 3-17 (2007).

