Быстрая фиксация in vivo и выделение трансляционных комплексов из эукариотических клеток
Summary
Представлена методика быстрой стабилизации поступательных (белковый биосинтез) комплексов со сшиванием формальдегида в живых дрожжевых и млекопитающих клетках. Этот подход позволяет препарировать переходные промежуточные продукты и динамические взаимодействия РНК:белок. Сшитые комплексы могут использоваться в нескольких последующих приложениях, таких как методы профилирования на основе глубокого секвенирования, микроскопия и масс-спектрометрия.
Abstract
Быстрые ответы, включающие быстрое перераспределение матричной(м)РНК и изменения трансляции мРНК, имеют отношение к текущим гомеостатическим корректировкам клеток. Эти корректировки имеют решающее значение для выживаемости эукариотических клеток и «контроля повреждений» во время колебаний уровня питательных веществ и солености, температуры и различных химических и радиационных стрессов. Из-за высокодинамического характера ответов на уровне РНК и нестабильности многих промежуточных продуктов РНК:РНК и РНК:белок получение значимого снимка состояния цитоплазматической РНК возможно только при ограниченном числе методов. Эксперименты по профилированию рибосом на основе транскриптома на основе РНК-seq являются одними из наиболее информативных источников данных для контроля трансляции. Однако отсутствие равномерной промежуточной стабилизации РНК и РНК:белок может привести к различным смещениям, особенно в быстро меняющихся путях клеточного ответа. В этой статье мы предоставляем подробный протокол быстрой фиксации, применимый к эукариотическим клеткам различной проницаемости, чтобы помочь в промежуточной стабилизации РНК и РНК:белок. Далее приведены примеры выделения стабилизированных комплексов РНК:белок на основе их совместного осаждения с рибосомными и поли(рибо)сомальными фракциями. Отделенный стабилизированный материал может быть впоследствии использован в рамках экспериментов типа профилирования рибосом, таких как подход секвенирования трансляционного комплексного профиля (TCP-seq) и его производных. Универсальность методов в стиле TCP-seq в настоящее время продемонстрирована приложениями в различных организмах и типах клеток. Стабилизированные комплексы также могут быть дополнительно очищены сродством и визуализированы с помощью электронной микроскопии, разделены на различные поли(рибо)сомальные фракции и подвергнуты секвенированию РНК, благодаря легкости разворота сшивки. Поэтому методы, основанные на охлаждении и фиксации формальдегида с последующим осаждением или другим типом обогащения комплекса РНК:белок, могут представлять особый интерес для исследования более тонких деталей быстрой динамики комплекса РНК:белок в живых клетках.
Introduction
Живые организмы подвержены динамическим внутри- и внеклеточным изменениям на протяжении всей своей жизни, которые требуют быстрых реакций для поддержания гомеостаза и обеспечения выживания. Чтобы обеспечить адаптацию к окружающей среде, эукариотические клетки регулируют свой метаболизм с помощью контроля экспрессии генов. Контроль экспрессии генов может осуществляться во время транскрипции и/или трансляции; с трансляционными ответами, как правило, происходящими быстрее1,2,3,4. Например, трансляционные изменения обычно возникают в течение 1-30 минут после начала стресса, в то время как изменения уровня транскрипции следуют черезнесколькочасов после воздействия стресса3,4,5. Изменения в трансляционном выходе достигаются быстрее благодаря постоянной доступности молекул матричной (м)РНК в цитоплазме. И наоборот, на уровне транскрипции новые молекулы мРНК должны синтезироваться, а у эукариот обрабатываться и экспортироваться из ядра, вызывая обширные задержки во времени отклика2,4,6,7,8.
Острая трансляционная реакция на стресс обычно характеризуется общим снижением трансляционного выхода с селективной регуляцией белков, необходимых для выживания клеток.1,3,4,9. Считается, что снижение производства белка имеет решающее значение из-за высоких энергетических затрат процесса.3,7. Для облегчения селективного торможения и повышения регуляции трансляционные реакции обслуживаются целым рядом сложных регуляторных механизмов. Регуляция может осуществляться на всех этапах трансляции: инициация, удлинение, прекращение биосинтеза полипептидов и рециркуляция рибосомы10,11,12,13, но наиболее сильно проявляется на этапе инициации5,7,9,10,13. Во время инициации малая рибосомная субъединица (SSU), поддерживаемая эукариотическими факторами инициации (eIF), связывается и сканирует 5′ нетранслированную область (UTR) мРНК до тех пор, пока не будет распознан стартовый кодон.2,5,6,8,11,12,13. Регулирующие механизмы часто нацелены на eIF, влияющие на прикрепление, сканирование и распознавание кодонов. Например, фактор инициации eIF2, существенный фактор трансляции, который помогает в наборе инициатора Met-tRNAiMet в СБУ, часто нацеливается на эукариот в стрессовых условиях4,6,11. В дрожжах фосфорилирование этого фактора может быть вызвано депривацией питательных веществ и осмотическим стрессом.1,4,11,14,15, а в клетках млекопитающих аминокислотное голодание, стресс эндоплазматического ретикулума (ER), УФ-стресс, вирусная инфекция и измененный уровень кислорода могут вызвать этот ответ8,9,11. Быстрое повышение регуляции специфической трансляции мРНК проявляется в реакции клеток млекопитающих на гипоксию, которая демонстрирует глобальное быстрое ингибирование трансляции и селективное повышение регуляции биосинтеза гипоксий-индуцируемых факторов (HIFs). HIF являются факторами транскрипции, которые затем вызывают долгосрочное клеточное перепрограммирование на уровне транскрипции ДНК.8,9,16. Аналогичные реакции наблюдались у дрожжей при тепловом стрессе, с быстрой трансляционной экспрессией белков теплового шока (HSP), за которой следовали замедленные реакции на уровне транскрипции.17,18. В дополнение к депривации питательных веществ и тепловому шоку, поступательные реакции в дрожжах были изучены при различном кислороде.8,19солёность5, фосфат, сера20,21 и азот22,23 Уровней. Это исследование имеет широкие последствия для промышленного использования дрожжей, таких как выпечка и ферментация.24,25. Трансляционные реакции также могут играть важную роль в углублении понимания таких заболеваний, как нейродегенеративные расстройства и болезни сердца, которые характеризуются внутриклеточными стрессами, такими как окислительный стресс. В целом, трансляционные реакции являются неотъемлемой частью контроля экспрессии генов и способствуют быстрой адаптации к широкому спектру стрессовых состояний в эукариотических организмах.
Для изучения трансляционных ответов требуются методы, обеспечивающие минимально искаженные снимки переводческого ландшафта. Полисомное профилирование — классический подход, используемый при изучении трансляции через мРНК, включающий разделение поли(рибо)сомальных фракций мРНК посредством ультрацентрифугирования через градиенты сахарозы26,27. Этот подход может быть использован для изучения уровней трансляции для отдельных мРНК (с помощью методов обнаружения, таких как обратная транскрипция и полимеразная цепная реакция,ОТ-ПЦР 26),или глобально в сочетании с высокопроизводительными методами (микрочипы или РНК-seq28,29). Более развитым подходом является профилирование рибосом, позволяющее изучать положения удлиняющихся рибосом вдоль молекулы мРНК в общегеномном масштабе, а также делать вывод об эффективности трансляции через транскриптом и использовании основного и альтернативного стартовых участков30,31. Профилирование рибосом включает в себя выделение и секвенирование фрагментов мРНК, защищенных рибосомным присутствием над ними. Профилирование рибосом обеспечило значительное понимание динамики трансляции в ряде состояний, включая гипоксический стресс, тепловой шок и окислительный стресс31,32. Метод был адаптирован к нескольким типам исходного материала, включая дрожжи и клетки млекопитающих.
В то время как профилирование полисом и рибосом было фундаментальным в расширении возможностей исследований в переводе, процесс перевода включает в себя различные трансляционные промежуточные продукты и комплексы, которые трудно охватить с помощью этих методов11,13. Дополнительное ограничение связано с отсутствием способности изучать типы быстрого ответа, поскольку трансляционные комплексы либо стабилизируются in vivo путем добавления специфических ингибиторов трансляции (антибиотиков), что приводит к определенным артефактам распределения рибосом, либо ex vivo при клеточном лизисе конкретно (антибиотики) или неспецифично (с высоким содержанием соли или ионов магния), что приводит к лишению более короткоживущих или менее стабильных промежуточных продуктов33, 34,35.
Формальдегид широко используется для сшивания нуклеиновых кислот и белков, например, в исследованиях иммунопреципитации хроматина (ChIP) и сшивки иммунопреципитации (CLIP). Его небольшие размеры и отличная проницаемость клеток позволяют осуществлять быстрое in vivo действие36. Основываясь на быстром сшивке формальдегида, подход профилирования рибосом был расширен с помощью секвенирования профиля translation Complex (TCP-seq)10,36,37,38,39,40. TCP-seq, впервые разработанный в дрожжах, позволяет захватывать все промежуточные трансляции, включая сканирующие или пост-терминальные комплексы SSU и множественные рибосомные конфигурации37,38,41,42. Метод был использован в нескольких исследованиях10,38, 39,41,42,некоторые из которых используют комбинаторный подход как ингибиторов трансляции, так и сшивки формальдегида для облегчения остановки трансляции. Еще одна модифицированная версия метода, селективный TCP-seq39,недавно была использована для включения иммуноочищения сшитых комплексов, расширяя сферу применения TCP-seq. Быстрый, эффективный и обратимый характер сшивки формальдегида делает эти подходы подходящими для изучения переходных сложных взаимодействий мРНК:трансляции, особенно в контексте высокодинамичных путей ответа на уровне трансляции.
Здесь мы подробно описываем процессы сшивки формальдегида in vivo с целью комплексной стабилизации и изоляции комплекса переводов. Мы предоставляем отдельные протоколы, нюансированные для дрожжей и клеток млекопитающих(рисунок 1). Далее мы приводим примеры последующего использования стабилизированного сшиванием материала(рисунок 1),например, для обнаружения коочищенного белкового фактора с использованием иммуноблоттинга (вестерн-блоттинг), иммуноассистированной очистки (или «иммунопреципитации»; IP) и обогащение трансляционных комплексов, содержащих специфические интересующие факторы, электронная микроскопия и секвенирование РНК.
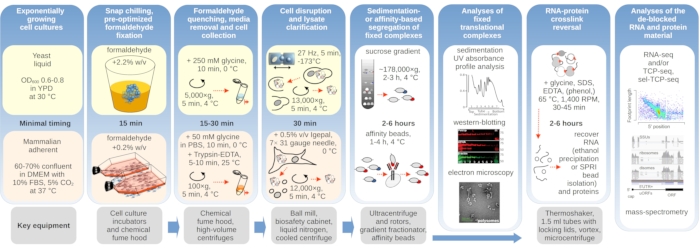
Рисунок 1:Схема, изображающая обзор типичной экспериментальной установки. Основные этапы стабилизации in vivo формальдегида трансляционных комплексов изображены в виде блок-схемы, дополненной информацией о ключевых необходимых инструментах. Описаны потенциальные последующие применения сшитого материала, включая примеры, которые были успешно использованы, но непосредственно не охвачены в этом протоколе, такие как очистка шариков SPRI РНК, секвенирование РНК и масс-спектрометрия. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Protocol
Representative Results
Discussion
Фиксация формальдегида является удобным и популярным методом достижения быстрого in vivo сшивания биомолекул10,36,45,46,47,48. По сравнению с другими потенциальными мишенями биомолекул, успешный захват трансляционных комплексов требует немедленной фиксации во время мгновенного охлаждения клеток или другого материала. Без неустановленной стабилизации существует вероятность продолжения различных процессов, связанных с трансляцией, смещения сложного распределения от невозмущенного состояния in vivo 49. По сравнению с другими методами трансляционной остановки и стабилизации рибосомного комплекса, быстрота действия формальдегида через клеточные мембраны и неизбирательный характер сшивок обещают сохранение максимального разнообразия промежуточных продуктов трансляционного комплекса ближе к их изначально распределенным состояниям50.
Представленный здесь подход был установлен и оптимизирован как в дрожжевых, так и в клетках млекопитающих, и в настоящее время методы были получены другими группами для использования в более разнообразном биологическом материале, например, у целых позвоночных (например, эмбрионов рыбок данио)10,38,39,49,51,52 . Хотя эти работы в совокупности убеждают в универсальности и широкой применимости подхода, быстрое сшивание формальдегида трансляционных комплексов можно считать несколько трудным для переноса на новые типы биологического материала из-за необходимости оптимизации и корректировки.
Главным требованием к успеху метода является повторная оптимизация концентрации формальдегида и метода сбора и разрушения клеток. Менее проницаемые, мелкие и круглые дрожжевые клетки требуют гораздо более высокой (по крайней мере, в 10 раз) концентрации формальдегида и физического разрушения фиксированных клеток. Напротив, крупные и уплощенные адгезивные клетки млекопитающих в культуре могут быть легко перефиксированы и требуют бережного обращения при фиксации, в то время как извлечение фиксированных комплексов может быть выполнено химическим путем с разрушением мембраны с использованием моющих средств. Недостаточное сшивание может позволить менее стабильным или более короткоживущим промежуточным продуктам диссоциировать или просачиваться в более позднее состояние. Чрезмерное сшивание может негативно повлиять на способность выделять и изучать рибосомные фракции и может создавать селективные смещения, такие как более глубокое истощение тяжелых комплексов. По нашим наблюдениям, даже незначительные изменения, такие как тип используемых адгезивных клеток человека, могут повлиять на выход восстановленных сшитых комплексов и могут потребовать повторной оптимизации режима сшивания. Мы также можем ожидать, что клетки с существенно отличающимися свойствами проницаемости, такие как растительные клетки, потребуют дополнительной обширной оптимизации условий фиксации52. Тем не менее, трудно представить себе тип биологического материала, который был бы совершенно несовместим с подходом.
Одним из соображений, относящихся к протоколу фиксации млекопитающих, является плотность и количество клеточного материала, используемого в качестве входных данных. Рекомендуется, чтобы клетки непрерывно росли без повторного посева или других возмущений в течение не менее 2 дней, чтобы избежать внешних воздействий на динамику клеточной трансляции. Применимо для большинства типов клеток, но для большинства адгезивных клеток последовательно достигнутые уровни слияния не более 70% обеспечат отсутствие серьезных эффектов ингибирования контакта, которые могут негативно и непредсказуемо влиять на скорость трансляции.
Еще одной интересной и потенциально уникально удобной особенностью фиксации формальдегида, вытекающей из его неизбирательной реакционной способности, является стабилизационное воздействие на поступательные комплексы в системах смешанной таксономии. Бактериальные, а тем более поступательные комплексы митохондрий, хлоропластов и различных внутриклеточных паразитов, как известно, трудно нацелить на специфические ингибиторы трансляции. Напротив, в данных TCP-seq следы, отображаемые с митотранскриптомом, легко наблюдаются в данных38,39,50. Интересным последующим событием могло бы стать использование подхода к исследованию трансляции в целых микросообществах, таких как образцы почвы, воды или кишечника, где надежная быстрая трансляционная остановка и комплексная стабилизация любыми другими средствами были бы проблематичными.
Следует также отметить, что для наиболее сложного материала (такого как твердые и/или громоздкие ткани) ничто не препятствует использованию стабилизации формальдегида сразу после разрушения клеток и гомогенизации материала. Этот подход уже часто используется для устранения задержки входа в клетку при стабилизации поступательных комплексов со специфическими ингибиторами малых молекул33,53,54,55. Учитывая, что фиксация формальдегида традиционно использовалась с отличными результатами для стабилизации образцов ex vivo/in vitro в таких приложениях, как электронная микроскопия45,56,57,58,мы можем ожидать еще меньших негативных эффектов в этом случае, особенно тех, которые связаны с плохим извлечением поступательных комплексов из тщательно зафиксированных клеток.
Наши результаты подтверждают удобство быстрой фиксации формальдегида для стабилизации высокопреходящих комплексов, таких как те, которые включают eIF4A. Примечательно, что в отличие от млекопитающих, дрожжи eIF4A гораздо слабее связаны с колпачковым связывающим комплексом eIF4F и, как следствие, трансляционными комплексами в целом. eIF4A обычно теряется при любой обширной очистке рибосомного материала в дрожжах29,59,60,61,62,63. Тем не менее, в in vivo-фиксированномдрожжевом материале можно добиться надежного обогащения eIF4A во всех фракциях поступательных комплексов, где ожидается его присутствие. Ранее опубликованные данные Sel-TCP-seq продемонстрировали обогащение eIF2 и eIF3, которые более прочно ассоциируются с рибосомами (но также выявили временно происходящую котрансляционную сборку белкового комплекса)39. Таким образом, метод подходит для обнаружения как более сильных, так и более слабых прикрепленных составляющих поступательных комплексов.
Подводя итог, мы представили подход, полезный для получения информации в первую очередь об изменениях, происходящих на начальной фазе трансляции и когда требуется минимально возмущенное рибосомное распределение по мРНК. Важно отметить, что подход подходит для стабилизации относительно лабильных и динамических компонентов поступательных комплексов, таких как eIF4A, и может широко использоваться при условии необходимой оптимизации. Мы также предоставили доказательства полезности фиксации формальдегида в сценариях быстрого динамического изменения трансляции, открывая области исследования, такие как быстро меняющиеся клеточные реакции на изменения окружающей среды или стрессовые условия.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Эта работа была поддержана грантом Австралийского исследовательского совета Discovery Project (DP180100111 для T.P. и N.E.S),грантом Национального совета по здравоохранению и медицинским исследованиям (GNT1175388 to N.E.S.) и исследовательской стипендией (APP1135928 to T.P.). Авторы признают возможности Microscopy Australia в Центре передовой микроскопии Австралийского национального университета, который финансируется Университетом и федеральным правительством.
Materials
| Yeast extract | Merck, Sigma-Aldrich | 70161 | |
| Peptone | Merck, Sigma-Aldrich | 70178 | |
| D-Glucose (Dextrose) | Merck, Sigma-Aldrich | 49139 | |
| Adenine sulphate | Amresco | 0607-50G | |
| Formaldehyde solution | Merck Sigma-Aldrich | F11635-500ML | ACS reagent, 37 wt. % in H2O, contains 10-15% Methanol as stabiliser (to prevent polymerisation) |
| RNaseOUT™ Recombinant Ribonuclease Inhibitor | Invitrogen™ byThermo Fischer Scientific | 10777019 | |
| cOmplete™, EDTA-free Protease Inhibitor Cocktail | COEDTAF-RO Roche by Merck | 11873580001 | |
| Magnesium chloride solution | (Merck/Sigma-Aldrich) | M1028 | |
| Ethylenediaminetetraacetic acid solution | (Merck/Sigma-Aldrich) | E7889 | |
| Ambion™ RNase I, cloned, 100 U/µL | Ambion | AM2294 | |
| SUPERase•In™ RNase Inhibitor (20 U/μL) | Invitrogen™ by Thermo Fisher Scientific | AM2694 | |
| Acidic phenol:chlorophorm:isoamyl alcohol 125:24:1 (pH 4.0-5.0) | (Merck/Sigma-Aldrich) | P1944-100ML | |
| Dynabeads™ Goat Anti-Mouse IgG | Invitrogen™ by Thermo Fisher Scientific) | 11033 | |
| Sodium Acetate (3 M), pH 5.5 | Invitrogen™ by Thermo Fisher Scientific) | AM9740 | |
| Glycogen (5 mg/ml) | Invitrogen™ by Thermo Fisher Scientific) | AM9510 | |
| Ethyl alcohol, Pure | Merck; Sigma Aldrich | E7023 | |
| Amersham™ Hybond® P Western blotting membranes, PVDF | Merck | GE10600023 | PVDF membrane for western blotting |
| Bolt™ 4 to 12%, Bis-Tris, 1.0 mm, Mini Protein Gel | Invitrogen™ by ThermoFischer Sientific | NW04120BOX | Protein gel |
| 4X Bolt™ LDS Sample Buffer | Invitrogen™ by ThermoFischer Sientific | B0007 | LDS sample loading buffer |
| Precision Plus Protein™ Kaleidoscope™ Prestained Protein Standards | BioRad | 1610375 | Protein ladder |
| 20X Bolt™ MES SDS Running Buffer | ThermoFischer Scientific | B0002 | PAGE runninjg buffer |
| Intercept® (PBS) Blocking Buffer | LI-COR | 927-70001 | Odyssey Blcoking buffer (PBS) |
| IRDye® 800CW Goat anti-Mouse IgG Secondary Antibody | LI-COR | 92632210 | |
| IRDye® 800CW Goat anti-Rabbit IgG Secondary Antibody | LI-COR | 92632211 | |
| TAP Tag Polyclonal Antibody | Invitrogen™ by ThermoFischer Sientific | CAB1001 | |
| Anti-beta Actin antibody | Abcam | ab8227 | |
| Sucrose | (Merck/Sigma-Aldrich) | 84097 | BioUltra, for molecular biology, ≥99.5% (HPLC) |
| DL-Dithiothreitol solution | (Merck/Sigma-Aldrich) | 43816 | BioUltra, for molecular biology, ~1 M in H2O |
| Terumo Syringe 1CC/mL | Terumo Syringe | 878499 | |
| Potassium chloride | (Merck/Sigma-Aldrich) | 60128 | |
| HEPES | (Merck/Sigma-Aldrich) | H3375 | |
| Dulbecco's Modified Eagle's Medium – high glucose | Sigma Aldrich | D5796 | |
| Fetal Bovine Serum | Sigma Aldrich | 12003C | |
| Trypsin-EDTA (0.05%), phenol red | Gibco | 25300062 | |
| Dulbecco's Phosphate Buffered Saline with Calcium and magnesium | Sigma-Aldrich | D8662 | |
| Glycine | Sigma-Aldrich | G7126 | |
| Tris hydrochloride | Merck/Sigma-Aldrich | 10812846001 | |
| Sodium dodecyl sulfate | Merck/Sigma-Aldrich | 436143 | |
| IGEPAL CA-630 | Merck/Sigma-Aldrich | I3021 | |
| Rnasin Ribonuclease Inhibitor | Promega | N2111 | |
| Stainless steel grinding jar | Retsch | 02.462.0059 | |
| MM400 mixer mill | Retsch | 20.745.0001 | |
| Gradient Fractionator | Brandel | BRN-BR-188 | |
| Thermomixer R | Eppendorf | Z605271 | |
| Nanodrop spectrophotometer | Thermo Fisher Scientific | ND-2000 | |
| 0.5-ml microcentrifuge tubes with locking devices | Eppendorf Safe-Lock | 30121023 | |
| Mini Gel Tank | (Thermo Fisher Scientific) | A25977 | PAGE running tank |
| 5 mL, Open-Top Thinwall Ultra-Clear Tube, 13 x 51mm | Beckman-Coulter | 344057 | |
| 13.2 mL, Certified Free Open-Top Thinwall Polypropylene, 14 x 89mm – 50Pk | Beckman-Coulter | 331372 | |
| Amicon Ultra-0.5 ultrafiltration devices | Merck | UFC5030 | Ultracel-30 regenerated cellulose membrane, 0.5 mL sample volume |
| Thermo Sorvall Evolution RC Floor Super Speed Centrifuge | Cambridge Scientific | 15566 | |
| Beckman Coulter Optima L-90K | GMI | 8043-30-1191 | |
| Nunc EasYFlask 175cm2 | Thermofisher Scientific | 159910 | |
| Falcon 50 mL Conical Centrifuge Tubes | Thermofisher Scientific | 14-432-22 | |
| 25 mL Serological Pipette | Sigma-Aldrich | SIAL1250 | |
| 10 mL Serological Pipette | Sigma-Aldrich | SIAL1100 | |
| DNA lobind tubes | Eppendorf | 30108051 | |
| Cold Centrifuge 5810 R | Eppendorf | EP022628188 | for 50 mL tubes |
| Orbital Shaking Incubator | Ratek | OM11 | |
| Frezco 17 Microcentrifuge | Thermofisher Scientific | 75002402 | |
| Eppendorf DNA lo-bind tubes | Merck/Sigma-Aldrich | EP0030108051 | |
| Eppendorf® Protein LoBind tubes | Merck/Sigma-Aldrich | EP0030108116 | |
| SW 41 Ti Swinging bucket rotor | Beckman-Coulter | 331362 | |
| Heracell™ 150i CO2 Incubator, 150 L | Thermofisher Scientific | 51026282 | |
| 0,3 mL ultra-fine II short insulin syringe | BD Medical | 328822 | |
| 3 mL syringe with Luer Lok tip | BD Medical | 302113 | |
| 25 G x 16 mm Hypodermic Needle | Terumo | TUAN2516R1 |
References
- Janapala, Y., Preiss, T., Shirokikh, N. E. Control of translation at the initiation phase during glucose starvation in yeast. International Journal of Molecular Sciences. 20 (16), 4043 (2019).
- Masvidal, L., Hulea, L., Furic, L., Topisirovic, I., Larsson, O. mTOR-sensitive translation: Cleared fog reveals more trees. RNA Biology. 14 (10), 1299-1305 (2017).
- Ashe, M. P., De Long, S. K., Sachs, A. B. Glucose depletion rapidly inhibits translation initiation in yeast. Molecular Biology of the Cell. 11 (3), 833-848 (2000).
- Crawford, R. A., Pavitt, G. D. Translational regulation in response to stress in Saccharomyces cerevisiae. Yeast. 36 (1), 5-21 (2019).
- Melamed, D., Pnueli, L., Arava, Y. Yeast translational response to high salinity: global analysis reveals regulation at multiple levels. RNA. 14 (7), 1337-1351 (2008).
- Hershey, J. W., Sonenberg, N., Mathews, M. B. Principles of translational control: An overview. Cold Spring Harbor Perspectives in Biology. 4 (12), 011528 (2012).
- Mata, J., Marguerat, S., Bähler, J. Post-transcriptional control of gene expression: a genome-wide perspective. Trends in Biochemical Sciences. 30 (9), 506-514 (2005).
- Spriggs, K. A., Bushell, M., Willis, A. E. Translational regulation of gene expression during conditions of cell stress. Molecular Cell. 40 (2), 228-237 (2010).
- Liu, B., Qian, S. B. Translational reprogramming in cellular stress response. Wiley Interdisciplinary Reviews RNA. 5 (3), 301-315 (2014).
- Archer, S. K., Shirokikh, N. E., Beilharz, T. H., Preiss, T. Dynamics of ribosome scanning and recycling revealed by translation complex profiling. Nature. 535 (7613), 570-574 (2016).
- Hinnebusch, A. G., Ivanov, I. P., Sonenberg, N. Translational control by 5′-untranslated regions of eukaryotic mRNAs. Science. 352 (6292), 1413-1416 (2016).
- Dever, T. E., Green, R. The elongation, termination, and recycling phases of translation in eukaryotes. Cold Spring Harbor Perspectives in Biology. 4 (7), 013706 (2012).
- Shirokikh, N. E., Preiss, T. Translation initiation by cap-dependent ribosome recruitment: Recent insights and open questions. Wiley Interdisciplinary Reviews RNA. 9 (4), 1473 (2018).
- Jiménez-Díaz, A., Remacha, M., Ballesta, J. P., Berlanga, J. J. Phosphorylation of initiation factor eIF2 in response to stress conditions is mediated by acidic ribosomal P1/P2 proteins in Saccharomyces cerevisiae. PLoS One. 8 (12), 84219 (2013).
- Sonenberg, N., Hinnebusch, A. G. Regulation of translation initiation in eukaryotes: mechanisms and biological targets. Cell. 136 (4), 731-745 (2009).
- Majmundar, A. J., Wong, W. J., Simon, M. C. Hypoxia-inducible factors and the response to hypoxic stress. Molecular Cell. 40 (2), 294-309 (2010).
- Barraza, C. E., et al. The role of PKA in the translational response to heat stress in Saccharomyces cerevisiae. PLoS One. 12 (10), 0185416 (2017).
- Richter, K., Haslbeck, M., Buchner, J. The heat shock response: Life on the verge of death. Molecular Cell. 40 (2), 253-266 (2010).
- Jamar, N. H., Kritsiligkou, P., Grant, C. M. The non-stop decay mRNA surveillance pathway is required for oxidative stress tolerance. Nucleic Acids Research. 45 (11), 6881-6893 (2017).
- Chen, Z., et al. The complete pathway for thiosulfate utilization in Saccharomyces cerevisiae. Applied and Environmental Microbiology. 84 (22), (2018).
- Marzluf, G. A. Molecular genetics of sulfur assimilation in filamentous fungi and yeast. Annual Review of Microbiology. 51, 73-96 (1997).
- Miller, D., Brandt, N., Gresham, D. Systematic identification of factors mediating accelerated mRNA degradation in response to changes in environmental nitrogen. PLoS Genetics. 14 (5), 1007406 (2018).
- Zhang, W., Du, G., Zhou, J., Chen, J. Regulation of sensing, transportation, and catabolism of nitrogen sources in Saccharomyces cerevisiae. Microbiology and Molecular Biology Reviews. 82 (1), (2018).
- Tokpohozin, S. E., Fischer, S., Becker, T. Selection of a new Saccharomyces yeast to enhance relevant sorghum beer aroma components, higher alcohols, and esters. Food Microbiology. 83, 181-186 (2019).
- Walker, G. M., Stewart, G. G. Saccharomyces cerevisiae in the production of fermented beverages. Beverages. 2 (4), 30 (2016).
- Chassé, H., Boulben, S., Costache, V., Cormier, P., Morales, J. Analysis of translation using polysome profiling. Nucleic Acids Research. 45 (3), 15 (2017).
- Jin, H. Y., Xiao, C. An integrated polysome profiling and ribosome profiling method to investigate in vivo translatome. Methods in Molecular Biology. 1712, 1-18 (2018).
- Arava, Y., et al. Genome-wide analysis of mRNA translation profiles in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 100 (7), 3889-3894 (2003).
- Lackner, D. H., et al. A network of multiple regulatory layers shapes gene expression in fission yeast. Molecular Cell. 26 (1), 145-155 (2007).
- Ingolia, N. T., Ghaemmaghami, S., Newman, J. R. S., Weissman, J. S. Genome-Wide Analysis in Vivo of Translation with Nucleotide Resolution Using Ribosome Profiling. Science. 324 (5924), 218-223 (2009).
- Ingolia, N. T., Hussmann, J. A., Weissman, J. S. Ribosome Profiling: Global Views of Translation. Cold Spring Harbor Perspectives in Biology. 11 (5), (2019).
- Gerashchenko, M. V., Lobanov, A. V., Gladyshev, V. N. Genome-wide ribosome profiling reveals complex translational regulation in response to oxidative stress. Proceedings of the National Academy of Sciences of the United States of America. 109 (43), 17394-17399 (2012).
- Hussmann, J. A., Patchett, S., Johnson, A., Sawyer, S., Press, W. H. Understanding biases in ribosome profiling experiments reveals signatures of translation dynamics in yeast. Proceedings of the National Academy of Sciences Genetics. 11 (12), 1005732 (2015).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Hoffman, E. A., Frey, B. L., Smith, L. M., Auble, D. T. Formaldehyde crosslinking: A tool for the study of chromatin complexes. Journal of Biological Chemistry. 290 (44), 26404-26411 (2015).
- Kage, U., Powell, J. J., Gardiner, D. M., Kazan, K. Ribosome profiling in plants: What is not lost in translation. Journal of Experimental Botany. 71 (18), 5323-5332 (2020).
- Shirokikh, N. E., Archer, S. K., Beilharz, T. H., Powell, D., Preiss, T. Translation complex profile sequencing to study the in vivo dynamics of mRNA-ribosome interactions during translation initiation, elongation and termination. Nature Protocols. 12 (4), 697-731 (2017).
- Wagner, S., et al. Selective translation complex profiling reveals staged initiation and co-translational assembly of initiation factor complexes. Molecular Cell. 79 (4), 546-560 (2020).
- Zlotorynski, E. Profiling ribosome dynamics. Nature Reviews Molecular Cell Biology. 17 (9), 535-535 (2016).
- Sen, N. D., Gupta, N., S, K. A., Preiss, T., Lorsch, J. R., Hinnebusch, A. G. Functional interplay between DEAD-box RNA helicases Ded1 and Dbp1 in preinitiation complex attachment and scanning on structured mRNAs in vivo. Nucleic Acids Research. 47 (16), 8785-8806 (2019).
- Zhao, J., Qin, B., Nikolay, R., Spahn, C. M. T., Zhang, G. Translatomics: The global view of translation. International Journal of Molecular Sciences. 20 (1), 20010212 (2019).
- Luthe, D. S. A simple technique for the preparation and storage of sucrose gradients. Analytical Biochemistry. 135 (1), 230-232 (1983).
- Wang, Z., Gerstein, M., Snyder, M. RNA-Seq: A revolutionary tool for transcriptomics. Nature Review Genetics. 10 (1), 57-63 (2009).
- Orlando, V. Mapping chromosomal proteins in vivo by formaldehyde-crosslinked-chromatin immunoprecipitation. Trends in Biochemical Sciences. 25 (3), 99-104 (2000).
- Schmiedeberg, L., Skene, P., Deaton, A., Bird, A. A Temporal Threshold for Formaldehyde Crosslinking and Fixation. PLoS One. 4 (2), 4636 (2009).
- Solomon, M. J., Varshavsky, A. Formaldehyde-mediated DNA-protein crosslinking: A probe for in vivo chromatin structures. Proceedings of the National Academy of Sciences. 82 (19), 6470-6474 (1985).
- Solomon, M. J., Larsen, P. L., Varshavsky, A. Mapping proteinDNA interactions in vivo with formaldehyde: Evidence that histone H4 is retained on a highly transcribed gene. Cell. 53 (6), 937-947 (1988).
- Bohlen, J., Fenzl, K., Kramer, G., Bukau, B., Teleman, A. A. Selective 40S footprinting reveals cap-tethered ribosome scanning in human cells. Molecular Cell. 79 (4), 561-574 (2020).
- Shirokikh, N. E. Translation complex stabilization on messenger RNA and footprint profiling to study the RNA responses and dynamics of protein biosynthesis in the cells. Critical Reviews in Biochemistry and Molecular Biology. , (2021).
- Giess, A., et al. Profiling of small ribosomal subunits reveals modes and regulation of translation initiation. Cell Reports. 31 (3), 107534 (2020).
- Firmino, A. A. P., et al. Separation and paired proteome profiling of plant chloroplast and cytoplasmic ribosomes. Plants (Basel). 9 (7), (2020).
- Gerashchenko, M. V., Gladyshev, V. N. Translation inhibitors cause abnormalities in ribosome profiling experiments. Nucleic Acids Research. 42 (17), 134 (2014).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Plénat, F., et al. Formaldehyde fixation in the third millennium. Annales De Pathologie. 21 (1), 29-47 (2001).
- Salic, A., Mitchison, T. J. A chemical method for fast and sensitive detection of DNA synthesis in vivo. Proceedings of the National Academy of Sciences. 105 (7), 2415-2420 (2008).
- Wang, N. S., Minassian, H. The formaldehyde-fixed and paraffin-embedded tissues for diagnostic transmission electron microscopy: A retrospective and prospective study. Human Pathology. 18 (7), 715-727 (1987).
- Grifo, J. A., et al. Characterization of eukaryotic initiation factor 4A, a protein involved in ATP-dependent binding of globin mRNA. Journal of Biological Chemistry. 257 (9), 5246-5252 (1982).
- Li, Y. Commonly used tag combinations for tandem affinity purification. Biotechnology and Applied Biochemistry. 55 (2), 73-83 (2010).
- Blum, S., et al. ATP hydrolysis by initiation factor 4A is required for translation initiation in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences. 89 (16), 7664-7668 (1992).
- Merrick, W. C. eIF4F: A Retrospective. Journal of Biological Chemistry. 290 (40), 24091-24099 (2015).
- Rogers, G. W., Komar, A. A., Merrick, W. C. eIF4A: The godfather of the DEAD box helicases. Progress in Nucleic Acid Research and Molecular Biology. 72, 307-331 (2002).

