डीएनए मेथिलट्रांसफेरेज़ इनहिबिटर के लिए स्क्रीन करने के लिए निरंतर फ्लोरेसेंस-आधारित एंडोन्यूक्लिज़-युग्मित डीएनए मिथाइलेशन परख
Summary
डीएनए मेथिलट्रांसफेरेज़ संभावित कैंसर दवा लक्ष्य हैं। यहां, डीएनए मेथिलट्रांसफेरेज़ निषेध के लिए छोटे अणुओं का आकलन करने के लिए एक प्रोटोकॉल प्रस्तुत किया गया है। यह परख डीएनए मिथाइलेशन को प्रतिदीप्ति पीढ़ी में जोड़ने के लिए एक एंडोन्यूक्लिज़ का उपयोग करती है और वास्तविक समय में एंजाइम गतिविधि की निगरानी करने की अनुमति देती है।
Abstract
डीएनए मिथाइलेशन, एपिजेनेटिक जीन विनियमन का एक रूप, सामान्य सेलुलर फ़ंक्शन के लिए महत्वपूर्ण है। कोशिकाओं में, डीएनए मेथिलट्रांसफेरेज़ (डीएनएमटी) नामक प्रोटीन डीएनए मिथाइलेशन पैटर्न को स्थापित और बनाए रखते हैं। सामान्य डीएनए मिथाइलेशन पैटर्न में परिवर्तन कैंसर के विकास और प्रगति से जुड़ा हुआ है, जिससे डीएनएमटी संभावित कैंसर दवा लक्ष्य बन जाते हैं। इस प्रकार, इन एंजाइमों के नए छोटे अणु अवरोधकों की पहचान और विशेषता बहुत महत्वपूर्ण है। यह पेपर एक प्रोटोकॉल प्रस्तुत करता है जिसका उपयोग डीएनए मेथिलट्रांसफेरेज़ इनहिबिटर के लिए स्क्रीन करने के लिए किया जा सकता है। निरंतर युग्मित कैनेटीक्स परख डीएनए मिथाइलेशन के प्रारंभिक वेगों को संभावित छोटे अणु अवरोधकों की उपस्थिति और अनुपस्थिति में निर्धारित करने की अनुमति देता है। परख प्रतिदीप्ति पीढ़ी के लिए हेमिमिथाइलेटेड डीएनए सब्सट्रेट के मिथाइलेशन को जोड़ने के लिए मिथाइल-संवेदनशील एंडोन्यूक्लिज़ जीएलए आई का उपयोग करता है।
यह निरंतर परख एंजाइम गतिविधि को वास्तविक समय में निगरानी करने की अनुमति देता है। माइक्रोटिटर प्लेटों में छोटी मात्रा में परख का संचालन अभिकर्मकों की लागत को कम करता है। इस परख का उपयोग करते हुए, मनुष्यों में सबसे प्रचुर मात्रा में डीएनएमटी आइसोजाइम, डीएनएमटी 1 के अवरोधकों के लिए एक छोटी उदाहरण स्क्रीन आयोजित की गई थी। अत्यधिक प्रतिस्थापित एंथ्राक्विनोन प्राकृतिक उत्पाद, लैक्केइक एसिड ए, डीएनएएमटी 1 का एक शक्तिशाली, डीएनए-प्रतिस्पर्धी अवरोधक है। यहां, हम परख प्रोटोकॉल का वर्णन करने के लिए दो सांद्रता में तीन संभावित छोटे अणु अवरोधकों की जांच करते हैं – एंथ्राक्विनोन या एंथ्राक्विनोन जैसे अणु एक से तीन प्रतिस्थापन के साथ। प्रारंभिक वेगों का उपयोग प्रत्येक अणु की उपस्थिति में देखी गई प्रतिशत गतिविधि की गणना करने के लिए किया जाता है। जांच किए गए तीन यौगिकों में से एक डीएनएमटी 1 गतिविधि के एकाग्रता-निर्भर निषेध को प्रदर्शित करता है, यह दर्शाता है कि यह डीएनएमटी 1 का एक संभावित अवरोधक है।
Introduction
डीएनए मिथाइलेशन एक महत्वपूर्ण एपिजेनेटिक चिह्न है जो जीन अभिव्यक्ति और क्रोमैटिन संरचना को नियंत्रित करता है। मिथाइलेशन मुख्य रूप से सीपीजी डाइन्यूक्लियोटाइड्स में होता है – साइटोसिन के बाद गुआनोसिन; मिथाइल समूह को साइटोसिन की 5-स्थिति में जोड़ा जाता है। सही डीएनए मिथाइलेशन पैटर्न, और इस प्रकार उचित जीन अभिव्यक्ति, उचित सेलुलर विकास और कार्य के लिए आवश्यक हैं। कई रोग अवस्थाएं सामान्य मिथाइलेशन पैटर्न 1,2,3 में परिवर्तन से जुड़ी हुई हैं। उदाहरण के लिए, कैंसर की शुरुआत और प्रगति और डीएनए मिथाइलेशन पैटर्न में परिवर्तन के बीच एक लिंक है। आमतौर पर, कैंसर कोशिकाएं मेथिलसाइटोसिन के निम्न समग्र स्तर का प्रदर्शन करती हैं, जो जीनोम अस्थिरता में योगदान देती है। इसी समय, जीनोम में मौजूद मिथाइलसाइटोसिन ट्यूमर शमन जीन के प्रमोटर क्षेत्रों में केंद्रित है, जो इन महत्वपूर्ण प्रोटीनों के जीन साइलेंसिंग की ओर जाता है। विशेष रूप से, एपिजेनेटिक परिवर्तन गतिशील और प्रतिवर्ती हैं, ट्यूमरजेनिसिस से जुड़े डीएनए उत्परिवर्तन के विपरीत। इसने एपिजेनेटिक जीन विनियमन में शामिल प्रोटीन को दिलचस्प दवा लक्ष्य 2,4 बना दिया है।
डीएनए मेथिलट्रांसफेरेज़ (डीएनएमटी) डीएनए मिथाइलेशन पैटर्न उत्पन्न करने और बनाए रखने के लिए जिम्मेदार प्रोटीन हैं। तीन उत्प्रेरक रूप से सक्रिय आइसोजाइम, DNMT1, DNMT3a, और DNMT3b, मनुष्यों में मौजूद हैं। विकास और भेदभाव के दौरान, डी नोवो मेथिलट्रांसफेरेज़, डीएनएमटी 3 ए और डीएनएमटी 3 बी, मिथाइलेशन पैटर्न स्थापित करते हैं। दोनों एंजाइम उत्प्रेरक रूप से निष्क्रिय डीएनएमटी 3 एल प्रोटीन को कॉम्प्लेक्स बनाने के लिए बांध सकते हैं जो बढ़ी हुई गतिविधि 1,5 प्रदर्शित करते हैं। कोशिका विभाजन के बाद, बेटी कोशिकाओं में हेमिमिथाइलेटेड डीएनए होता है – डुप्लेक्स के केवल एक स्ट्रैंड में मेथिलसाइटोसिन युक्त डीएनए – क्योंकि नए संश्लेषित डीएनए मिथाइलेशन निशान से रहित होते हैं। डीएनएमटी 1 का प्रमुख कार्य इस हेमिमिथाइलेटेड डीएनए को मिथाइलेटेड करना है, इस प्रकार पूर्ण मिथाइलेशन पैटर्न 1,5 को फिर से स्थापित करना है।
डीएनएमटी गतिविधि और कैंसर के बीच संबंध अच्छी तरह से स्थापित हैं। डीएनएमटी 1 का ओवरएक्प्रेशन, या तो ट्रांसक्रिप्शनल या पोस्ट-ट्रांसलेशनल तंत्र द्वारा, कई सामान्य ऑन्कोजेनिकमार्गों 6,7,8,9 का परिणाम है। हाइपोमॉर्फिक एलील्स का उपयोग करके डीएनएमटी 1 गतिविधि को कम करने के लिए आनुवंशिक दृष्टिकोण के परिणामस्वरूप एपीसी (मिन) चूहों में ट्यूमर गठन में कमी आई है। एंटीसेंस ऑलिगोन्यूक्लियोटाइड्स जो डीएनएमटी 1 को नष्ट करते हैं, सेल संस्कृति और माउस ट्यूमर मॉडल11,12 में नियोप्लासिया को रोकते हैं। इस प्रकार, डीएनएमटी 1 गतिविधि को रोकना एक आशाजनक कैंसर चिकित्सा दृष्टिकोण की तरह लगता है। हालांकि, DNMT3 आइसोजाइम जो भूमिका निभाते हैं, वे इतनी सीधी नहीं हैं। डीएनएमटी 3 ए उत्परिवर्तन तीव्र माइलॉयड ल्यूकेमिया13 और मायलोडीस्प्लास्टिक सिंड्रोम14 में पाए जाते हैं। पहचाने गए उत्परिवर्तनों में से कम से कम एक को एंजाइम15 की डीएनए मिथाइलेशन गतिविधि को कम करने के लिए दिखाया गया है। हालांकि, डीएनएमटी 3 बी स्तन कैंसर16 और कोलोरेक्टल कैंसर17 में अतिरंजित है। कार्सिनोजेनेसिस में विभिन्न डीएनएमटी आइसोजाइम विभिन्न भूमिका निभा रहे हैं, आइसोजाइम-विशिष्ट अवरोधकों की पहचान करना महत्वपूर्ण होगा। न केवल ये यौगिक चिकित्सीय के विकास के लिए उपयोगी होंगे, बल्कि आइसोजाइम-विशिष्ट अवरोधक कैंसर एटियलजि में प्रत्येक डीएनएमटी आइसोजाइम की भूमिका का विश्लेषण करने के लिए एक अमूल्य उपकरण भी होंगे।
साहित्य में कई डीएनएमटी अवरोधकों की सूचना दी गई है। ज्ञात डीएनएमटी अवरोधकों को दो वर्गों में विभाजित किया जा सकता है: न्यूक्लियोसाइड और गैर-न्यूक्लियोसाइड। न्यूक्लियोसाइड इनहिबिटर आमतौर पर साइटिडीन एनालॉग होते हैं। इन यौगिकों को डीएनए में शामिल किया जाता है और सहसंयोजक रूप से डीएनएमटी को फंसाया जाता है। 5-एज़ासाइटिडीन और 5-एज़ा -2′-डीऑक्सीसाइटिडीन को मायलोडीस्प्लास्टिक सिंड्रोम और तीव्र माइलॉयड ल्यूकेमिया 4,18 के उपचार के लिए अनुमोदित किया गया है। इन यौगिकों की उच्च विषाक्तता, कम जैव उपलब्धता और रासायनिक अस्थिरता समस्याएं पेश करती हैं। चल रहे काम न्यूक्लियोसाइड अवरोधकों की अगली पीढ़ी की प्रभावकारिता की जांच कर रहे हैं; एसजीआई -110, 5-एज़ा -2′-डीऑक्सीसाइटिडीन से प्राप्त, एक उदाहरण19,20 है। न्यूक्लियोसाइड इनहिबिटर आइसोजाइम-विशिष्ट नहीं हैं और किसी भी डीएनएमटी आइसोजाइम का सामना करने को निष्क्रिय कर देंगे। इसलिए, न्यूक्लियोसाइड-डीमिथाइलेटिंग एजेंट के साथ उपचार के परिणामस्वरूप सभी डीएनएमटी आइसोजाइम 4,18 की कमी होती है। गैर-न्यूक्लियोसाइड अवरोधकों को उनके निरोधात्मक प्रभावों को बढ़ाने के लिए डीएनए में शामिल करने की आवश्यकता नहीं है। इसके बजाय, ये अणु सीधे डीएनएमटी से जुड़ते हैं, जो आइसोजाइम-विशिष्ट अवरोध की संभावना पेश करते हैं। आज तक कई गैर-न्यूक्लियोसाइड अवरोधकों की खोज की गई है, जिनमें एसजीआई –1027 21, हाइड्रालज़िन22, प्रोकैनामाइड23, आरजी 108 और डेरिवेटिव24, और प्राकृतिक उत्पाद, (−)-एपिगैलोकैटेचिन 3-गैलेट (ईजीसीजी)25 और लैक्केइक एसिड ए26,27 शामिल हैं। आज तक खोजे गए अधिकांश गैर-न्यूक्लियोसाइड अवरोधक आइसोजाइम-चयनात्मक नहीं हैं या एक डीएनएमटी आइसोजाइम के लिए कमजोर प्राथमिकताएं प्रदर्शित करते हैं। इसके अलावा, इन अणुओं की शक्ति में सुधार करने की आवश्यकता है, खासकर कोशिकाओं 4,18 में। इस प्रकार, अधिक शक्तिशाली, आइसोजाइम-चयनात्मक डीएनएमटी अवरोधकों को खोजने या विकसित करने की आवश्यकता है।
DNMTs के नए छोटे अणु अवरोधकों की खोज के लिए एक बाधा पारंपरिक रूप से DNMT गतिविधि28 की जांच करने के लिए उपयोग की जाने वाली श्रमसाध्य परख है। परख आमतौर पर कई चरणों के साथ असंतुलित होते हैं। डीएनएमटी की एंजाइमेटिक गतिविधि अभी भी रेडियोधर्मी एस-एडेनोसिल मेथिओनिन (एसएएम) 29,30,31,32,33,34 का उपयोग करके नियमित रूप से परख की जाती है। डीएनए मिथाइलेशन के लिए गैर-रेडियोधर्मी परख भी विकसित किए गए हैं। उदाहरण के लिए, पाचन उत्पादों को अलग करने के लिए मिथाइल-संवेदनशील प्रतिबंध एंडोन्यूक्लिज़ और वैद्युतकणसंचलन का उपयोग करने वाले परख35,36 वर्णित किए गए हैं। इस प्रकार के असंतुलित, मल्टीस्टेप परख दवा की खोज के लिए आसानी से उत्तरदायी नहीं हैं। 2000 के दशक के मध्य से, उच्च थ्रूपुट के साथ कई डीएनए मिथाइलेशनपरख विकसित किए गए हैं। डीएनएमटी 1 इनहिबिटर37 के लिए स्क्रीन करने के लिए एक शानदार निकटता परख का उपयोग किया गया था। मिथाइल-संवेदनशील प्रतिबंध एंडोन्यूक्लिज़ का उपयोग करने वाली एक और परख का उपयोग डीएनएमटी 3 ए इनहिबिटर 25,38 के लिए स्क्रीन करने के लिए किया गया था। जबकि दोनों परखों ने पारंपरिक डीएनए मिथाइलेशन परख की तुलना में उच्च थ्रूपुट के लिए अनुमति दी, परख को कई चरणों की आवश्यकता होती है और वास्तविक समय में मिथाइलेशन गतिविधि के अवलोकन की अनुमति नहीं देते हैं। हाल ही में, एक निरंतर कैनेटीक्स परख का वर्णन किया गया है जो एनएडीपीएच ऑक्सीकरण39 से जुड़े 340 एनएम पर स्पेक्ट्रोस्कोपिक परिवर्तन के लिए मिथाइलेशन प्रतिक्रिया के एक उत्पाद एस-एडेनोसिलहोमोसिस्टीन (एसएएच) के गठन को जोड़ता है। यह परख एक स्पेक्ट्रोस्कोपिक संकेत उत्पन्न करने के लिए तीन युग्मन एंजाइमों का उपयोग करता है।
हमने एक प्रतिदीप्ति-आधारित एंडोन्यूक्लिज़-युग्मित डीएनए मिथाइलेशन परख विकसित की है जो एक व्यावसायिक रूप से उपलब्ध युग्मन एंजाइम का उपयोग करती है और वास्तविक समय में डेटा उत्पन्न कर सकती है (चित्रा 1)। एक हेयरपिन ऑलिगोन्यूक्लियोटाइड जिसमें तीन मिथाइलसाइटोसिन होते हैं, का उपयोग सब्सट्रेट के रूप में किया जाता है। सब्सट्रेट डीएनए में 5 ‘ अंत पर एक फ्लोरोफोरे और 3 ‘ अंत पर एक बुझाने वाला होता है। हेमिमिथाइलेटेड सीपीजी साइट का मिथाइलेशन एंडोन्यूक्लिज़ जीएलए आई के लिए दरार साइट उत्पन्न करता है – पूरी तरह से मिथाइलेटेड जीसीजीसी। उत्पाद ऑलिगोन्यूक्लियोटाइड का जीएलए आई दरार बुझाने वाले से फ्लोरोफोरे को जारी करता है और वास्तविक समय में प्रतिदीप्ति उत्पन्न करता है। परख का उपयोग डीएनएमटी के किसी भी आइसोफॉर्म की गतिविधि की जांच करने के लिए किया जा सकता है; हालांकि, डीएनएमटी 1 के साथ उच्च गतिविधि देखी जाती है क्योंकि यह आइसोजाइम अधिमानतः हेमिमिथाइलेटेड डीएनए 1,5 को मिथाइलेटेड करता है। यदि डीएनएमटी 1 से ऑटोइनहिबिटरी रेप्लिकेशन फॉसी टारगेटिंग सीक्वेंस (आरएफटीएस) डोमेन को हटा दिया जाता है तो और भी मजबूत गतिविधि देखी जाती है। एन-टर्मिनल नियामक क्षेत्र में पाया जाने वाला यह डोमेन उत्प्रेरक साइट को बांधता है और डीएनए बाइंडिंग को रोकता है। पहले ~ 600 अमीनो एसिड को हटाने से एक कटा हुआ एंजाइम होता है जो पूर्ण लंबाई वाले एंजाइम (के कैट / के एम में ~ 640 गुना वृद्धि) की तुलना मेंकाफी अधिक सक्रियहोता है। एंजाइम का यह सक्रिय रूप, जिसे आरएफटीएस-कमी डीएनएमटी 1 (एमिनो एसिड 621-1616) के रूप में जाना जाता है, इसकी बढ़ी हुई उत्प्रेरक शक्ति के कारण अवरोधकों की आसान पहचान के लिए अनुमति देता है। यह पेपर संभावित छोटे अणु अवरोधकों की जांच के लिए परख में आरएफटीएस-कमी डीएनएमटी 1 का उपयोग करने के लिए एक प्रोटोकॉल प्रस्तुत करता है। एंडोन्यूक्लिज़-युग्मित निरंतर परख का उपयोग करके, प्रारंभिक वेग कुछ छोटे अणुओं की उपस्थिति और अनुपस्थिति में निर्धारित किया जाता है। एकाग्रता-निर्भर डीएनएमटी 1 अवरोध की तलाश के लिए प्रत्येक संभावित अवरोधक की दो सांद्रता में जांच की जाती है। प्रत्येक मामले में छोटे अणुओं की उपस्थिति में देखी गई प्रतिशत गतिविधि की गणना की गई थी।
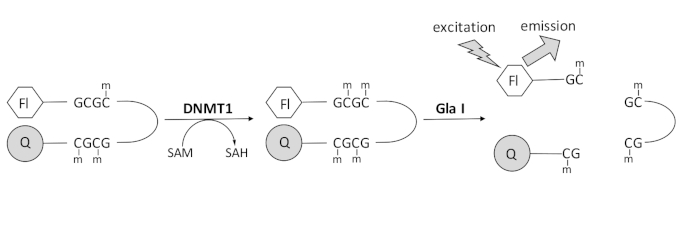
चित्रा 1: डीएनए मिथाइलेशन परख। 5’छोर पर फ्लोरोफोरे और 3′ छोर पर एक बुझाने वाले के साथ एक हेमिमिथाइलेटेड हेयरपिन डीएनए का उपयोग सब्सट्रेट के रूप में किया जाता है। डीएनएमटी 1 एस-एडेनोसिलमेथियोनिन से नॉनमिथाइलेटेड सीपीजी साइट तक मिथाइल समूह के हस्तांतरण को उत्प्रेरित करता है, जिससे एस-एडेनोसिलहोमोसिस्टीन और पूरी तरह से मिथाइलेटेड डीएनए उत्पन्न होता है। डीएनए उत्पाद में एंडोन्यूक्लिज़ जीएलए आई के लिए दरार साइट होती है, जो पूरी तरह से मिथाइलेटेड जीसीजीसी साइटों को छोड़ देती है। उत्पाद डीएनए की दरार 3′ बुझाने वाले से 5 ‘फ्लोरोफोरे जारी करती है, जिससे प्रतिदीप्ति उत्पन्न होती है। संक्षिप्तरूप: एफएल = फ्लोरोफोरे; क्यू = बुझाने वाला; डीएनएमटी 1 = डीएनए मेथिलट्रांसफेरेज़ 1; एसएएम = एस-एडेनोसिलमेथिओनिन; एसएएच = एस-एडेनोसिलहोमोसिस्टीन। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें।
Protocol
Representative Results
Discussion
डीएनए मेथिलट्रांसफेरेज़ के अवरोधकों की पहचान और विशेषता के लिए, एंजाइम की गतिविधि को मापा जाना चाहिए। डीएनए मेथिलट्रांसफेरेज़ गतिविधि की जांच के लिए कई तरीके मौजूद हैं। गतिविधि की निगरानी आमतौर पर र…
Divulgations
The authors have nothing to disclose.
Acknowledgements
लेखक इस काम के समर्थन के लिए बकनेल विश्वविद्यालय और रसायन विज्ञान विभाग को धन्यवाद देते हैं।
Materials
| 96-well Half Area Black Flat Bottom Polystyrene Not Treated Microplate | Corning | 3694 | |
| 96-Well Polystyrene Conical Bottom Plates | ThermoFisher | 249570 | |
| Bovine Serum Albumin | NEB | B9000S | |
| compound 1 | ChemBridge | 5812086 | screening compound; resuspended in DMSO to 10 mM |
| compound 2 | ChemBridge | 6722175 | screening compound; resuspended in DMSO to 10 mM |
| compound 3 | ChemBridge | 5249376 | screening compound; resuspended in DMSO to 10 mM |
| Dithiothreitol | Sigma | D0632 | |
| Gla I | SibEnzyme | E494 | methyl-sensitive endonuclease |
| Glycerol | RPI | G22025 | |
| Magnesium Chloride | Sigma | M0250 | |
| Oligonucleotide (5'-FAM-CCTATGCGmCATCAGTTTTCTGATGmCGmCATAGG-3'-Iowa Black Quencher) | IDT | custom synthesized | internally quenched hairpin DNA (substrate) |
| Potassium Glutamate | Sigma | G1501 | |
| S-adenosylmethionine | Sigma | A4377 | methyl-donating co-factor (substrate) |
| Tris Base | RPI | T60040 |
References
- Jurkowska, R. Z., Jurkowski, T. P., Jeltsch, A. Structure and function of mammalian DNA methyltransferases. Chembiochem. 12 (2), 206-222 (2011).
- Hamidi, T., Singh, A. K., Chen, T. Genetic alterations of DNA methylation machinery in human diseases. Epigenomics. 7 (2), 247-265 (2015).
- Norvil, A. B., Saha, D., Dar, M. S., Gowher, H. Effect of disease-associated germline mutations on structure function relationship of DNA methyltransferases. Genes. 10 (5), 369 (2019).
- Foulks, J. M., et al. Epigenetic drug discovery: targeting DNA methyltransferases. Journal of Biomolecular Screening. 17 (1), 2-17 (2012).
- Goll, M. G., Bestor, T. H. Eukaryotic cytosine methyltransferases. Annual Review of Biochemistry. 74, 481-514 (2005).
- Bigey, P., Ramchandani, S., Theberge, J., Araujo, F. D., Szyf, M. Transcriptional regulation of the human DNA Methyltransferase (dnmt1) gene. Gene. 242 (1-2), 407-418 (2000).
- Detich, N., Ramchandani, S., Szyf, M. A conserved 3′-untranslated element mediates growth regulation of DNA methyltransferase 1 and inhibits its transforming activity. Journal of Biological Chemistry. 276 (27), 24881-24890 (2001).
- MacLeod, A. R., Rouleau, J., Szyf, M. Regulation of DNA methylation by the Ras signaling pathway. Journal of Biological Chemistry. 270 (19), 11327-11337 (1995).
- Slack, A., Cervoni, N., Pinard, M., Szyf, M. DNA methyltransferase is a downstream effector of cellular transformation triggered by simian virus 40 large T antigen. Journal of Biological Chemistry. 274 (15), 10105-10112 (1999).
- Eads, C. A., Nickel, A. E., Laird, P. W. Complete genetic suppression of polyp formation and reduction of CpG-island hypermethylation in Apc(Min/+) Dnmt1-hypomorphic mice. Recherche en cancérologie. 62, 1296-1299 (2002).
- MacLeod, A. R., Szyf, M. Expression of antisense to DNA methyltransferase mRNA induces DNA demethylation and inhibits tumorigenesis. Journal of Biological Chemistry. 270 (14), 8037-8043 (1995).
- Ramchandani, S., MacLeod, A. R., Pinard, M., von Hofe, E., Szyf, M. Inhibition of tumorigenesis by a cytosine-DNA, methyltransferase, antisense oligodeoxynucleotide. Proceedings of the National Academy Sciences of the United States of America. 94 (2), 684-689 (1997).
- Ley, T. J., et al. DNMT3A mutations in acute myeloid leukemia. New England Journal of Medicine. 363, 2424-2433 (2010).
- Walter, M. J., et al. Recurrent DNMT3A mutations in patients with myelodysplastic syndromes. Leukemia. 25 (7), 1153-1158 (2011).
- Russler-Germain, D. A., et al. The R882H DNMT3A mutation associated with AML dominantly inhibits wild-type DNMT3A by blocking its ability to form active tetramers. Cancer Cell. 25 (4), 442-454 (2014).
- Roll, J. D., Rivenbark, A. G., Jones, W. D., Coleman, W. B. DNMT3b overexpression contributes to a hypermethylator phenotype in human breast cancer cell lines. Molecular Cancer. 7, 15 (2008).
- Nosho, K., et al. DNMT3B expression might contribute to CpG island methylator phenotype in colorectal cancer. Clinical Cancer Research. 15 (11), 3663-3671 (2009).
- Erdmann, A., Halby, L., Fahy, J., Arimondo, P. B. Targeting DNA methylation with small molecules: what’s next. Journal of Medicinal Chemistry. 58 (6), 2569-2583 (2015).
- Chuang, J. C., et al. S110, a 5-Aza-2′-deoxycytidine-containing dinucleotide, is an effective DNA methylation inhibitor in vivo and can reduce tumor growth. Molecular Cancer Therapeutics. 9 (5), 1443-1450 (2010).
- Issa, J. J., et al. Safety and tolerability of guadecitabine (SGI-110) in patients with myelodysplastic syndrome and acute myeloid leukaemia: a multicentre, randomised, dose-escalation phase 1 study. Lancet Oncology. 16 (9), 1099-1110 (2015).
- Datta, J., et al. A new class of quinoline-based DNA hypomethylating agents reactivates tumor suppressor genes by blocking DNA methyltransferase 1 activity and inducing its degradation. Recherche en cancérologie. 69 (10), 4277-4285 (2009).
- Zambrano, P., et al. A phase I study of hydralazine to demethylate and reactivate the expression of tumor suppressor genes. BMC Cancer. 5, 44 (2005).
- Lee, B. H., Yegnasubramanian, S., Lin, X., Nelson, W. G. Procainamide is a specific inhibitor of DNA methyltransferase 1. Journal of Biological Chemistry. 280 (49), 40749-40756 (2005).
- Asgatay, S., et al. Synthesis and evaluation of analogues of N-phthaloyl-l-tryptophan (RG108) as inhibitors of DNA methyltransferase 1. Journal of Medicinal Chemstry. 57 (2), 421-434 (2014).
- Ceccaldi, A., et al. C5-DNA methyltransferase inhibitors: from screening to effects on zebrafish embryo development. Chembiochem. 12 (9), 1337-1345 (2011).
- Fagan, R. L., Wu, M., Chédin, F., Brenner, C. An ultrasensitive high throughput screen for DNA methyltransferase 1-targeted molecular probes. PLoS One. 8 (11), 78752 (2013).
- Fagan, R. L., Cryderman, D. E., Kopelovich, L., Wallrath, L. L., Brenner, C. Laccaic acid A is a direct, DNA-competitive inhibitor of DNA methyltransferase 1. Journal of Biological Chemistry. 288 (33), 23858-23867 (2013).
- Eglen, R. M., Reisine, T. Screening for compounds that modulate epigenetic regulation of the transcriptome: an overview. Journal of Biomolecular Screening. 16 (10), 1137-1152 (2011).
- Holz-Schietinger, C., Matje, D. M., Reich, N. O. Mutations in DNA methyltransferase (DNMT3A) observed in acute myeloid leukemia patients disrupt processive methylation. Journal of Biological Chemistry. 287 (37), 30941-30951 (2012).
- Norvil, A. B., et al. Dnmt3b methylates DNA by a noncooperative mechanism, and its activity is unaffected by manipulations at the predicted dimer interface. Biochimie. 57 (29), 4312-4324 (2018).
- Bashtrykov, P., Ragozin, S., Jeltsch, A. Mechanistic details of the DNA recognition by the Dnmt1 DNA methyltransferase. FEBS Letters. 586 (13), 1821-1823 (2012).
- Bashtrykov, P., et al. Targeted mutagenesis results in an activation of DNA methyltransferase 1 and confirms an autoinhibitory role of its RFTS domain. Chembiochem. 15 (5), 743-748 (2014).
- Berkyurek, A. C., et al. The DNA methyltransferase Dnmt1 directly interacts with the SET and RING finger-associated (SRA) domain of the multifunctional protein Uhrf1 to facilitate accession of the catalytic center to hemi-methylated DNA. Journal of Biological Chemistry. 289 (1), 379-386 (2014).
- Kanada, K., Takeshita, K., Suetake, I., Tajima, S., Nakagawa, A. Conserved threonine 1505 in the catalytic domain stabilizes mouse DNA methyltransferase 1. Journal of Biochemistry. 162 (4), 271-278 (2017).
- Bashtrykov, P., et al. Specificity of Dnmt1 for methylation of hemimethylated CpG sites resides in its catalytic domain. Chemistry & Biology. 19 (5), 572-578 (2012).
- Dolen, E. K., McGinnis, J. H., Tavory, R. N., Weiss, J. A., Switzer, R. L. Disease-associated mutations G589A and V590F relieve replication focus targeting sequence-mediated autoinhibition of DNA methyltransferase 1. Biochimie. 58 (51), 5151-5159 (2019).
- Kilgore, J. A., et al. Identification of DNMT1 selective antagonists using a novel scintillation proximity assay. Journal of Biological Chemistry. 288 (27), 19673-19684 (2013).
- Ceccaldi, A., et al. Identification of novel inhibitors of DNA methylation by screening of a chemical library. ACS Chemical Biology. 8 (3), 543-548 (2013).
- Duchin, S., Vershinin, Z., Levy, D., Aharoni, A. A continuous kinetic assay for protein and DNA methyltransferase enzymatic activities. Epigenetics & Chromatin. 8, 56 (2015).
- Syeda, F., et al. The replication focus targeting sequence (RFTS) domain is a DNA-competitive inhibitor of Dnmt1. Journal of Biological Chemistry. 286 (17), 15344-15351 (2011).
- Switzer, R. L., Medrano, J., Reedel, D. A., Weiss, J. Substituted anthraquinones represent a potential scaffold for DNA methyltransferase 1-specific inhibitors. PLoS One. 14 (7), 0219830 (2019).

