Påvisning af neutraliseringsfølsomme epitoper i antigener, der vises på VLP-baserede vacciner (Virus-Like Particle) ved hjælp af en capture assay
Summary
Her præsenterer vi en protokol til at opdage neutralisering epitoper på antigen-displaying virus-lignende partikler (VIP’er). Immunprecipitation af human immundefektvirus (HIV)-afledte VLPs udføres ved hjælp af konvolutglycoproteinerspecifikke monoklonale antistoffer koblet til protein G-konjugerede magnetiske perler. Tilfangetagne VLPs udsættes efterfølgende for SDS-PAGE og Western blot-analyse, der anvender viralt kerneprotein Gag-specifikke antistoffer.
Abstract
Den virus-lignende partikel (VLP) fange assay er en immunprecipitation metode, almindeligvis kendt som en ‘pull-down assay’, der anvendes til at rense og isolere antigen-displaying VLPs. Overflade antigen-specifikke antistoffer er koblet til, og dermed immobiliseret på en solid og uopløselig matrix såsom perler. På grund af deres høje affinitet til målet antigen, disse antistoffer kan fange VIP’er dekoreret med cognate antigen forankret i membranen kuvert af VIP’er. Denne protokol beskriver bindingen af antigenspecifikke antistoffer mod protein A- eller G-konjugeret magnetiske perler. I vores undersøgelse undersøges human immundefektvirus (HIV)-afledte VLPs dannet af det gruppespecifikke antigen (Gag) virale kerneprækursorprotein p55 Gag og viser konvolutglycoproteiner (Env) af HIV. VLPs er fanget ved hjælp af bredt neutraliserende antistoffer (bNAbs) rettet mod neutralisering-følsomme epitoper i Env. VLP-opsamlingsanalysen, der er skitseret her, repræsenterer en følsom og let at udføre metode til at påvise, at (i) VLPs er dekoreret med det respektive målantigen, (ii) overfladeantigen bevarede sin strukturelle integritet, som det fremgår af den epitopspecifikke binding af bNAbs, der anvendes i analysen, og iii) VLPs strukturelle integritet afsløret ved påvisning af Gag-proteiner i en efterfølgende vestlig blotanalyse. Derfor letter udnyttelsen af bNAbs til immunprecipitation en forudsigelse af, om VLP-vacciner vil være i stand til at fremkalde et neutraliserende B-cellerespons hos vaccinerede mennesker. Vi forventer, at denne protokol vil give andre forskere en værdifuld og ligetil eksperimentel tilgang til at undersøge potentielle VLP-baserede vacciner.
Introduction
Viruslignende partikler (VLPs) ligner den oprindelige viruspartikelstruktur, mens de mangler det virale genom, hvilket giver en høj sikkerhedsprofil1,2. VLPs repræsenterer en individuel klasse af vacciner, der i stigende grad udvikles på grund af deres høje immunogenicitet3,4,5,6,7. Dette er især tilfældet for membran-indhyllede VIP’er, der giver mulighed for visning af ikke kun homologe viral overfladeantigener, men også heterologe antigener som tumorantigener8,9,10. Figur 1 giver et eksemplarisk overblik over strukturen af en indhyllet antigen-dekoreret VLP. Under udviklingsprocessen af VLP-baserede vacciner er analyser uundværlige, hvilket gør det muligt at analysere det respektive målantigen, der vises på VLP-overfladen. Sådanne analyser bør være medvirkende til at belyse sammensætningen af en partikelvaccine: (i) Er VLPs dekoreret med det respektive overfladeantigen? ii) Har overfladeantigen bevaret sin oprindelige struktur, som det fremgår af epitopgenkendelse af neutraliserende antistoffer (bNAbs) og iii) kan VLPs strukturelle integritet bekræftes på grund af påvisning af VLP-formationen af virusprotein?
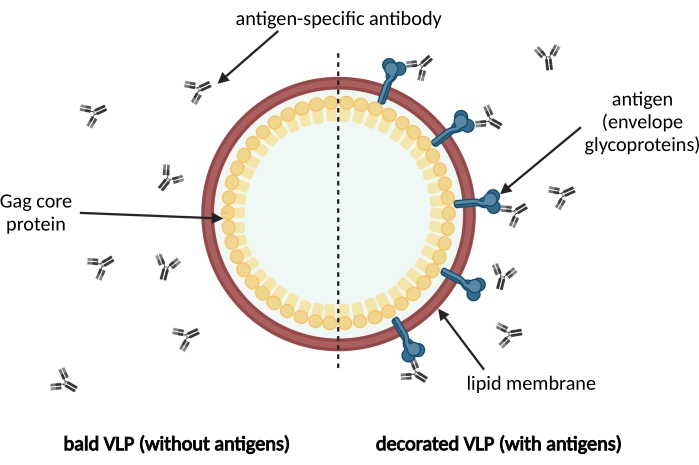
Figur 1: Skematisk illustration af en membrankonvoluterede VLP. VIP’er er dannet af umodne forløber Gag kerneproteiner og omgivet af en lipidmembran afledt af værtscellen. Antigener, f.eks kuvert glycoproteiner, er indarbejdet i lipidmembranen og vises på overfladen af VLP (til højre). Antigenspecifikke antistoffer genkender antigen. Til venstre vises en skaldet VLP uden antigendekoration. Klik her for at se en større version af dette tal.
Især VLPs dannet af viral gruppe-specifikke antigen (Gag) kerne prækursor protein p55 af human immundefekt virus type 1 (HIV-1) foretrækkes stilladser for antigen display i vaccine udvikling som talrige antistoffer, og ELISA kits er tilgængelige, muliggør kvantificering af disse VLPs11,12. HIV-1 kuvert glycoproteiner (Env), nemlig transmembran protein gp41 (gp41-TM) og den opløselige overflade enhed gp120 (gp120-SU), der danner heterodimers, er indarbejdet i membranen kuvert af partikler og er afgørende mål antigener til udvikling af vacciner mod hiv-infektion13,14,15 . Visning af neutraliseringsfølsomme epitoper i disse målantigener er en forudsætning for at fremkalde et bredt neutraliserende antistofrespons hos vacciner. Udover en T-cellerespons rettet mod Gag-proteinerne betragtes dette som en vigtig korrelering af beskyttelse mod hiv-infektion16. Derfor, og ved design og produktion af VIP’er dekoreret med mål antigen kandidater, den efterfølgende analyse af kvaliteten af de viste antigener udgør et kritisk skridt i processen med vaccine udvikling.
Immunprecipitation (IP) er en meget anvendt teknik til påvisning af protein-protein interaktioner og rensning af proteinkomplekser i lille skala17. Barret et al. første gang rapporteret om udviklingen i IP i 1960, men denne metode er blevet konstant yderligere forbedret. IP gør det muligt at fange og isolere et målantigen (bytte) fra en opløsning ved at anvende et antigenspecifikt antistof (agn), der er immobiliseret ved kobling til perler18,19. I denne protokol demonstrerer vi en variation af den klassiske IP-applikation ved hjælp af membrankonvoluterede p55 Gag-dannede VIP’er som bytte og bNAbs, der genkender neutraliseringsfølsomme epitoper i konvolutproteinerne, der vises på overfladen af VIP’erne som agnproteiner. Den vellykkede anvendelse af denne VLP capture assay letter forudsigelsen af, om de testede antigen-positive VLPs vil være i stand til at fremkalde en neutraliserende B-cellerespons hos vaccinerede mennesker. Sådanne immunogene egenskaber af VLP-baserede vaccinekandidater påvises ofte i små dyremodeller20,21,22.
For at vurdere kvaliteten af den nyudviklede VLP-vaccinekandidat er VLP-opsamlingsanalyser med succes blevet anvendt5,23,24. Antallet af offentliggjorte metoder er dog begrænset. Den VLP capture assay præsenteret her starter med immobilisering af Env-specifikke bNAbs på protein G-konjugerede perler, som binder sig til Fc-regionen af pattedyr-afledte antistoffer. Typiske matricer til immobilisering af det foretrukne antistof er agarose eller magnetiske perler. Men magnetiske perler er gunstige for high-throughput applikationer25. I det næste trin, VLPs viser målet antigen er fanget af bNAb-belagt perler. De dannede immunkomplekser bestående af Env-positive VIP’er og immobiliserede bNAbs beriges let ved hjælp af en magnet. De isolerede immunkomplekser er eluted i det sidste trin. Efterfølgende kan VLPs være biokemisk karakteriseret. Her udførte vi vestlig blot-analyse, der anvender p55 Gag virale kerneproteinspecifikke antistoffer for at vise, at det udfældede mål Env-antigener ikke kun husede de neutraliseringsfølsomme epitoper, men blev også vist på Gag-dannede VIP’er. Desuden øger påvisning af den virale kerne Gag proteiner følsomheden af fangst assay, da Gag proteiner er mere rigelige end Env i en VLP. I HIV-1 er Env-proteiner kun til stede ved et enkelt- eller tocifret nummer26, mens mere end 3.500 Gag-molekyler udgør kernen i en partikel27.
Sammenlignet med andre teknikker til undersøgelse af protein-protein interaktioner28,29, VLP capture assay giver en alternativ metode til forskningslaboratorier ikke har adgang til dyre analytiske instrumenter. For eksempel kan transmissionselektronmikroskopisk analyse (TEM), overfladeplasmon resonansspektroskopi (SPR) og nanopartiklersporingsanalyse (NTA) være omkostningskrævende. Fangst assay præsenteret her giver også mulighed for senere underkastelse af fanget antigen-positive VLP prøver til yderligere protein karakterisering, f.eks beskæftiger gel elektroforese, immunblotting, elektronmikroskopi, og massespektrometri (MS), henholdsvis. I betragtning af at den oprindelige struktur af målet antigen er bevaret under VLP fange assay, også udførelsen af en indfødt SIDE og efterfølgende immunblæser teknikker kan udnyttes.
VLP capture assay repræsenterer en nem at bruge og følsom metode til at undersøge udsmykningen af VLPs med mål antigener udsætter neutralisering-følsomme epitoper, og dermed deres nytte som fremtidige vaccine kandidater.
Protocol
Representative Results
Discussion
Forud for VLP-opsamlingsanalysen evalueres dannelsen af VIP’er og udtrykket af målantigen i VLP-producentcellelinjerne. Instrumentale metoder er flowcytometrisk analyse af antigens celleoverfladeudtryk samt antigen- og viral kerneproteinspecifik ELISA af CFSN og pelleterede VLPs.
Kritiske trin i VLP capture assay er belægningen af perlerne med fange antistoffer – her bNAbs – og den efterfølgende fangst af antigen-positive VIP’er af antistof-coatede perler. Vellykket belægning af perlerne med antistoffer afhænger af valget af det konjugerede immunoglobulin (Ig)-bindende protein. Donorarterne samt antistoffernes Ig-klasse afgør, om protein G- eller protein A-konjugerede perler er at foretrække. For de fleste arter og Ig klasser, protein G er ligand valg33. Som et alternativ til protein A /G-konjugerede perler, streptavidin perler til belægning med biotinylerede antistoffer er tilgængelige. Perler kan også være kovalent kombineret med antistoffer.
Opsamlingen af VLPs af antistofbelagte perler afhænger af grundig blanding, tilstrækkelig inkubationstid, antigen overflod og affinitet af fangeantistoffet. Det er vores erfaring, at en grundig blanding af de antistofbelagte perler med VLP-prøverne bedst opnås ved udnyttelse af mængder >500 μL i 1,5 mL rør under rotation i mindst 2 timer ved stuetemperatur eller 4 °C. En anden potentiel forhindring er den for lave mængde VIP’er i stikprøven. For antistoffer, der binder målantigen stærkt, tilførslen af VLP helt ned til 15 ng Gag-protein giver normalt mulighed for let påviselige mængder af de virale kerneproteiner, der anvender vestlig blot-analyse. Antistoffer med lav affinitet kræver dog højere inputmængder, f.eks. 100 ng Gag-protein, for at opnå afgørende resultater (figur 3, bNAb 3).
Nogle overfladeantigener er tilbøjelige til proteaseforringelse. Her anbefaler vi tilsætning af proteasehæmmere til VLP-prøverne og inkubationen ved 4 °C. Ikke-specifik vedhæftning af værtscelleproteiner og VIP’er til de perlebundne antistoffer observeres sjældent og bør udelukkes ved at anvende passende negative kontroller, som vi her viste ved hjælp af mock og skaldede VLP-prøver og isotypekontrolantistoffer. Strategier til reduktion af ikke-specifik binding omfatter udvidede vasketrin og tilsætning af kasein i vaskebufferen34. Desuden kan opsamlingsanalysen også forbedres ved at bestemme det optimale forhold mellem antistof og VLP-mængden, der viser antigen.
I det sidste trin af VLP capture assay, beskriver vi udløsning af immunkomplekser fra perlerne ved kogning i at reducere Laemmli buffer. I løbet af dette trin adskilles VIP’erne, og opsamlingsantistofferne og målantigener adskilles fra perlerne. Især skal donorarten af det primære antistof, der anvendes i den efterfølgende vestlige blot-analyse, afvige fra donoren af capture antistoffet for at undgå utilsigtet påvisning af tilfangetagelsesantistoffet fra de sekundære antidonor IgG HRP-konjugerede antistoffer.
VLP capture assay præsenteret her giver en nem at bruge og følsom metode til at opdage neutralisering-følsomme epitoper i strukturelle intakte mål antigener vises på VLP overflader. Opsamlingsanalysen muliggør dog ikke direkte kvantificering af epitopen. ELISA, der udføres med bNAbs, er afgørende til dette formål og bør gennemføres parallelt, især hvis undersøgte VIP’er er beregnet til at blive anvendt i prækliniske undersøgelser, der anvender dyremodeller35. Dette er afgørende, da mængden af antigen direkte kan korrelere med elicitation af et neutraliserende antistofrespons hos immuniserede dyr, som vist for porcine circovirus type 2 (PCV2) vacciner36.
En ideel vaccine bør resultere i elicitation af bNAbs rettet mod de neutraliseringsfølsomme epitoper på virionoverfladen. Analysen af disse epitoper, især med henvisning til deres fulde strukturelle integritet på partikelvaccineoverfladen, er afgørende for at identificere potentielle vaccinekandidater. Dette er ikke kun tilfældet for hiv-afledte VLPs, men også for mange andre VLP-vacciner under udvikling37. Fremtrædende VLP-baserede vacciner er f.eks. afledt af ikke-indhyllede eller capsid forældrevirus såsom human papillomavirus (HPV). I modsætning til HIV-1 partikler, som kun dannes af et strukturelt kerneprotein, nemlig p55 Gag, og indhyllet af membranen, der stammer fra VLP-producentcellen, består HPV-partikler kun af et eller to strukturelle kerneproteiner38,39. Ligeledes og som præsenteret her for indhyllede VLPs, VLP capture assay kan også være gældende for påvisning af neutralisering-følsomme epitoper af ikke-indhyllede VLPs.
Som et alternativ til opsamlingsanalysen kan VLP-prøverne direkte underkastes native PAGE efterfulgt af vestlig blotanalyse ved hjælp af bNAbs og passende sekundære antistoffer koblet til HRP40. Men og til analyse af HIV Env-dekoreret VLPs, denne analyse er mindre følsom, da kun et lavt antal antigen proteiner pr VLP kan forventes. I modsætning hertil letter opsamlingsanalysen påvisning af de kerneproteiner, der er rigelige med store mængder pr. VLP, for hiv-afledte VLPs udgør mere end 3.500 Gag-proteiner en VLP27. Dette giver mulighed for den meget følsomme indirekte påvisning af epitoper i Env, der vises selv ved lave tætheder på VIP’er.
Antallet af veletablerede metoder til at undersøge neutraliseringsfølsomme epitoper i overfladeantigener af VIP’er er begrænset. Mærkning af antigener, der vises på VLPs, er mulig med epitopspecifikke antistof-fluorophore konjugates og efterfølgende påvisning ved nanopartiklersporingsanalyse (NTA), der muliggør detektion og kvantificering af VLPs. Denne metode er også blevet udviklet og optimeret til exosomer, der præsenterer celleoverflademarkører41. Også overflade plasmon resonans (SPR) spektroskopi giver mulighed for analyse af interaktioner mellem ukonkret neutraliserende antistoffer og cognate epitoper præsenteret på VIP’er. Selvom VLPs ikke er egnede til analyse af højere gennemløb, kan de også mærkes med bNAbs koblet til guldpartikler og efterfølgende transmissionselektronmikroskopisk (TEM)-undersøgelse42.
Konklusionen er, at VLP-opsamlingsanalysen giver nogle betydelige fordele: i) Vurdering af den neutraliseringsfølsomme epitopes strukturelle integritet på VLP’ernes overflade, ii) følsom og indirekte påvisning af antigener, selv når de vises ved lave tætheder på VLPs, og iii) metoden kræver ikke omkostningskrævende analyseudstyr.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet af et tilskud fra det tyske forbundsministerium for uddannelse og forskning, finansieringsprogram Forschung en Fachhochschulen, kontraktnumrene 13FH767IA6 og 13FH242PX6 til JS. Figur 1 og 2 blev oprettet med BioRender.com.
Materials
| 1.5 mL reaction tubes | Eppendorf | ||
| 10x PBS | gibco | 70011044 | |
| 4%–15% Mini-PROTEAN TGX stain-free protein gels | BioRad | 4568085 | |
| Antibodies (bnAbs) | Polymun Scientic | ||
| Isotype control antibody | invitrogen (Thermo Fisher Scientific) | 02-7102 | |
| Chemidoc XRS+ imaging system | BioRad | 1708265 | |
| Chicken anti-rabbit IgG HRP-coupled | Life technologies | A15987 | 1:5000 in TBS-T + 2 % (w/v) powdered milk |
| Dynabeads Protein G Immunoprecipitation Kit | invitrogen (Thermo Fisher Scientific) | 10007D | includes buffers and washing solutions |
| FreeStyle 293-F cells | invitrogen (Thermo Fisher Scientific) | R790-07 | |
| FreeStyle 293 Expression Medium | invitrogen (Thermo Fisher Scientific) | 12338026 | |
| Gel blotting papers | Whatman | GB005 | |
| Glycine | Carl Roth | 0079 | blotting buffer |
| Magnetic separation rack | New England Biolabs | S1509S | for 12 x 1.5 mL or 6 x 1.5 mL tubes |
| Methanol | Carl Roth | 4627 | blotting buffer |
| Mini-PROTEAN Tetra Cell electrophoresis system | BioRad | ||
| Optima XE-90 ultracentrifuge | Beckman Coulter | ||
| PageRuler prestained protein ladder | Thermo Scientific | 26616 | |
| Polyvinylidene fluoride (PVDF) syringe filters, 0.45 µm | Carl Roth | KC89.1 | |
| Powdered milk | Carl Roth | T145 | blocking buffer |
| PVDF transfermembrane, 0.45 µm | Carl Roth | T830.1 | |
| QuickTiter HIV p24 ELISA | Cell Biolabs | VPK-108-H | |
| Rabbit polyclonal to HIV1 p55 + p24 + p17 | abcam | ab63917 | 1:2000 in TBS-T + 2 % (w/v) powdered milk |
| Rotator | Heidolph | REAX2 | |
| ROTI Load 1 (laemmli buffer) | Carl Roth | K929.1 | 4x concentrated reducing protein gel loading buffer |
| ROTIPHORESE 10x SDS-PAGE | Carl Roth | 3060 | |
| Sodium chloride | Carl Roth | 3957 | TBS-T buffer |
| SuperSignal West Pico PLUS chemiluminescent substrate | Thermo Scientific | 34579 | |
| SW28 rotor | Beckman Coulter | ||
| Thermomixer | Cel Media | basic | |
| Trans-Blot Turbo | BioRad | ||
| Trehalose dihydrate | Carl Roth | 8897.2 | |
| TRIS | Carl Roth | 5429 | blotting buffer |
| TRIS hydrochloride | Carl Roth | 9090 | TBS-T buffer |
| Tween-20 | Carl Roth | 9127 | TBS-T buffer |
| Ultra Clear centrifuge tubes | Beckman Coulter | 344058 |
References
- Roldão, A., Mellado, M. C. M., Castilho, L. R., Carrondo, M. J. T., Alves, P. M. Virus-like particles in vaccine development. Expert Review of Vaccines. 9 (10), 1149-1176 (2010).
- Noad, R., Roy, P. Virus-like particles as immunogens. Trends in Microbiology. 11 (9), 438-444 (2003).
- Qian, C., et al. Recent progress on the versatility of virus-like particles. Vaccines. 8 (1), 139 (2020).
- Zabel, F., Kündig, T. M., Bachmann, M. F. Virus-induced humoral immunity: On how B cell responses are initiated. Current Opinion in Virology. 3 (3), 357-362 (2013).
- Garg, H., Mehmetoglu-Gurbuz, T., Joshi, A. Virus Like Particles (VLP) as multivalent vaccine candidate against Chikungunya, Japanese Encephalitis, Yellow Fever and Zika Virus. Scientific Reports. 10 (1), 4017 (2020).
- Hodgins, B., Pillet, S., Landry, N., Ward, B. J. A plant-derived VLP influenza vaccine elicits a balanced immune response even in very old mice with co-morbidities. PLoS ONE. 14 (1), 0210009 (2019).
- Lai, C. C., et al. Process development for pandemic influenza VLP vaccine production using a baculovirus expression system. Journal of Biological Engineering. 13, 78 (2019).
- Caldeira, J. C., Perrine, M., Pericle, F., Cavallo, F. Virus-like particles as an immunogenic platform for cancer vaccines. Viruses. 12 (5), 488 (2020).
- Nika, L., et al. An HER2-displaying virus-like particle vaccine protects from challenge with mammary carcinoma cells in a mouse model. Vaccines. 7 (2), 41 (2019).
- Mohsen, M. O., Zha, L., Cabral-Miranda, G., Bachmann, M. F. Major findings and recent advances in virus-like particle (VLP)-based vaccines. Seminars in Immunology. 34, 123-132 (2017).
- Fontana, D., Garay, E., Cevera, L., Kratje, R., Prieto, C., Gòdia, F. Chimeric VLPs based on hiv-1 gag and a fusion rabies glycoprotein induce specific antibodies against rabies and foot-and-mouth disease virus. Vaccines. 9 (3), 251 (2021).
- Cervera, L., et al. Production of HIV-1-based virus-like particles for vaccination: achievements and limits. Applied Microbiology and Biotechnology. 103 (18), 7367-7384 (2019).
- Gonelli, C. A., King, H. A. D., Mackenzie, C., Sonza, S., Center, R. J., Purcell, D. F. J. Immunogenicity of HIV-1-based virus-like particles with increased incorporation and stability of membrane-bound env. Vaccines. 9 (3), 1-36 (2021).
- Trkola, A. HIV not as simple as one, two, three. Nature. 568, 321-322 (2019).
- Berman, P. W., et al. Protection of chimpanzees from infection by HIV-1 after vaccination with recombinant glycoprotein gp120 but not gp160. Nature. 345 (6276), 622-625 (1990).
- Barouch, D. H. Challenges in the development of an HIV-1 vaccine. Nature. 455 (7213), 613-619 (2008).
- DeCaprio, J., Kohl, T. O. Immunoprecipitation. Cold Spring Harbor Protocols. 2020 (11), 449-461 (2020).
- Barret, B., Wood, P. A., Volwiler, W. Quantitation of gamma globulins in human serum by immunoprecipitation. Journal of Laboratory and Clinical Medicine. 55, 605-615 (1960).
- Kaboord, B., Perr, M. Isolation of proteins and protein complexes by immunoprecipitation. Methods in Molecular Biology. 424, 349-364 (2008).
- Lee, S. H., Chu, K. B., Kang, H. J., Quan, F. S. Virus-like particles containing multiple antigenic proteins of Toxoplasma gondii induce memory T cell and B cell responses. PLoS ONE. 14 (8), 0220865 (2019).
- Lee, Y. T., et al. Intranasal vaccination with M2e5x virus-like particles induces humoral and cellular immune responses conferring cross-protection against heterosubtypic influenza viruses. PLoS ONE. 13 (1), 0190868 (2018).
- Wang, J., et al. Large-scale manufacture of VP2 VLP vaccine against porcine parvovirus in Escherichia coli with high-density fermentation. Applied Microbiology and Biotechnology. 104 (9), 3847-3857 (2020).
- Swenson, D. L., et al. Generation of Marburg virus-like particles by co-expression of glycoprotein and matrix protein. FEMS Immunology and Medical Microbiology. 40 (1), 27-31 (2004).
- Latham, T., Galarza, J. M. Formation of wild-type and chimeric influenza virus-like particles following simultaneous expression of only four structural proteins. Journal of Virology. 75 (13), 6154-6165 (2001).
- Doyle, J., Ray, M., Ouyang, A., Benton, B., Bell, P. A. Abstract 4877: High throughput proteomic applications using protein A/G magnetic beads. Association for Cancer Research (AACR) 102nd Annual Meeting. 20, 4877 (2011).
- Zhu, P., et al. Electron tomography analysis of envelope glycoprotein trimers on HIV and simian immunodeficiency virus virions. Proceedings of the National Academy of Sciences of the United States of America. 100 (26), 15812-15817 (2003).
- Lavado-García, J., Jorge, I., Boix-Besora, A., Vázquez, J., Gòdia, F., Cervera, L. Characterization of HIV-1 virus-like particles and determination of Gag stoichiometry for different production platforms. Biotechnology and Bioengineering. 118 (7), 2660-2675 (2021).
- Miura, K. An overview of current methods to confirm protein-protein interactions. Protein & Peptide Letters. 25 (8), 728-733 (2018).
- Rao, V. S., Srinivas, K., Sujini, G. N., Kumar, G. N. Advances in molecular techniques to study diversity. Plant Biotechnology, Volume 1: Principles, Techniques, and Applications. , 341-365 (2017).
- Rosengarten, J. F., Schatz, S., Wolf, T., Barbe, S., Stitz, J. Components of a HIV-1 vaccine mediate virus-like particle (VLP)-formation and display of envelope proteins exposing broadly neutralizing epitopes. Virology. , 41-48 (2022).
- JoVE, Grundlegende Methoden in der Zell- und Molekularbiologie. Separating Protein with SDS-PAGE. JoVE Science Education Database. , (2021).
- Eslami, A., Lujan, J. Western blotting: sample preparation to detection. Journal of Visualized Experiments: JoVE. (44), e2359 (2010).
- Sheng, S., Kong, F. Separation of antigens and antibodies by immunoaffinity chromatography. Pharmaceutical Biology. 50 (8), 1038-1044 (2012).
- Guzzo, C., et al. Virion incorporation of integrin 47 facilitates HIV-1 infection and intestinal homing. Science Immunology. 2 (11), (2017).
- Wei, M., et al. Bacteria expressed hepatitis E virus capsid proteins maintain virion-like epitopes. Vaccine. 32 (24), 2859-2865 (2014).
- Jin, J., Park, C., Cho, S. H., Chung, J. The level of decoy epitope in PCV2 vaccine affects the neutralizing activity of sera in the immunized animals. Biochemical and Biophysical Research Communications. 496 (3), 846-851 (2018).
- Zhang, X., et al. Lessons learned from successful human vaccines: Delineating key epitopes by dissecting the capsid proteins. Human Vaccines and Immunotherapeutics. 11 (5), 1277-1292 (2015).
- DiGiuseppe, S., Bienkowska-Haba, M., Guion, L. G. M., Keiffer, T. R., Sapp, M. Human papillomavirus major capsid protein L1 remains associated with the incoming viral genome throughout the entry process. Journal of Virology. 91 (16), 00537 (2017).
- Wang, J. W., Roden, R. B. S. L2, the minor capsid protein of papillomavirus. Virology. 445 (1-2), 175-186 (2013).
- Binley, J. M., et al. Profiling the specificity of neutralizing antibodies in a large panel of plasmas from patients chronically infected with human immunodeficiency virus type 1 subtypes B and C. Journal of Virology. 82 (23), 11651-11668 (2008).
- Thane, K. E., Davis, A. M., Hoffman, A. M. Improved methods for fluorescent labeling and detection of single extracellular vesicles using nanoparticle tracking analysis. Scientific Reports. 9 (1), 12295 (2019).
- Mulder, A. M., et al. Toolbox for non-intrusive structural and functional analysis of recombinant VLP based vaccines: A case study with hepatitis B vaccine. PLoS ONE. 7 (4), 0033235 (2012).

