Vereenvoudigde, high-throughput analyse van eencellige contractiliteit met behulp van microgepatterde elastomeren
Summary
Dit werk presenteert een flexibel protocol voor het gebruik van fluorescerend gelabelde elastomeer contracteerbare oppervlakken (FLECS) -technologie in microwell-formaat voor vereenvoudigde, hands-off kwantificering van contractiele krachten met één cel op basis van gevisualiseerde verplaatsingen van fluorescerende eiwitmicropatronen.
Abstract
Cellulaire contractiele krachtgeneratie is een fundamentele eigenschap die door vrijwel alle cellen wordt gedeeld. Deze contractiele krachten zijn cruciaal voor een goede ontwikkeling, functioneren op zowel cellulair als weefselniveau en reguleren de mechanische systemen in het lichaam. Talrijke biologische processen zijn krachtafhankelijk, waaronder beweeglijkheid, adhesie en deling van afzonderlijke cellen, evenals samentrekking en ontspanning van organen zoals het hart, de blaas, de longen, de darmen en de baarmoeder. Gezien het belang ervan bij het handhaven van een goede fysiologische functie, kan cellulaire contractiliteit ook ziekteprocessen stimuleren wanneer ze overdreven of verstoord zijn. Astma, hypertensie, vroeggeboorte, fibrotische littekens en onderactieve blaas zijn allemaal voorbeelden van mechanisch aangedreven ziekteprocessen die mogelijk kunnen worden verlicht met de juiste controle van cellulaire contractiele kracht. Hier presenteren we een uitgebreid protocol voor het gebruik van een nieuwe op microplaat gebaseerde contractiliteitstesttechnologie die bekend staat als fluorescerend gelabelde elastomeer contracteerbare oppervlakken (FLECS), die vereenvoudigde en intuïtieve analyse van contractiliteit met één cel op een enorm geschaalde manier biedt. Hierin bieden we een stapsgewijs protocol voor het verkrijgen van twee zespunts dosis-responscurven die de effecten beschrijven van twee contractiele remmers op de samentrekking van primaire menselijke blaas gladde spiercellen in een eenvoudige procedure met behulp van slechts een enkele FLECS-testmicroplaat, om de juiste techniek aan gebruikers van de methode te demonstreren. Met behulp van FLECS-technologie krijgen alle onderzoekers met biologische basislaboratoria en fluorescerende microscopiesystemen toegang tot het bestuderen van dit fundamentele maar moeilijk te kwantificeren functionele celfenotype, waardoor de toetredingsdrempel op het gebied van krachtbiologie en fenotypische screening van contractiele celkracht effectief wordt verlaagd.
Introduction
Celgegenereerde mechanische krachten zijn essentieel voor een goede werking in verschillende organen in het lichaam, zoals de darmen, blaas, hart en anderen. Deze organen moeten stabiele patronen van celcontractie en ontspanning genereren om de interne homeostatische toestand te behouden. Abnormale gladde spiercel (SMC) contractie kan leiden tot het begin van verschillende aandoeningen, waaronder bijvoorbeeld intestinale dysmotiliteit, gekenmerkt door abnormale patronen van intestinale gladde spiercontractie1, evenals de urologische omstandigheden van overactieve2 of onderactieve blaas3. Binnen de luchtwegen kunnen SMC’s die onregelmatige contractiepatronen vertonen astmatische hyperresponsiviteit4 veroorzaken, waardoor de luchtwegen mogelijk strakker worden en de luchtstroom van zuurstof in de longen afneemt. Een andere wijdverspreide fysieke aandoening, hypertensie, wordt veroorzaakt door fluctuaties in de gladde spiercontractie in bloedvaten5. Het is duidelijk dat contractiele mechanismen in cellen en weefsels kunnen leiden tot ziekten die behandelingsopties vereisen. Omdat deze aandoeningen onmiskenbaar voortkomen uit het disfunctionele contractiele gedrag van cellen, wordt het logisch en noodzakelijk om de celcontractiele functie zelf te meten bij het screenen van potentiële kandidaat-geneesmiddelen.
Erkennend de behoefte aan hulpmiddelen om cellulaire contractiele kracht te bestuderen, zijn verschillende kwantitatieve contractie-assaymethoden ontwikkeld door academische onderzoekers, waaronder tractiekrachtmicroscopie (TFM)6, micropatterned TFM7, zwevende gel-assays8 en elastomeer micropost-assays9. Deze technologieën zijn in tal van studies gebruikt in single-dish formaat en multi-well-plate formaat en zijn zelfs voorgesteld voor driedimensionale krachtmetingen10,11,12,13,14. Hoewel deze technologieën baanbrekend onderzoek binnen het uitgestrekte veld van celkrachtbiologie mogelijk hebben gemaakt, zijn ze allemaal grotendeels beperkt tot laboratoria met specifieke mogelijkheden en middelen, in het bijzonder: vermogen om TFM-substraten te fabriceren, vermogen om complexe en niet-intuïtieve algoritmen op de juiste manier toe te passen om TFM-verplaatsingskaarten op te lossen, en relatief nauwkeurige microscopiesystemen die beelden kunnen registreren die zijn genomen voor en na monsterverwijdering van het podium (voor celdissociatie). Voor een ongetrainde onderzoeker kan de toegangsdrempel om deze methoden te gebruiken dus vrij hoog zijn, gezien de uitgebreide reeks vereisten om deze technologieën toe te passen. Bovendien kan de beeldvormingsresolutie die vereist is voor veel bestaande technologieën (40x doelstellingen of meer) de experimentele doorvoer aanzienlijk beperken, terwijl bulkmeettechnologieën bijdragen van uitschieters kunnen maskeren en de ontdekking van mildere contractiele verschillen kunnen voorkomen. Voor zover de auteurs weten, is alleen de low-throughput en semi-kwantitatieve floating gel assay-benadering voldoende gerijpt om beschikbaar te komen voor onderzoekers (zie figuur 1).
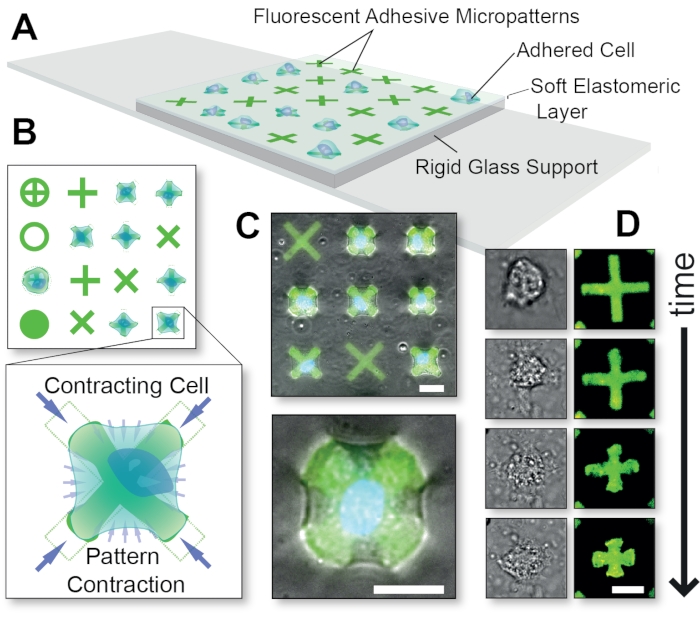
Figuur 1: Algemeen schema van de FLECS-technologiemethode. (A) Cellen worden gehecht aan klevende eiwitmicropatronen die covalent zijn ingebed in een dunne elastomeerlaag ondersteund door glas. (B) Bovenaanzicht van verschillende mogelijke micropatronen en een opblazen van een cel die een ‘X’-vormig micropatroon samentrekt. (C) Overlay van fluorescerende micropatronen en fasecontrastbeelden van een samentrekkende cel. (D) Tijdsverloopbeelden van een enkele samentrekkende cel. Schaalbalken = 25 μm. Dit cijfer werd aangepast met toestemming van Pushkarsky et al15. Klik hier om een grotere versie van deze figuur te bekijken.
Naar aanleiding van recente ontwikkelingen in de microtechnologie ontwikkelden de auteurs een op microplaten gebaseerde technologie die kwantitatieve metingen van eencellige contractie in honderdduizenden cellen mogelijk maakt, FLECS genaamd (fluorescerend gelabelde elastomeer contracteerbare oppervlakken)15,16,17,18,19,20 , als alternatief voor TFM. In deze benadering worden fluorescerende eiwitmicropatronen ingebed in zachte films die vervormen en krimpen wanneer cellen er tractiekrachten op uitoefenen, op een intuïtieve en meetbare manier. Belangrijk is dat de eiwitmicropatronen de celpositie, vorm en verspreidingsgebied beperken, wat leidt tot uniforme testomstandigheden. Deze maken eenvoudige metingen mogelijk op basis van alleen hun dimensionale veranderingen, die ruimtelijk zeer nauwkeurig worden opgelost, zelfs in 4x vergrotingsbeelden. De methode omvat een browsergebaseerde beeldanalysemodule en maakt een eenvoudige analyse van contractiele celkracht mogelijk zonder dat delicate hanteringsprocedures of registratie van fiduciaire markers nodig zijn, zodat deze door elke onderzoeker met een basiscelkweekfaciliteit en een eenvoudige fluorescerende microscoop met lage vergroting moet kunnen worden bediend (figuur 2 ). Deze technologie, die schapklaar en commercieel beschikbaar is, is ontworpen met de eindgebruiker in gedachten en heeft tot doel de toegangsdrempel voor elke laboratoriumwetenschapper om cellulaire krachtbiologie te bestuderen te verminderen.

Figuur 2: Schema van het 24-well plaatformaat voor de eencellige contractiliteitstest. Dit formaat werd gebruikt in de experimenten die hierin worden beschreven en weergegeven in het videogedeelte van het artikel. Schaalbalken = 25 μm. Klik hier om een grotere versie van deze figuur te bekijken.
In dit werk presenteren we een protocol voor het toepassen van het 24 well plate-formaat van het FLECS Technology-platform om de effecten van krachtmodulerende geneesmiddelen op cellulaire contractiliteit in primaire blaas gladde spiercellen te kwantificeren. Dit algemene protocol kan indien nodig worden aangepast en aangepast om rekening te houden met verschillende andere tijdschalen, celtypen en behandelingsomstandigheden van belang, en worden geschaald om andere vragen in de krachtbiologie te beantwoorden.
Protocol
Representative Results
Discussion
Deze vereenvoudigde methode om kwantitatief contractie te meten in honderdduizenden cellen tegelijk onder verschillende behandelingsomstandigheden en met behulp van alleen standaard microscopie-instrumenten biedt een toegankelijk alternatief voor traditionele TFM voor onderzoekers om cellulaire krachtbiologie te bestuderen. Omdat de gepresenteerde technologie een visuele weergave van celcontractie biedt door veranderingen in regelmatig gevormde fluorescerende micropatronen te analyseren, wordt de omvang van de contractie geproduceerd door een bepaalde cel intuïtief begrepen – hoe kleiner het micropattern, hoe groter de contractiele kracht die door de cel wordt uitgeoefend.
Met name door controle te bieden over factoren zoals vorm, verspreidingsgebied en adhesiemolecuul waaruit de micropatronen bestaan (alle factoren waarvan bekend is dat ze de celcontractiliteit reguleren22,23,24), elimineert de gepresenteerde technologie systematisch aanvullende variabelen die interpretaties van celcontractiestudies kunnen verstoren.
In dit experiment werd 10 kPa stijfheid gebruikt in de gel en een 70 μm (diagonale lengte) micropattern bestaande uit type IV collageen. Naast deze parameters kan het lijmmolecuul worden vervangen door verschillende collageen, fibronectine, gelatine en andere extracellulaire matrix (ECM). De stijfheid van de gel kan worden afgestemd tot 0,1 kPa en tot in het MPa-bereik. De micropatterngeometrie kan de novo worden ontworpen om elke vorm te zijn met een minimale functiegrootte van ~ 5 μm. Deze parameters zijn ontkoppeld en kunnen onafhankelijk worden geoptimaliseerd voor een bepaalde biologische context.
Deze technologie is uitgebreid gevalideerd om compatibel te zijn met zeer klevende en contractiele celtypen van een mesenchymaal fenotype, waaronder verschillende gladde spierceltypen (primaire menselijke blaas, intestinale, tracheale, bronchiale, baarmoeder, aorta en arteriële), mesenchymale stamcellen en hun gedifferentieerde nakomelingen, verschillende fibroblasten (pulmonale, dermale en cardiale), myofibroblasten en endotheelcellen. Bovendien zullen van monocyten afgeleide macrofagen ook een grote meetbare fagocytische kracht op de micropatrionen produceren, vooral als het micropatroon bestaat uit een bekend opsonine. Verschillende kankerlijnen kunnen ook worden getest met behulp van de methode.
De methode kan enkele uitdagingen opleveren voor het gebruik met cellen die relatief klein zijn, zoals T-cellen en neutrofielen, of celtypen met een overwegend epitheelfenotype. De belangrijkste reden hiervoor is dat de methode vertrouwt op sterke hechting en volledige verspreiding van cellen over het micropatroon om het meetbare contractiele signaal te genereren. Cellen die zwak binden, aan elkaar binden of zich niet volledig verspreiden, produceren geen meetbare contractiele signalen. Dit gedrag, dat relatief zeldzaam is, kan worden verzacht door de grootte van het micropatroon aan te passen om kleiner te zijn, of door alternatieve kleefmoleculen in de micropatronen te gebruiken die de hechting en verspreiding in die cellen beter bevorderen.
Gebruikers van de technologie moeten zorgvuldig verschillende mogelijke celkweekmediumformuleringen evalueren voor hun specifieke celtype van belang, omdat verschillende componenten, groeifactoren, serumspiegels en pH-gevoeligheden variabel gedrag in verschillende cellen kunnen veroorzaken. Optimalisatie van het protocol moet voorafgaan aan het schalen van experimentele workflows en mediacomponenten moeten altijd vers, steriel en consistent zijn met eerdere batches.
Uiteindelijk, als eencellige resolutie niet nodig is voor de doelen van een gebruiker, of als het doelceltype een minimale verspreidingscapaciteit heeft, kan traditionele TFM even geschikt of meer geschikt zijn voor dergelijke experimenten. Het doel en de hoop van de auteurs is dat deze tool een extra mogelijkheid biedt voor celbiologen om cellulaire contractie te bestuderen, met name in de context van geautomatiseerde fenotypische medicijnschermen met hoge doorvoer.
Specifiek voor toekomstig gebruik in medicijnschermen kunnen platen met een hogere doorvoer worden gebruikt, zoals een 384-well FLECS-plaat. In dergelijke platen kunnen 4x objectieven op veel microscopen een hele put in hun gezichtsveld vastleggen, zodat alle cellulaire contractiele reacties worden vastgelegd. Door gebruik te maken van een high-throughput imaging-systeem kan een volledige 384-well plaat in ongeveer 5 minuten worden afgebeeld, waardoor dit systeem aanzienlijk sneller is dan andere opties en daarom geschikt is voor het ontdekken van fenotypische geneesmiddelen met hoge doorvoer. Inderdaad, de auteurs voeren routinematig wekelijkse medicijnschermen uit op ~ 50 384-wellplates (in totaal meer dan 19.000 putten) met behulp van automatisering.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Het laboratoriumwerk werd uitgevoerd met de steun van de UCLA Molecular Shared Screening Resource (MSSR), waar Forcyte onderzoeksactiviteiten sponsort, en de Magnify Incubator aan het California NanoSystems Institute (CNSI), waar Forcyte Biotechnologies, Inc. een gevestigd bedrijf is. De auteurs verlenen op verzoek toegang tot de Biodock.ai FLECS-analysemodule aan alle academische onderzoekers. L.H. en I.P. hebben evenveel bijgedragen aan dit werk.
Materials
| Bladder smooth muscle cell culture | Sciencell | #4310 | |
| Blebbistatin | Sigma-Aldrich | B0560 | |
| Cell culture media | Thermofisher | 11765054 | Ham's F12 medium supplemented with 10% FBS and 1% p/s |
| Cell strainer | Fisher Scientific | 7201432 | |
| Conical Tube | Fisher Scientific | 05-539-13 | |
| Culture flask | Fisher Scientific | FB012941 | |
| Cytochalasin D | Sigma-Aldrich | C8273 | |
| DMSO (Dimethyl sulfoxide) | Fisher Scientific | D1284 | |
| Eppendorf tubes | Fisher Scientific | 05-402-31 | |
| Fluorescent microscope | Molecular Devices | ImageXpress Confocal | |
| Forcyte-manufactured 24-well plate | Forcyte Biotechnologies | 24-HC4R-X1-QB12 | |
| Hoescht 3342 Live Nuclear Stain | Thermofisher | 62249 | |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | BP39920 |
References
- Ohama, T., Hori, M., Ozaki, H. Mechanism of abnormal intestinal motility in inflammatory bowel disease: How smooth muscle contraction is reduced. Journal of Smooth Muscle Research. 43 (2), 43-54 (2007).
- Peyronnet, B., et al. A comprehensive review of overactive bladder pathophysiology: On the way to tailored treatment. European Urology. 75 (6), 988-1000 (2019).
- Aldamanhori, R., Osman, N. I., Chapple, C. R. Underactive bladder: Pathophysiology and clinical significance. Asian Journal of Urology. 5 (1), 17-21 (2018).
- Sanderson, M. J., Delmotte, P., Bai, Y., Perez-Zogbhi, J. F. Regulation of airway smooth muscle cell contractility by Ca2+ signaling and sensitivity. Proceedings of the American Thoracic Society. 5 (1), 23-31 (2008).
- Brozovich, F. V., et al. Mechanisms of vascular smooth muscle contraction and the basis for pharmacologic treatment of smooth muscle disorders. Pharmacological Reviews. 68 (2), 476-532 (2016).
- Munevar, S., Wang, Y., Dembo, M. Traction force microscopy of migrating normal and H-ras transformed 3T3 fibroblasts. Biophysical Journal. 80 (4), 1744-1757 (2001).
- Tseng, Q., et al. A new micropatterning method of soft substrates reveals that different tumorigenic signals can promote or reduce cell contraction levels. Lab on a Chip. 11 (13), 2231-2240 (2011).
- Bell, E., Ivarsson, B., Merrill, C. Production of a tissue-like structure by contraction of collagen lattices by human fibroblasts of different proliferative potential in vitro. Proceedings of the National Academy of Sciences. 76 (3), 1274-1278 (1979).
- Tan, J. L., et al. Cells lying on a bed of microneedles: an approach to isolate mechanical force. Proceedings of the National Academy of Sciences. 100 (4), 1484-1489 (2003).
- Rokhzan, R., et al. high-throughput measurements of cell contraction and endothelial barrier function. Laboratory Investigation. 99 (1), 138-145 (2019).
- Park, C. Y., et al. High-throughput screening for modulators of cellular contractile force. Integrative Biology. 7 (10), 1318-1324 (2015).
- Kaylan, K. B., Kourouklis, A. P., Underhill, G. H. A high-throughput cell microarray platform for correlative analysis of cell differentiation and traction forces. Journal of Visualized Experiments. (121), e55362 (2017).
- Huang, Y., et al. Traction force microscopy with optimized regularization and automated Bayesian parameter selection for comparing cells. Scientific Reports. 9, 539 (2019).
- Franck, C., Maskarinec, S. A., Tirrell, D. A., Ravichandran, G. Three-dimensional traction force microscopy: A new tool for quantifying cell-matrix interactions. PLOS ONE. 6, 17833 (2011).
- Pushkarsky, I., et al. Elastomeric sensor surfaces for high-throughput single-cell force cytometry. Nature Biomedical Engineering. 2 (2), 124-137 (2018).
- Pushkarsky, I. FLECS technology for high-throughput single-cell force biology and screening. ASSAY and Drug Development Technologies. 16 (1), 7-11 (2017).
- Koziol-White, C. J., et al. Inhibition of PI3K promotes dilation of human small airways in a rho kinase-dependent manner. British Journal of Pharmacology. 173 (18), 2726-2738 (2016).
- Orfanos, S., et al. Obesity increases airway smooth muscle responses to contractile agonists. American Journal of Physiology-Lung Cellular and Molecular Physiology. 315 (5), 673-681 (2018).
- Tseng, P., Pushkarsky, I., Carlo, D. D. Metallization and biopatterning on ultra-flexible substrates via dextran sacrificial layers. PLOS ONE. 9, 106091 (2014).
- Yoo, E. J., et al. Gα12 facilitates shortening in human airway smooth muscle by modulating phosphoinositide 3-kinase-mediated activation in a RhoA-dependent manner. British Journal of Pharmacology. 174 (4), 4383-4395 (2017).
- MacGlashan, D., Vilariño, N. Polymerization of actin does not regulate desensitization in human basophils. Journal of Leukocyte Biology. 85 (4), 627-637 (2009).
- Hocking, D. C., Sottile, J., Langenbach, K. J. Stimulation of integrin-mediated cell contractility by fibronectin polymerization. Journal of Biological Chemistry. 275 (14), 10673-10682 (2000).
- Tolić-Nørrelykke, I. M., Wang, N. Traction in smooth muscle cells varies with cell spreading. Journal of Biomechanics. 38 (7), 1405-1412 (2005).
- Ye, G. J. C., et al. The contractile strength of vascular smooth muscle myocytes is shape dependent. Integrative Biology. 6 (2), 152-163 (2014).

