Design til implementeringsundersøgelse til udvikling og patientvalidering af papirbaseret tåholdskontaktdiagnostik
Summary
Adgang til decentraliseret, billig og højkapacitetsdiagnostik, der kan implementeres i samfundet til decentraliseret test, er afgørende for at bekæmpe globale sundhedskriser. Dette manuskript beskriver, hvordan man opbygger papirbaseret diagnostik til virale RNA-sekvenser, der kan detekteres med en bærbar optisk læser.
Abstract
Adgang til molekylær diagnostik med lav byrde, der kan anvendes i samfundet til testning, bliver stadig vigtigere og har meningsfulde bredere konsekvenser for samfundets trivsel og økonomisk stabilitet. I de senere år er der opstået flere nye isotermiske diagnostiske modaliteter for at imødekomme behovet for hurtig, billig molekylær diagnostik. Vi har bidraget til denne indsats gennem udvikling og patientvalidering af tåholdskontaktbaseret diagnostik, herunder diagnostik for myggebårne Zika- og chikungunya-vira, som gav ydeevne, der kan sammenlignes med guldstandard reverse transkription-kvantitativ polymerasekædereaktion (RT-qPCR) baserede assays. Disse diagnoser er billige at udvikle og fremstille, og de har potentialet til at levere diagnostisk kapacitet til miljøer med lav ressource. Her giver protokollen alle de trin, der er nødvendige for udviklingen af et switch-baseret assay til påvisning af Zika-virus. Artiklen tager læserne gennem den trinvise diagnostiske udviklingsproces. For det første tjener genomiske sekvenser af Zika-virus som input til beregningsdesign af kandidatkontakter ved hjælp af open source-software. Dernæst vises samlingen af sensorerne til empirisk screening med syntetiske RNA-sekvenser og optimering af diagnostisk følsomhed. Når valideringen er færdig, udføres valideringen med patientprøver parallelt med RT-qPCR og en specialbygget optisk læser, PLUM. Dette arbejde giver en teknisk køreplan for forskere til udvikling af billige toehold switch-baserede sensorer til applikationer inden for menneskers sundhed, landbrug og miljøovervågning.
Introduction
RT-qPCR er forblevet guldstandardteknologien til klinisk diagnostik på grund af dens fremragende følsomhed og specificitet. Selvom metoden er meget robust, afhænger den af dyrt, specialiseret udstyr og reagenser, der kræver temperaturstyret distribution og opbevaring. Dette udgør betydelige hindringer for tilgængeligheden af kvalitetsdiagnostik globalt, især i tider med sygdomsudbrud og i regioner, hvor adgangen til veludstyrede laboratorier er begrænset 1,2. Dette blev observeret under udbruddet af zikavirus i Brasilien i 2015/2016. Med kun fem centraliserede laboratorier til rådighed til at levere RT-qPCR-test resulterede betydelige flaskehalse, hvilket begrænsede adgangen til diagnostik. Dette var især udfordrende for personer i bynære omgivelser, som blev hårdere ramt af udbruddet 3,4. I et forsøg på at forbedre adgangen til diagnostik viser protokollen en platform, der er udviklet med potentiale til at levere decentraliseret, billig og høj kapacitetsdiagnostik i indstillinger med lav ressource. Som en del af dette blev der etableret en diagnostisk opdagelsesrørledning, der koblede isotermisk amplifikation og syntetiske RNA-switchbaserede sensorer med papirbaserede cellefrie ekspressionssystemer 5,6.
Cellefri proteinsyntese (CFPS) systemer, især E. coli-baserede cellefrie systemer, er en attraktiv platform for en bred vifte af biosensing applikationer fra miljøovervågning 7,8 til patogendiagnostik 5,6,9,10,11,12 . CFPS-systemer omfatter de komponenter, der er nødvendige for transkription og oversættelse, og har betydelige fordele i forhold til helcellebiosensorer. Specifikt er sensing ikke begrænset af en cellevæg, og generelt er de modulære i design, biosikre, billige og kan frysetørres til bærbar brug. Evnen til at frysetørre genkredsløbsbaserede reaktioner på substrater som papir eller tekstiler muliggør transport, langtidsopbevaring ved stuetemperatur5 og endda inkorporering i bærbar teknologi13.
Tidligere arbejde har vist, at E. coli-cellefrie systemer kan bruges til at detektere adskillige analytter, for eksempel giftige metaller såsom kviksølv, antibiotika såsom tetracyclin7,14, hormonforstyrrende kemikalier15,16, biomarkører såsom hippursyre 17, patogenassocierede quorum sensing molekyler 9,18 og ulovlige stoffer såsom kokain 17 og gammahydroxybutyrat (GHB)19 . Til sekvensspecifik påvisning af nukleinsyrer har strategier for det meste været afhængige af brugen af switchbaserede biosensorer koblet til isotermiske forstærkningsteknikker. Toehold-switche er syntetiske riboregulatorer (også kaldet simpelthen ‘switches’ i resten af teksten), der indeholder en hårnålestruktur, der blokerer downstream-oversættelse ved at binde det ribosomale bindingssted (RBS) og startkodonen. Ved interaktion med deres måludløser-RNA lettes hårnålestrukturen, og efterfølgende oversættelse af en reporter åben læseramme aktiveres20.
Isotermisk forstærkning kan også anvendes som molekylær diagnostik21; disse metoder er imidlertid tilbøjelige til uspecifik forstærkning, hvilket kan reducere testens specificitet og dermed nøjagtighed til under RT-qPCR 22. I det arbejde, der er rapporteret her, blev isotermisk forstærkning opstrøms for de switchbaserede sensorer brugt til at tilvejebringe kombineret signalforstærkning, der muliggør klinisk relevant påvisning af nukleinsyrer (femtomolar til attomolær ). Denne parring af de to metoder giver også to sekvensspecifikke kontrolpunkter, der i kombination giver et højt niveau af specificitet. Ved hjælp af denne tilgang har tidligere arbejde vist påvisning af vira som Zika6, Ebola5, Norovirus10 samt patogene bakterier som C. difficile23 og antibiotikaresistent Tyfus12. Senest er cellefrie tåholdsafbrydere blevet demonstreret til SARS-CoV-2-detektion i bestræbelserne på at give tilgængelig diagnostik til COVID-19-pandemien11,12,13.
Følgende protokol skitserer udviklingen og valideringen af cellefri, papirbaseret syntetisk tåholdskontaktassay til påvisning af Zika-virus, fra in silico biosensordesign gennem monterings- og optimeringstrin til feltvalidering med patientprøver. Protokollen begynder med in silico-design af RNA-tåholdskontaktbaserede sensorer og isotermiske amplifikationsprimere, der er specifikke for Zika-viralt RNA. Selvom der findes adskillige isotermiske amplifikationsmetoder, blev der her demonstreret anvendelse af nukleinsyresekvensbaseret amplifikation (NASBA) for at øge koncentrationen af viralt RNA-mål, der var til stede i reaktionen, hvilket muliggjorde klinisk signifikant følsomhed. Praktisk set har isotermiske forstærkningsmetoder fordelen ved at fungere ved en konstant temperatur, hvilket eliminerer behovet for specialudstyr, såsom termiske cyklister, som generelt er begrænset til centraliserede steder.
Dernæst beskrives processen med at samle de syntetiske tåholdskontaktsensorer med reporterkodningssekvenser gennem overlapningsforlængelse PCR og screening af de syntetiske tåholdskontaktsensorer for optimal ydeevne i cellefrie systemer ved hjælp af syntetisk RNA. Til dette sæt Zika-virussensorer har vi valgt lacZ-genet , der koder for β-galactosidase-enzymet, som er i stand til at spalte et kolorimetrisk substrat, chlorphenolrød-β-D-galactopyranosid (CPRG), for at producere en gul til lilla farveændring, der kan detekteres af øjet eller med en pladelæser. Når de mest effektive syntetiske switche er identificeret, beskrives processen til screening af primere for nukleinsyresekvensbaseret isotermisk amplifikation af den tilsvarende målsekvens ved hjælp af syntetisk RNA for at finde sæt, der giver den bedste følsomhed.
Endelig valideres diagnoseplatformens ydeevne på stedet i Latinamerika (figur 1). For at bestemme den kliniske diagnostiske nøjagtighed udføres det papirbaserede cellefrie assay ved hjælp af Zika-virusprøver fra patienter; parallelt udføres et guldstandard RT-qPCR-assay til sammenligning. For at overvåge kolorimetriske cellefrie assays muliggør vi kvantificering på stedet af resultater i regioner, hvor termiske cyklister ikke er tilgængelige. Den håndsamlede pladelæser kaldet Portable, Low-Cost, User-friendly, Multimodal (PLUM; i det følgende benævnt bærbar pladelæser) introduceres også her24. Oprindeligt udviklet som en ledsagende enhed til cellefri syntetisk tåholdskontaktdiagnostik, tilbyder den bærbare pladelæser en tilgængelig måde at inkubere og læse resultater på en måde med høj kapacitet, hvilket giver integreret, computervisionsbaseret softwareanalyse til brugerne.
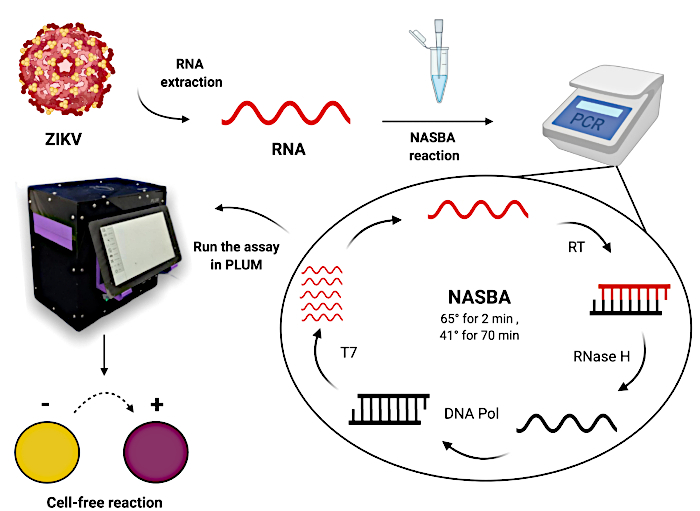
Figur 1: Arbejdsgang for test af patientprøver ved hjælp af papirbaserede cellefrie tåholdskontaktreaktioner. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Det kombinerede papirbaserede system, der er beskrevet her, kan bringe klinisk relevant molekylær diagnostik med ydeevne, der funktionelt kan sammenlignes med RT-qPCR, til behovspunktet6. Det er vigtigt, at tilgængeligheden af diagnostik på stedet for fjernindstillinger kan reducere tiden til resultater fra dage til timer. Ved at fremhæve programmerbarheden af denne tilgang kan den rørledning, der er beskrevet, bruges til at detektere stort set ethvert patogenmål. Vi har parret de molekylære værktøjer med en specialbygget bærbar pladelæser, som er kompakt og kompatibel med batteridrift (8-9 timer) og giver indbygget dataanalyse for at muliggøre distribuerede applikationer. I andet arbejde har vi valideret den kombinerede hardware- og Zika-virusdiagnostiske platform med 268 patientprøver parallelt med RT-qPCR og fundet en diagnostisk nøjagtighed på 98.5%24. Samlet set er vores mål at muliggøre teknologioverførsel af denne platform til forskere, så den kan genbruges og forbedres af samfundet for at imødekomme uopfyldte diagnostiske behov.
Design af in silico toehold switch-designprocessen er blevet integreret og automatiseret i en pipeline, der kan opdeles i tre faser. Den første fase genererer en pulje af tåholdskontaktdesign, der hybridiserer til målsekvensen i en nukleotidtrin. Den anden fase undersøger den sekundære struktur og tilgængeligheden af tåholdskontakten og eliminerer sensorer med for tidlige stopkodoner i rammen. En scoringsfunktion, der tager højde for flere faktorer (f.eks. defektniveau for tåholdskontakten, tilgængelighed af toehold-switch og tilgængelighed på målstedet) implementeres derefter for at vælge design af toptåholdskontakt baseret på samlede scorer. I den sidste fase genereres en liste over sekvenser for de øverste tåholdskontaktdesign og deres tilsvarende måludløsere. De øverste sensorsekvenser skal screenes for specificitet mod det humane transkriptom og nært beslægtede virale genomer ved hjælp af NCBI/Primer-BLAST25. Det er også bedste praksis at screene sensormålstederne for sekvensbevarelse i Zika-virusgenomet for at sikre, at sensorerne giver bred og robust detektion. Flere versioner af toehold switch design software er blevet udviklet, og designalgoritmen giver brugerne mulighed for at generere to versioner, enten serie A 6 eller serie B toehold switche6. I denne artikel har fokus været på serie B tåhold switch design.
Efter kommerciel DNA-syntese kan tåholdskontakterne hurtigt samles og derefter testes ved at udføre en indledende skærm mod en syntetisk måludløsersekvens, der svarer til korte regioner (200-300 nt) af målgenomet. Til screening af ydeevnen af tåholdskontaktbaserede sensorer er det ideelt at tilføje målsekvensen i form af RNA. I denne artikel er de trin, der kræves for at tilføje in vitro transkriberet trigger RNA, blevet skitseret. Men hvis de er tilgængelige, kan genomskabeloner i fuld længde såsom kvantificerede virale RNA-ekstrakter eller kommercielle syntetiske RNA-genomer eller -standarder anvendes. Brug af RNA-genomer i fuld længde til indledende toehold-switch-screening er gavnligt, da det kan informere om, hvorvidt yderligere faktorer, såsom RNA-sekundær struktur, vil påvirke sensorens ydeevne. For at optimere ON/OFF-forholdet mellem kandidatkontakter kan tåholdskontaktens DNA titreres til den cellefrie reaktion. Dette trin kan også tjene til at identificere højtydende tåholdsafbrydere (foldforstærkning eller højt ON / OFF-forhold) og udelade utætte tåholdskontakter (højt signal i fravær af mål-RNA’et) fra nedstrøms karakteriseringstrin.
For at forbedre detektionsgrænsen for de bedst præsterende tåholdsswitchkandidater bruges NASBA til at øge klinisk relevante koncentrationer af mål Zika viralt RNA til et niveau, der kan detekteres ved tåholdskontakter6. Forskellige kombinationer af fremadgående og omvendte primersæt screenes for at bestemme de bedste NASBA-primer- og tåholdskontaktkombinationer for at muliggøre detektion ved klinisk relevante koncentrationer. Når et ideelt primersæt og tåholdskontaktkombination er blevet identificeret, føres analysen videre til klinisk validering. Det er vigtigt at bemærke, at tåholdskontakten og NASBA-screeningsfaserne kan være arbejds- og ressourceintensive, og derfor er testudvikling bedst egnet til velfinansierede forskningssteder. Selvom vi ikke har anvendt procesautomatisering, er det sandsynligt, at dette kan fremskynde den iterative design-, build- og testcyklus32. Heldigvis kan behandlingstiden fra sensordesign og test til implementering være bemærkelsesværdig kort (mindre end en uge), hvilket gør denne strategi ideel til tidskritiske situationer, såsom epidemiudbrud6.
Selv efter at en biosensor med klinisk relevant følsomhed er udviklet, er der tekniske udfordringer, der skal løses. Da denne protokol involverer manuel betjening og er en flertrinsprocedure, er der risiko for krydskontaminering mellem prøver. Vi gør vores bedste for at mindske denne risiko gennem omhyggelig laboratoriepraksis. I et nyligt klinisk forsøg med 268 patientprøver stødte vi ikke på nogen forureningsproblemer; Det er dog en vigtig overvejelse24. Med dette i tankerne forbliver protokollen et laboratorieassay og kræver en dygtig bruger med kommando af korrekte molekylærbiologiske teknikker. En yderligere overvejelse for implementering er RNA-isolering fra patientprøver. Her beskriver vi RNA-isolering ved hjælp af kolonnebaserede nukleinsyreekstraktionssæt. I andet arbejde har vi imidlertid demonstreret en effektiv og enkel kogende lysemetode (95 °C i 2 min) til behandling af patientprøver med lav belastning6. Denne strategi eliminerer næsten omkostningerne forbundet med RNA-ekstraktion og undgår brugen af kolonnebaserede nukleinsyreekstraktionssæt, hvilket kan udgøre en logistisk udfordring i lavressourceindstillinger eller forsyningskædeproblemer under kriser, såsom COVID-19-pandemien33.
Som vi har set under COVID-19-pandemien, kan de instrumenter, der bruges til at udføre RT-qPCR, i sig selv tjene som en flaskehals og begrænse patienternes adgang til test. Denne faktor, som også stort set er økonomisk, fører til en centraliseret testtilstand, der kan begrænse diagnostisk adgang. For eksempel var der under Zika-udbruddet i 2015/2016 kun fem nationale referencelaboratorier tilgængelige i Brasilien, hvilket forårsagede forsinkelser i patienttest. Uden at overveje den potentielle fordel ved stordriftsfordele er de nuværende vareomkostninger for den bærbare pladelæser ~ $ 500 USD, som selvom de øges fem gange for at tage højde for arbejdskraft og kommerciel margin, stadig giver et overkommeligt instrument. Dette kan sammenlignes godt med RT-qPCR-instrumenter, der varierer i omkostninger fra $ 15,000 – $ 90,000 USD34. Desuden er den anslåede pris pr. test for det cellefrie assay i Latinamerika omkring $ 5.48 USD, mens omkostningerne pr. Test af RT-qPCR i Brasilien var ~ $ 10-11 USD på tidspunktet for Zika-udbruddet36. Ud over omkostningerne ved udstyr har den bærbare pladelæser et lille fodaftryk (20 cm3), automatisk analyse, dataupload til skyen via internettet og kan køres på batteristrøm. Disse funktioner udvider dramatisk de potentielle indstillinger, hvor test kan implementeres, og udvider samtidig patientpopulationen, der kan betjenes.
Til dato er de mest almindelige kommercielle E. coli CFPS-platforme S30- og PURE-systemerne37; En vigtig overvejelse for at forbedre adgangen til diagnostik i lav- og mellemindkomstlande er imidlertid den begrænsede indenlandske tilgængelighed af disse reagenser. Et vigtigt skridt i retning af at løse denne udfordring er udviklingen af lokal CFPS-produktion. Federici-laboratoriet har for nylig gjort betydelige fremskridt i retning af at udvikle en ikke-kommerciel platform til implementering af toehold-switch-baserede sensorer i lysatbaserede cellefrie systemer og nåede en 2.7 fM LOD med Zika-virus RNA14. Denne præstation gør det ikke kun muligt at fremstille reagenserne i brugslandet, hvilket undgår importtold og forsinkelser, men lønomkostningerne skaleres også til lokale satser, og dermed kan de samlede omkostninger sænkes betydeligt. I det arbejde, der blev skitseret af Federici-gruppen, var omkostningerne ved at producere CFPS-ekspressionsreaktionen (5 μL) i Chile 6,9 cent (USD) 35,38, hvilket gav et dobbelt incitament (forbedret logistik og omkostninger) til implementering af lysatbaserede systemer 35,38.
Placeringen af RT-qPCR-sammenlignelig test i distribuerede diagnostiske netværk kan medføre betydelige fordele i forhold til nuværende praksis, der er afhængig af transport af prøver til centraliserede RT-qPCR-faciliteter. I bynære omgivelser, hvor zika-tilfælde var koncentreret, forsinker den fysiske afstand mellem en patient og diagnosefaciliteten diagnosen og øger risikoen for, at resultaterne ikke når patienten på et klinisk relevant tidspunkt. Det er vores håb, at det arbejde, der præsenteres her, kan bidrage til, at forskersamfundet gennem overførsel af viden kan skabe decentraliserede bioteknologier og bærbar hardware til menneskers sundhed, landbrug og miljøovervågning.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Forfatterne takker alle medlemmer af Green, Pardee og Pena labs samt alle medforfattere af tidligere manuskripter vedrørende det arbejde, der er beskrevet i dette manuskript. S.J.R.d.S. blev støttet af et ph.d.-stipendium sponsoreret af Foundation for Science and Technology of Pernambuco (FACEPE), Brasilien, referencenummer IBPG-1321-2.12/18, og understøttes i øjeblikket af et postdoc-stipendium sponsoreret af University of Toronto, Canada. P.B. støttes af William Knapp Buckley Award fra Det Farmaceutiske Fakultet, University of Toronto. M.K. blev støttet af Precision Medicine Initiative (PRiME) ved University of Toronto interne stipendienummer PRMF2019-002. Dette arbejde blev støttet af midler til KP fra Canada Research Chairs Program (filer 950-231075 og 950-233107), University of Toronto’s Major Research Project Management Fund, CIHR Foundation Grant Program (201610FDN-375469) og til L.P, A.A.G. og K.P gennem CIHR / IDRC Team Grant: Canada-Latin / America-Caribbean Zika Virus Program (FRN: 149783) samt af midler til K.P. fra Canadas International Development Research Centre (bevilling 109434-001) gennem den canadiske 2019 Novel Coronavirus (COVID-19) Rapid Research Funding Opportunity. Dette arbejde blev også støttet af midler til A.A.G. fra en Arizona Biomedical Research Commission New Investigator Award (ADHS16-162400), Gates Foundation (OPP1160667), en NIH Director’s New Innovator Award (1DP2GM126892), en NIH R21-pris (1R21AI136571-01A1) til K.P./A.A.G og et Alfred P. Sloan Fellowship (FG-2017-9108). Figur 1 blev oprettet med Biorender.com under akademisk licens til K.P.
Materials
| 384 well plate covers – aluminum | Sarstedt | 95.1995 | Used to cover the 384-well plates before they are inserted into the PLUM reader |
| 384 well plate covers – transparent | Sarstedt | 95.1994 | Used to cover the 384-well plates before they are inserted into the BioTek plate reader |
| 384 well plates | VWR | CA11006-180 | 2 mm paper-based diagnostics are placed into the wells of these plates for quantification |
| Agarose | BioShop Canada | AGA001.500 | Gel electrophoresis |
| BSA | BioShop Canada | ALB001.500 | Blocking agent for the Whatman filter paper |
| Cell free reactions | New England Biolabs | E6800L | PURExpress |
| CPRG | Roche | 10884308001 | Chlorophenol red-b-D-galactopyranoside |
| Disposable Sterile Biopsy Punches | Integra Miltex | 23233-31 | Used to create 2 mm paper discs that fit into a 384-well plate |
| DNAse I | Thermo Scientific | K2981 | Digests template DNA following incubation of the in vitro transcription reaction |
| DNAse I Kit | Thermo Scientific | 74104 | DNase I Kit For removing template DNA from IVT RNA |
| dNTPs | New England Biolabs | N0446S | Used for PCRs |
| electrophoresis system | Bio-Rad | 1704487 | Used to run the agarose gels |
| Gel imaging station | Bio-Rad | 1708265 | ChemiDoc XRS+ Imaging System |
| IVT kit | New England Biolabs | E2040S | Used for in vitro transcribing template (trigger) RNA for switch screening |
| Nanodrop One | Thermo Scientific | ND-ONE-W | Used for determining nucleic acid concentrations |
| NASBA kit | Life Sciences Advanced Technologies | NWK-1 | Isothermal amplification reaction components |
| Nuclease free H20 | invitrogen | 10977015 | Added to reaction mixes |
| PAGE electrophoresis system | Biorad | 1658001FC | Used to cast and run polyacrylamide gels |
| pCOLADuet-LacZ DNA | Addgene | 75006 | https://www.addgene.org/75006/ |
| Phusion polymerase/reactioin buffer | New England Biolabs | M0530L | Used for PCRs |
| Plate reader | BioTek | BioTek NEO2 | Multi Mode Plate Reader, Synergy Neo2 |
| Primers | Integrated DNA Technologies | Custom oligo synthesis | |
| Q5 polymerase/reaction buffer | New England Biolabs | M0491L | Used for PCRs |
| Qiagen PCR Puriifcation Kit | QIAGEN | 27106 | QIAprep Spin Miniprep Kit |
| RNA loading dye | New England Biolabs | B0363S | 2X RNA loading dye |
| RNA Purification Kit | QIAGEN | EN0521 | QIAamp Viral RNA extraction kit |
| RNase inhibitor | New England Biolabs | M0314S | Used to prevent contamination of RNases A, B, and C |
| RT-qPCR kit | QIAGEN | 208352 | QuantiNova Probe RT-PCR Kit |
| SYBR Gold | Invitrogen S11494 | S11494 | PAGE gel stain for nucleic acids |
| TAE Buffer | BioShop Canada | TAE222.4 | Gel electrophoresis buffer |
| Thermal Cycler | Applied Biosystems | 4484073 | Used for temperature cycling and incubating reactions |
| Whatman 42 filter paper | GE Healthcare | 1442-042 | Used to imbed molecular components for paper-based diagnostics |
References
- Urdea, M., et al. Requirements for high impact diagnostics in the developing world. Nature. 444, 73-79 (2006).
- Yager, P., Domingo, G. J., Gerdes, J. Point-of-care diagnostics for global health. Annual Review of Biomedical Engineering. 10, 107-144 (2008).
- Faria, N. R., et al. Mobile real-time surveillance of Zika virus in Brazil. Genome Medicine. 8 (1), 97 (2016).
- Faria, N. R., et al. Zika virus in the Americas: Early epidemiological and genetic findings. Science. 352 (6283), 345-349 (2016).
- Pardee, K., et al. Paper-based synthetic gene networks. Cell. 159 (4), 940-954 (2014).
- Pardee, K., et al. Rapid, low-cost detection of Zika virus using programmable biomolecular components. Cell. 165 (5), 1255-1266 (2016).
- Duyen, T. T. M., et al. Paper-based colorimetric biosensor for antibiotics inhibiting bacterial protein synthesis. Journal of Bioscience and Bioengineering. 123 (1), 96-100 (2017).
- Jung, J. K., et al. Cell-free biosensors for rapid detection of water contaminants. Nature Biotechnology. 38 (12), 1451-1459 (2020).
- Yang, Y. H., et al. Cell-free Escherichia coli-based system to screen for quorum-sensing molecules interacting with quorum receptor proteins of streptomyces coelicolor. Applied and Environmental Microbiology. 75 (19), 6367 (2009).
- Ma, D., Shen, L., Wu, K., Diehnelt, C. W., Green, A. A. Low-cost detection of norovirus using paper-based cell-free systems and synbody-based viral enrichment. Synthetic Biology. 3 (1), (2018).
- Park, S., Lee, J. W. Detection of coronaviruses using RNA toehold switch sensors. International Journal of Molecular Sciences. 22 (4), 1-13 (2021).
- Amalfitano, E., et al. A glucose meter interface for point-of-care gene circuit-based diagnostics. Nature Communications. 12 (1), 1-10 (2021).
- Nguyen, P. Q., et al. Wearable materials with embedded synthetic biology sensors for biomolecule detection. Nature Biotechnology. 39 (11), 1366-1374 (2021).
- Pellinen, T., Huovinen, T., Karp, M. A cell-free biosensor for the detection of transcriptional inducers using firefly luciferase as a reporter. Analytical Biochemistry. 330 (1), 52-57 (2004).
- Salehi, A. S. M., et al. Cell-free protein synthesis approach to biosensing hTRβ-specific endocrine disruptors. Analytical Chemistry. 89 (6), 3395-3401 (2017).
- Salehi, A. S. M., et al. Biosensing estrogenic endocrine disruptors in human blood and urine: A RAPID cell-free protein synthesis approach. Toxicology and Applied Pharmacology. 345, 19-25 (2018).
- Voyvodic, P. L., et al. Plug-and-play metabolic transducers expand the chemical detection space of cell-free biosensors. Nature Communications. 10 (1), 1-8 (2019).
- Yang, W. C., Patel, K. G., Wong, H. E., Swartz, J. R. Simplifying and streamlining Escherichia coli-based cell-free protein synthesis. Biotechnology Progress. 28 (2), 413-420 (2012).
- Gräwe, A., et al. A paper-based, cell-free biosensor system for the detection of heavy metals and date rape drugs. PLOS One. 14 (3), 0210940 (2019).
- Green, A. A., Silver, P. A., Collins, J. J., Yin, P. Toehold Switches: De-Novo-Designed Regulators of Gene Expression. Cell. 159 (4), 925-939 (2014).
- Craw, P., Balachandran, W. Isothermal nucleic acid amplification technologies for point-of-care diagnostics: a critical review. Lab on a Chip. 12 (14), 2469-2486 (2012).
- Zyrina, N. V., Antipova, V. N. Nonspecific Synthesis in the Reactions of Isothermal Nucleic Acid Amplification. Biochemistry (Moscow). 86 (7), 887-897 (2021).
- Takahashi, M. K., et al. A low-cost paper-based synthetic biology platform for analyzing gut microbiota and host biomarkers. Nature Communications. 9 (1), 1-12 (2018).
- Karlikow, M., et al. Field validation of the performance of paper-based tests for the detection of the Zika and chikungunya viruses in serum samples. Nature Biomedical Engineering. 6 (3), 246-256 (2022).
- Agarwala, R., et al. Database resources of the National Center for Biotechnology Information. Nucleic Acids Research. 44 (1), 7-19 (2016).
- . BLAST: Basic Local Alignment Search Tool Available from: https://blast.ncbi.nlm.nih.gov/Blast.cgi (2022)
- Deiman, B., Van Aarle, P., Sillekens, P. Characteristics and applications of nucleic acid sequence-based amplification (NASBA). Molecular Biotechnology. 20 (2), 163-179 (2002).
- Zadeh, J. N., Wolfe, B. R., Pierce, N. A. Nucleic acid sequence design via efficient ensemble defect optimization. Journal of Computational Chemistry. 32 (3), 439-452 (2011).
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. DNA Gel Electrophoresis. Journal of Visualized Experiments: JoVE. , (2021).
- Lanciotti, R. S., et al. Genetic and serologic properties of Zika virus associated with an epidemic, Yap State, Micronesia, 2007. Emerging Infectious Diseases. 14 (8), 1232 (2008).
- Walsh, D. I., et al. Standardizing automated DNA assembly: Best practices, metrics, and protocols using robots. SLAS Technology. 24 (3), 282 (2019).
- Silva, S. J. R., de Magalhães, J. J. F., de Pena, L. Simultaneous circulation of DENV, CHIKV, ZIKV and SARS-CoV-2 in Brazil: An inconvenient truth. One Health. 12, 100205 (2021).
- Kimura, S., Fujinaga, K., Sekiya, T. PCR machine. Tanpakushitsu kakusan koso. Protein, Nucleic Acid, Enzyme. 41 (5), 514-517 (1996).
- Arce, A., et al. Decentralizing cell-free RNA sensing with the use of low-cost cell extracts. Frontiers in Bioengineering and Biotechnology. 9, 727584 (2021).
- Silva, S. J. R., Pardee, K., Balasuriya, U. B. R., Pena, L. Development and validation of a one-step reverse transcription loop-mediated isothermal amplification (RT-LAMP) for rapid detection of ZIKV in patient samples from Brazil. Scientific Reports. 11 (1), 1-13 (2021).
- Shimizu, Y. Cell-free translation reconstituted with purified components. Nature Biotechnology. 19 (8), 751-755 (2001).
- Lavickova, B., Maerkl, S. J. A simple, robust, and low-cost method to produce the PURE cell-free system. ACS Synthetic Biology. 8 (2), 455-462 (2019).

