जीवित ज़ेबराफ़िश लार्वा में आंखों को हटाने के लिए इनरवेशन-निर्भर विकास और दृश्य प्रणाली के विकास की जांच करने के लिए
Summary
लेख बताता है कि जीवित ज़ेब्राफ़िश लार्वा से आंखों को शल्य चिकित्सा से कैसे हटाया जाए, यह जांचने की दिशा में पहला कदम है कि रेटिना इनपुट ऑप्टिक टेक्टम विकास और विकास को कैसे प्रभावित करता है। इसके अलावा, लेख लार्वा एनेस्थेटाइजेशन, फिक्सेशन और मस्तिष्क विच्छेदन के बारे में जानकारी प्रदान करता है, जिसके बाद इम्यूनोहिस्टोकेमिस्ट्री और कॉन्फोकल इमेजिंग होती है।
Abstract
ज़ेब्राफ़िश उल्लेखनीय जीवन भर की वृद्धि और पुनर्योजी क्षमताओं का प्रदर्शन करते हैं। उदाहरण के लिए, भ्रूणजनन के दौरान स्थापित विशेष स्टेम सेल niches आंख और मस्तिष्क दोनों में पूरे दृश्य प्रणाली के निरंतर विकास का समर्थन करते हैं। रेटिना और ऑप्टिक टेकटम के बीच समन्वित विकास सटीक रेटिनोटोपिक मैपिंग सुनिश्चित करता है क्योंकि आंखों और मस्तिष्क में नए न्यूरॉन्स जोड़े जाते हैं। यह पता लगाने के लिए कि क्या रेटिना अक्षतंतु टेक्टल स्टेम और पूर्वज सेल व्यवहार जैसे अस्तित्व, प्रसार और / या भेदभाव को विनियमित करने के लिए महत्वपूर्ण जानकारी प्रदान करते हैं, एक ही जानवर के भीतर और जानवरों में इनरवेटेड और डिनेरवेटेड टेक्टल लोब की तुलना करने में सक्षम होना आवश्यक है।
ऑप्टिक टेक्टम के अवलोकन के बाद जीवित लार्वा ज़ेबराफ़िश से एक आंख को सर्जिकल रूप से हटाने से इस लक्ष्य को प्राप्त किया जाता है। साथ का वीडियो दर्शाता है कि लार्वा को एनेस्थेटिक कैसे किया जाए, इलेक्ट्रोलाइटिक रूप से टंगस्टन सुइयों को तेज किया जाए, और एक आंख को हटाने के लिए उनका उपयोग किया जाए। यह अगले से पता चलता है कि कैसे निश्चित zebrafish लार्वा से मस्तिष्क विच्छेदन करने के लिए. अंत में, वीडियो इम्यूनोहिस्टोकेमिस्ट्री के लिए प्रोटोकॉल का अवलोकन प्रदान करता है और माइक्रोस्कोपी के लिए कम-पिघलने-बिंदु एगारोज़ में दाग वाले भ्रूण को माउंट करने के तरीके का एक प्रदर्शन प्रदान करता है।
Introduction
इस विधि का लक्ष्य यह जांचना है कि रेटिना इनपुट ऑप्टिक टेक्टम के विकास और विकास को कैसे प्रभावित करता है, जो ज़ेब्राफ़िश मस्तिष्क में दृश्य प्रसंस्करण केंद्र है। एक आंख को हटाकर और फिर ऑप्टिक टेक्टम के दो पक्षों की तुलना करके, एक ही नमूने के भीतर टेक्टल परिवर्तनों को देखा जा सकता है और सामान्यीकृत किया जा सकता है, जिससे कई नमूनों में तुलना की जा सकती है। इस तकनीक के साथ संयुक्त आधुनिक आणविक दृष्टिकोण दृश्य प्रणाली के विकास और विकास के अंतर्निहित तंत्र में अंतर्दृष्टि प्राप्त करेंगे, साथ ही साथ अक्षीय अध: पतन और पुनर्जनन भी।
संवेदी प्रणालियां – दृश्य, श्रवण, और सोमाटोसेंसरी – बाहरी अंगों से जानकारी इकट्ठा करती हैं और उस जानकारी को केंद्रीय तंत्रिका तंत्र को रिले करती हैं, जिससे मिडब्रेन 1,2 में बाहरी दुनिया के “मानचित्र” उत्पन्न होते हैं। दृष्टि लगभग सभी कशेरुकियों के लिए प्रमुख संवेदी रूपरेखा है, जिसमें कई मछलियां भी शामिल हैं। रेटिना, आंखों में तंत्रिका ऊतक, एक न्यूरोनल सर्किट के साथ जानकारी एकत्र करता है जिसमें मुख्य रूप से फोटोरिसेप्टर, द्विध्रुवी कोशिकाएं और रेटिना गैंग्लियन कोशिकाएं (आरजीसी), रेटिना के प्रक्षेपण न्यूरॉन्स शामिल होते हैं। आरजीसी में लंबे अक्षतंतु होते हैं जो रेटिना की आंतरिक सतह पर ऑप्टिक तंत्रिका सिर तक अपना रास्ता ढूंढते हैं, जहां वे मस्तिष्क के माध्यम से एक साथ यात्रा करते हैं, अंततः पृष्ठीय मिडब्रेन में दृश्य प्रसंस्करण केंद्र में समाप्त हो जाते हैं। इस संरचना को मछली और अन्य गैर-स्तनधारी कशेरुकियों में ऑप्टिक टेक्टम कहा जाता है और स्तनधारियों में बेहतर कोलिकुलस के लिए समरूप है।
ऑप्टिक टेक्टम पृष्ठीय मध्यस्तिष्क में एक द्विपक्षीय सममित बहुस्तरीय संरचना है। ज़ेब्राफ़िश और अधिकांश अन्य मछलियों में, ऑप्टिक टेकटम का प्रत्येक लोब पूरी तरह से contralateral आंख से दृश्य इनपुट प्राप्त करता है, जैसे कि बाएं ऑप्टिक तंत्रिका दाएं टेक्टल लोब में समाप्त हो जाती है और दाईं ऑप्टिक तंत्रिका बाएं टेक्टल लोब4 (चित्रा 1) में समाप्त हो जाती है। अपने स्तनधारी समकक्ष की तरह, बेहतर कोलिकुलस, ऑप्टिक टेकटम अन्य संवेदी इनपुट के साथ दृश्य जानकारी को एकीकृत करता है, जिसमें ऑडिशन और सोमाटोसेंसेशन शामिल हैं, दृश्य ध्यान और आंखों के आंदोलनों में बदलाव को नियंत्रित करते हैं जैसे कि सैकेड्स 1,5,6। हालांकि, स्तनधारी बेहतर कोलिकुलस के विपरीत, ऑप्टिक टेकटम लगातार टेक्टल लोब के औसत दर्जे के और पुच्छल किनारों के पास एक विशेष स्टेम सेल आला से नए न्यूरॉन्स और ग्लिया उत्पन्न करता है जिसे टेक्टल प्रसार क्षेत्र7 कहा जाता है। ऑप्टिक टेकटम और केंद्रीय तंत्रिका तंत्र के अन्य क्षेत्रों में प्रोलिफेरेटिव पूर्वजों का रखरखाव, भाग में, ज़ेबराफ़िश 8 में प्रलेखित उल्लेखनीय पुनर्योजी क्षमता में योगदान देताहै।
अंधे या एक आंखों वाली मछलियों के दिमाग की जांच करने वाले पिछले काम से पता चला कि ऑप्टिक टेक्टम का आकार रेटिना इनर्वेशन की मात्रा के लिए सीधे आनुपातिक है जोइसे 9,10,11 प्राप्त करता है। वयस्क गुफा मछली में, जिनकी आंखें प्रारंभिक भ्रूणजनन में पतित होती हैं, ऑप्टिक टेकटम निकटता से संबंधित, दृष्टिहीन सतह मछली9 की तुलना में काफी छोटा होता है। गुफा मछली आंख अध: पतन भ्रूणजनन के दौरान एक सतह मछली से एक लेंस के साथ अंतर्जात लेंस को बदलकर अवरुद्ध किया जा सकता है। जब इन एक आंखों वाली गुफा मछलियों को वयस्कता में पाला जाता है, तो इनरवेटेड टेक्टल लोब में गैर-इनरवेटेड टेक्टल लोब 9 की तुलना में लगभग 10% अधिक कोशिकाएं होतीहैं। इसी तरह, लार्वा किलीफ़िश में जो एक ही व्यक्ति के भीतर विभिन्न आकारों की आंखों को उत्पन्न करने के लिए रासायनिक उपचार के साथ इनक्यूबेट किए गए थे, अधिक संरक्षण के साथ टेक्टम का पक्ष बड़ा था और इसमें अधिक न्यूरॉन्स10 शामिल थे। वयस्क सुनहरी मछली में ऑप्टिक तंत्रिका क्रश प्रयोगों से सबूत इंगित करता है कि संरक्षण प्रसार को बढ़ावा देता है, टेक्टल सेल प्रसार के साथ कम हो जाता है जब इनरवेशन बाधित हो गया था11।
इन शास्त्रीय अध्ययनों की पुष्टि और विस्तार करते हुए, कई हालिया रिपोर्टें डेटा प्रदान करती हैं जो सुझाव देती हैं कि इनरवेशन के जवाब में प्रसार को कम से कम भाग में, BDNF-TrkB Pathway12,13 द्वारा संशोधित किया जाता है। ऑप्टिक टेक्टम विकास और विकास के बारे में कई खुले प्रश्न बने हुए हैं, जिसमें यह भी शामिल है कि एक विकासशील संवेदी प्रणाली चोट और अक्षतंतु अध: पतन के साथ कैसे सामना करती है, जो सेलुलर और आणविक संकेत ऑप्टिक टेकटम विकास को विनियमित करने के लिए रेटिना इनपुट को सक्षम करते हैं, जब ये तंत्र सक्रिय हो जाते हैं, और क्या इनरवेशन-लिंक्ड प्रसार और भेदभाव रेटिना और इसके लक्ष्य ऊतक को विकास दरों का समन्वय करने और सटीक रेटिनोटोपिक मैपिंग सुनिश्चित करने में सक्षम बनाते हैं। इसके अलावा, गतिविधि-निर्भर विकास के बारे में बहुत बड़े प्रश्न हैं जिन्हें सर्जिकल दृष्टिकोण के साथ ज़ेब्राफ़िश दृश्य प्रणाली से पूछताछ करके संबोधित किया जा सकता है जैसे कि नीचे वर्णित एक।
सेलुलर और आणविक तंत्र की जांच करने के लिए जिसके द्वारा तंत्रिका गतिविधि, विशेष रूप से दृश्य इनपुट से, सेल अस्तित्व और प्रसार को बदल देती है, वर्णित दृष्टिकोण सीधे व्यक्तिगत ज़ेब्राफ़िश लार्वा के भीतर आंतरिक और व्युत्पन्न टेक्टल लोब (चित्रा 1) की तुलना करता है। यह विधि ऑप्टिक टेकटम में आरजीसी अक्षतंतु अध: पतन के प्रलेखन और पुष्टि के लिए अनुमति देती है कि माइटोटिक कोशिकाओं की संख्या इनरवेशन के साथ सहसंबंधित है।
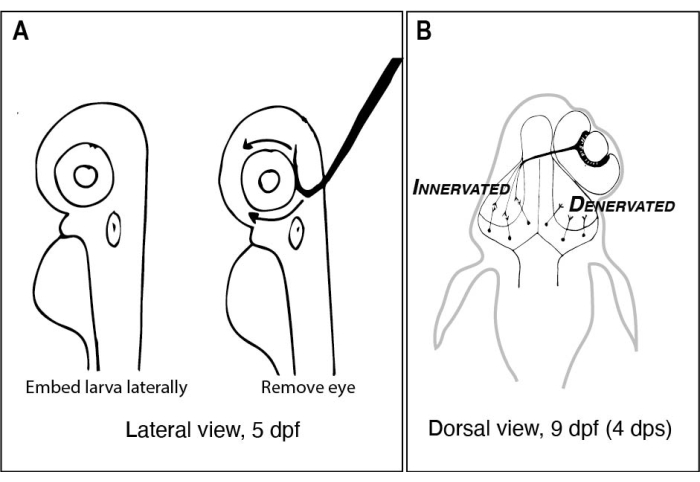
चित्र 1: एकतरफा आंख हटाने से पहले और बाद में ज़ेब्राफ़िश लार्वा के स्केच। (A) विच्छेदन माइक्रोस्कोप के नीचे देखे गए 5 dpf लार्वा का आरेखण। प्रत्येक लार्वा कम पिघलने-बिंदु agarose में एम्बेडेड है और एक तेज, झुका हुआ टिप के साथ एक टंगस्टन सुई से पहले पार्श्व रूप से उन्मुख है, ऊपर का सामना कर रही आंख (इस उदाहरण में बाईं आंख) का सामना कर रही आंख को स्कूप करने के लिए उपयोग किया जाता है। (बी) ए में दर्शाई गई सर्जरी के परिणामस्वरूप 9 डीपीएफ लार्वा के पृष्ठीय दृश्य का ड्राइंग। दाईं आंख से केवल तीन अत्यधिक योजनाबद्ध आरजीसी अक्षतंतुओं को बाएं टेक्टल लोब में न्यूरॉन्स के साथ विघटित और कनेक्ट करते हुए दिखाया गया है। संक्षेप: dpf = निषेचन के बाद के दिन; डीपीएस = सर्जरी के बाद के दिन; RGC = रेटिना गैंग्लियन कोशिकाएं। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
Protocol
Representative Results
Discussion
इस पेपर में वर्णित तकनीकें ज़ेब्राफ़िश में कशेरुक दृश्य प्रणाली के विकास का अध्ययन करने के लिए कई दृष्टिकोणों में से एक को दर्शाती हैं। अन्य शोधकर्ताओं ने भ्रूण रेटिना को विच्छेदित करने और जीन अभिव्?…
Divulgations
The authors have nothing to disclose.
Acknowledgements
इस काम के लिए धन मुख्य रूप से रीड कॉलेज से केएलसी तक स्टार्ट-अप फंड, ओएलएच के लिए हेलेन स्टैफोर्ड रिसर्च फेलोशिप फंड, और वाईके के लिए रीड कॉलेज साइंस रिसर्च फैलोशिप द्वारा समर्थित था। यह परियोजना स्टीव विल्सन की प्रयोगशाला में एचआर के सहयोग के रूप में शुरू हुई, जिसे वेलकम ट्रस्ट स्टूडेंटशिप (2009-2014) द्वारा समर्थित किया गया था। हम इस परियोजना के बारे में प्रारंभिक चर्चा के लिए मैटे वर्गा, स्टीव विल्सन और विल्सन प्रयोगशाला के अन्य सदस्यों को धन्यवाद देते हैं, और हम विशेष रूप से फ्लोरेंसिया कैवोडेसी और केट एडवर्ड्स को धन्यवाद देते हैं, जो केएलसी को सिखाने वाले पहले व्यक्ति थे कि एगारोज़ में भ्रूण कैसे माउंट करें और ज़ेबराफ़िश मस्तिष्क विच्छेदन कैसे करें। हम ग्रेटा ग्लोवर और जे इविंग को हमारे टंगस्टन सुई-शार्पनिंग डिवाइस को इकट्ठा करने में मदद के लिए भी धन्यवाद देते हैं।
Materials
| Equipment and supplies: | |||
| Breeding boxes | Aquaneering | ZHCT100 | |
| Dow Corning high vacuum grease | Sigma or equivalent supplier | Z273554 | |
| Erlenmeyer flasks (125 mL) | For making Marc's Modified Ringers (MMR) with antibiotics for post-surgery incubation | ||
| Fine forceps – Dumont #5 | Fine Science Tools (FST) | 11252-20 | |
| Glass Pasteur pipettes | DWK Lifescience | 63A53 & 63A53WT | For pipetting embryos and larvae |
| Glass slides for microscopy | VWR or equivalent supplier | 48311-703 | Standard glass microscope slides can be ordered from many different laboratory suppliers. |
| Glassware including graduated bottles and graduated cylinders | For making and storing solutions | ||
| 2-part epoxy resin | ACE Hardware or other equivalent supplier of Gorilla Glue or equivalent | 0.85 oz syringe | https://www.acehardware.com/departments/paint-and-supplies/tape-glues-and-adhesives/glues-and-epoxy/1590793 |
| Microcentrifuge tube (1.7 mL) | VWR or equivalent supplier | 22234-046 | |
| Nickel plated pin holder (17 cm length) | Fine Science Tools (FST) | 26018-17 | To hold tungsten wire while sharpening and performing surgeries/dissections. |
| Nylon mesh tea strainer or equivalent | Ali Express or equivalent | For harvesting zebrafish eggs after spawning; https://www.aliexpress.com/item/1005002219569756.html | |
| Paper clip | For Tungsten needle sharpening device. | ||
| Petri dishes 100 mm | Fischer Scientific or equivalent supplier | 50-190-0267 | |
| Petri dishes 35 mm | Fischer Scientific or equivalent supplier | 08-757-100A | |
| Pipette pump | SP Bel-Art or equivalent | F37898-0000 | |
| Potassium hydroxide (KOH) | Sigma | 909122 | For Tungsten needle sharpening device. Make a 10% w/v solution of KOH in the hood by adding pellets to deionized water. |
| Power supply (variable voltage) | For Tungsten needle sharpening device. Any power supply with variable voltage will work (even one used for gel electrophoresis). | ||
| Sylgard 184 Elastomer kit | Dow Corning | 3097358 | |
| Tungsten wire (0.125 mm diameter) | World Precision Instruments (WPI) | TGW0515 | Sharpen to remove eye and dissect larvae. |
| Variable temperature heat block | The Lab Depot or equivalent supplier | BSH1001 or BSH1002 | Set to 40-42 °C ahead of experiments. |
| Wide-mouth glass jar with lid (e.g., clean jam or salsa jar) | For Tungsten needle sharpening device. | ||
| Wires with alligator clip leads | For Tungsten needle sharpening device. | ||
| Microscopes: | |||
| Dissecting microscope | Any type will work but having adjustable transmitted light on a mirrored base is preferred. | ||
| Laser scanning confocal microscope | High NA, 20-25x water dipping objective lens is recommended. Microscope control and image capture software (Elements) is used here but any confocal microscope will work. |
||
| Reagents for surgeries and dissections: | |||
| Calcium chloride dihydrate | Sigma | C7902 | For Marc's Modified Ringers (MMR) and embryo medium (E3). |
| HEPES | Sigma | H7006 | For Marc's Modified Ringers (MMR). |
| Low melting point agarose | Invitrogen | 16520-050 | Make 1% in embryo medium (E3) or Marc's Modified Ringers (MMR). |
| Magnesium chloride hexahydrate | Sigma | 1374248 | For embryo medium (E3). |
| Magnesium sulfate | Sigma | M7506 | For Marc's Modified Ringers (MMR). |
| Paraformaldehyde | Electron Microscopy Sciences | 19210 | Dilute 8% (w/v) stock with 2x concentrated PBS (diluted from 10x PBS stock). |
| Penicillin/Streptomycin | Sigma | P4333-20ML | Dilute 1:100 in Marc's Modified Ringers. |
| Phosphate buffered saline (PBS) tablets | Diagnostic BioSystems | DMR E404-01 | Make 10x stock in deionized water, autoclave and store at room temperature. Dilute to 1x working concentration. |
| Potassium chloride | Sigma | P3911 | For Marc's Modified Ringers (MMR) and embryo medium (E3). |
| Sodium chloride | Sigma | S9888 | For Marc's Modified Ringers (MMR) and embryo medium (E3). |
| Sodium hydroxide | Sigma | S5881 | Make 10 M and use to adjust pH of MMR to 7.4. |
| Sucrose | Sigma | S9378 | |
| Tricaine-S | Pentair | 100G #TRS1 | Recipe: https://zfin.atlassian.net/wiki/spaces/prot/pages/362220023/TRICAINE |
| Reagents for immunohistochemistry: | |||
| Alexafluor 568 tagged Secondary antibody to detect rabbit IgG | Invitrogen | A-11011 | Use at 1:500 dilution for wholemount immunohistochemistry. |
| DAPI or ToPro3 | Invitrogen | 1306 or T3605 | Make up 1 mg/mL solutions in DMSO; 1:5,000 dilution for counterstaining. |
| Dimethyl sulfoxide (DMSO) | Sigma | D8418 | A component of immunoblock buffer. |
| Methanol (MeOH) | Sigma | 34860 | Mixing MeOH with aqueous solutions like PBST is exothermic. Make the MeOH/PBST solutions at least several hours ahead of time or cool them on ice before using. |
| Normal goat serum | ThermoFisher Scientific | 50-062Z | A component of immunoblock buffer. Can be aliquoted in 1-10 mL volumes and stored at -20 °C. |
| Primary antibody to detect phosphohistone H3 | Millipore | 06-570 | Use at 1:300 dilution for wholemount immunohistochemistry. |
| Primary antibody to detect Red Fluorescent Protein (RFP; detects dsRed derivatives) | MBL International | PM005 | Use at 1:500 dilution for wholemount immunohistochemistry. |
| Proteinase K (PK) | Sigma | P2308-10MG | Make up 10 mg/mL stock solutions in PBS and use at 10 µg/mL. |
| Triton X-100 | Sigma | T8787 | Useful to make a 20% (v/v) stock solution in PBS. |
| Software for data analysis | |||
| ImageJ (Fiji) | freeware for image analysis; https://imagej.net/software/fiji/ | ||
| Rstudio | freeware for statistical analysis and data visualization; https://www.rstudio.com/products/rstudio/download/ | ||
| Adobe Photoshop or GIMP | Proprietary image processing software (Adobe Photoshop and Illustrator) are often used to compose figures). A freeware alternative is Gnu Image Manipulation Program (GIMP; https://www.gimp.org/) | ||
| Zebrafish strains | available from the Zebrafish International Resource Centers in the US (https://zebrafish.org/home/guide.php) or in Europe (https://www.ezrc.kit.edu/). Specialized transgenic strains that have not yet been deposited in either resource center can be requested from individual labs after publication. |
References
- Butler, A. B., Hodos, W. Optic tectum. Comparative Vertebrate Neuroanatomy: Evolution and Adaptation. , 311-340 (2005).
- Cang, J., Feldheim, D. A. Developmental mechanisms of topographic map formation and alignment. Annual Review of Neuroscience. 36 (1), 51-77 (2013).
- Basso, M. A., Bickford, M. E., Cang, J. Unraveling circuits of visual perception and cognition through the superior colliculus. Neuron. 109 (6), 918-937 (2021).
- Burrill, J. D., Easter, S. S. Development of the retinofugal projections in the embryonic and larval zebrafish (Brachydanio rerio). The Journal of Comparative Neurology. 346 (4), 583-600 (1994).
- Regeneration in the goldfish visual system. Webvision: The Organization of the Retina and Visual System Available from: https://webvision.med.utah.edu/book/part-x-repair-and-regeneration-in-the-visual-system/regeneration-in-the-goldfish-visual-system/ (2021)
- Regeneration in the visual system of adult mammals. Webvision: The Organization of the Retina and Visual System Available from: https://webvision.med.utah.edu/book/part-x-repair-and-regeneration-in-the-visual-system/regeneration-in-the-visual-system-of-adult-mammals/ (2021)
- Cerveny, K. L., Varga, M., Wilson, S. W. Continued growth and circuit building in the anamniote visual system. Developmental Neurobiology. 72 (3), 328-345 (2012).
- Lindsey, B. W., et al. Midbrain tectal stem cells display diverse regenerative capacities in zebrafish. Scientific Reports. 9 (1), 4420 (2019).
- Soares, D., Yamamoto, Y., Strickler, A. G., Jeffery, W. R. The lens has a specific influence on optic nerve and tectum development in the blind cavefish Astyanax. Developmental Neuroscience. 26 (5-6), 308-317 (2004).
- White, E. L. An experimental study of the relationship between the size of the eye and the size of the optic tectum in the brain of the developing teleost, Fundulus heteroclitus. Journal of Experimental Zoology. 108 (3), 439-469 (1948).
- Raymond, P., Easter, S., Burnham, J., Powers, M. Postembryonic growth of the optic tectum in goldfish. II. Modulation of cell proliferation by retinal fiber input. The Journal of Neuroscience. 3 (5), 1092-1099 (1983).
- Sato, Y., Yano, H., Shimizu, Y., Tanaka, H., Ohshima, T. Optic nerve input-dependent regulation of neural stem cell proliferation in the optic tectum of adult zebrafish. Developmental Neurobiology. 77 (4), 474-482 (2017).
- Hall, Z. J., Tropepe, V. Visual experience facilitates BDNF-dependent adaptive recruitment of new neurons in the postembryonic optic tectum. The Journal of Neuroscience. 38 (8), 2000-2014 (2018).
- Nusslein-Volhard, C., Dahm, R. . Zebrafish. , (2002).
- Cold Spring Harbor Protocols. Marc’s modified Ringer’s (MMR) (10X, pH 7.4). Cold Spring Harbor Protocols. , (2009).
- Turner, K. J., Bracewell, T. G., Hawkins, T. A. Anatomical dissection of zebrafish brain development. Brain Development. 1082, 197-214 (2014).
- Brady, J. A simple technique for making very fine, durable dissecting needles by sharpening tungsten wire electrolytically. Bulletin of the World Health Organization. 32 (1), 143-144 (1965).
- . ZFIN Tricaine recipe Available from: https://zfin.atlassian.net/wiki/spaces/prot/pages/362220023/TRICAINE (2018)
- Zhang, L., Leung, Y. F. Microdissection of zebrafish embryonic eye tissues. Journal of Visualized Experiments: JoVE. (40), e2028 (2010).
- . ZFIN protocols Available from: https://zfin.atlassian.net/wiki/spaces/prot/overview (2021)
- Engerer, P., Plucinska, G., Thong, R., Trovò, L., Paquet, D., Godinho, L. Imaging subcellular structures in the living zebrafish embryo. Journal of Visualized Experiments: JoVE. (110), e53456 (2016).
- ImageJ with batteries included. Fiji Available from: https://figi.sc/ (2021)
- O’Brien, J., Hayder, H., Peng, C. Automated quantification and analysis of cell counting procedures using ImageJ plugins. Journal of Visualized Experiments: JoVE. (117), e54719 (2016).
- Poggi, L., Vitorino, M., Masai, I., Harris, W. A. Influences on neural lineage and mode of division in the zebrafish retina in vivo. The Journal of Cell Biology. 171 (6), 991-999 (2005).
- Karlstrom, R. O., et al. Zebrafish mutations affecting retinotectal axon pathfinding. Development. 123 (1), 427-438 (1996).
- Harvey, B. M., Baxter, M., Granato, M. Optic nerve regeneration in larval zebrafish exhibits spontaneous capacity for retinotopic but not tectum specific axon targeting. PLOS ONE. 14 (6), 0218667 (2019).
- Robles, E., Filosa, A., Baier, H. Precise lamination of retinal axons generates multiple parallel input pathways in the tectum. Journal of Neuroscience. 33 (11), 5027-5039 (2013).
- Vargas, M. E., Barres, B. A. Why Is Wallerian degeneration in the CNS so slow. Annual Review of Neuroscience. 30 (1), 153-179 (2007).
- Hughes, A. N., Appel, B. Microglia phagocytose myelin sheaths to modify developmental myelination. Nature Neuroscience. 23 (9), 1055-1066 (2020).
- de Calbiac, H., Dabacan, A., Muresan, R., Kabashi, E., Ciura, S. Behavioral and physiological analysis in a zebrafish model of epilepsy. Journal of Visualized Experiments: JoVE. (176), e58837 (2021).
- Adams, S. L., Zhang, T., Rawson, D. M. The effect of external medium composition on membrane water permeability of zebrafish (Danio rerio) embryos. Theriogenology. 64 (7), 1591-1602 (2005).
- Fredj, N. B., et al. Synaptic activity and activity-dependent competition regulates axon arbor maturation, growth arrest, and territory in the retinotectal projection. Journal of Neuroscience. 30 (32), 10939-10951 (2010).
- Alberio, L., et al. A light-gated potassium channel for sustained neuronal inhibition. Nature Methods. 15 (11), 969-976 (2018).
- Kay, J. N., Finger-Baier, K. C., Roeser, T., Staub, W., Baier, H. Retinal ganglion cell genesis requires lakritz, a zebrafish atonal homolog. Neuron. 30 (3), 725-736 (2001).
- Gnuegge, L., Schmid, S., Neuhauss, S. C. F. Analysis of the activity-deprived zebrafish mutant macho reveals an essential requirement of neuronal activity for the development of a fine-grained visuotopic map. The Journal of Neuroscience. 21 (10), 3542-3548 (2001).
- Jeffery, W. R. Astyanax surface and cave fish morphs. EvoDevo. 11 (1), 14 (2020).
- Sieger, D., Peri, F. Animal models for studying microglia: The first, the popular, and the new. Glia. 61 (1), 3-9 (2013).
- Svahn, A. J., et al. Development of ramified microglia from early macrophages in the zebrafish optic tectum. Developmental Neurobiology. 73 (1), 60-71 (2013).
- Herzog, C., et al. Rapid clearance of cellular debris by microglia limits secondary neuronal cell death after brain injury in vivo. Development. 146 (9), (2019).
- Chen, J., Poskanzer, K. E., Freeman, M. R., Monk, K. R. Live-imaging of astrocyte morphogenesis and function in zebrafish neural circuits. Nature Neuroscience. 23 (10), 1297-1306 (2020).

