Standardisering og vedligeholdelse af 3D-hundes lever- og tarmorganoidkulturer til brug i biomedicinsk forskning
Summary
Eksperimentelle metoder til at høste voksne stamceller fra hundetarm- og levervæv for at etablere 3D-organoidkulturer er beskrevet. Desuden diskuteres laboratorieteknikkerne til at sikre ensartet vækst og tilvejebringe standardprocedurer til høst, biobank og genoplivning af hundetarm- og leverorganoidkulturer.
Abstract
Hunde udvikler komplekse multifaktorielle sygdomme analogt med mennesker, herunder inflammatoriske sygdomme, metaboliske sygdomme og kræft. Derfor repræsenterer de relevante store dyremodeller med det translationelle potentiale til humanmedicin. Organoider er 3-dimensionelle (3D), selvmonterede strukturer afledt af stamceller, der efterligner mikroanatomien og fysiologien i deres oprindelsesorgan. Disse translationelle in vitro-modeller kan bruges til lægemiddelpermeabilitet og opdagelsesapplikationer, toksikologivurdering og til at give en mekanistisk forståelse af patofysiologien af multifaktorielle kroniske sygdomme. Desuden kan hundeorganoider forbedre livet for selskabshunde, give input inden for forskellige områder af veterinærforskning og lette personlige behandlingsapplikationer inden for veterinærmedicin. En lille gruppe donorer kan oprette en biobank af organoidprøver, hvilket reducerer behovet for kontinuerlig vævshøst, da organoidcellelinjer kan subdyrkes på ubestemt tid. Heri præsenteres tre protokoller, der fokuserer på kulturen af tarm- og leverkolseorganoider afledt af voksne stamceller. Canine Organoid Isolation Protocol skitserer metoder til behandling af væv og indlejring af celleisolatet i en understøttende matrix (opløselig ekstracellulær membranmatrix). Hundeorganoid vedligeholdelsesprotokollen beskriver organoidvækst og vedligeholdelse, herunder rengøring og passering sammen med passende timing for ekspansion. Organoid Harvesting and Biobanking Protocol beskriver måder at udvinde, fryse og bevare organoider til yderligere analyse.
Introduction
Gnavere er den mest anvendte dyremodel til biomedicinsk og translationel forskning1. De er usædvanligt nyttige til at undersøge grundlæggende molekylær patogenese af sygdommene, selv om deres kliniske relevans for kroniske multifaktorielle sygdomme for nylig er blevet stillet spørgsmålstegn ved2. Hundemodellen udviser flere fordele i forhold til gnavere3,4. Hunde og mennesker deler ligheder i metabolomics og intestinal mikrobiom, der udviklede sig på grund af forbrug af menneskelig kost gennem forskellige perioder af deres domesticering5,6,7. Ligheder mellem hundes og menneskets mave-tarm-anatomi og fysiologi er et andet af eksemplerne8.
Derudover deler hunde ofte lignende miljøer og livsstil med deres ejere9. Hundens længere levetid i forhold til gnavere giver mulighed for en naturlig udvikling af mange kroniske tilstande10. Inflammatorisk tarmsygdom eller metabolisk syndrom er eksempler på multifaktorielle kroniske sygdomme, der deler vigtige ligheder mellem mennesker og hunde11,12. Prækliniske forsøg med hunde, der involverer hunde med naturligt forekommende sygdomme, kan generere mere pålidelige data end dem, der er opnået fra gnavermodeller13. For at minimere brugen af levende dyreforskning og overholde principperne i 3R’erne (Reduce, Refine, Replace)14 er der imidlertid opstået alternativer til in vivo-test ved hjælp af 3D in vitro-hundeorganoider15.
Organoider er selvsamlede 3D-stamcelleafledte strukturer, der rekapitulerer fysiologien og mikroanatomien i deres oprindelige organer16,17. Denne teknologi blev først beskrevet af Sato et al. i 200917 og tillod mere oversættelige in vitro-undersøgelser i epitelcellelinjer, end det tidligere var muligt ved hjælp af 2D-kræftcellekulturer18,19,20. Organoider er nyttige in vitro-modeller i mange biomedicinske discipliner såsom i præklinisk toksikologiske21,22,23, absorptions- eller metabolismeundersøgelser24,25,26,27,28 samt i personlige medicinske tilgange29,30,31 . Den vellykkede kultur af hundes tarmorganoider er blevet beskrevet for første gang i 201912, mens leverorganoider afledt af en hund først blev rapporteret af Nantasanti et al. i 201532. Hundeorganoider er siden blevet anvendt med succes i undersøgelser, der undersøger kroniske enteropatier hos hunde, gastrointestinale stromale tumorer, kolorektal adenocarcinom12 og Wilsons sygdom33,34.
Mens voksne stamceller kan høstes via obduktioner, kræver organoidteknologien ikke altid ofring af dyrene. Endoskopiske og laparoskopiske biopsier eller endda finnålespirater af organer35 er en levedygtig kilde til voksne stamceller til epitelorganoidisolering12. Udbredt anvendelse af sådanne ikke-invasive teknikker i veterinærpraksis letter mulighederne for omvendt translationel forskning (oversættelse af oplysninger fra veterinær klinisk praksis til human klinisk praksis og omvendt)15. Yderligere fremskridt inden for organoidteknologi kan sikres ved standardisering af organoidkultur og vedligeholdelsesmetoder. Den organoidprotokol, der præsenteres her, er delvist baseret på tidligere offentliggjort arbejde af Saxena et al. fra 201536, og metoder blev tilpasset til at passe til specifikationer for hundetarm og leverorganoidkultur. Den overordnede arbejdsgang for hundens organoidprotokoller er afbildet i figur 1.
Canine Organoid Isolation Protocol introducerer metoder til opnåelse af prøver fra endoskopiske, laparoskopiske og kirurgiske biopsier samt obduktioner. Den skitserer den indledende forbehandling af vævsprøver og metoder, der anvendes til transport til laboratoriet. Materialer og reagenser, der er nødvendige for organoidisolering, er opsummeret i afsnittet ‘Forberedelse til isolering’. Processen med isolering af voksne stamceller fra vævsprøver er nærmere beskrevet. Endelig diskuteres processen med plettering af organoider i kuppellignende strukturer ved hjælp af en opløselig ekstracellulær membranmatrix.
Den anden protokol, Canine Organoid Maintenance Protocol, beskriver metoder til dokumentation og dyrkning af organoider. Medieændringer og deres hyppighed diskuteres i dette afsnit. Desuden beskrives laboratorieprocedurerne såsom passaging og rengøring af cellekulturerne, som er afgørende for at sikre en vellykket vedligeholdelse af 3D-hundeorganoider. Passende passaging er et kritisk trin i protokollen, og mulige justeringer og fejlfinding af dette trin diskuteres yderligere i manuskriptet.
Den sidste protokol er Canine Organoid Harvesting and Biobanking Protocol, der indeholder metoder til fremstilling af fuldvoksne organoider til paraffinindlejring og RNA-konservering. Metoder til biobanking af organoidprøver i flydende nitrogenlagring er også beskrevet her. Endelig diskuteres måderne til optøning af frosne prøver og støtte deres vækst.
Afslutningsvis har denne artikel til formål at tilvejebringe konsekvente procedurer for hundeorganoidkultur gennem standardisering af protokoller mellem laboratorier. Dermed har manuskriptet til formål at lette reproducerbarheden af data fra hundeorganoidmodeller for at øge deres relevans i translationel biomedicinsk forskning.
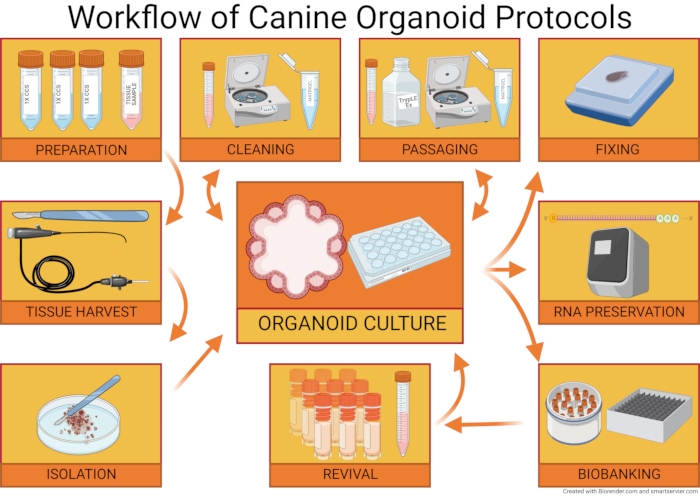
Figur 1: Arbejdsgang af hundeorganoidprotokoller. Canine Organoid Isolation Protocol beskriver forberedelsen af de materialer, der er nødvendige for organoidisolering, høst af en vævsprøve (ved hjælp af obduktioner, endoskopiske, laparoskopiske og kirurgiske biopsier) og vejledning om celle dissociation og plettering af den cellulære population. Hundeorganoidvedligeholdelsesprotokollen diskuterer rengøring og passering af organoidkulturen. Organoid Harvesting and Biobanking Protocol diskuterer forberedelsen af organoidprøver til paraffinindlejring og yderligere organoidkarakterisering. Metoder til biobankorganoidkulturer og genoplivning af dem fra opbevaring i flydende nitrogen diskuteres også. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Der mangler i øjeblikket standardiserede protokoller til isolering og vedligeholdelse af hundes lever- og tarmorganoider. Etablering af standardprocedurer for organoidkulturer er berettiget for, at denne model kan anvendes i forskellige laboratorieindstillinger. Specifikt er tilvejebringelse af standardiserede driftsprotokoller til dyrkning af disse hundeorganoidmodeller nøglen til at karakterisere organoidernes normale vækst under kultur og passaging for at udlede optimale tidspunkter for udvidelse og vedligeholdelse. Hunde tarmorganoider dyrket ved hjælp af protokollen har tidligere været karakteriseret ved Chandra et al.12.
Et af de mest kritiske trin i protokollen er passaging af organoider. Den optimale tid for den første passage af leversfæroider blev bestemt til at være på dag 7 efter isolering baseret på de hepatiske sfæroidmålinger. Det maksimale volumen af sfæroider blev opnået på dag 7, og samtidig begyndte sfæroider at knoppe og dannede leverorganoider. Stigningen i det samlede organoidvolumen fra dag 2-7 efter isolation var mere end 365 gange, hvilket tyder på, at den optimale passagetid er længere end hundens tarmorganoidkultur. Efter 7 dage i dyrkning blev der ikke observeret grove tegn på cellulær apoptose i leversfæroiden, selv uden rengøring eller passaging (figur 7). Passaging af tarm- og leverorganoider kan være udfordrende, da proceduren kan føre til tab af celler og ændret levedygtighed. Resultaterne tyder på, at langvarig inkubation af leverorganoider med trypsinlignende protease (op til 12 minutter) ikke påvirker subkulturen negativt. Inkubation af organoiderne i trypsinlignende protease i mere end 24 minutter kan være skadeligt for den efterfølgende subkultur af organoiderne.
I tilfælde af suboptimal brud i celleklyngerne med organoidpassagen kan mekanisk dissociation i stedet for langvarig inkubation med trypsinlignende protease være mere gavnlig. Hvis der opstår problemer med korrekt dissociation af organoiderne, kan kort hvirvel af prøverne forsøges for at forbedre passageudbyttet. På den anden side har hvirvel potentialet til at ødelægge en kultur og beskadige celler, så det bør kun bruges, når andre procedurer gentagne gange har fejlet. At bryde leverorganoider i enkeltceller sænker organoidernes væksthastighed, mens de brydes i klynger af celler, kan i høj grad forbedre deres levedygtighed. Ti minutter blev valgt som inkubationstid for organoidprotokollen. Et inkubationstidspunkt på 12 minutter blev anset for ikke cytotoksisk sammenlignet med en 24 minutters inkubation i det trypsinlignende proteaseeksperiment.
Overlevelsesforsøget bekræftede, at hundes leverorganoider kunne overleve i op til 19,5 dage under ugunstige forhold (strukturel og ernæringsmæssig udtømning). Organoider, der overlevede disse forhold længst, blev dyrket med CMGF + medier. Denne observation kan have været forårsaget af den langsommere vækst af leverorganoider i medier, der ikke er suppleret med Rock-hæmmer og GSK3β. Organoidkulturer med CMGF + R / G voksede hurtigere og kan have udtømt deres ressourcer hurtigere. Dette eksperiment åbner muligheder for at miniaturisere hundens organoidkultur for at opnå en systemkonvertering med høj gennemstrømning. En sådan teknologi viser potentialet til at lette lægemiddelopdagelse eller toksikologiske undersøgelser til en væsentligt reduceret pris.
Nogle almindelige problemer, der opstår under vedligeholdelse af hundeorganoidkultur, er forkert prøvestørkning ved plettering, kulturforurening og etablering af den korrekte tæthed og størrelse af organoiderne. Hvis opløselig ECM størkner for tidligt under plettering, skal du straks placere den på is i 10 minutter. Hvis opløselig ECM ikke danner kuppellignende strukturer, er det sandsynligt, at der ikke blev fjernet nok medier fra prøven. Hvis dette er tilfældet, fortyndes prøven med en mere opløselig ECM, indtil der dannes kupler.
Når der findes svampe- eller bakterieforurening i en hel plade (se figur 4), er den bedste løsning at kassere pladen. Behandling med svampedræbende eller antibiotiske lægemidler kan forsøges, men succesen med et sådant forsøg er ekstremt lavt. Hvis en enkelt brønd er forurenet i en plade, kan levedygtige og upåvirkede brønde rengøres (følg trin 4.1 til 4.5) til en ny plade og overvåges nøje. Hvis prøven allerede er nødfrosset, anbefales det at kassere hele prøven, da optøning af prøven udsætter inkubatoren for yderligere forureningsrisiko.
Sund organoidkultur bør være mindst i kategorien mellemstørrelse og medium densitet eller større. Optimal tæthed er afgørende for organoid kultur vækst. Lavere densitet skal korrigeres ved at rense organoiderne til medium densitet. Hvis situationen med ekstrem tæthed opstår (overbelægning), skal organoiderne udvides til flere brønde. Grove tegn på cellulær apoptose ledsager ofte både overbelægning og lav densitet af organoidkulturen. Hvis disse problemer ikke korrigeres i tide, vil hele organoidkulturen blive apoptotisk i løbet af få dage. Hvis organoider opnår ekstra stor størrelse eller meget høj densitet, skal kulturen bruges til et eksperiment, frysning eller fiksering.
Organoidmediet indeholder i øjeblikket 17 komponenter, og tilføjelsen af vækstfaktorer, der er nødvendige for vedligeholdelse og ekspansion af organoider, kan derfor være dyr. Dette problem kan løses ved at dyrke 2D-cellekulturer, der syntetiserer vækstfaktorerne for at producere betinget CMGF +. Cellekultur L-WRN producerer Wnt-3a, R-Spondin-3 og Noggin vækstfaktorer37. Cellekolonien bruger 90% DMEM / F12 og 10% FBS kulturmedier. Når kulturen opnår 90 procent sammenløb, høstes medier hver dag i 1 uge. De høstede medier blandes derefter med 2x CMGF+ (uden disse vækstfaktorer). Mens 2D-kulturer kan producere de nødvendige vækstfaktorer til en brøkdel af prisen, må den ekstra tid og forberedelse til at producere medierne forventes. Koncentrationerne af vækstfaktorer mellem konditionerede mediebatcher kan også variere37,38.
Voksne stamcelleafledte organoidkulturer af hunde er en unik biomedicinsk model, der kan hjælpe med at nå målene for One Health Initiative39. Organoidteknologien kan anvendes inden for mange grundlæggende og biomedicinske forskningsområder, der spænder fra udviklingsbiologi, patofysiologi, lægemiddelopdagelse og -testning, toksikologi til undersøgelse af infektionssygdomme og regenerativ medicin40. Translationel og omvendt translationel forskning er begge områder, hvor hundeorganoider er anvendelige15. Hunde er blevet brugt i århundreder i translationelle eksperimentelle omgivelser, og deres ledsagende dyrstatus har også lettet deres position som en af de mest udforskede arter inden for veterinærmedicin.
Afslutningsvis giver dette manuskript standardiserede driftsprotokoller til isolering, vedligeholdelse, høst og biobanking af hundes lever- og tarmorganoider for at lette anvendelsen af denne model på forskellige biomedicinske områder. Denne model er unikt egnet til at fremme omvendt translationel forskning som et redskab i One Health-initiativet til at fremme inter- og intradisciplinær deling af viden.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker at udtrykke taknemmelighed over for Veterinary Diagnostic Laboratory of Iowa State University medarbejdere, nemlig Haley M. Lambert, Emily Rahe, Rosalyn M. Branaman, Victoria J. Green og Jennifer M. Groeltz-Thrush, for rettidig behandling af de leverede prøver. Forfatterne ønsker at anerkende støtte fra fakultetets opstart, ISU VPR Miller Award, ISU VPR Miller Award og NSF SBIR sub-award til ISU # 1912948.
Materials
| Chelating solution | |||
| D-Sorbitol | Fisher Chemical | BP439-500 | |
| DTT | Promega | V3151 | |
| KCl | Fisher Chemical | P217-500 | |
| KH2PO4 | Sigma | P5655-100G | |
| Na2HPO4-2H2O | Sigma | S5136-100G | |
| NaCl | Fisher Chemical | S271-500 | |
| Pen Strep | Gibco | 15140-122 | |
| Sucrose | Fisher Chemical | S5-500 | |
| Organoid media | |||
| [Leu15]-Gastrin I human | Sigma | G9145-.5MG | |
| A-83-01 | PeproTech | 9094360 | |
| Advanced DMEM/F12 | Gibco | 12634-010 | |
| B27 supplement | Gibco | 17504-044 | |
| FBS | Corning | 35-010-CV | |
| Glutamax | Gibco | 35050-061 | |
| HEPES | VWR Life Science | J848-500ML | |
| Human R-Spondin-1 | PeproTech | 120-38-500UG | |
| Murine EGF | PeproTech | 315-09-1MG | |
| Murine Noggin | PeproTech | 250-38-250UG | |
| Murine Wnt-3a | PeproTech | 315-20-10UG | |
| N2 supplement | Gibco | 17502-048 | |
| N-Acetyl-L-cysteine | Sigma | A9165-25G | |
| Nicotinamide | Sigma | N0636-100G | |
| Primocin | InvivoGen | ant-pm-1 | |
| ROCK inhibitor (Y-27632) | EMD Millipore Corp. | SCM 075 | |
| SB202190 (P38 inhibitor) | Sigma | S7067-25MG | |
| Stemolecule CHIR99021 (GSK3β) | Reprocell | 04-0004-base | |
| Trimethoprim | Sigma | T7883-5G | |
| Sulfamethoxazole | Sigma-Aldrich | S7507-10G | |
| Reagents | |||
| Acetic Acid, Glacial | Fisher Chemical | A38-500 | |
| Dimethyl Sulfoxide (DMSO) | Fisher Chemicals | D128-500 | |
| EDTA, pH 8.0, 0.5 M | Invitrogen | 15575-038 | |
| Formaldehyde (37%) | Fisher Chemical | F79P-4 | |
| Glutaraldehyde solution | Sigma | G5882 | |
| Matrigel Matrix For Organoid Culture | Corning | 356255 | Extracellular Membrane Matrix |
| Paraformaldehyde, 97% | Alfa Aesar | A11313 | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| RNAlater Soln. | Invitrogen | AM7021 | RNA Storage Reagent |
| TrypLE Express | Gibco | 12604-021 | Trypsin-like Protease |
| Other | |||
| 6 Well Cell Culture Plate | Corning | 3516 | |
| ACD Hybez II Hybridization System | ACD a biotechne brand | 321710 | |
| Centrifuge Tube, 15 mL | Corning | 430766 | |
| CoolCell LX | Corning | BCS-405MC | |
| Cryogenic Vials | Corning | 430488 | |
| Disposable Centrifuge Tube (50 mL) | Fisherbrand | 05-539-13 | |
| GyroMini Nutating mixer (Rocker) | Labnet | S0500-230V-EU | |
| Heat Bath | Lab-Line Instruments | 3000 | |
| Mr. Frosty Freezing Container | ThermoFisher Scientific | 5100-0001 | |
| NanoDrop 2000 | ThermoFisher Scientific | ND2000CLAPTOP | SpectrophotometerAnalysis |
| Panasonic incubator | Panasonic | MCO-170ML-PA | |
| Parafilm M Wrapping Film | Bemis Company Inc | PM996/EMD | Laboratory Flexible Film Tape |
| Protected Disposable Scalpels | Bard-Parker | 239844 | |
| RNAscope 2.5 HD Assay – RED | ACD a biotechne brand | 322350 | |
| RNAscope H2O2 & Protease Plus Reagents | ACD a biotechne brand | 322330 | |
| RNAscope Target Retrieval Reagents | ACD a biotechne brand | 322000 | |
| RNAscope Wash Buffer Reagents | ACD a biotechne brand | 310091 | |
| Tissue Culture Dish | Dot Scientific | 6676621 | |
| Tissue Culture Plate 24 wells | Fisherbrand | FB012929 |
References
- Hickman, D. L., Johnson, J., Vemulapalli, T. H., Crisler, J. R., Shepherd, R. Commonly used animal models. Principles of Animal Research for Graduate and Undergraduate Students. , 117-175 (2017).
- De Jong, M., Maina, T. Of mice and humans: Are they the same? – Implications in cancer translational research. Journal of Nuclear Medicine. 51 (4), 501-504 (2010).
- Cannarozzi, G., Schneider, A., Gonnet, G. A phylogenomic study of human, dog, and mouse. PLoS Computational Biology. 3 (1), 0009-0014 (2007).
- Jacob, J. A. Researchers turn to canine clinical trials to advance cancer therapies. JAMA – Journal of the American Medical Association. 315 (15), 1550-1552 (2016).
- Ziegler, A., Gonzalez, L., Blikslager, A. Large animal models: The key to translational discovery in digestive disease research. Cellular and Molecular Gastroenterology and Hepatology. 2 (6), 716-724 (2016).
- Swanson, K. S., et al. Phylogenetic and gene-centric metagenomics of the canine intestinal microbiome reveals similarities with humans and mice. ISME Journal. 5 (4), 639-649 (2011).
- Coelho, L. P., et al. Similarity of the dog and human gut microbiomes in gene content and response to diet. Microbiome. 6 (1), 72 (2018).
- Nguyen, T. L. A., Vieira-Silva, S., Liston, A., Raes, J. How informative is the mouse for human gut microbiota research. DMM Disease Models and Mechanisms. 8 (1), 1-16 (2015).
- Bontempo, V. Nutrition and health of dogs and cats: Evolution of petfood. Veterinary Research Communications. 29, 45-50 (2005).
- Allenspach, K., Gaschen, F. Canine chronic enteropathies: A review. Schweizer Archiv fur Tierheilkunde. 145 (5), 209-222 (2003).
- Tribuddharatana, T., Kongpiromchean, Y., Sribhen, K., Sribhen, C. Biochemical alterations and their relationships with the metabolic syndrome components in canine obesity. Kasetsart Journal – Natural Science. 45 (4), 622-628 (2011).
- Chandra, L., et al. Derivation of adult canine intestinal organoids for translational research in gastroenterology. BMC Biology. 17 (1), 33 (2019).
- Schaefer, K., Rensing, S., Hillen, H., Burkhardt, J. E., Germann, P. G. Is Science the only driver in species selection? An internal study to evaluate compound requirements in the minipig compared to the dog in preclinical studies. Toxicologic Pathology. 44 (3), 474-479 (2016).
- MacArthur Clark, J. The 3Rs in research: A contemporary approach to replacement, reduction and refinement. British Journal of Nutrition. 120, 1-7 (2018).
- Schneider, B., et al. Model-based reverse translation between veterinary and human medicine: The one health initiative. CPT: Pharmacometrics and Systems Pharmacology. 7 (2), 65-68 (2018).
- Lehmann, R., et al. Human organoids: A new dimension in cell biology. Molecular Biology of the Cell. 30 (10), 1129-1137 (2019).
- Sato, T., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Kim, J., Koo, B. K., Knoblich, J. A. Human organoids: model systems for human biology and medicine. Nature Reviews Molecular Cell Biology. 21 (10), 571-584 (2020).
- Jensen, C., Teng, Y. Is it time to start transitioning from 2D to 3D cell culture. Frontiers in Molecular Biosciences. 7, 33 (2020).
- Ho, B. X., Pek, N. M. Q., Soh, B. S. Disease modeling using 3D organoids derived from human induced pluripotent stem cells. International Journal of Molecular Sciences. 19 (4), 936 (2018).
- Truskey, G. A. Human microphysiological systems and organoids as in vitro models for toxicological studies. Frontiers in Public Health. 6, 185 (2018).
- Caipa Garcia, A. L., Arlt, V. M., Phillips, D. H. Organoids for toxicology and genetic toxicology: applications with drugs and prospects for environmental carcinogenesis. Mutagenesis. , (2021).
- Augustyniak, J., et al. Organoids are promising tools for species-specific in vitro toxicological studies. Journal of Applied Toxicology. 39 (12), 1610-1622 (2019).
- Zietek, T., et al. Organoids to study intestinal nutrient transport, drug uptake and metabolism – Update to the human model and expansion of applications. Frontiers in Bioengineering and Biotechnology. 8, 577656 (2020).
- Zietek, T., Rath, E., Haller, D., Daniel, H. Intestinal organoids for assessing nutrient transport, sensing and incretin secretion. Scientific Reports. 5 (1), 1-10 (2015).
- Kar, S. K., et al. Organoids: a promising new in vitro platform in livestock and veterinary research. Veterinary Research. 52 (1), 1-17 (2021).
- Borcherding, D. C., et al. Sa1976 polyphenols reverse the pathologic effects of palmitic acid and high fat diet in canine enteroids. Gastroenterology. 158 (6), 486 (2020).
- Ambrosini, Y. M., et al. Recapitulation of the accessible interface of biopsy-derived canine intestinal organoids to study epithelial-luminal interactions. PLoS ONE. 15 (4), 0231423 (2020).
- Zdyrski, C., et al. Su124 homology directed repair in canine duodenal enteroids to mimic the wild-type P-glycoprotein mutation. Gastroenterology. 160 (6), 625 (2021).
- Li, Y., Tang, P., Cai, S., Peng, J., Hua, G. Organoid based personalized medicine: from bench to bedside. Cell Regeneration. 9 (1), 21 (2020).
- Kurr, L. A., Allenspach, K., Jergens, A., Mochel, J. P. Harnessing the biology of intestinal organoids to accelerate drug discovery in inflammatory bowel disease: A one health approach. The FASEB Journal. 34, 1 (2020).
- Nantasanti, S., et al. Disease modeling and gene therapy of copper storage disease in canine hepatic organoids. Stem Cell Reports. 5 (5), 895-907 (2015).
- Favier, R. P., et al. COMMD1-Deficient dogs accumulate copper in hepatocytes and provide a good model for chronic hepatitis and fibrosis. PLoS ONE. 7 (8), 42158 (2012).
- Kruitwagen, H. S., et al. Long-term survival of transplanted autologous canine liver organoids in a COMMD1-deficient dog model of metabolic liver disease. Cells. 9 (2), 410 (2020).
- Vilgelm, A. E., et al. Fine-needle aspiration-based patient-derived cancer organoids. iScience. 23 (8), 101408 (2020).
- Saxena, K., et al. Human intestinal enteroids: A new model to study human rotavirus infection, host restriction, and pathophysiology. Journal of Virology. 90 (1), 43-56 (2016).
- VanDussen, K. L., Sonnek, N. M., Stappenbeck, T. S. L-WRN conditioned medium for gastrointestinal epithelial stem cell culture shows replicable batch-to-batch activity levels across multiple research teams. Stem Cell Research. 37, 101430 (2019).
- Powell, R. H., Behnke, M. S. WRN conditioned media is sufficient for in vitro propagation of intestinal organoids from large farm and small companion animals. Biology Open. 6 (5), 698-705 (2017).
- Mackenzie, J. S., Jeggo, M. The one health approach-why is it so important. Tropical Medicine and Infectious Disease. 4 (2), 88 (2019).
- Artegiani, B., Clevers, H. Use and application of 3D-organoid technology. Human Molecular Genetics. 27 (2), 99-107 (2018).

