Standardisering och underhåll av 3D-hund lever- och intestinala organoidkulturer för användning inom biomedicinsk forskning
Summary
Experimentella metoder för att skörda vuxna stamceller från hund intestinala och levervävnader för att etablera 3D organoid kulturer beskrivs. Dessutom diskuteras laboratorieteknikerna för att säkerställa konsekvent tillväxt och tillhandahålla standardrutiner för att skörda, biobank och återuppliva hund intestinala och leverorganoida kulturer.
Abstract
Hundar utvecklar komplexa multifaktoriella sjukdomar som är analoga med människor, inklusive inflammatoriska sjukdomar, metabola sjukdomar och cancer. Därför representerar de relevanta stora djurmodeller med translationell potential för humanmedicin. Organoider är 3-dimensionella (3D), självmonterade strukturer som härrör från stamceller som efterliknar mikroanatomi och fysiologi hos deras ursprungsorgan. Dessa translationella in vitro-modeller kan användas för drug permeability och discovery applikationer, toxikologi bedömning och för att ge en mekanistisk förståelse av patofysiologi av multifaktoriella kroniska sjukdomar. Dessutom kan hundorganoider förbättra livet för följeslagare, ge input inom olika områden av veterinärforskning och underlätta personliga behandlingsapplikationer inom veterinärmedicinen. En liten grupp donatorer kan skapa en biobank av organoida prover, vilket minskar behovet av kontinuerlig vävnadsskörd, eftersom organoida cellinjer kan underkultureras på obestämd tid. Häri presenteras tre protokoll som fokuserar på kulturen av intestinala och lever hundorganoider som härrör från vuxna stamceller. Canine Organoid Isolation Protocol beskriver metoder för att bearbeta vävnad och inbäddning av cellisolat i en stödjande matris (solubilized extracellulär membranmatris). Canine Organoid Maintenance Protocol beskriver organoid tillväxt och underhåll, inklusive rengöring och passaging tillsammans med lämplig tidpunkt för expansion. Organoid harvesting and biobanking protocol beskriver sätt att extrahera, frysa och bevara organoider för vidare analys.
Introduction
Gnagare är den vanligaste djurmodellen för biomedicinsk och translationell forskning1. De är exceptionellt användbara för att undersöka grundläggande molekylär patogenes av sjukdomarna, även om deras kliniska relevans för kroniska multifaktoriella sjukdomar nyligen har ifrågasatts2. Hundmodellen uppvisar flera fördelar jämfört med gnagare3,4. Hundar och människor delar likheter i metabolomik och tarmmikrobiom som utvecklats på grund av konsumtion av mänsklig kost under olika perioder av deras domesticering5,6,7. Likheter mellan hund och mänsklig gastrointestinal anatomi och fysiologi är ett annat av exemplen8.
Dessutom delar hundar ofta liknande miljöer och livsstilar med sina ägare9. Hundens längre livslängd i jämförelse med gnagare möjliggör naturlig utveckling av många kroniska tillstånd10. Inflammatorisk tarmsjukdom eller metaboliskt syndrom är exempel på multifaktoriella kroniska sjukdomar som delar viktiga likheter mellan människor och hundar11,12. Hund prekliniska prövningar som involverar hundar med naturligt förekommande sjukdomar kan generera mer tillförlitliga data än de som erhållits från gnagaremodeller13. För att minimera användningen av levande djurforskning och följa principerna i 3R (Reduce, Refine, Replace)14 har dock alternativ till in vivo-testning med hjälp av 3D-in vitro-hundorganoider dykt upp15.
Organoider är självmonterade 3D-stamcellsbaserade strukturer som rekapitulerar fysiologin och mikroanatomin i sina ursprungliga organ16,17. Denna teknik beskrevs först av Sato et al. 200917 och möjliggjorde mer översättningsbara in vitro-studier i epitelceller än vad som tidigare var möjligt med hjälp av 2D-cancercellskulturer18,19,20. Organoider är användbara in vitro-modeller inom många biomedicinska discipliner som i preklinisk toxikologiska21,22,23, absorptions– eller metabolismstudier24,25,26,27,28, liksom i personliga medicinska metoder29,30,31 . Den framgångsrika kulturen av hund intestinala organoider har beskrivits för första gången 201912, medan leverorganoider som härrör från en hund först rapporterades av Nantasanti et al. Hundorganoider har sedan dess framgångsrikt använts i studier som undersöker hund kronisk enteropathies, gastrointestinala stromal tumörer, kolorektal adenocarcinom12 och Wilsons sjukdom33,34.
Medan vuxna stamceller kan skördas via obduktioner, kräver den organoida tekniken inte alltid att offra djuren. Endoskopiska och laparoskopiska tarmbiopsier, eller till och med fina nåla aspirationer av organ35, är en livskraftig källa till vuxna stamceller för epitelial organoid isolering12. Utbredd användning av sådana icke-invasiva tekniker i veterinärpraxis underlättar alternativ för omvänd translationell forskning (översättning av information från veterinär klinisk praxis till klinisk praxis på människa och vice versa)15. Ytterligare framsteg av organoid teknik kan säkerställas genom standardisering av organoid kultur och underhållsmetoder. Det organoida protokoll som presenteras här är delvis baserat på tidigare publicerade arbeten av Saxena et al. från 201536, och metoderna anpassades för att passa detaljer i hund intestinala och leverorganoid kultur. Det övergripande arbetsflödet för hundens organoidprotokoll visas i figur 1.
Canine Organoid Isolation Protocol introducerar metoder för att erhålla prover från endoskopisk, laparoskopisk och kirurgiska tarmbiopsier, samt obduktioner. Den beskriver den första förbehandlingen av vävnadsprover och metoder som används för transport till laboratoriet. Material och reagenser som behövs för organoid isolering sammanfattas i avsnittet “Förberedelse för isolering”. Processen med vuxna stamcellsisolering från vävnadsprover beskrivs vidare i detalj. Slutligen diskuteras processen att plätera organoider i kupolliknande strukturer med hjälp av en löslubiliserad extracellulär membranmatris.
Det andra protokollet, Canine Organoid Maintenance Protocol, beskriver metoder för att dokumentera och odla organoider. Medieförändringar och deras frekvens diskuteras i det här avsnittet. Dessutom beskrivs laboratorieprocedurer som passaging och rengöring av cellkulturerna, som är nödvändiga för att säkerställa ett framgångsrikt underhåll av 3D-hundorganoider. Lämplig passaging är ett kritiskt steg i protokollet, och möjliga justeringar och felsökning av detta steg diskuteras vidare i manuskriptet.
Det sista protokollet är Canine Organoid Harvesting and Biobanking Protocol som innehåller metoder för att förbereda fullvuxna organoider för paraffininbäddning och RNA-konservering. Metoder för biobanking organoid prover i flytande kväve lagring beskrivs också här. Slutligen diskuteras sätten att tina frysta prover och stödja deras tillväxt.
Sammanfattningsvis syftar denna artikel till att tillhandahålla konsekventa hundorganoida odlingsförfaranden genom standardisering av protokoll mellan laboratorier. Manuskriptet syftar till att underlätta reproducerbarheten av data som härrör från hundorganoidmodeller för att öka deras relevans inom translationell biomedicinsk forskning.
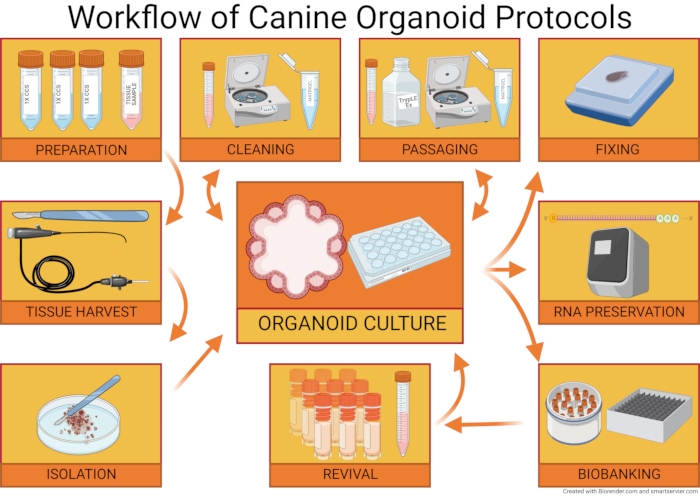
Bild 1: Arbetsflöde för hundorganoidprotokoll. Canine Organoid Isolation Protocol beskriver beredningen av de material som behövs för organoid isolering, skörd av ett vävnadsprov (med hjälp av obduktioner, endoskopisk, laparoskopisk och kirurgiska tarmbiopsier) och vägledning om cellavsociation och plätering av cellpopulationen. Canine Organoid Maintenance Protocol diskuterar rengöring och passaging av den organoida kulturen. I protokollet för organoid skörd och biobanking diskuteras beredning av organoida prover för paraffininbäddning och ytterligare organoid karakterisering. Metoder för biobankorganoida kulturer och återuppliva dem från lagring i flytande kväve diskuteras också. Klicka här för att se en större version av den här figuren.
Protocol
Representative Results
Discussion
Det finns för närvarande en brist på standardiserade protokoll tillgängliga för isolering och underhåll av hund lever och intestinala organoider. Fastställande av standardrutiner för organoida kulturer är motiverat för att denna modell ska kunna tillämpas i olika laboratoriemiljöer. Specifikt, att tillhandahålla standardiserade driftsprotokoll för kulturen av dessa hundorganoid modeller är nyckeln till att karakterisera organoider normala tillväxt under kultur och passaging för att härleda optimala tidpunkter för expansion och underhåll. Hund intestinala organoider odlade med hjälp av protokollet har tidigare kännetecknats av Chandra et al.12.
Ett av de mest kritiska stegen i protokollet är passaging av organoider. Den optimala tiden för den första passagen av lever sfäroider bestämdes vara på dag 7 efter isolering baserat på lever sfäroid mätningar. Den maximala volymen av sfäroider uppnåddes dag 7, och samtidigt började sfäroider att knoppa och bildade leverorganoider. Ökningen av den totala organoidvolymen från dag 2-7 efter isolering var mer än 365 gånger, vilket tyder på att den optimala passagetiden är längre än hundens intestinala organoidkultur. Efter 7 dagar i kultur observerades inga grova tecken på cellulär apoptos i leversfäroiden, även utan rengöring eller passaging (figur 7). Passaging intestinala och leverorganoider kan vara utmanande eftersom förfarandet kan leda till förlust av celler och förändrad livskraft. Resultaten visar att långvarig inkubation av leverorganoider med trypsinliknande proteas (upp till 12 min) inte påverkar subkulturen negativt. Inkubation av organoiderna i trypsinliknande proteas längre än 24 min kan vara skadligt för den efterföljande subkulturen av organoiderna.
Vid suboptimal brott i cellklustren med organoid passagen, mekanisk dissociation i stället för långvarig inkubation med trypsin-liknande proteas kan vara mer fördelaktigt. Om problem uppstår med korrekt dissociation av organoiderna, kan kort virvel av proverna försöka förbättra passageutbytet. Å andra sidan har virvelvindar potential att förstöra en kultur och skada celler, så det bör bara användas när andra förfaranden har misslyckats upprepade gånger. Att bryta leverorganoider i enstaka celler sänker tillväxttakten hos organoiderna, samtidigt som de bryts in i kluster av celler kan avsevärt förbättra deras livskraft. Tio minuter valdes som inkubationstid för det organoida protokollet. En inkubationstid på 12 minuter bedömdes inte vara cytotoxisk jämfört med en inkubation på 24 minuter i det trypsinliknande proteasexperimentet.
Överlevnadsexperimentet bekräftade att hund leverorganoider kunde överleva i upp till 19,5 dagar under ogynnsamma förhållanden (strukturell och näringsmässig utarmning). Organoider som överlevde dessa villkor längst odlades med CMGF + media. Denna observation kan ha orsakats av långsammare tillväxt av leverorganoider i medier som inte kompletterats med Rock inhibitor och GSK3β. Organoid kulturer med CMGF + R/G växte snabbare och kan ha utarmat sina resurser snabbare. Detta experiment öppnar möjligheter att miniatyrisera hundens organoidkultur för att uppnå en hög genomströmningssystemkonvertering. En sådan teknik visar på potentialen att underlätta läkemedelsupptäckt eller toxikologiska studier till en väsentligt reducerad kostnad.
Några vanliga problem som uppstår under hundorganoid kultur underhåll är felaktig prov stelning vid plätering, kultur förorening, och fastställa rätt densitet och storlek av organoider. Om solubiliserad ECM stelnar i förtid under plätering, placera den omedelbart på is i 10 minuter. Om solubiliserad ECM inte bildar kupolliknande strukturer är det troligt att inte tillräckligt med media togs bort från provet. Om så är fallet, späd provet med en mer lösgjord ECM tills kupoler bildas.
När svamp- eller bakterieförorening finns i en hel platta (se figur 4) är den bästa lösningen att kassera plattan. Behandling med svampdödande eller antibiotiska läkemedel kan försökas, men framgången med ett sådant försök är extremt låg. Om en enda brunn är förorenad i en platta kan livskraftiga och opåverkade brunnar rengöras (följ steg 4.1 till 4.5) till en ny platta och övervakas noggrant. Om provet redan har varit Emergency Frozen, är det lämpligt att kassera hela provet, eftersom upptining av provet utsätter inkubatorn för ytterligare föroreningsrisk.
En hälsosam organoidkultur bör åtminstone vara i kategorin medelstorlek och medeldensitet eller större. Optimal densitet är avgörande för organoid kultur tillväxt. Lägre densitet måste korrigeras genom rengöring av organoiderna till medeldensitet. Om situationen med extrem densitet uppstår (överbeläggning) bör organoiderna utökas till fler brunnar. Grova tecken på cellulär apoptos åtföljer ofta både överbefolkning och låg densitet av den organoida kulturen. Om dessa frågor inte korrigeras i tid kommer hela den organoida kulturen att bli apokatisk på några dagar. Om organoider uppnår extra stor storlek eller mycket hög densitet, bör kulturen användas för ett experiment, frysning eller fixering.
Organoidmedierna innehåller för närvarande 17 komponenter, och tillägg av tillväxtfaktorer som behövs för organoid underhåll och expansion kan därför vara dyrt. Detta problem kan lösas genom att växa 2D-cellkulturer som syntetiserar tillväxtfaktorerna för att producera betingade CMGF +. Cellodling L-WRN producerar Wnt-3a, R-Spondin-3 och Noggin tillväxtfaktorer37. Cellkolonin använder 90% DMEM/F12 och 10% FBS-kulturmedier. När kulturen uppnår 90 procent sammanflöde skördas media varje dag i 1 vecka. Det skördade mediet blandas sedan med 2x CMGF+ (utan dessa tillväxtfaktorer). Medan 2D-kulturer kan producera de nödvändiga tillväxtfaktorerna till en bråkdel av kostnaden, måste den extra tiden och förberedelserna för att producera media förväntas. Koncentrationerna av tillväxtfaktorer mellan konditionerade mediepartier kan också skilja sig37,38.
Canine vuxna stamcells-härledda organoidkulturer är en unik biomedicinsk modell som kan bidra till att uppnå målen för One Health Initiative39. Den organoida tekniken kan användas inom många grundläggande och biomedicinska forskningsområden, som sträcker sig från utvecklingsbiologi, patofysiologi, läkemedelsupptäckt och testning, toxikologi till studier av infektionssjukdomar och regenerativ medicin40. Translationell och omvänd translationell forskning är båda områden där hundorganoider är tillämpliga15. Hundar har använts i århundraden i translationella experimentella miljöer, och deras följeslagare djurstatus har också underlättat deras position som en av de mest utforskade arterna inom veterinärmedicin.
Sammanfattningsvis ger detta manuskript standardiserade driftsprotokoll för isolering, underhåll, skörd och biobanking av hund lever och intestinala organoider för att underlätta tillämpningen av denna modell inom olika biomedicinska områden. Denna modell är unikt lämplig för att främja omvänd translationell forskning som ett verktyg i One Health Initiative för att främja ett interdisciplinärt och tvärvetenskapligt kunskapsutbyte.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Författarna vill uttrycka tacksamhet till Veterinary Diagnostic Laboratory of Iowa State University anställda, nämligen Haley M. Lambert, Emily Rahe, Rosalyn M. Branaman, Victoria J. Green och Jennifer M. Groeltz-Thrush, för snabb behandling av de prover som tillhandahålls. Författarna vill bekräfta stöd från Faculty Startup, ISU VPR Miller Award, ISU VPR Miller Award och NSF SBIR-underutmärkelsen till ISU # 1912948.
Materials
| Chelating solution | |||
| D-Sorbitol | Fisher Chemical | BP439-500 | |
| DTT | Promega | V3151 | |
| KCl | Fisher Chemical | P217-500 | |
| KH2PO4 | Sigma | P5655-100G | |
| Na2HPO4-2H2O | Sigma | S5136-100G | |
| NaCl | Fisher Chemical | S271-500 | |
| Pen Strep | Gibco | 15140-122 | |
| Sucrose | Fisher Chemical | S5-500 | |
| Organoid media | |||
| [Leu15]-Gastrin I human | Sigma | G9145-.5MG | |
| A-83-01 | PeproTech | 9094360 | |
| Advanced DMEM/F12 | Gibco | 12634-010 | |
| B27 supplement | Gibco | 17504-044 | |
| FBS | Corning | 35-010-CV | |
| Glutamax | Gibco | 35050-061 | |
| HEPES | VWR Life Science | J848-500ML | |
| Human R-Spondin-1 | PeproTech | 120-38-500UG | |
| Murine EGF | PeproTech | 315-09-1MG | |
| Murine Noggin | PeproTech | 250-38-250UG | |
| Murine Wnt-3a | PeproTech | 315-20-10UG | |
| N2 supplement | Gibco | 17502-048 | |
| N-Acetyl-L-cysteine | Sigma | A9165-25G | |
| Nicotinamide | Sigma | N0636-100G | |
| Primocin | InvivoGen | ant-pm-1 | |
| ROCK inhibitor (Y-27632) | EMD Millipore Corp. | SCM 075 | |
| SB202190 (P38 inhibitor) | Sigma | S7067-25MG | |
| Stemolecule CHIR99021 (GSK3β) | Reprocell | 04-0004-base | |
| Trimethoprim | Sigma | T7883-5G | |
| Sulfamethoxazole | Sigma-Aldrich | S7507-10G | |
| Reagents | |||
| Acetic Acid, Glacial | Fisher Chemical | A38-500 | |
| Dimethyl Sulfoxide (DMSO) | Fisher Chemicals | D128-500 | |
| EDTA, pH 8.0, 0.5 M | Invitrogen | 15575-038 | |
| Formaldehyde (37%) | Fisher Chemical | F79P-4 | |
| Glutaraldehyde solution | Sigma | G5882 | |
| Matrigel Matrix For Organoid Culture | Corning | 356255 | Extracellular Membrane Matrix |
| Paraformaldehyde, 97% | Alfa Aesar | A11313 | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| RNAlater Soln. | Invitrogen | AM7021 | RNA Storage Reagent |
| TrypLE Express | Gibco | 12604-021 | Trypsin-like Protease |
| Other | |||
| 6 Well Cell Culture Plate | Corning | 3516 | |
| ACD Hybez II Hybridization System | ACD a biotechne brand | 321710 | |
| Centrifuge Tube, 15 mL | Corning | 430766 | |
| CoolCell LX | Corning | BCS-405MC | |
| Cryogenic Vials | Corning | 430488 | |
| Disposable Centrifuge Tube (50 mL) | Fisherbrand | 05-539-13 | |
| GyroMini Nutating mixer (Rocker) | Labnet | S0500-230V-EU | |
| Heat Bath | Lab-Line Instruments | 3000 | |
| Mr. Frosty Freezing Container | ThermoFisher Scientific | 5100-0001 | |
| NanoDrop 2000 | ThermoFisher Scientific | ND2000CLAPTOP | SpectrophotometerAnalysis |
| Panasonic incubator | Panasonic | MCO-170ML-PA | |
| Parafilm M Wrapping Film | Bemis Company Inc | PM996/EMD | Laboratory Flexible Film Tape |
| Protected Disposable Scalpels | Bard-Parker | 239844 | |
| RNAscope 2.5 HD Assay – RED | ACD a biotechne brand | 322350 | |
| RNAscope H2O2 & Protease Plus Reagents | ACD a biotechne brand | 322330 | |
| RNAscope Target Retrieval Reagents | ACD a biotechne brand | 322000 | |
| RNAscope Wash Buffer Reagents | ACD a biotechne brand | 310091 | |
| Tissue Culture Dish | Dot Scientific | 6676621 | |
| Tissue Culture Plate 24 wells | Fisherbrand | FB012929 |
References
- Hickman, D. L., Johnson, J., Vemulapalli, T. H., Crisler, J. R., Shepherd, R. Commonly used animal models. Principles of Animal Research for Graduate and Undergraduate Students. , 117-175 (2017).
- De Jong, M., Maina, T. Of mice and humans: Are they the same? – Implications in cancer translational research. Journal of Nuclear Medicine. 51 (4), 501-504 (2010).
- Cannarozzi, G., Schneider, A., Gonnet, G. A phylogenomic study of human, dog, and mouse. PLoS Computational Biology. 3 (1), 0009-0014 (2007).
- Jacob, J. A. Researchers turn to canine clinical trials to advance cancer therapies. JAMA – Journal of the American Medical Association. 315 (15), 1550-1552 (2016).
- Ziegler, A., Gonzalez, L., Blikslager, A. Large animal models: The key to translational discovery in digestive disease research. Cellular and Molecular Gastroenterology and Hepatology. 2 (6), 716-724 (2016).
- Swanson, K. S., et al. Phylogenetic and gene-centric metagenomics of the canine intestinal microbiome reveals similarities with humans and mice. ISME Journal. 5 (4), 639-649 (2011).
- Coelho, L. P., et al. Similarity of the dog and human gut microbiomes in gene content and response to diet. Microbiome. 6 (1), 72 (2018).
- Nguyen, T. L. A., Vieira-Silva, S., Liston, A., Raes, J. How informative is the mouse for human gut microbiota research. DMM Disease Models and Mechanisms. 8 (1), 1-16 (2015).
- Bontempo, V. Nutrition and health of dogs and cats: Evolution of petfood. Veterinary Research Communications. 29, 45-50 (2005).
- Allenspach, K., Gaschen, F. Canine chronic enteropathies: A review. Schweizer Archiv fur Tierheilkunde. 145 (5), 209-222 (2003).
- Tribuddharatana, T., Kongpiromchean, Y., Sribhen, K., Sribhen, C. Biochemical alterations and their relationships with the metabolic syndrome components in canine obesity. Kasetsart Journal – Natural Science. 45 (4), 622-628 (2011).
- Chandra, L., et al. Derivation of adult canine intestinal organoids for translational research in gastroenterology. BMC Biology. 17 (1), 33 (2019).
- Schaefer, K., Rensing, S., Hillen, H., Burkhardt, J. E., Germann, P. G. Is Science the only driver in species selection? An internal study to evaluate compound requirements in the minipig compared to the dog in preclinical studies. Toxicologic Pathology. 44 (3), 474-479 (2016).
- MacArthur Clark, J. The 3Rs in research: A contemporary approach to replacement, reduction and refinement. British Journal of Nutrition. 120, 1-7 (2018).
- Schneider, B., et al. Model-based reverse translation between veterinary and human medicine: The one health initiative. CPT: Pharmacometrics and Systems Pharmacology. 7 (2), 65-68 (2018).
- Lehmann, R., et al. Human organoids: A new dimension in cell biology. Molecular Biology of the Cell. 30 (10), 1129-1137 (2019).
- Sato, T., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Kim, J., Koo, B. K., Knoblich, J. A. Human organoids: model systems for human biology and medicine. Nature Reviews Molecular Cell Biology. 21 (10), 571-584 (2020).
- Jensen, C., Teng, Y. Is it time to start transitioning from 2D to 3D cell culture. Frontiers in Molecular Biosciences. 7, 33 (2020).
- Ho, B. X., Pek, N. M. Q., Soh, B. S. Disease modeling using 3D organoids derived from human induced pluripotent stem cells. International Journal of Molecular Sciences. 19 (4), 936 (2018).
- Truskey, G. A. Human microphysiological systems and organoids as in vitro models for toxicological studies. Frontiers in Public Health. 6, 185 (2018).
- Caipa Garcia, A. L., Arlt, V. M., Phillips, D. H. Organoids for toxicology and genetic toxicology: applications with drugs and prospects for environmental carcinogenesis. Mutagenesis. , (2021).
- Augustyniak, J., et al. Organoids are promising tools for species-specific in vitro toxicological studies. Journal of Applied Toxicology. 39 (12), 1610-1622 (2019).
- Zietek, T., et al. Organoids to study intestinal nutrient transport, drug uptake and metabolism – Update to the human model and expansion of applications. Frontiers in Bioengineering and Biotechnology. 8, 577656 (2020).
- Zietek, T., Rath, E., Haller, D., Daniel, H. Intestinal organoids for assessing nutrient transport, sensing and incretin secretion. Scientific Reports. 5 (1), 1-10 (2015).
- Kar, S. K., et al. Organoids: a promising new in vitro platform in livestock and veterinary research. Veterinary Research. 52 (1), 1-17 (2021).
- Borcherding, D. C., et al. Sa1976 polyphenols reverse the pathologic effects of palmitic acid and high fat diet in canine enteroids. Gastroenterology. 158 (6), 486 (2020).
- Ambrosini, Y. M., et al. Recapitulation of the accessible interface of biopsy-derived canine intestinal organoids to study epithelial-luminal interactions. PLoS ONE. 15 (4), 0231423 (2020).
- Zdyrski, C., et al. Su124 homology directed repair in canine duodenal enteroids to mimic the wild-type P-glycoprotein mutation. Gastroenterology. 160 (6), 625 (2021).
- Li, Y., Tang, P., Cai, S., Peng, J., Hua, G. Organoid based personalized medicine: from bench to bedside. Cell Regeneration. 9 (1), 21 (2020).
- Kurr, L. A., Allenspach, K., Jergens, A., Mochel, J. P. Harnessing the biology of intestinal organoids to accelerate drug discovery in inflammatory bowel disease: A one health approach. The FASEB Journal. 34, 1 (2020).
- Nantasanti, S., et al. Disease modeling and gene therapy of copper storage disease in canine hepatic organoids. Stem Cell Reports. 5 (5), 895-907 (2015).
- Favier, R. P., et al. COMMD1-Deficient dogs accumulate copper in hepatocytes and provide a good model for chronic hepatitis and fibrosis. PLoS ONE. 7 (8), 42158 (2012).
- Kruitwagen, H. S., et al. Long-term survival of transplanted autologous canine liver organoids in a COMMD1-deficient dog model of metabolic liver disease. Cells. 9 (2), 410 (2020).
- Vilgelm, A. E., et al. Fine-needle aspiration-based patient-derived cancer organoids. iScience. 23 (8), 101408 (2020).
- Saxena, K., et al. Human intestinal enteroids: A new model to study human rotavirus infection, host restriction, and pathophysiology. Journal of Virology. 90 (1), 43-56 (2016).
- VanDussen, K. L., Sonnek, N. M., Stappenbeck, T. S. L-WRN conditioned medium for gastrointestinal epithelial stem cell culture shows replicable batch-to-batch activity levels across multiple research teams. Stem Cell Research. 37, 101430 (2019).
- Powell, R. H., Behnke, M. S. WRN conditioned media is sufficient for in vitro propagation of intestinal organoids from large farm and small companion animals. Biology Open. 6 (5), 698-705 (2017).
- Mackenzie, J. S., Jeggo, M. The one health approach-why is it so important. Tropical Medicine and Infectious Disease. 4 (2), 88 (2019).
- Artegiani, B., Clevers, H. Use and application of 3D-organoid technology. Human Molecular Genetics. 27 (2), 99-107 (2018).

