Tarmorganoider hos hunder i et dobbeltkammergjennomtrengelig støttesystem
Summary
Her presenterer vi en protokoll som beskriver kulturen til hundens tarmorganoider i et dobbeltkammer, gjennomtrengelig støttesystem. Organoidsåing i de permeable støttene, monolagsvedlikeholdet og påfølgende legemiddelpermeabilitetseksperimenter er beskrevet.
Abstract
Det gjennomtrengelige støttesystemet brukes vanligvis sammen med tradisjonelle todimensjonale (2D) cellelinjer som et in vitro-verktøy for å evaluere den orale permeabiliteten til nye terapeutiske legemiddelkandidater. Imidlertid har bruken av disse konvensjonelle cellelinjene begrensninger, for eksempel endret uttrykk for tette kryss, delvis celledifferensiering og fravær av viktige nukleare reseptorer. Til tross for disse manglene er Caco-2- og MDCK-modellene allment akseptert og validert for prediksjon av human in vivo oral permeabilitet.
Hunder er en relevant translasjonsmodell for biomedisinsk forskning på grunn av deres likheter i gastrointestinal anatomi og tarmmikroflora med mennesker. Følgelig, og til støtte for parallell legemiddelutvikling, er utarbeidelsen av et effektivt og nøyaktig in vitro-verktøy for å forutsi in vivo legemiddelpermeabilitetsegenskaper både hos hunder og mennesker svært ønskelig. Et slikt verktøy kan være hundens tarmorganoidsystem, preget av tredimensjonale (3D), selvmonterte epitelstrukturer avledet fra voksne stamceller.
(1) Permeable Support Seeding Protocol beskriver eksperimentelle metoder for dissosiering og såing av hundeorganoider i innsatsene. Organoid isolering, kultur og innhøsting av hunder er tidligere beskrevet i et eget sett med protokoller i dette spesialnummeret. Metoder for generell vedlikehold av hundens intestinale organoid monolag er grundig omtalt i (2) Monolayer Maintenance Protocol. I tillegg beskriver denne protokollen metoder for å vurdere monolagets strukturelle integritet via transepitelial elektrisk motstand (TEER) målinger og lysmikroskopi. Til slutt beskriver (3) Permeability Experimental Protocol oppgavene direkte før et eksperiment, inkludert in vitro validering av eksperimentelle resultater.
Samlet sett overvinner hundens organoidmodell, kombinert med en tokammercellekulturteknologi, begrensninger forbundet med 2D-eksperimentelle modeller, og forbedrer dermed påliteligheten av spådommer om den tilsynelatende orale permeabiliteten til terapeutiske legemiddelkandidater både hos hunden og den menneskelige pasienten.
Introduction
Permeable støttesystemer brukes vanligvis til å bestemme den tilsynelatende permeabiliteten til terapeutiske legemiddelkandidater gjennom tarmepitelbarrieren 1,2. De kan også brukes til å vurdere cellulær sekresjon3, cellemigrasjon4 og legemiddeltoksisitet5. In vitro orale legemiddelpermeabilitetsanalyser er et sentralt trinn i legemiddeloppdagelses- og utviklingsprosessen2, med individuelle legemiddelkandidater som testes i det tidlige stadiet av stoffets FoU-livssyklus6. Det permeable støttesystemet er et dobbeltkammercellekulturapparat bestående av en innsats med en semiporøs membran plassert i en multiwell plate. Dette systemet gir direkte tilgang til de apikale og basolaterale sidene av et cellemonolag dyrket i innsatsen7. Monolaget som brukes i disse systemene er vanligvis avledet fra gastrointestinale epitelceller (f.eks. Human kolorektal adenokarsinom Caco-2 cellelinje)8. Cellekulturer vokser i en polarisert tilstand som etterligner den naturlige mikroarkitekturen til tarmepitelceller, noe som muliggjør ytterligere cellulær differensiering, lignende mikroanatomi og funksjon7. Detaljer om det gjennomtrengelige støtteinnlegget finner du i figur 1. Såingen av innsatsene med 2D-cellekulturer, tradisjonelt brukt til å vurdere intestinal legemiddelpermeabilitet, er relativt rimelig og lett å dyrke9. Disse systemene presenterer flere store begrensninger, inkludert deres begrensede kapasitet til å forutsi tarmmetabolismen til terapeutiske legemiddelkandidater10,11. Dette gjelder for alle mekanismer for legemiddelabsorpsjon, det være seg passiv absorpsjon gjennom de tette kryssene mellom epitelceller, aktiv transepitelial absorpsjon gjennom effluks eller opptakstransportører (f.eks. P-glykoprotein, monokarboksylattransportør 1) og legemidler som metaboliseres av enterocytter.
Hunder deler et felles miljø og kosthold med mennesker12. Hundens tarmanatomi og mikrobiomsammensetning ligner på mennesker13, som har blitt tilskrevet domestisering og delte dietter de siste 36 000 årene14. Dessverre kan disse likhetene også være vanlige årsaker /utløsere for sykdomsutvikling. Hunder utvikler lignende kroniske sykeligheter som mennesker, som fedme15, inflammatorisk tarmsykdom16, kolorektal adenokarsinom17, gastrointestinal stromal tumor (GIST)18 og forskjellige andre patologier assosiert med deres relative levetid19. Følgelig kan hundeorganoider med hell brukes til omvendt translasjonsforskning av disse kroniske multifaktorielle sykdommene i ånden av One Health Initiative20.
Caco-2-celler er de mest brukte cellelinjene for legemiddel oral absorpsjonsanalyser21. Disse cellene regnes for tiden som “gullstandard” -modellen for in vitro intestinal permeabilitetsanalyser 2,22,23. Caco-2-cellelinjen uttrykker effluks- og opptakstransportører som finnes i menneskets tarmkanal, men på forskjellige uttrykksnivåer 24,25,26. Caco-2-celler er også mye brukt som modeller for å avgjøre om et stoff er et substrat eller en hemmer av intestinale efflukstransportører22,27. Selv om Caco-2-cellene er av kolon opprinnelse, etterligner de en enterocytcelle. Dessverre representerer Caco-2-celler bare en celletype fra epitellaget i tynntarmen9, som ikke klarer å rekapitulere den komplekse tarmepitelcelletypesammensetningen nøyaktig. For eksempel er begerceller dedikert til slimproduksjon fraværende fra Caco-2-kulturer slik at slim-legemiddelinteraksjoner ikke kan vurderes uten kokultur med andre cellelinjer28. Videre uttrykker ikke Caco-2-kulturer flere av de viktige nukleære reseptorene som vanligvis er tilstede i tarmen, for eksempel pregnane X-reseptor (PXR), steroid X-reseptor (SXR) og konstitutiv androstanreseptor (CAR)29. Følgelig klarer ikke Caco-2-kulturer å modellere induksjonen av legemiddeltransportører og enzymer av visse legemidler som er induktorer av disse reseptorene (f.eks. rifampin)30.
3D intestinal organoid-teknologien adresserer noen av disse begrensningene19. Organoider er selvmonterte konstruksjoner avledet fra voksne stamceller som kan etableres fra vevsprøver høstet ved hjelp av mikroinvasive teknikker20. Menneskeinduserte pluripotente stamceller brukes til intestinale permeabilitetsmodeller31,32. Hundeorganoider gir et relevant alternativ til menneskelige organoider fordi menneskelig stamcelleforskning er begrenset av etiske problemstillinger33. Videre gir hundeorganoider et in vitro-system for å utforske hundens legemiddelpermeabilitet, metabolisme, aktiv transport og legemiddelinteraksjoner. For å løse dette teknologigapet er den konsistente og pålitelige veksten av hundens tarmorganoider i et gjennomtrengelig støttesystem beskrevet34. En permeabilitetsanalyse med hundens tarmorganoider kan potensielt forutsi hundens tarmpermeabilitet og metabolisme av små legemiddelmolekyler sammenlignet med nåværende analyser (Caco-2). Bekreftelse av disse sentrale egenskapene gir dette nye in vitro-systemet til fremtidig arbeid med å utforske den potensielle effekten av induktorer på intracellulær metabolisme og aktiv transport.
Canine organoider består av alle celletyper som vanligvis er tilstede i epitellaget i tarmen. Fra et funksjonelt og mikroanatomisk syn replikerer de pålitelig miljøet i epitellaget av hundens tarm19,35. Videre er tilstedeværelsen av slim, hundespesifikke legemiddeltransportører og enzymer, og generell cellulær differensiering i hundens tarmorganoider sammenlignbar med det som ses in vivo hos hunder34. Dermed kan organoider isoleres fra syke veterinærpasienter og brukes til å modellere effekten av ulike sykdomsprosesser (f.eks. Kronisk tarmbetennelse) på hundens orale legemiddelpermeabilitet19,36. Hundens tarmorganoidsystem kan også brukes i andre innstillinger enn eksperimenter med legemiddelpermeabilitet. Disse 3D-strukturene kan også isoleres fra syke pasienter som tidligere beskrevet av Chandra et al. for inflammatorisk tarmsykdom, kolorektal adenokarsinom og gastrointestinal stromal tumor19.
Permeable Support Seeding Protocol beskriver metoder for å etablere tarmorganoidkulturer hos hunder i innleggene. Denne første protokollen skisserer metoder for å dissosiere etablerte hundeorganoidkulturer belagt i den ekstracellulære membranmatrisen. Videre diskuteres forfyllingen av innsatsene med kollagen I og den ekstracellulære membranmatrisen i denne protokollen. Innebygging av hundeorganoider i de permeable støtteinnsatsene er også beskrevet i detalj.
Den andre protokollen er Monolayer Maintenance Protocol, som inkluderer generell vedlikehold av hundens 3D-organoider belagt i et innlegg. Frekvensen og volumene av organoidmediet som brukes til å oppdatere kulturen, og måter å forhindre cellekulturskader på, presenteres i denne andre protokollen, sammen med eksperimentelle metoder for å vurdere sammenløpet av epitelmonolaget.
Endelig fokuserer permeabilitetseksperimentell protokoll på måter å avgjøre om hundens intestinale 3D-organoider i en permeabilitetsanalyse er klare for eksperimentell bruk og verifikasjonstrinnene som trengs før du utfører et eksperiment. Denne delen beskriver også oppsettet og vellykket gjennomføring av et permeabilitetseksperiment, sammen med inkubasjon og prøvetaking av terapeutiske legemiddelkandidater i kamrene i monolagskulturen. Bruken av fluoresceinisotiocyanat med lav permeabilitet (FITC-dextran) for å overvåke monolagsintegritet diskuteres også. Til slutt beskrives en in vitro evalueringsmetode for validering av resultatene etter avslutningen av et eksperiment. Permeabilitetseksperimenter er et ekstremt stort tema og er veldig godt oppsummert av Hubatsch et al.37. Arbeidsflyten til protokollene er oppsummert i figur 2.
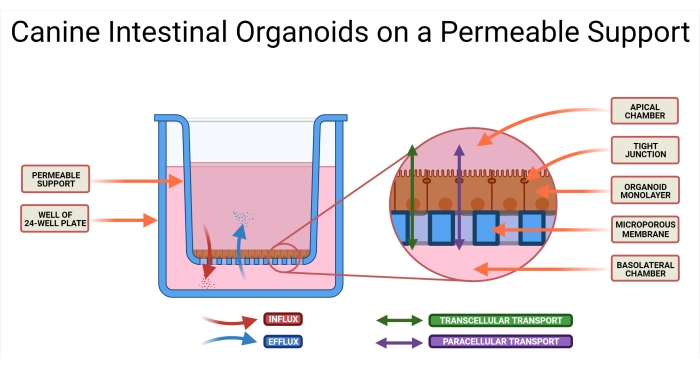
Figur 1: Tarmorganoider hos hunder på et gjennomtrengelig støttesystem. Den permeable støtteinnsatsen er plassert i en brønn på en 24-brønns plate. Den mikroporøse membranen tillater såing av dissosierte tarmorganoider hos hunder, og disse cellene vil til slutt danne et organoid 2D-monolag. Denne teknologien gir tilgang til både AP- og BL-sidene av monolaget. Organoid medium er introdusert i både AP- og BL-kamrene i den gjennomtrengelige støtten. Absorpsjonen (AP→BL) og sekresjonen (BL→AP) av legemiddelkandidaten er illustrert, samt to mulige former for narkotikatransport. Forkortelser: AP = apikal; BL = basolateral. Klikk her for å se en større versjon av denne figuren.
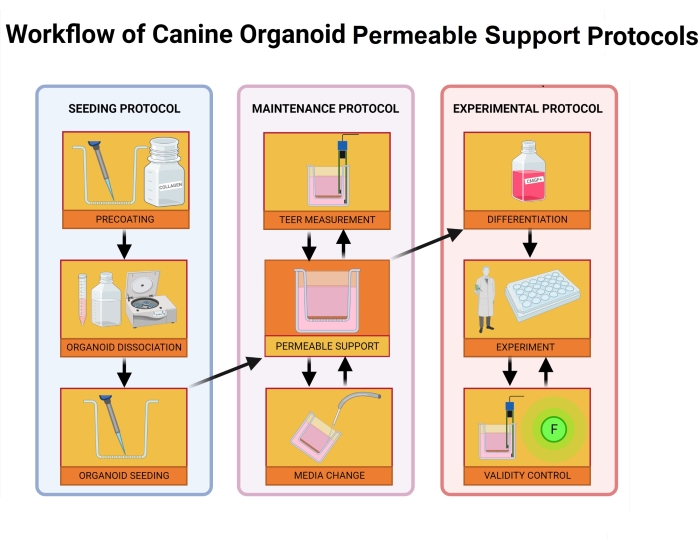
Figur 2: Arbeidsflyt for hundeorganoidpermeable støtteprotokoller. Den permeable støtteinnsatsen er forbelagt med en blanding av den ekstracellulære membranmatrisen og kollagen I og inkuberes i 1 time. Under inkubasjonsprosessen dissosieres organoidkulturen. Individuelle organoidceller blir sådd i innsatsen, medium i basolateralt kammer tilsettes umiddelbart etter såing, mens medium til apikalt kammer tilsettes 24 timer etter at såprosessen er avsluttet. Vedlikehold og overvåking av organoider inkluderer regelmessige mediumendringer, TEER-verdimålinger og lysmikroskopi for å evaluere monolagets integritet. Før forsøket må organoidene differensieres ved å fjerne ROCK-hemmer og GSKiβ fra mediet. TEER-verdiene måles på forsøksdagen, og det organoide monolaget inspiseres via lysmikroskopi for skade på cellene. Medium byttes deretter ut med en passende buffer og inkuberes før eksperimentet. FITC-dextran-analysen brukes under intestinal permeabilitetseksperimenter39 som en markør for monolagsintegritet. TEER-målinger tas etter forsøket, og lysmikroskopi vil validere resultatene etter 24 timer. Forkortelser: TEER = transepitelial elektrisk motstand; ROCK = rho-assosiert kinase; GSKiβ = glykogensyntasekinase beta; F = fluorescens. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Canine intestinal organoid kulturer i det gjennomtrengelige støtteapparatet er et unikt konsept som forbinder tradisjonelle legemiddelpermeabilitetsanalyser40 med en ny in vitro hundemodell41. Ulike typer tarmorganoider fra hunder kan brukes og evalueres basert på målet med forsøket med minimale justeringer. Det anbefales å teste flere konsentrasjoner av stoffet av interesse i 3-4 brønner per gruppe. Konsentrasjonene kan være basert på forventet tarmkonsentrasjon av legemidlet. Videre kan bruk av tidligere forskning bidra til å bestemme passende tidspunkter for studiedesignet. Passende dokumentasjon av studiedesign bør gjøres for å øke replikerbarheten og bistå i feilsøking.
Denne teknologien har flere begrensninger på grunn av nyheten av metoden42, hovedsakelig på grunn av mangel på standardisering i eksperimentell design og utførelse av protokollen på tvers av laboratorier. Denne mangelen på standardisering har blitt anerkjent av andre grupper43, og Canine 3D Organoid Monolayer Protocols vil føre til interlaboratorisk reproduserbarhet og introdusere standardisering til dette systemet. Standardiserte tilnærminger til dataanalyse forbedrer replikerbarheten og kan styrke resultatene av foreløpig narkotikatesting ved bruk av hundeorganoider i det gjennomtrengelige støttesystemet på tvers av forskjellige laboratorier. Hundens 3D-organoidmodell mangler også datasett som sammenligner in vitro Papp-verdier av modellmedikamenter med deres kjente humane eller hund in vivo intestinal absorpsjon, omtrent som Caco-2-celler 44,45,46. Når slike data er generert, kan denne hundeorganoidmodellen brukes til å vurdere intestinal permeabilitet under legemiddelutvikling.
Det er avgjørende at det tas hensyn når man sår organoider på det permeable støttesystemet for å frø en høy nok tetthet av passende dissosierte celler. TEER-verdiene til systemet er mer pålitelige og reproduserbare når de dyrkes i strenge monolag. Langvarig kultur av monolagene kan føre til en eksponentiell økning i TEER-verdier som når videre fra tarmens fysiologiske verdier. H&E-seksjoner av slike 3D-strukturer viser deretter flere lag med celler over hverandre med endrede strukturer av enterocytter nærmere membranen.
Etter vellykket utvidelse av hundens intestinale organoid monolag, kan resultatene analyseres på samme måte som tradisjonelle 2D-celleanalyser ved å beregne et legemiddels tilsynelatende permeabilitetskoeffisient (Papp) formel44. P-appverdien (se Eq (2)) beskriver transporthastigheten over mobilmonolaget47.
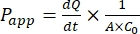 (2)
(2)
Det 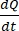 er den første helningen av konsentrasjonen versus tidskurven (f.eks. nmol / s). A er innsatsområdet (cm2), og C0 er den opprinnelige konsentrasjonen av legemidlet eller forbindelsen i donorkammeret37. Pålitelig anerkjennelse av monolagsintegritet er en avgjørende del av permeabilitetsanalysen som krever standardisering. Lysmikroskopi og TEER-målinger anbefales for å vurdere hundeorganoider i et gjennomtrengelig støttesystem og bidra til å bestemme riktig tidspunkt for forsøket. I tillegg kan nullmolekylære permeabilitetsmarkører (f.eks. FITC-dextran, Lucifer gul, PEG-400) brukes til å funksjonelt evaluere organoid monolagsintegritet. Det må tas hensyn til om forbindelsen som testes påvirkes av en transportør. P-glykoprotein (P-gp) brukes som et vanlig eksempel på efflukspumpe. Det må genereres et effluksforhold (Papp,BL-AP/Papp,AP-BL) sammenlignet med et velkjent P-gp sondesubstrat.
er den første helningen av konsentrasjonen versus tidskurven (f.eks. nmol / s). A er innsatsområdet (cm2), og C0 er den opprinnelige konsentrasjonen av legemidlet eller forbindelsen i donorkammeret37. Pålitelig anerkjennelse av monolagsintegritet er en avgjørende del av permeabilitetsanalysen som krever standardisering. Lysmikroskopi og TEER-målinger anbefales for å vurdere hundeorganoider i et gjennomtrengelig støttesystem og bidra til å bestemme riktig tidspunkt for forsøket. I tillegg kan nullmolekylære permeabilitetsmarkører (f.eks. FITC-dextran, Lucifer gul, PEG-400) brukes til å funksjonelt evaluere organoid monolagsintegritet. Det må tas hensyn til om forbindelsen som testes påvirkes av en transportør. P-glykoprotein (P-gp) brukes som et vanlig eksempel på efflukspumpe. Det må genereres et effluksforhold (Papp,BL-AP/Papp,AP-BL) sammenlignet med et velkjent P-gp sondesubstrat.
Lysmikroskopi (vanlig eller forbedret med fasekontrast) er en uvurderlig metode for å kontrollere integriteten til 2D- eller 3D-monolaget og filterinnsatsen mens du vurderer mulig cellulær gjengroing. Figur 7 kan tjene som en veiledning for å gjenkjenne sunne tarmorganoidcellekulturer hos hunder. TEER-verdier er et viktig mål på dannelsen av intercellulære veikryss og differensiering av organoidkulturene til et intakt tarmepitel. Hundens tarmorganoider skiller seg ut i enterocytter og begerceller (figur 6). Disse slimproduserende cellene tillater studier av legemiddel-slim-interaksjoner, noe som har vært vanskelig å oppnå ved bruk av tradisjonelle 2D-cellekulturer48. Tilstedeværelsen av enteroendokrine celler har tidligere blitt bekreftet i hundens tarmorganoider av Chandra et al.33.
Ytterligere karakterisering av hundens organoid monolag avledet fra jejunal-, ileal- og kolonorganoider ved bruk av TEM er gitt. TEM-bilder viser cellulær mikroarkitektur, inkludert tette kryss og mikrovillidannelse, noe som ytterligere illustrerer kompleksiteten og nytten av disse organoidmodellene i translasjonsmedisin. Basert på de eksperimentelle resultatene var organoidkulturene på den permeable støtten klare for eksperimentering mellom dag 11 og dag 13 etter såing (figur 9). TEER-verdiene på dette tidspunktet varierte mellom 1 500 og 2 500 Ω,cm2. Platåfasen med TEER-verdier varer i et svært begrenset tidsvindu der eksperimentet må startes før TEER-verdiene begynner å avta sakte. TEER-verdier kan også være en avgjørende del av å vise viktige eksperimentelle resultater, da noen stoffer eller hjelpestoffer kan interagere med monolaget (f.eks. Tette kryss), noe som i stor grad kan påvirke TEER-verdiavlesningene. Dette alene kan tjene som data for et eksperiment.
Canine intestinal organoider i et dobbeltkammercellekulturapparat kan brukes på andre felt enn oral legemiddelpermeabilitet på grunn av den unike arkitekturen til det resulterende cellemonolaget. For eksempel kan de brukes i mikrobiologisk forskning (f.eks. Virkningen av å endre GI mikrobiell flora), virale opptaksstudier, legemiddelinteraksjoner og narkotikatransportmekanismer49. Donorkammeret er vanligvis fylt med testmedikamentet eller forbindelsen av valg, og aliquots fra mottakerkammeret tas på forskjellige tidspunkter. Disse aliquotene kan analyseres ved hjelp av høyytelses væskekromatografi, massespektrometri, enzymbundet immunosorbentanalyse eller andre teknikker for å bestemme mengden og hastigheten som løsningsmidlet gjennomsyrer gjennom monolaget.
Disse studiene krever et intakt monolag for å vurdere legemiddelpermeabilitet nøyaktig. Dette krever vanligvis voksende monolag som overstiger de som trengs for å ta hensyn til ubrukelige brønner. Organoidcellemonolag kan også brukes til å måle viralt opptak enten fra apikal eller basal side av et monolag, med avlesninger inkludert immunfluorescensanalyser – ved bruk av antistoffer for å oppdage virusets cellulære opptak. Endelig kan flere legemidler (dvs. substrat og inhibitor) påføres donorkammeret for å identifisere transportørbaserte legemiddelinteraksjoner.
Basert på de nåværende observasjonene, vil disse metodene ikke bare være anvendelige for hundeorganoider i kulturinnsatser, men vil også være egnet for andre veterinære arter og organsystemer, med mindre modifikasjoner som trengs for å passe best til den valgte arten eller organmodellen. Protokoller for vekst av tarmorganoider hos hunder måtte justeres basert på kulturens unike egenskaper. Dermed kan protokollen justeres til en annen art, men vil kreve subtile endringer i protokollen. Modifikasjoner kan begynne med endringer i cellesåingstettheten og utvides til endringer i mediesammensetningen for å skille organoider av interesse på riktig måte.
Standardisering, detaljert dokumentasjon av eksperimentelle prosedyrer og konsekvent overvåking av cellemonolagene er avgjørende praksis som trengs på tvers av de gjennomtrengelige støtteanalysene og er ikke begrenset til hundesystemet. Disse mulige artene eller organmodifikasjonene er avgjørende for å dokumentere og rapportere for videre fremskritt på feltet. Denne modellen har flere begrensninger, for eksempel kostnadskrav, interlaboratorisk variabilitet og begrensede data om evnen til å forutsi intestinal absorpsjon in vivo. Hunder har i noen tilfeller forskjellige stofftransportører og metaboliserende enzymer enn mennesker50.
Videre må hundens organoidsystem testes på en rekke andre dobbeltkammerapparater fra andre produsenter for å bestemme egnetheten til en slik modell (f.eks. Egnetheten til forskjellige filtermembransammensetninger må bestemmes). En annen ulempe er at legemiddelpermeabilitetseksperimentets del av manuskriptet er mindre beskrivende enn de foregående delene. Dette skyldes et overskudd av informasjon på dette feltet. Målet for denne delen av manuskriptet var å beskrive disse metodene på en modifiserbar måte uten å kutte kantene på hjørnesteinene i disse eksperimentene. Mer detaljert informasjon om permeabilitetseksperimenter er samlet inn av Hubatsch et al.37. I tillegg kan permeable innsatser brukes i kokultur, cellemigrasjon og invasjonsanalyseeksperimenter4.
Avslutningsvis har hundens tarmorganoider i tokammerkulturapparater potensial til å bli brukt i et bredt spekter av applikasjoner, inkludert biomedisinske felt og translasjonsmedisin, for å nevne noen. Protokollene skaper flere strategier for å planlegge et eksperiment og fremme interlaboratorisk dataavhengighet for organoidmodeller på tvers av biologifeltet.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi ønsker å uttrykke takknemlighet til Veterinær Diagnostic Laboratory of Iowa State University ansatte, nemlig Haley Lambert, Emily Rahe, Rosalyn Branaman, Victoria Green, og Jennifer Groeltz-Thrush, for rettidig behandling av prøver. Vi vil også takke Jodi Smith og Bethann Valentine for å gi materiale til permeabilitetseksperimentene. Vi vil også takke David Diaz-Reganon for hans hjelp med figur 9. Med unntak av figur 6 er alle figurer laget i BioRender.com. Forfatterne ønsker å anerkjenne støtte fra fakultetet Oppstart, ISU VPR Miller Award, ISU VPR Miller Award, og NSF SBIR subaward til ISU # 1912948.
Materials
| Organoid media | |||
| ROCK inhibitor (Y-27632) | EMD Millipore Corp. | SCM 075 | |
| [Leu15]-Gastrin I human | Sigma | G9145-.5MG | |
| A-83-01 | PeproTech | 9094360 | |
| Advanced DMEM/F12 | Gibco | 12634-010 | |
| B27 supplement | Gibco | 17504-044 | |
| FBS | Corning | 35-010-CV | |
| Glutamax | Gibco | 35050-061 | glutamine substitute |
| HEPES | VWR Life Science | J848-500ML | |
| Human R-Spondin-1 | PeproTech | 120-38-500UG | |
| Murine EGF | PeproTech | 315-09-1MG | |
| Murine Noggin | PeproTech | 250-38-250UG | |
| Murine Wnt-3a | PeproTech | 315-20-10UG | |
| N2 supplement | Gibco | 17502-048 | |
| N-Acetyl-L-cysteine | Sigma | A9165-25G | |
| Nicotinamide | Sigma | N0636-100G | |
| Primocin | InvivoGen | ant-pm-1 | |
| SB202190 (P38 inhibitor) | Sigma | S7067-25MG | |
| Stemolecule CHIR99021 (GSK3β) | Reprocell | 04-0004-base | |
| TMS (trimethoprim sulfate) | Sigma | T7883-5G | |
| Reagents | |||
| Acetic Acid, Glacial | Fisher Chemical | A38-500 | |
| alpha-D(+)-Glucose, 99+%, anhydrous | Acros Organics | 170080010 | |
| Cell Recovery Solution | Corning | 354253 | |
| Collagen I, Rat Tail 3 mg/mL | Gibco | A10483-01 | |
| FITC-CM-Dextran | Millipore Sigma | 68059-1G | |
| Formaldehyde (37%) | Fisher Chemical | F79P-4 | |
| Glutaraldehyde solution | Sigma | G5882 | |
| HBSS (1x) | Gibco | 14025-076 | |
| Matrigel Matrix For Organoid Culture | Corning | 356255 | Extracellular Membrane Matrix |
| Paraformaldehyde, 97% | Alfa Aesar | A11313 | |
| PBS, 1x (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| TrypLE Express | Gibco | 12604-021 | Trypsin-like Protease |
| Materials and Equipment | |||
| 15 mL Centrifuge Tube | Corning | 430766 | |
| 9" Pasteur Pipets | Fisherbrand | 13-678-6B | |
| Corning Transwell 6.5 mm Polyester Membrane Inserts Preloaded in 24-Well Culture Plates, Pore Size: 0.4 µm, Sterile | Corning | 3470 | Permeable Support |
| Millicell ERS (Probes) | Millipore Sigma | MERSSTX01 | |
| Millicell ERS-2 Voltohmmeter | Millipore Sigma | MERS00002 | |
| Panasonic incubator | Panasonic | MCO-170ML-PA | |
| Parafilm M Wrapping Film | Bemis Company Inc | PM996/EMD | Flexible Laboratory Film |
| Tissue Culture Plate 24 wells | Fisherbrand | FB012929 |
References
- Ghaffarian, R., Muro, S. Models and methods to evaluate transport of drug delivery systems across cellular barriers. Journal of Visualized Experiments JoVE. (80), e50638 (2013).
- Youhanna, S., Lauschke, V. M. The Past, present and future of intestinal in vitro cell systems for drug absorption studies. Journal of Pharmaceutical Sciences. 110 (1), 50-65 (2021).
- Belic, S., et al. Comparative analysis of inflammatory cytokine release and alveolar epithelial barrier invasion in a transwell®bilayer model of mucormycosis. Frontiers in Microbiology. 3204, 3204 (2019).
- Justus, C. R., Leffler, N., Ruiz-Echevarria, M., Yang, L. V. In vitro cell migration and invasion assays. Journal of Visualized Experiments: JoVE. (88), e51046 (2014).
- Rönkkö, S., Vellonen, K. S., Järvinen, K., Toropainen, E., Urtti, A. Human corneal cell culture models for drug toxicity studies. Drug Delivery and Translational Research. 6 (6), 660-675 (2016).
- Dahlgren, D., Lennernäs, H. Intestinal permeability and drug absorption: predictive experimental, computational and in vivo approaches. Pharmaceutics. 11 (8), 411 (2019).
- Schoultz, I., Keita, &. #. 1. 9. 7. ;. V. The intestinal barrier and current techniques for the assessment of gut permeability. Cells. 9 (8), 1909 (2020).
- Hilgers, A. R., Conradi, R. A., Burton, P. S. Caco-2 cell monolayers as a model for drug transport across the intestinal mucosa. Pharmaceutical Research. 7 (9), 902-910 (1990).
- Natoli, M., Leoni, B. D., D’Agnano, I., Zucco, F., Felsani, A. Good Caco-2 cell culture practices. Toxicology in Vitro. 26 (8), 1243-1246 (2012).
- Kapałczyńska, M., et al. 2D and 3D cell cultures – a comparison of different types of cancer cell cultures. Archives of Medical Science. 14 (4), 910-919 (2018).
- Sun, H., Chow, E. C. Y., Liu, S., Du, Y., Pang, K. S. The Caco-2 cell monolayer: Usefulness and limitations. Expert Opinion on Drug Metabolism and Toxicology. 4 (4), 395-411 (2008).
- Chandler, M., et al. Obesity and associated comorbidities in people and companion animals: a One Health perspective. Journal of Comparative Pathology. 156 (4), 296-309 (2017).
- Coelho, L. P., et al. Similarity of the dog and human gut microbiomes in gene content and response to diet. Microbiome. 6 (1), 72 (2018).
- Galeta, P., Lázničková-Galetová, M., Sablin, M., Germonpré, M. Morphological evidence for early dog domestication in the European Pleistocene: New evidence from a randomization approach to group differences. Anatomical Record. 304 (1), 42-62 (2021).
- Kleinert, M., et al. Animal models of obesity and diabetes mellitus. Nature Reviews Endocrinology. 14 (3), 140-162 (2018).
- Allenspach, K., Wieland, B., Gröne, A., Gaschen, F. Chronic enteropathies in dogs: Evaluation of risk factors for negative outcome. Journal of Veterinary Internal Medicine. 21 (4), 700-708 (2007).
- Wang, J., et al. Proliferative and invasive colorectal tumors in pet dogs provide unique insights into human colorectal cancer. Cancers. 10 (9), 330 (2018).
- Gillespie, V., Baer, K., Farrelly, J., Craft, D., Luong, R. Canine gastrointestinal stromal tumors: Immunohistochemical expression of CD34 and examination of prognostic indicators including proliferation markers Ki67 and AgNOR. Veterinary Pathology. 48 (1), 283-291 (2011).
- Chandra, L., et al. Derivation of adult canine intestinal organoids for translational research in gastroenterology. BMC Biology. 17 (1), 33 (2019).
- Schneider, B., et al. Model-based reverse translation between veterinary and human medicine: the One Health initiative. CPT: Pharmacometrics and Systems Pharmacology. 7 (2), 65-68 (2018).
- Artursson, P., Palm, K., Luthman, K. Caco-2 monolayers in experimental and theoretical predictions of drug transport. Advanced Drug Delivery Reviews. 22 (1-2), 67-84 (1996).
- Balimane, P. V., Han, Y. H., Chong, S. Current industrial practices of assessing permeability and P-glycoprotein interaction. AAPS Journal. 8 (1), 1-13 (2006).
- Sambuy, Y., et al. The Caco-2 cell line as a model of the intestinal barrier: Influence of cell and culture-related factors on Caco-2 cell functional characteristics. Cell Biology and Toxicology. 21 (1), 1-26 (2005).
- Calcagno, A. M., Ludwig, J. A., Fostel, J. M., Gottesman, M. M., Ambudkar, S. V. Comparison of drug transporter levels in normal colon, colon cancer, and caco-2 cells: Impact on drug disposition and discovery. Molecular Pharmaceutics. 3 (1), 87-93 (2006).
- Hilgendorf, C., et al. Expression of thirty-six drug transporter genes in human intestine, liver, kidney, and organotypic cell lines. Drug Metabolism and Disposition. 35 (8), 1333 (2007).
- Seithel, A., Karlsson, J., Hilgendorf, C., Björquist, A., Ungell, A. L. Variability in mRNA expression of ABC- and SLC-transporters in human intestinal cells: Comparison between human segments and Caco-2 cells. European Journal of Pharmaceutical Sciences. 28 (4), 291-299 (2006).
- Volpe, D. A. Transporter assays as useful in vitro tools in drug discovery and development. Expert Opinion on Drug Discovery. 11 (1), 91-103 (2016).
- Hoffmann, P., et al. Caco-2/HT29-MTX co-cultured cells as a model for studying physiological properties and toxin-induced effects on intestinal cells. PLoS ONE. 16 (10), 257824 (2021).
- Sun, H., Chow, E. C. Y., Liu, S., Du, Y., Pang, K. S. The Caco-2 cell monolayer: Usefulness and limitations. Expert Opinion on Drug Metabolism and Toxicology. 4 (4), 395-411 (2008).
- Thummel, K. E., et al. Transcriptional control of intestinal cytochrome P-4503A by 1α,25-dihydroxy vitamin D3. Molecular Pharmacology. 60 (6), 1399-1406 (2001).
- Kodama, N., et al. Characteristic analysis of intestinal transport in enterocyte-like cells differentiated from human induced pluripotent stem cells. Drug Metabolism and Disposition. 44 (10), 1662-1667 (2016).
- Akazawa, T., et al. Application of intestinal epithelial cells differentiated from human induced pluripotent stem cells for studies of prodrug hydrolysis and drug absorption in the small intestine. Drug Metabolism and Disposition: The Biological Fate of Chemicals. 46 (11), 1497-1506 (2018).
- Lo, B., Parham, L. Ethical issues in stem cell research. Endocrine Reviews. 30 (3), 204-213 (2009).
- Ambrosini, Y. M., et al. Recapitulation of the accessible interface of biopsy-derived canine intestinal organoids to study epithelial-luminal interactions. PLoS ONE. 15 (4), 0231423 (2020).
- Zdyrski, C., et al. Su124 homology directed repair in canine duodenal enteroids to mimic the wild-type P-glycoprotein mutation. Gastroenterology. 160 (6), 625 (2021).
- Nantasanti, S., et al. Disease modeling and gene therapy of copper storage disease in canine hepatic organoids. Stem Cell Reports. 5 (5), 895-907 (2015).
- Hubatsch, I., Ragnarsson, E. G. E., Artursson, P. Determination of drug permeability and prediction of drug absorption in Caco-2 monolayers. Nature Protocols. 2 (9), 2111-2119 (2007).
- Gabriel, V., et al. Standardization and maintenance of 3D canine hepatic and intestinal organoid cultures for use in biomedical research. Journal of Visualized Experiments: JoVE. (179), e63515 (2022).
- Frost, T. S., Jiang, L., Lynch, R. M., Zohar, Y. Permeability of epithelial/endothelial barriers in transwells and microfluidic bilayer devices. Micromachines. 10 (8), 533 (2019).
- van Breemen, R. B., Li, Y. Caco-2 cell permeability assays to measure drug absorption. Expert Opinion on Drug Metabolism and Toxicology. 1 (2), 175-185 (2005).
- Huch, M., Knoblich, J. A., Lutolf, M. P., Martinez-Arias, A. The hope and the hype of organoid research. Development. 144 (6), 938-941 (2017).
- Sato, T., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Olivatti, T. O. F., Alcantara, G. P., Lemos, A. C. C. E., Silva, M. G., Miot, H. A. Standardization of organoid culture for evaluation of melanogenesis induced by UVB, UVA and visible light. Anais Brasileiros de Dermatologia. 95 (1), 46-51 (2020).
- Volpe, D. A., et al. Classification of drug permeability with a Caco-2 cell monolayer assay. Clinical Research and Regulatory Affairs. 24 (1), 39-47 (2007).
- Chen, C., Ma, M. G., Fullenwider, C. L., Chen, W. G., Sadeque, A. J. M. Biopharmaceutics permeability classification of lorcaserin, a selective 5-hydroxytryptamine 2C agonist: Method suitability and permeability class membership. Molecular Pharmaceutics. 10 (12), 4739-4745 (2013).
- Jarc, T., et al. Demonstrating suitability of the Caco-2 cell model for BCS-based biowaiver according to the recent FDA and ICH harmonised guidelines. Journal of Pharmacy and Pharmacology. 71 (8), 1231-1242 (2019).
- Newby, D., Freitas, A. A., Ghafourian, T. Decision trees to characterise the roles of permeability and solubility on the prediction of oral absorption. European Journal of Medicinal Chemistry. 90, 751-765 (2015).
- Navabi, N., McGuckin, M. A., Lindén, S. K. Gastrointestinal cell lines form polarized epithelia with an adherent mucus layer when cultured in semi-wet interfaces with mechanical stimulation. PLoS ONE. 8 (7), 68761 (2013).
- Puschhof, J., et al. Intestinal organoid cocultures with microbes. Nature Protocols. 16 (10), 4633-4649 (2021).
- Martinez, M. N., Mochel, J. P., Neuhoff, S., Pade, D. Comparison of canine and human physiological factors: understanding interspecies differences that impact drug pharmacokinetics. The AAPS Journal. 23 (3), 59 (2021).

