Analisi della forma della linea di spettri NMR dinamici per caratterizzare i riarrangiamenti delle sfere di coordinazione in un complesso di poliidruro di renio chirale
Summary
L’analisi della forma della linea degli spettri NMR raccolti su un intervallo di temperature serve come guida per il riarrangiamento degli atomi della sfera di coordinazione interna in un complesso chirale, a otto coordinate, poliidruro di renio (V), ReH5 (PPh3) 2 (ammina sec-butile). L’analisi della forma della linea viene anche utilizzata per determinare i parametri di attivazione ΔH‡, ΔS‡ e ΔG‡ per questi riarrangiamenti atomici.
Abstract
La spettroscopia di risonanza magnetica nucleare (NMR) a soluzione dinamica è il metodo tipico per caratterizzare i riarrangiamenti dinamici degli atomi all’interno della sfera di coordinazione per i complessi di poliidruro dei metalli di transizione. L’adattamento della forma della linea degli spettri NMR dinamici può portare a stime per i parametri di attivazione dei processi di riarrangiamento dinamico. Una combinazione di spettroscopia NMR dinamica 31 P-{1 H} di atomi di fosforo legati al metallo con spettroscopia NMR dinamica 1H-{31P} di ligandi idruriche può identificare riarrangiamenti di leganti idruro che si verificano in concomitanza con un riarrangiamento atomico di fosforo. Per le molecole che presentano una tale coppia accoppiata di riarrangiamenti, la spettroscopia NMR dinamica può essere utilizzata per testare modelli teorici per i riarrangiamenti del ligando. La spettroscopia NMR dinamica 1H-{31P} e il line shape fitting possono anche identificare la presenza di un processo di scambio che sposta uno specifico ligando dell’idruro oltre la sfera di coordinazione interna del metallo attraverso uno scambio protonico con una molecola di solvente come l’acqua avventizia. La preparazione di un nuovo composto, ReH5 (PPh3) 2 (sec-butililammina), che esemplifica molteplici processi di riarrangiamento dinamico è presentata insieme all’adattamento della forma della linea degli spettri NMR dinamici del complesso. I risultati del fitting della forma della linea possono essere analizzati dall’equazione di Eyring per stimare i parametri di attivazione per i processi dinamici identificati.
Introduction
La spettroscopia NMR è comunemente usata per caratterizzare i processi dinamici che si verificano all’interno o tra le molecole. Per molti semplici riarrangiamenti intramolecolari, la stima di ΔG‡ è semplice come misurare la differenza di frequenza, Δν, tra due risonanze al limite di scambio lento e determinare la temperatura di coalescenza per quelle stesse risonanze (Figura 1)1. La relazione,
ΔG‡ = 4,575 x 10-3 kcal/mol x T c [9,972 + log (Tc/Δν)]
dove Tc è la temperatura di coalescenza per una coppia di risonanze che rappresentano la forma di scambio lento di un campione dinamico, può essere usata per risolvere l’energia libera di attivazione per tale riarrangiamento dinamico. Sistemi dinamici più complessi richiedono l’adattamento a forma di linea di spettri NMR dinamici o un’altra tecnica NMR come la spettroscopia di scambio bidimensionale (2D-EXSY) o la spettroscopia ad effetto Overhauser a telaio rotante bidimensionale (2D-ROESY) per stimare i parametri di attivazione.
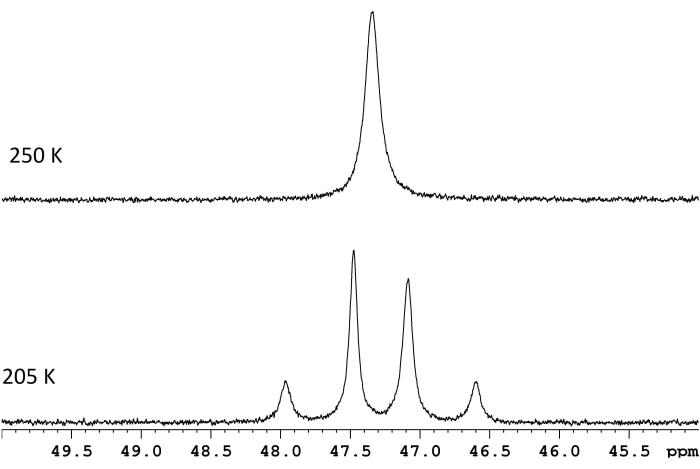
Figura 1: Spettri NMR per una soluzione d 8-toluene di ReH5(PPh3)2(sec-butililammina) a due temperature. La differenza di frequenza tra i due doppietti a scambio lento (traccia inferiore, 117,8 Hz) e una temperatura di coalescenza di 250 K (traccia superiore) corrispondono a una barriera di energia (ΔG‡) di 11,8 kcal/mol. Fare clic qui per visualizzare una versione più grande di questa figura.
Il Line Shape Fitting degli spettri NMR dinamici è una tecnica comune che è stata a lungo utilizzata per la stima dei parametri di attivazione che descrivono i riarrangiamenti dinamici per sostanze con un’energia di attivazione di circa 5-25 kcal/mol 2,3,4,5. La determinazione delle barriere energetiche allo scambio protonico tra acqua e molecole amminiche6, la barriera energetica alla rotazione attorno al legame C-N nella dimetilformammide7, o la dimensione generale delle frazioni organiche8 sono solo alcuni esempi delle molte proprietà che sono state valutate attraverso il line shape fitting di spettri NMR dinamici. Questo manoscritto dimostra l’uso del line shape fitting per caratterizzare i processi dinamici intermolecolari e intramolecolari che si verificano per il complesso ReH5 (PPh3) 2 (sec-butililammina). Gli obiettivi di questo e di altri simili esperimenti NMR sono: 1) caratterizzare tutti i processi di scambio atomico dinamico intramolecolare osservabili NMR se presenti, 2) identificare e caratterizzare i processi di scambio atomico dinamico intramolecolare osservabili NMR se presenti, 3) identificare gli scambi atomici intramolecolari correlati che si verificano, in questo esempio, sia per gli atomi di idrogeno che di fosforo, e 4) per l’esempio qui presentato, confrontare due modelli pubblicati per i processi dinamici che si verificano nel complesso ReH5 (PPh3) 2 (sec-butililammina).
I sistemi di poliidruro di renio (V) a otto coordinate sono sistemi dinamici complessi in cui i ligandi partecipano a più processi dinamici e gli atomi di fosforo possono partecipare a un singolo processo dinamico che è un secondo aspetto di un processo di scambio di liganti idruri. 9,10,11,12,13,14,15,16,17,18 ,19,20,21,22,23,24,25,26,
27,28,29. I complessi di poliidruro di renio(V) pseudododecaedrali a otto coordinate, pseudododecaedrali adottano una geometria molecolare (Figura 2), che può essere descritta come una coppia di trapezi ortogonali di ligandi17,26. I vertici sui bordi lunghi dei trapezi sono comunemente etichettati come siti B e, nei complessi di poliidruro di renio, sono solitamente i siti occupati da ligandi donatori neutri a due elettroni come fosfine terziarie o ligandi amminici. I vertici sui bordi corti dei trapezi sono comunemente etichettati come siti A e sono tipicamente occupati da ligandi anionici, donatori di due elettroni, idruro. Gli spettri NMR a temperatura ambiente dei complessi di poliidruro di renio (V) sono, tipicamente, ingannevolmente semplici a causa dei numerosi processi dinamici che si verificano nelle soluzioni a temperatura ambiente.
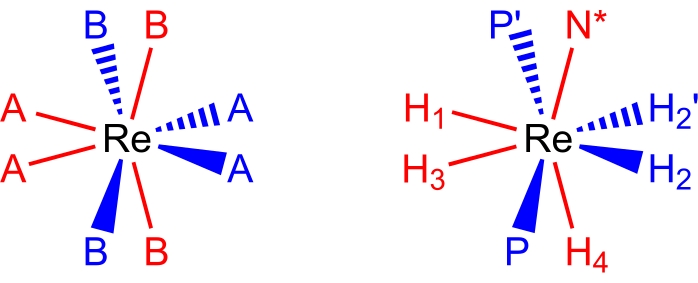
Figura 2: Un insieme di coordinazione dodecaedrica (a sinistra) e il complesso ReH5 (PPh3) 2 (sec-butililammina) dalla stessa prospettiva (a destra). I siti di colore rosso rappresentano i siti di coordinamento che formano un trapezio verticale e i siti di colore blu rappresentano i siti di coordinamento che formano un trapezio orizzontale. Fare clic qui per visualizzare una versione ingrandita di questa figura.
I complessi della forma ReH5(PPh3)2(ammina) sono la classe più studiata di complessi di poliidruro di renio rispetto ai processi dinamici 9,10,12,13,16,30,31. Sono stati identificati tre processi dinamici (Figura 3) per complessi ReH5(PPh3)2(ammina): 1) uno scambio protonico tra l’unico ligando dell’idruro del sito B e un protone da una molecola d’acqua (accidentale o intenzionale)9,13, 2) uno scambio del tornello di una coppia di ligandi di idruro del sito A con un ligando adiacente all’idruro del sito B 9, 11,13,30,31 e 3) un’inversione sterica (o pseudorotazione) che si manifesta come uno scambio a coppie dei ligandi idruro del sito A e un movimento a coppie degli atomi del sito B sul lato opposto del centro del renio (come illustrato nella Figura 4)4,5,6,8,26,27 . Il movimento degli atomi del sito B sul lato opposto del renio è osservabile mediante spettroscopia NMR dinamica come: 1) un processo che rende i protoni inequivalenti 3 e 5 di N = equivalente piridina a temperatura ambiente10,30,31, 2) un processo che fa sì che gli isomeri E e Z di N = leganti amminici aromatici sostituiti in modo asimmetrico subiscano uno scambio rapido a temperatura ambiente9, 10,13,30,31, o 3) un processo che provoca un rapido scambio delle prospettive steriche di una coppia diastereotopica di atomi di fosforo rispetto ad un centro chirale situato sul ligando amminico 9,30,31. Il complesso chirale ReH5 (PPh3) 2 (sec-butililammina) precedentemente non riportato offre l’opportunità di descrivere in generale i metodi che possono essere utilizzati per identificare e caratterizzare i riarrangiamenti dinamici dei complessi di poliidruro di renio.
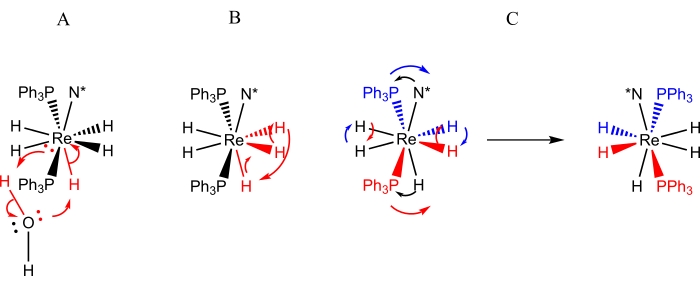
Figura 3: Rappresentazioni dei processi dinamici osservati dalla spettroscopia NMR per soluzioni di ReH5(PPh3)2(sec-butililammina). La rappresentazione A raffigura lo scambio di un singolo protone di acqua avventizia per l’unico ligando dell’idruro del sito B. La rappresentazione B raffigura lo scambio del tornello di tre ligandi idruro adiacenti, due dei quali risiedono nel sito A mentre il terzo è l’unico ligando idruro del sito B. La rappresentazione C rappresenta sia lo scambio a coppie di ligandi di idruro del sito A sia l’inversione sterica degli atomi di fosforo rispetto al ligando amminico chirale (N*). Va notato che lo scambio a coppie del ligando dell’idruro del sito A non richiede uno spostamento dei ligandi dell’idruro del sito A sul lato opposto del centro del renio. Fare clic qui per visualizzare una versione ingrandita di questa figura.
Per sistemi chimici come i complessi di poliidruro di renio, che presentano un insieme complesso di processi dinamici, il line shape fitting degli spettri NMR dinamici è la tecnica NMR più utilizzata per caratterizzare i processi 9,11,13,16,21,29. EXSY 9,32 o 2D-ROESY11 bidimensionali sono tecniche NMR dinamiche alternative che possono essere utilizzate anche per caratterizzare quantitativamente i processi dinamici. Gli spettri EXSY bidimensionali sono tipicamente misurati nel dominio della temperatura a scambio lento; gli spettri ROESY bidimensionali sono tipicamente misurati nel dominio della temperatura di scambio rapido. Entrambe le tecniche bidimensionali possono richiedere molto tempo nello spettrometro per l’acquisizione dei dati, in quanto ciascuna delle tecniche sta acquisendo un set di dati molto più grande, a una data temperatura, rispetto ai set di dati unidimensionali necessari per l’analisi del line shape fitting. Semplici processi dinamici che sono ben compresi, come lo scambio dinamico dei due gruppi metilici della dimetilformammide, possono essere facilmente caratterizzati da una qualsiasi delle tre tecniche NMR. Sistemi più complessi, come ReH5 (PPh3) 2 (sec-butilammina), in cui i singoli ligandi dell’idruro partecipano a molteplici processi dinamici, o sistemi che non sono necessariamente ben compresi, come un nuovo complesso di poliidruro di metalli di transizione che può o non può scambiare protoni tra un ligando di idruro e acqua avventizia, sono più facilmente caratterizzati quantitativamente dal metodo NMR di adattamento della linea che dai metodi NMR bidimensionali. A differenza dei metodi NMR bidimensionali, il metodo line shape fitting fornisce una visualizzazione facilmente interpretabile della corrispondenza tra un modello testato e i dati sperimentali, nonché la prova visiva di uno scambio che sposta un ligando idruro oltre la sfera di coordinazione interna del renio. Sulla base delle altezze dei picchi e delle forme dei picchi negli spettri di scambio lento, anche un sistema dinamico complesso come ReH5 (PPh3) 2 (sec-butililammina) può portare a una serie iniziale di modelli di scambio facilmente testati. Inoltre, quando sono stati riportati più modelli teorici per una trasformazione molecolare, l’adattamento della forma della linea degli spettri NMR dinamici può consentire un confronto visivo di ciascun modello rispetto agli spettri osservati.
Oltre alle tre tecniche NMR sopra menzionate, esperimenti NMR di sostituzione isotopica che coinvolgono D2O o HD sono stati utilizzati per dimostrare qualitativamente lo scambio intermolecolare di atomi per complessi sistemi di poliidruro di renio, ma non sono stati utilizzati per caratterizzazioni quantitative 9,33,34,35. I calcoli teorici presentano un metodo aggiuntivo per caratterizzare i processi dinamici di sistemi dinamici complessi30,31,36. I calcoli teorici hanno il vantaggio rispetto al line shape fitting in quanto possono essere utilizzati per differenziare tra possibilità che non possono essere distinte dall’analisi line shape fitting. Ad esempio, calcoli teorici sono stati utilizzati per descrivere uno scambio che coinvolge tre ligandi idruro adiacenti su determinati complessi di renio (V) come uno scambio del tornello di tutti e tre i ligandi dell’idruro, piuttosto che una coppia alternata di scambi a coppie con ogni scambio a coppie comprendente un unico legante dell’idruro e uno dei due ligandi dell’idruro chimicamente equivalenti30, 31. I risultati dei calcoli teorici sono tipicamente confrontati con caratterizzazioni quantitative osservate sperimentalmente da una delle tre tecniche NMR sopra menzionate come controllo sulla validità dei risultati calcolati.
L’adattamento della forma della linea degli spettri NMR dinamici sfrutta il cambiamento nell’aspetto degli spettri NMR che si verifica quando i nuclei NMR-attivi si spostano tra diversi ambienti chimici durante una misurazione NMR. Gli spettri NMR a scambio lento (spettri con risonanze lorentziane indipendenti per ogni insieme di nuclei in scambio) si verificano a temperature in cui la differenza di frequenza tra le risonanze per i nuclei che scambiano è grande rispetto alla velocità di scambio dei nuclei37. Gli spettri NMR a scambio rapido (spettri con una singola risonanza lorentziana per lo scambio di nuclei) si verificano a temperature in cui la velocità di scambio dei nuclei è molto maggiore della differenza di frequenza tra le risonanze a scambio lento37. I tassi di cambio intermedi si verificano per le temperature tra il dominio della temperatura di scambio lento e il dominio della temperatura di scambio rapido37. Se sono noti i parametri fondamentali della frequenza di Larmor, dello spostamento chimico dei nuclei in scambio, delle costanti di accoppiamento (se presenti) per i nuclei in scambio e delle popolazioni relative di ciascun tipo di nucleo, le costanti di velocità per gli scambi putativi tra nuclei possono essere determinate confrontando spettri simulati con spettri osservati a diverse temperature intermedie. Buoni adattamenti per simulazioni a diverse temperature si traducono in dati costanti di temperatura e velocità che possono essere utilizzati con l’equazione di Eyring per stimare i parametri di attivazione per gli scambi putativi. I risultati del metodo sono risultati accurati e riproducibili.
Protocol
Representative Results
Discussion
Ci sono quattro elementi nella preparazione di ReH7 (PPh3) 2 che possono influire sulla quantità e sulla purezza del materiale prodotto. In primo luogo, l’uso di un bagno di ghiaccio durante i primi 15 minuti della reazione è importante per rimuovere il calore dalla reazione che si verifica tra boroidruro di sodio e acqua. Temperature iniziali più elevate portano ad una diminuzione della resa del prodotto ReH7(PPh 3)2 a causa della formazione del prodotto di decomposizione t…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Gli autori ringraziano il Dipartimento di Chimica e Fisica e il Creativity and Research Grant Program (Naik, Moehring) della Monmouth University per il sostegno finanziario di questo lavoro.
Materials
| Bruker Avance II 400 MHz NMR spectrometer | Bruker Biospin | The instrument includes a two channel probe (1H and X) with the X channel tunable from 162 MHz to 10 Mhz. The instrument is also VT capable with a dewar and heat exchanger for VT work. | |
| d8-toluene | MilliporeSigma | 434388 | |
| Powerstat variable transformer | Powerstat | ||
| sec-butyl amine | MilliporeSigma | B89000 | |
| Sodium borohydride | MilliporeSigma | 452882 | |
| Tetrahydrofuran | MilliporeSigma | 186562 | |
| Thermowell C3AM 100 mL | Thermowell | ||
| Topspin 3.0 or 4.1.4 with dNMR | Bruker Biospin | Data was acquired with Topspin version 3.0 and data handling was performed on a second computer that was running Topspin version 4.1.4.. | |
| Trichlorooxobis(triphenylphosphine) rhenium(V) | MilliporeSigma | 370193 | |
| Vacuubrand PC3000 vacuum pump with a CVC 3000 controller | Vacuubrand |
References
- Zimmer, K. D., Shoemaker, R., Ruminski, R. R. Synthesis and characterization of a fluxional Re(I) carbonyl complex fac-[Re(CO)3(dpop’)Cl] with the nominally tri-dentate ligand dipyrido(2,3-α:3′,2′-j)phenazine (dpop). Inorganica Chimica Acta. 359 (5), 1478-1484 (2006).
- McGlinchey, M. J. Symmetry breaking in NMR spectroscopy: the elucidation of hidden molecular rearrangement processes. Symmetry. 6 (3), 622-654 (2014).
- Casarini, D., Luazzi, L., Mazzanti, A. Recent advances in stereodynamics and conformational analysis by dynamic NMR and theoretical calculations. European Journal of Organic Chemistry. 2010 (11), 2035 (2010).
- Palmer, A. G., Williams, J., McDermott, A. Nuclear magnetic resonance studies of biopolymer dynamics. Journal of Physical Chemistry. 100 (31), 13293-13310 (1996).
- Kern, D., Kern, G., Scherer, G., Fischer, G., Drakenberg, T. Kinetic analysis of cyclophilin-catalyzed prolyl cis/trans isomerization by dynamic NMR spectroscopy. Biochimie. 34 (41), 13594-13602 (1995).
- Menger, F. M., Lynn, J. L. Fast proton transfer at a micelle surface. Journal of the American Chemical Society. 97 (4), 948-949 (1975).
- Pines, A., Rabinovitz, M. A nuclear magnetic resonance total line-shape treatment of internal rotation in dimethylformamide. Tetrahedron Letters. 9 (31), 3529-3532 (1968).
- Mancinelli, M., Bencivenni, G., Pecorari, D., Mazzanti, A. Stereochemistry and recent applications of axially chiral organic molecules. European Journal of Organic Chemistry. 2020 (27), 4070-4086 (2020).
- Streisel, D. J., et al. Fluxionality, substitution, and hydrogen exchange at eight-coordinate rhenium(V) polyhydride centers. Inorganica Chimica Acta. 496 (1), 119028 (2019).
- Jimenez, Y., Strepka, A. M., Borgohain, M. D., Hinojosa, P. A., Moehring, G. A. Ortho-metalation, rotational isomerization, and hydride-hydride coupling at rhenium(V) polyhydride complexes stabilized by aromatic amine ligands. Inorganica Chimica Acta. 362 (9), 3259-3266 (2009).
- Lee, J. C., Yao, W., Crabtree, R. H., Ruegger, H. Fluxionality in [ReH5(PPh3)2(pyridine)]. Inorganic Chemistry. 35 (3), 695-699 (1996).
- Patel, B. P., Kavallieratos, K., Crabtree, R. H. Effects of dihydrogen bonding on fluxionality in ReH5(PPh3)2L. Journal of Organometallic Chemistry. 528 (1), 205-207 (1997).
- Geetha, B., et al. Chiral amine ligands at rhenium(V) pentahydride complexes allow for characterization of an energetically accessible and reversible steric inversion of diastereotopic phosphorus atoms. Inorganica Chimica Acta. 531 (1), 120741 (2022).
- Paulo, A., Ascenso, J., Domingos, A., Galvao, A., Santos, I. Rhenium-(III) and -(V) hydride complexes with modified poly(pyrazolyl)borates. Journal of the Chemical Society, Dalton Transactions. 1999 (8), 1293-1300 (1999).
- Bianchini, C., et al. Synthesis and characterization of rhenium polyhydrides stabilized by the tripodal ligand MeC(CH2PPh2)3. Journal of Organometallic Chemistry. 451 (1), 97-106 (1993).
- Scorzelli, A. G., Macalush, B. E., Naik, D. V., Moehring, G. A. Comparative study of fluxional processes at two different classes of eight-coordinate rhenium(V) polyhydride complexes. Inorganica Chimica Acta. 516 (1), 120120 (2021).
- Luo, X. -. L., Crabtree, R. H. Synthesis and spectroscopic characterization of rhenium complexes ReH5(triphos)] and [ReH6(triphos)]+ [triphos = PPh(CH2CH2PPh2)2]. Journal of the Chemical Society. 1991 (5), 587-590 (1991).
- Kim, Y., Deng, H., Gallucci, J. C., Wojcicki, A. Rhenium polyhydride complexes containing PhP(CH2CH2CH2PCy2)2 (Cyttp): protonation, insertion, and ligand substitution reactions of ReH5(Cyttp) and structural characterization of ReH5(Cyttp) and [ReH4(η2-H2)(Cyttp)]SbF6. Inorganic Chemistry. 35 (24), 7166-7173 (1996).
- Bolano, S., et al. Synthesis, characterization, protonation studies and X-ray crystal structure of ReH5(PPh3)2(PTA) (PTA = 1,3,5-triaza-7-phosphaadamantane). Journal of Organometallic Chemistry. 691 (4), 629-637 (2006).
- Ginsberg, A. P., Abrahams, S. C., Jamieson, P. B. Nonrigid stereochemistry in eight-coordinate pentahydridorhenium complexes. Journal of the American Chemical Society. 95 (14), 4751-4752 (1973).
- Bolano, S., Bravo, J., Garcia-Fontan, S. Mono- and dinuclear rhenium polyhydride complexes bearing the chelating ligand 1,2-bis(dicyclohexylphosphinanyloxy)ethane. European Journal of Inorganic Chemistry. 2004 (24), 4812-4819 (2004).
- Leeaphon, M., Rohl, K., Thomas, R. J., Fanwick, P. E., Walton, R. A. Reactions of the polyhydride complex ReH7(PPh3)2 with quinoline, 2-hydroxyquinoline, and 2-mercaptoquinoline. The preparation and characterization of hydrido complexes of rhenium(V) and chloro complexes of rhenium(III). Inorganic Chemistry. 32 (24), 5562-5568 (1993).
- Mejia, E., Togni, A. Rhenium complexes containing the chiral tridentate ferrocenyl ligand pigiphos. Organometallics. 30 (17), 4765-4770 (2011).
- Moehring, G. A., Walton, R. A. Reactions of heptahydrobis(triphenylphosphine)rhenium with bidentate aromatic heterocycles. Inorganic Chemistry. 26 (17), 2910-2912 (1987).
- Kosanovich, A. J., Reibenspies, J. H., Ozerov, A. V. Complexes of high-valent rhenium supported by the PCP pincer. Organometallics. 35 (4), 513-519 (2016).
- Emge, T. J., Koetzle, T. F., Bruno, J. W., Caulton, K. G. Pentahydridorhenium: crystal and molecular structure of ReH5(PMePh2)3. Inorganic Chemistry. 23 (24), 4012-4017 (1984).
- Costello, M. T., Fanwick, P. E., Green, M. A., Walton, R. A. Reactions of Heptahydridobis(triphenylphosphine)rhenium with 1-(diphenylphosphino)-2-(diphenylarsino)ethane (arphos) and 1,2-bis(diphenylarsino)ethane (dpae). Structural characterization of ReH5(PPh3)2(arphos-As) and ReH5(PPh3)2(dpae-As). Inorganic Chemistry. 30 (4), 861-864 (1991).
- Alvarez, D., Lundquist, E. G., Ziller, J. W., Evans, W. J., Caulton, K. G. Synthesis, structure and applications of transition-metal polyhydride anions. Journal of the American Chemical Society. 111 (22), 8392-8398 (1989).
- Albinati, A., et al. Synthesis, characterization, and interconversion of the rhenium polyhydrides ReH3(η4-NP3)] and [ReH4(η4-NP3)]+ {NP3 = tris[2-(diphenylphosphanyl)ethyl]amine}. European Journal of Inorganic Chemistry. 2002 (6), 1530-1539 (2002).
- Bosque, R., et al. Site preference energetics, fluxionality, and intramolecular M−H···H−N hydrogen bonding in a dodecahedral transition metal polyhydride. Inorganic Chemistry. 36 (24), 5505-5511 (1997).
- Tao, Y., Sou, W., Luo, G. -. G., Kraka, E. Describing polytopal rearrangement processes of octacoordinate structures. I. renewed insights into fluxionality of the rhenium polyhydride complex ReH5(PPh3)2(Pyridine). Inorganic Chemistry. 60 (4), 2492-2502 (2021).
- Beringhelli, T., D’Alfonso, G., Minoja, A. P. Rhenium-platinum mixed metal clusters. Characterization in solution and dynamic behavior of the isomers of [Re3Pt(µ-H3)(CO)14]. An example of a labile metal fragment that undergoes intermolecular exchange. Organometallics. 13 (2), 663-668 (1994).
- Grieco, G., Blacque, O. Solution and solid-state structure of the first NHC-substituted rhenium heptahydrides. European Journal of Inorganic Chemistry. 2019 (34), 3810-3819 (2019).
- Wazio, J. A., Jimenez, V., Soparawalla, S., John, S., Moehring, G. A. Hydrogen exchange of rhenium(VII) heptahydridobis(triphenylphosphine) with water, aniline, methanol, and itself. Inorganica Chimica Acta. 362 (1), 159-165 (2009).
- Chatt, J., Coffey, R. S. Hydrido-complexes of rhenium-containing tertiary phosphines. Journal of the Chemical Society, A. 1969, 1963-1972 (1969).
- Tao, Y., Wang, X., Zou, W., Luo, G. -. G., Kraka, E. Unusual intramolecular motion of ReH92- in K2ReH9 crystal: circle dance and three-arm turnstile mechanisms revealed by computational study. Inorganic Chemistry. 61 (2), 1041-1050 (2022).
- Berger, X., Braun, S. . 200 and More NMR Experiments a Practical Course. , (2004).
- He, G., Chen, J., Sung, H. H. -. Y., Williams, I. D., Jia, G. Substituent effect on reactions of ReH5(PMe2Ph)3 with propargyl alcohols. Inorganica Chimica Acta. 518 (1), 120239 (2021).
- Donnelly, L. J., Parsons, S., Morrison, C. A., Thomas, S. P., Love, J. B. Synthesis and structures of anionic rhenium polyhydride complexes of boron-hydride ligands and their application in catalysis. Chemical Science. 11 (9), 9994-9999 (2020).
- Donnelly, L. J., et al. C-H borylation catalysis of heteroaromatics by a rhenium boryl polyhydride. ACS Catalysis. 11 (12), 7394-7400 (2021).
- Jin, H., et al. CO-enabled rhenium hydride catalyst for directed C(sp2)-H bond alkylation with olefins. Organic Chemistry Frontiers. 2 (4), 378-382 (2015).
- Takaya, H., Ito, M., Murahashi, S. -. I. Rhenium-catalyzed addition of carbonyl compounds to the carbon−nitrogen triple bonds of nitriles: α-C−H activation of carbonyl compounds. Journal of the American Chemical Society. 131 (31), 10824-10825 (2009).
- Carr, S. W., Fowles, E. H., Fontaine, X. L. R., Shaw, B. L. Multihydride complexes of rhenium, osmium or iridium containing monodentate ditertiary phosphine ligands: selective hydrogen-deuterium exchanges of the rhenium multihydrides. Journal of the Chemical Society, Dalton Transactions. 1990 (2), 573-579 (1990).
- Jin, H., et al. Rhenium-catalyzed acceptorless dehydrogenative coupling via dual activation of alcohols and carbonyl compounds. ACS Catalysis. 3 (10), 2195-2198 (2013).
- Loza, M. L., de Gala, S., Crabtree, R. H. Steric crowding in a rhenium polyhydride induced by a chelating disilyl ligand: synthesis, characterization, and reactivity of ReH5(disil)(PPh3)2 (disil = 1,2-Bis(dimethylsilyl)benzene and 1,2-Bis(dimethylsilyl)ethane). Inorganic Chemistry. 33 (22), 5073-5078 (1994).
- Lin, Y., Zhu, X., Xiang, M. Transition metal polyhydrides-catalyzed addition of activated nitriles to aldehydes and ketones via Knoevenagel condensation. Journal of Organometallic Chemistry. 448 (1-2), 215-218 (1993).
- Abdukader, A., Jin, H., Cheng, Y., Zhu, C. Rhenium-catalyzed amination of alcohols by hydrogen transfer process. Tetrahedron Letters. 55 (30), 4172-4174 (2014).
- Lin, Y., Zhou, Y. Selective transfer hydrogenation catalyzed by transition metal polyhydrides. Fenzi Cuihua. 5 (2), 119-124 (1991).
- Green, M. A., Huffman, J. C., Caulton, K. G., Rybak, W. K., Ziolkowski, J. J. Ligand scavenging and catalytic utilization of the phototransient ReH5(PMe2Ph)2. Journal of Organometallic Chemistry. 218 (2), 39-43 (1981).
- Komiya, S., Chigira, T., Suzuki, T., Hirano, M. Polymerization of alkyl methacrylate catalyzed by hydridorhenium complexes. Chemistry Letters. 4 (4), 347-348 (1999).
- Michos, D., Luo, X. L., Faller, J. W., Crabtree, R. H. Tungsten(VI) hexahydride complexes supported by chelating triphosphine ligands: protonation to give η2-dihydrogen complexes and catalytic dehydrogenation of cyclooctane to cyclooctene. Inorganic Chemistry. 32 (8), 1370-1375 (1993).

