एंटीबॉडी-निर्भर सेलुलर साइटोटॉक्सिसिटी संशोधित यौगिकों की पहचान के लिए उच्च-सामग्री स्क्रीनिंग परख
Summary
यह प्रोटोकॉल एक चिकित्सीय एंटी-एचईआर -2 एंटीबॉडी की उपस्थिति में प्राकृतिक हत्यारा सेल-मध्यस्थता स्तन कैंसर सेल हत्या को संशोधित करने वाले यौगिकों की पहचान करने के लिए एक स्वचालित, छवि-आधारित उच्च-थ्रूपुट तकनीक प्रस्तुत करता है।
Abstract
एंटीजन-विशिष्ट एंटीबॉडी या प्रतिरक्षा चेकपॉइंट इनहिबिटर के साथ इम्यूनोथेरेपी ने स्तन कैंसर की चिकित्सा में क्रांति ला दी है। एपिडर्मल ग्रोथ फैक्टर रिसेप्टर एचईआर 2 को व्यक्त करने वाली स्तन कैंसर कोशिकाओं को एंटी-एचईआर -2 एंटीबॉडी ट्रास्टुज़ुमाब द्वारा लक्षित किया जा सकता है। एंटीबॉडी-निर्भर सेलुलर साइटोटॉक्सिसिटी (एडीसीसी) एचईआर -2 की एंटीट्यूमर कार्रवाई में फंसा हुआ एक महत्वपूर्ण तंत्र है। कैंसर कोशिकाओं से बंधे ट्रास्टुज़ुमाब को एडीसीसी प्रभावक कोशिकाओं (जैसे, प्राकृतिक हत्यारा (एनके) कोशिकाओं, मैक्रोफेज और ग्रैनुलोसाइट्स) के एफसी रिसेप्टर्स द्वारा पहचाना जा सकता है, जिससे इन प्रतिरक्षा कोशिकाओं की साइटोटोक्सिक गतिविधि शुरू होती है जिससे कैंसर कोशिका मृत्यु हो जाती है। हमने उच्च-सामग्री स्क्रीनिंग द्वारा उपन्यास एडीसीसी मॉड्यूलेटर यौगिकों की पहचान करने के लिए एडीसीसी की मात्रा का ठहराव के लिए एक छवि-आधारित परख विकसित करने के लिए तैयार किया। परख में, एचईआर 2 ने जेआईएमटी -1 स्तन कैंसर कोशिकाओं को ट्रास्टुज़ुमाब की उपस्थिति में एनके -92 कोशिकाओं के साथ सह-संवर्धित किया है, और लक्ष्य कोशिका मृत्यु को स्वचालित माइक्रोस्कोपी और मात्रात्मक छवि विश्लेषण द्वारा निर्धारित किया जाता है। लक्ष्य कोशिकाओं को उनके ईजीएफपी प्रतिदीप्ति के आधार पर प्रभावक कोशिकाओं से अलग किया जाता है। हम दिखाते हैं कि एडीसीसी मॉड्यूलेटर दवाओं की पहचान करने के लिए परख में यौगिक पुस्तकालयों का परीक्षण कैसे किया जा सकता है। इस उद्देश्य के लिए, लैब शेल्फ से यादृच्छिक रूप से चयनित ठीक रसायनों का उपयोग करके एक यौगिक पुस्तकालय परीक्षण प्लेट स्थापित की गई थी। एनके सेल माइग्रेशन और डिग्रैनुलेशन में हस्तक्षेप करने के लिए अपेक्षित तीन सूक्ष्मनलिकाएं अस्थिर यौगिकों (कोलचिसीन, विन्क्रिस्टिन, पोडोफिलोटॉक्सिन) को भी परीक्षण पुस्तकालय में शामिल किया गया था। परीक्षण स्क्रीन ने सभी तीन सकारात्मक नियंत्रण यौगिकों को एक रासायनिक पुस्तकालय में एडीसीसी-संशोधित दवाओं की पहचान करने के लिए विधि की उपयुक्तता साबित करने वाले हिट के रूप में पहचाना। इस परख के साथ, एडीसीसी-बढ़ाने वाले यौगिकों की पहचान करने के लिए यौगिक लाइब्रेरी स्क्रीन का प्रदर्शन किया जा सकता है जिनका उपयोग एंटीकैंसर इम्यूनोथेरेपी प्राप्त करने वाले रोगियों के उपचार के लिए सहायक चिकित्सीय एजेंटों के रूप में किया जा सकता है। इसके अलावा, विधि का उपयोग विभिन्न संकेतों के लिए कैंसर रोगियों द्वारा ली गई चिकित्सीय दवाओं के किसी भी अवांछनीय एडीसीसी-अवरोधक दुष्प्रभावों की पहचान करने के लिए भी किया जा सकता है।
Introduction
एंटीकैंसर एंटीबॉडी, प्रतिरक्षा चेकपॉइंट इनहिबिटर, या चिमेरिक एंटीजन रिसेप्टर-व्यक्त टी (सीएआर-टी) कोशिकाओं के साथ इम्यूनोथेरेपी कैंसर के उपचारके लिए एक शक्तिशाली दृष्टिकोण का प्रतिनिधित्व करती है। ट्रास्टुज़ुमाब एक मानवकृत मोनोक्लोनल एंटी-एचईआर -2 (मानव एपिडर्मल ग्रोथ फैक्टर रिसेप्टर 2) एंटीबॉडी है जिसका उपयोग एचईआर -2 पॉजिटिव प्रारंभिक चरण या मेटास्टैटिक स्तन कैंसर के इलाज के लिए किया जाता है, साथ ही एचईआर -2 पॉजिटिव मेटास्टैटिक गैस्ट्रिक कैंसर 4,5,6। यह मुख्य रूप से एपिडर्मल विकास कारक4 के प्रसार उत्तेजक प्रभाव को रोककर कार्य करता है। हालांकि, यह बताया गया है कि ट्रास्टुज़ुमाब कुशलतापूर्वक कैंसर कोशिका मृत्यु को ट्रिगर करता है, भले ही कैंसर कोशिकाओं ने एचईआर -2 उत्तेजना7 के प्रति अपनी प्रतिक्रिया खो दी हो। एंटीबॉडी का यह विरोधाभासी प्रभाव एंटीबॉडी-निर्भर सेल-मध्यस्थता साइटोटॉक्सिसिटी (एडीसीसी) 7 के कारण है। एडीसीसी को प्राकृतिक हत्यारा (एनके) कोशिकाओं, ग्रैनुलोसाइट्स और मैक्रोफेज द्वारा मध्यस्थ किया जा सकता है जिन्हें सामूहिक रूप से एडीसीसी 8,9 के प्रभावक कोशिकाओं के रूप में जाना जाता है। यदि एक एंटीबॉडी, जैसे कि ट्रास्टुज़ुमाब, ट्यूमर कोशिकाओं को बांधता है, तो ये प्रभावक कोशिकाएं एंटीबॉडी के निरंतर (एफसी) क्षेत्र को बांधने के लिए अपने एफसी रिसेप्टर्स का उपयोग करती हैं। एंटीबॉडी ट्यूमर कोशिकाओं और एफसी रिसेप्टर-असर प्रभावक कोशिकाओं को पुल करता है, जिससे उनके साइटोटोक्सिकमध्यस्थों की रिहाई शुरू होती है। प्राकृतिक हत्यारा कोशिकाएं लक्ष्य कोशिका झिल्ली में छिद्र उत्पन्न करने के लिए पर्फोरिन युक्त अपने कणिकाओं के साइटोटोक्सिक कार्गो को छोड़ती हैं और प्रतिरक्षा सिनैप्स में ग्रैनजाइम (ट्रिगर सेल डेथ सिग्नलिंग मार्ग) जिससे कैंसर कोशिकाओं का एपोप्टोसिस होता है (चित्रा 1 देखें)।
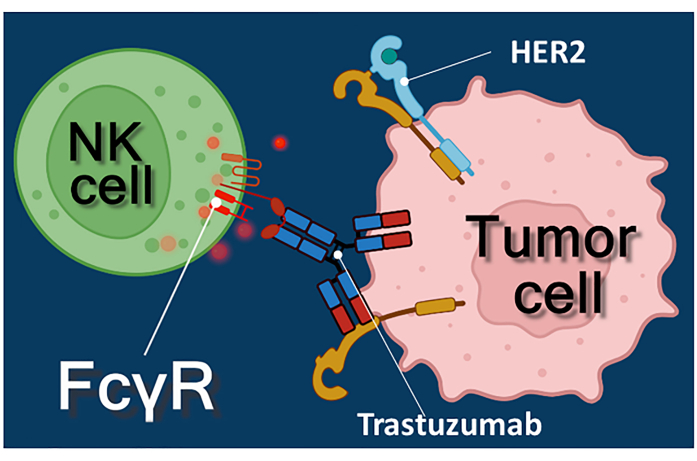
चित्रा 1: एडीसीसी में प्रभावक और लक्ष्य सेल इंटरैक्शन। प्रभावक एनके सेल का सेल सतह एफसीओ रिसेप्टर ट्यूमर सेल की सतह पर व्यक्त एचईआर 2 अणु के लिए विशिष्ट एंटी-एचईआर 2 ट्रास्टुज़ुमाब एंटीबॉडी के एफसी क्षेत्र को पहचानता है। इस प्रकार, तथाकथित इम्यूनोलॉजिकल सिनैप्स दो कोशिकाओं के बीच स्थापित किया जाता है, जो प्रभावक कोशिका के साइटोटोक्सिक कणिकाओं के निर्देशित एक्सोसाइटोसिस को प्रेरित करता है। जारी किए गए पर्फोरिन और ग्रैनजाइम अणुओं के परिणामस्वरूप अंततः लक्ष्य कोशिका का एपोप्टोसिस होता है। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
एडीसीसी सहित साइटोटॉक्सिसिटी को मापने के लिए पहले कई परख विकसित किए गए हैं। सोने का मानक रेडियोधर्मी क्रोमियम रिलीज विधि है, जहां लक्ष्य कोशिकाओं को रेडियोधर्मी 51सीआर आइसोटोप के साथ लेबल किया जाता है, और एडीसीसी को लाइसेड लक्ष्य कोशिकाओं11 के सुपरनैटेंट से रेडियोधर्मिता को मापकर निर्धारित किया जाता है। रेडियोधर्मी फार्माकोन और कचरे के सख्ती से विनियमित हैंडलिंग, भंडारण और निपटान के कारण स्पष्ट समस्याओं के कारण, यह विधि जीवन वैज्ञानिकों के बीच तेजी से गैर-लोकप्रिय हो गई है। इसके अलावा, यह उच्च-थ्रूपुट अनुप्रयोगों के लिए उत्तरदायी नहीं है। मारे गए लक्ष्य कोशिकाओं से जारी एंजाइमों (जैसे, लैक्टेट-डिहाइड्रोजनेज) की गतिविधि को मापना 51सीआर परख12 के लिए एक गैर-रेडियोधर्मी विकल्प प्रदान कर सकता है। हालांकि, ये परख लक्ष्य और प्रभावक कोशिका मृत्यु के बीच अंतर करने में विफल रहते हैं। इलेक्ट्रिक सेल-सब्सट्रेट प्रतिबाधा संवेदन (ईसीआईएस) एडीसीसी13 के परिमाणीकरण के लिए उपयुक्त साबित हुआ, लेकिन ईसीआईएस उपकरण अधिकांश प्रयोगशालाओं में उपलब्ध नहीं है, और तकनीक उच्च-थ्रूपुट अनुप्रयोगों / स्क्रीनिंग के साथ संगत नहीं है। फ्लोरोसेंटली लेबल वाली कोशिकाएं कई सेल जीव विज्ञान परखों में एक लोकप्रिय विकल्प का प्रतिनिधित्व करती हैं और अक्सर फ्लो साइटोमेट्री या प्लेट रीडर-आधारित अनुप्रयोगों 14,15,16 में उपयोग की जाती हैं। हालांकि, इन परखों में अक्सर धोने के चरण होते हैं या अन्यथा उच्च-थ्रूपुट अनुप्रयोगों (जैसे, फ्लो साइटोमेट्री-आधारित तकनीकों) के साथ असंगत होते हैं। कुछ लोकप्रिय साइटोटॉक्सिसिटी परख, जो सिद्धांत रूप में एडीसीसी परिमाणीकरण के लिए उपयुक्त होना चाहिए, एडीसीसी दक्षता13 को विश्वसनीय रूप से निर्धारित करने में विफल रहते हैं। हाल ही में, फ्लोरोसेंट कॉन्फोकल माइक्रोस्कोपी के प्रसार के साथ, छवि-आधारित, उच्च-सामग्री परख जीवन विज्ञान के विभिन्न क्षेत्रों में तेजी से लोकप्रिय हो रहेहैं। एक तरफ, सेल इमेजिंग उपकरण अब सर्वव्यापी हैं, जबकि दूसरी ओर, अधिग्रहित छवियों से लगभग अंतहीन रूपात्मक पैरामीटर एकत्र किए जा सकते हैं। इसलिए, हम एक उच्च-सामग्री स्क्रीनिंग संगत एडीसीसी परख विकसित करने और यौगिक पुस्तकालय स्क्रीनिंग के लिए इसकी उपयुक्तता का प्रदर्शन करने के लिए तैयार हैं।
यहां, हम एक छवि-आधारित एडीसीसी परख प्रस्तुत करते हैं और प्रदर्शित करते हैं कि एडीसीसी मॉड्यूलेटिंग यौगिकों की पहचान करने के लिए इस परख का उपयोग उच्च-सामग्री स्क्रीनिंग (एचसीएस) के लिए कैसे किया जा सकता है। मॉडल JIMT-1 स्तन कार्सिनोमा लक्ष्य कोशिकाओं, CD16.176V.NK-92 प्रभावक कोशिकाओं और मानवकृत मोनोक्लोनल एंटी-एचईआर 2 एंटीबॉडी ट्रास्टुज़ुमाब पर आधारित है। इस विधि के साथ, उन दवाओं की पहचान करना संभव है जो एनके कोशिकाओं की ट्यूमर-हत्या कार्रवाई को बढ़ा सकते हैं या एडीसीसी के साथ हस्तक्षेप करने वाले छोटे अणुओं की पहचान करके एनके सेल-मध्यस्थता एडीसीसी के तंत्र में अंतर्दृष्टि प्राप्त कर सकते हैं। हम सुझाव देते हैं कि एडीसीसी के विशेष संबंध में सेल-मध्यस्थता साइटोटॉक्सिसिटी को निर्धारित करने का लक्ष्य रखने वाले जीवन वैज्ञानिकों को खोज विज्ञान या दवा विकास के लिए इस परख का उपयोग करने से लाभ हो सकता है। यह परख एक विकल्प हो सकता है यदि एक प्रयोगशाला के पास फ्लोरोसेंट इमेजिंग और मात्रात्मक छवि विश्लेषण में पहुंच और कुछ अनुभव है।
Protocol
Representative Results
Discussion
एडीसीसी प्रतिक्रिया को अपेक्षाकृत लंबे समय पहले वर्णित किया गया है। प्रक्रिया की प्रमुख आणविक घटनाओं का भी वर्णन किया गयाहै। एडीसीसी को मापने के तरीके सोने के मानक रेडियोधर्मी क्रोमियम रिल…
Divulgations
The authors have nothing to disclose.
Acknowledgements
एलवी को राष्ट्रीय अनुसंधान, विकास और नवाचार कार्यालय अनुदान जीआईएनओपी-2.3.2-15-2016-00010 ट्यूमरडीएनएस”, जीआईएनओपी-2.3.2-15-2016-00048-स्टेअलाइव और ओटीकेए के132193, के147482 से धन प्राप्त हुआ। सीडी 16.176वी.एनके -92 कोशिकाओं को ब्रिंक बायोलॉजिक्स, एलएनसी की ओर से डॉ केरी एस कैंपबेल (फॉक्स चेस सेंटर, फिलापेडल्फिया, पीए) से प्राप्त किया गया था। सैन डिएगो, सीए), दुनिया भर में पेटेंट द्वारा संरक्षित हैं, और नांटकवेस्ट, एलएनसी द्वारा लाइसेंस प्राप्त थे। लेखक एनके -92 सेल लाइन के उपयोग के साथ उनकी मदद और तकनीकी सलाह के लिए ग्योर्गी वेरेब और आर्पड स्ज़ोर के आभारी हैं।
Materials
| 5-fluorouracil | Applichem | A7686 | in compound library |
| 96-well Cell Carrier Ultra plate | PerkinElmer | LLC 6055302 | |
| Betulin | Sigma | B9757 | in compound library |
| CD16.176V.NK92 cells | Nankwest Inc. | ||
| Cerulenin | ChemCruz | sc-396822 | in compound library |
| Cisplatin | Santa Cruz Biotechnology | sc-200896 | in compound library |
| Colchicine | Sigma | C9754 | in compound library |
| Concanavalin-A | Calbiochem | 234567 | in compound library |
| Dexamethasone | Sigma | D4902 | in compound library |
| DMEM/F-12 medium | Sigma | D8437 | in JIMT-1 EGFP medium |
| DMSO | Sigma | D2650 | in compound library |
| Etoposide | Sigma | E1383 | E1383 |
| Fetal bovine serum (FBS) | Biosera | FB-1090/500 | JIMT-1 EGFP and NK medium |
| Fisetin | Sigma | F4043 | in compound library |
| Freedom EVO liquid handling robot | TECAN | ||
| Gallotannin | Fluka Chemical Corp. | 16201 | in compound library |
| Glutamine | Gibco | 35,050–061 | in NK medium |
| Harmony software | PerkinElmer | ||
| Humanized anti-HER2 monoclonal antibody (Herzuma) | EGIS Pharmaceuticals, Budapest Hungary | N/A | |
| Humulin R (insulin) | Eli Lilly | HI0219 | JIMT-1 EGFP medium |
| IL-2 | Novartis Hungária Kft. | PHC0026 | in NK medium |
| Isatin | Sigma | 114618 | in compound library |
| MEM Non-essential Amino Acids (MEM-NEAA) | Gibco | 11,140–050 | in NK medium |
| Na-pyruvate | Lonza | BE13-115E | in NK medium |
| Naringenin | Sigma | N5893 | in compound library |
| NQDI-1 | Sigma | SML0185 | in compound library |
| Opera Phenix High-Content Analysis equipment | PerkinElmer | ||
| Penicillin–streptomycin | Biosera | LM-A4118 | JIMT-1 EGFP and NK medium |
| Pentoxyfilline | Sigma | P1784 | in compound library |
| Phosphate buffered saline (PBS) | Lonza | BE17-517Q | to wash the cells |
| Podophyllotoxin | Sigma | P4405 | in compound library |
| Quercetin | Sigma | Q4951 | in compound library |
| Tannic acid | Sigma | T8406 | in compound library |
| Temozolomide | Sigma | T2577 | in compound library |
| Trypan blue 0.4% solution | Sigma | T8154 | for cell counting |
| Vincristine sulfate | Sigma | V0400000 | in compound library |
| α-MEM | Sigma | M8042 | in NK medium |
References
- Gupta, S. L., Basu, S., Soni, V., Jaiswal, R. K. Immunotherapy: an alternative promising therapeutic approach against cancers. Molecular Biology Reports. 49 (10), 9903-9913 (2022).
- Moretti, A., et al. The past, present, and future of non-viral CAR T cells. Frontiers in Immunology. 13, 867013 (2022).
- June, C. H., O’Connor, R. S., Kawalekar, O. U., Ghassemi, S., Milone, M. C. CAR T cell immunotherapy for human cancer. Science. 359 (6382), 1361-1365 (2018).
- Ross, J. S., et al. The HER-2 receptor and breast cancer: ten years of targeted anti-HER-2 therapy and personalized medicine. Oncologist. 14 (4), 320-368 (2009).
- Shitara, K., et al. Discovery and development of trastuzumab deruxtecan and safety management for patients with HER2-positive gastric cancer. Gastric Cancer. 24 (4), 780-789 (2021).
- Gianni, L., et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncology. 13 (1), 25-32 (2012).
- Barok, M., et al. Trastuzumab causes antibody-dependent cellular cytotoxicity-mediated growth inhibition of submacroscopic JIMT-1 breast cancer xenografts despite intrinsic drug resistance. Molecular and Cancer Therapy. 6 (7), 2065-2072 (2007).
- Gauthier, M., Laroye, C., Bensoussan, D., Boura, C., Decot, V. Natural Killer cells and monoclonal antibodies: Two partners for successful antibody dependent cytotoxicity against tumor cells. Crit Rev Oncol Hematol. 160, 103261 (2021).
- Gruijs, M., Sewnath, C. A. N., van Egmond, M. Therapeutic exploitation of neutrophils to fight cancer. Semin Immunol. 57, 101581 (2021).
- Mando, P., Rivero, S. G., Rizzo, M. M., Pinkasz, M., Levy, E. M. Targeting ADCC: A different approach to HER2 breast cancer in the immunotherapy era. Breast. 60, 15-25 (2021).
- van der Haar Avila, I., Marmol, P., Kiessling, R., Pico de Coana, Y. Evaluating antibody-dependent cell-mediated cytotoxicity by chromium release assay. Methods in Molecular Biology. 1913, 167-179 (2019).
- Broussas, M., Broyer, L., Goetsch, L. Evaluation of antibody-dependent cell cytotoxicity using lactate dehydrogenase (LDH) measurement. Methods in Molecular Biology. 988, 305-317 (2013).
- Toth, G., Szollosi, J., Vereb, G. Quantitating ADCC against adherent cells: Impedance-based detection is superior to release, membrane permeability, or caspase activation assays in resolving antibody dose response. Cytometry A. 91 (10), 1021-1029 (2017).
- Chung, S., Nguyen, V., Lin, Y. L., Kamen, L., Song, A. Thaw-and-use target cells pre-labeled with calcein AM for antibody-dependent cell-mediated cytotoxicity assays. Journal of Immunological Methods. 447, 37-46 (2017).
- Lee-MacAry, A. E., et al. Development of a novel flow cytometric cell-mediated cytotoxicity assay using the fluorophores PKH-26 and TO-PRO-3 iodide. Journal of Immunological Methods. 252 (1-2), 83-92 (2001).
- Tanito, K., et al. Comparative evaluation of natural killer cell-mediated cell killing assay based on the leakage of an endogenous enzyme or a pre-loaded fluorophore. Analytical Science. 37 (11), 1571-1575 (2021).
- Lin, S., Schorpp, K., Rothenaigner, I., Hadian, K. Image-based high-content screening in drug discovery. Drug Discovery Today. 25 (8), 1348-1361 (2020).
- Guti, E., et al. The multitargeted receptor tyrosine kinase inhibitor sunitinib induces resistance of HER2 positive breast cancer cells to trastuzumab-mediated ADCC. Cancer Immunology, Immunotherapy. 71 (9), 2151-2168 (2022).
- Li, F., Liu, S. Focusing on NK cells and ADCC: A promising immunotherapy approach in targeted therapy for HER2-positive breast cancer. Frontiers in Immunology. 13, 1083462 (2022).
- Perussia, B., Loza, M. J. Assays for antibody-dependent cell-mediated cytotoxicity (ADCC) and reverse ADCC (redirected cytotoxicity) in human natural killer cells. Methods in Molecular Biology. 121, 179-192 (2000).
- Garcia-Alonso, S., Ocana, A., Pandiella, A. Trastuzumab emtansine: Mechanisms of action and resistance, clinical progress, and beyond. Trends in Cancer. 6 (2), 130-146 (2020).

