In vitro og in vivo evaluering af fotokontrollerede biologisk aktive forbindelser - potentielle lægemiddelkandidater til kræft fotofarmakologi
Summary
Denne protokol præsenterer et sæt eksperimenter vedtaget til evaluering af fotoomskiftelige anticancerpeptider, der kan anvendes til præklinisk screening af sådanne forbindelser. Dette omfatter cytotoksicitetsvurdering i 2D- og 3D-cellekulturer, evaluering af ex vivo (modelvæv) fotoisomeriseringseffektivitet og in vivo-effektivitet .
Abstract
Fotokontrollerede, biologisk aktive forbindelser er en ny klasse af “smarte” lægemiddelkandidater. De giver ekstra sikkerhed i systemisk kemoterapi på grund af deres præcise rumlige tidsmæssige aktivering ved at lede et godartet, ikke-ioniserbart lys til et bestemt sted i patientens krop. Dette papir præsenterer et sæt metoder til evaluering af in vitro-styrken og ex vivo-effektiviteten af fotoaktiveringen af fotokontrollerede, biologisk aktive forbindelser samt in vivo-effektiviteten på tidlige stadier af lægemiddeludvikling. Metoden anvendes til anticancer cytotoksiske peptider, nemlig de diarylethenholdige analoger af et kendt antibiotikum, gramicidin S. Eksperimenterne udføres ved hjælp af 2D (klæbende celler) og 3D (sfæroider) cellekulturer af en kræftcellelinje (Lewis lungecarcinom, LLC), levende vævssurrogater (svinekødshakkekød) og en allograft kræftmodel (subkutan LLC) i immunkompetente mus. Udvælgelsen af de mest effektive forbindelser og estimering af realistiske fototerapeutiske vinduer udføres via automatiseret fluorescensmikroskopi. Fotoaktiveringseffektiviteten ved forskellige belysningsregimer bestemmes i forskellige dybder i et modelvæv, og den optimale lysdosering anvendes i det endelige terapeutiske in vivo-eksperiment.
Introduction
Fotokontrollerede biologisk aktive forbindelser er opstået i de seneste årtier som en lovende komponent i sikre kemoterapier til menneskelige sygdomme og til specifikt at udrydde ondartede solide tumorer1. Disse forbindelser indeholder reversibelt fotoisomeriserbare fragmenter (molekylære fotokontakter) og kan skifte mellem inaktive og aktive fotoisomerer ved bestråling med lys med forskellige bølgelængder.
Sammenlignet med deres ikke-fotostyrbare analoger kan fotokontrollerede lægemidler være sikrere, fordi de systematisk kan indføres i patientens krop i mindre aktive og i det væsentlige ikke-toksiske former og derefter kun aktiveres af lys, hvor det er nødvendigt, såsom i tumorer, sår og sår. Selvom flere spændende demonstrationer af sådanne molekylære lægemiddelprototyper kan findes i nyere akademiske artikler 2,3,4,5,6,7, eksisterer området klinisk fotofarmakologi – en anvendelse af godkendte kombinationer af lægemiddel / medicinsk udstyr / sygdom – ikke. Fotofarmakologi er endnu i lægemiddelopdagelsesstadiet, og systematiske prækliniske undersøgelser er ukendte.
Vi har først for nylig demonstreret in vivo-sikkerhedsfordelen for nogle fotokontrollerede anticancerpeptider, nemlig analogerne af peptidantibiotikummet gramicidin S8. Disse fotostyrede derivater indeholder en diarylethenfotoswitch (DAE), som gennemgår reversible fotoinducerede transformationer mellem de såkaldte røde lysgenererede “ringåbne” og UV-genererede “ringlukkede” fotoformer (illustreret i figur 1 for et af derivaterne, forbindelsen LMB002).
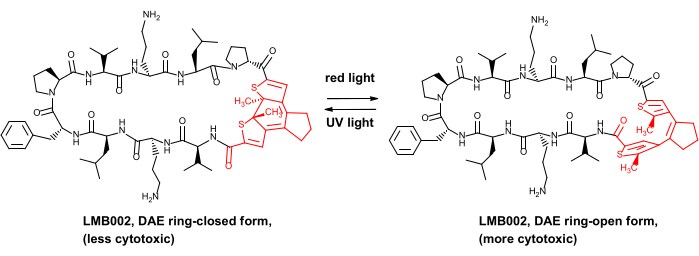
Figur 1: Fotokontrolleret cytotoksisk peptid LMB002 og dets fotoisomerisering. Dagbogsfragmentet er vist med rødt. Forkortelse: DAE = dagbog. Klik her for at se en større version af denne figur.
At finde hits og udføre hit-to-lead-optimering kræver ofte in vitro– og in vivo-screening af passende sammensatte biblioteker 9,10. Her demonstrerer vi en metode, der er egnet til systematisk high-throughput screening af cytotoksicitet af fotokontrollerede forbindelser. Vi bestemmer også fotoisomeriseringseffektiviteten, estimerer lysdosis i modelvæv og evaluerer in vivo-effekten af de bedst præsterende kandidater. Tilgangen er i overensstemmelse med bioetik og dyrepleje.
I dette arbejde modificeres traditionelle prækliniske metoder for at undgå ikke-kontrolleret fotoisomerisering af testede forbindelser. Det overordnede mål med at anvende disse modificerede metoder heri er at udvikle en generel strategi, der er ligetil og hurtig og giver statistisk signifikante data til pålideligt at sammenligne in vitro-aktiviteter og rationalisere de vivo-effektivitetstestning af fotoswitchable forbindelser til identifikation og videreudvikling af bly.
Strategien består af tre på hinanden følgende trin. Det første trin involverer bestemmelse af IC 50 (tilsyneladende50 % cellelevedygtighed) i serielle fortyndinger for de aktive og inaktive fotoformer af udvalgte fotokontrollerede biologisk aktive forbindelser ved anvendelse af todimensionale (2D, monolag) og tredimensionale (3D, sfæriske) cellekulturer og konfokal automatiseret fluorescensmikroskopi med høj kapacitet. Fototerapeutiske vinduer sammenlignes med hensyn til IC50-forskellen mellem de to fotoformer, og de bedst præsterende kandidater vælges. Der er ingen specifik fordel ved toksicitetsvurdering ved hjælp af automatiseret mikroskopi og andre cytotoksicitetsscreeningsplatforme (assays)11; Mere komplekse cellebaserede tumormodeller12 kunne let implementeres på dette stadium.
For de forbindelser, der er udvalgt i trin 1, er det andet trin realistisk at vurdere deres fotokoblingseffektivitet inde i vævene som funktion af dybden fra den bestrålede vævsoverflade ved at kvantificere fotokoblingseffektiviteten af de mindre aktive fotoformer i en vævssurrogat ved hjælp af UV-detekteret højtryksvæskekromatografi (HPLC) af bestrålede prøveekstrakter. In vivo kunne fotoskifteeffektivitet undersøges, men vi foreslår at bruge et simpelt vævsurrogat – hakket svinekød. Vi har testet gyldigheden af denne tilgang. Vi målte konverteringen af vores fotoomskiftelige forbindelser in vivo på en musekræftmodel og observerede omtrent den samme fotokonvertering i en dybde målt i tidligere forsøg med mus8. Ethvert egnet alternativt kunstigt væv13, 3D bioprintet væv/organ14, biopsimateriale eller andet undtaget animalsk materiale kan anvendes. Denne opsætning er dog et godt kompromis, da den er økonomisk, hurtig og etisk.
Det tredje trin er bestemmelsen af in vivo anticancer effekt i en murine cancer model. De forbindelser, der udviser overlegne egenskaber i in vitro-forsøgene og effektivt fotoskifter i en dybde på mindst 1-1,5 cm i modelvævene, udvælges til dette forsøg.
Denne protokol kan anvendes på forbindelser, der besidder forskellige typer fotoafbrydere, forudsat at deres fotoformer (eller deres fotostationære tilstande, PSS) er stabile i en rimelig tid (nogle få dage eller længere). Til illustration anvendes en tidligere beskrevet DAE-afledt LMB00215. LMB002 fotoformerne er termisk stabile og kan opbevares ved -20 °C i mindst et år uden væsentlig nedbrydning. Lewis lungecarcinom (LLC) celler vælges til denne in vitro og in vivo demonstration, men der pålægges ingen begrænsninger på celletypen. LLC-celler er klæbende, let dyrkelige i 3D og bruges til at generere tumoroider (som beskrevet i reference16). In vivo LLC-celler bruges til at modellere metastatiske processer og kan let generere solide tumorer hos immunkompetente mus efter subkutan injektion. Denne in vivo-metode kan anvendes universelt på andre kræftmodeller17,18. Den detaljerede gennemførelse af denne strategi er beskrevet nedenfor.
Protocol
Representative Results
Discussion
Fotokontrollerede forbindelser er uden fortilfælde i lægemiddeludvikling; Der er imidlertid ikke fastlagt metoder til præklinisk og klinisk evaluering heraf. Den nærmeste monoterapianalog, fotodynamisk terapi (PDT), er behandlingsmodaliteten til klinisk brug, der er vedtaget af mange lande mod kræft og er under udvikling for andre indikationer19,20. I lighed med fotofarmakologi er PDT også baseret på brugen af lys til at aktivere det bioaktive stof (singlet oxygen). Derfor kan nogle eksperimentelle metoder, der anvendes til prækliniske og kliniske undersøgelser i PDT, vedtages til fotofarmakologi. For eksempel er lyskilder, lysleveringsmetoder og medicinsk udstyr veludviklede og godkendt til PDT; De kan bruges direkte til evaluering af fotokontrollerede lægemidler. PDT og fotofarmakologi adskiller sig imidlertid i mange tilfældefra hinanden 4, hvilket begrunder behovet for at fastlægge specifikke metoder for sidstnævnte.
For det første er det ikke-aktiverede stof i PDT (oxygen) altid til stede i levende væv i ikke-toksiske koncentrationer. I modsætning hertil kan ikke-aktiverede fotokontrollerede biologisk aktive forbindelser have restaktivitet og uønsket toksicitet. Derfor bør ideelle fotofarmakologiske lægemidler have minimeret biologisk aktivitet i deres administrerede form og skal være meget aktive i deres lysgenererede form, det “fototerapeutiske vindue”21 skal være så stort som muligt. At finde hittet og udføre hit-to-lead-optimering kræver identifikation af egnede forbindelser og screening af relativt store biblioteker, allerede på tidlige stadier af lægemiddeludvikling. Her foreslog vi en automatiseret konfokal fluorescerende mikroskopi med høj kapacitet for at identificere effektive fotoswitchingforbindelser.
Den valgte metode til cytotoksicitetsevaluering muliggør nem implementering af det mest kritiske krav – vedligeholdelse af PSS eller stabilitet af den synlige lysfølsomme fotoisomer. Dette skyldes, at lyseksponeringen minimeres ved implementeringen. Derfor, hvis du vælger alternative metoder, bør automatiserede foretrækkes. Denne tilgang er pålidelig og informativ. Brugen af 3D-cellekulturer (sfæroider) på dette stadium giver en holistisk forståelse af cellens reaktion på behandlingen i et mere realistisk vævslignende mikromiljø. Derudover kan værdifuld indsigt i forbindelsernes virkningsmekanisme opnås ved anvendelse af mikroskopi som den direkte metode. Den konfokale fluorescerende mikroskopi med korrekt farvningsprotokol muliggør visuel vurdering af cellernes og sfæroidernes morfologi; Vigtige detaljer om celledød og ændringer inde i cellerne kan også detekteres.
For det andet kræver let anvendelse et omhyggeligt valg af lysdosering. I PDT er let overdosering ekstremt skadelig for væv22. Fotofarmakologisk terapi kan være fordelagtig under overdreven lysbestråling. Den øvre grænse for det aktiverede stof defineres ved den administrerede dosis af det ikke-aktiverede stof og dets farmakokinetik. Imidlertid er lysdosering stadig et problem i fotofarmakologi. Det skal omhyggeligt sikres, at bestrålingseffekten, tætheden og eksponeringstiden ikke er mindre end behovet for behandlingen. I princippet kan dannelsen af det aktive stof overvåges in vivo. Af bioetiske grunde foreslog vi imidlertid et forsøg med et modelvæv (fersk hakket kød) blandet med den ikke-aktiverede forbindelse15. Dette eksperiment er enkelt og kan ændres til at bruge forskellige lyskilder. Det kan også tilpasses til fotofysisk estimering af lysdosering og måling af termiske påvirkninger. Også her er det ved hjælp af modelvæv muligt at minimere lyseksponeringen sammenlignet med for eksempel den mere nøjagtige bestemmelse af fotoskifteeffektivitet under in vivo-forholdene , et alternativ, der altid kan være interessant at overveje.
Endelig kan de forbindelser, der demonstrerer overlegne egenskaber i in vitro-toksicitetsskærmene og effektivt fotoskifter mindst 1-1,5 cm dybt i modelvævet, vælges til dyre, besværlige og langvarige in vivo-undersøgelser. I denne protokol brugte vi den samme cellelinje (LLC) som i in vitro-vurderingen til at generere allograftcancermodellen. Tumorvækstdynamikken, dødeligheden og metastasetællingen er de parametre, der er bedst egnede til vurdering af kræfteffektivitet. Sammenlignet med konventionel kemoterapi anvendes en yderligere faktor i den fotofarmakologiske behandling – lyset. Der er derfor behov for to kontroldyregrupper: en, der kun modtager køretøjet, og en anden, der modtager køretøjet og bestråling. Denne opsætning muliggør evaluering af lysets indvirkning på de målte parametre. I vores forsøg modtog dyrene i de to forsøgsgrupper den ikke-aktiverede forbindelse, og tumorerne hos musene i en gruppe blev bestrålet. Bestrålingsordningen var identisk for kontrol- og behandlingsgrupperne. Sammenligning med benchmark kemoterapi er ikke nødvendig på dette stadium, fordi hovedformålet med forsøget er at demonstrere den kombinerede effekt af lys og sammensat anvendelse. De forbindelser, der udviser denne effekt, kan derefter udvælges til yderligere undersøgelse af deres in vivo-toksicitet og sammenligning med benchmarks for at træffe vigtige go-no-go-beslutninger om deres udvikling. Teknisk set kan in vivo-eksperimentet, som vi beskriver, let tilpasses farmakokinetiske eller farmakodynamiske undersøgelser, for eksempel af en forbindelse, der allerede er valgt som lægemiddelledning.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Forfatterne anerkender EU-finansiering fra H2020-MSCA-RISE-programmet gennem PELICO (#690973) og ALISE (#101007256) projekter. Dette arbejde blev støttet af DFG-GRK 2039 (SA, TS og ASU), NACIP-programmet for Helmholtz Society (SA og ASU) og VIP + for BMBF (OB og ASU). Vi anerkender Dr. Serhii Koniev, Karlsruhe Institute of Technology, som har syntetiseret forbindelsen LMB002, renset den og venligt leveret forbindelsen til undersøgelsen. Forfatterne takker også Chupryna Maksym, der filmede og kompilerede videoen i Ukraine, og til alle modige forsvarere af Ukraine, der gjorde det eksperimentelle arbejde, skrivning og filmoptagelse af denne publikation mulig.
Materials
| Agilent 1100 Series capillary LC system | ALSI-Chrom (Agilent distributor) | – | |
| ATCC CRL-1642, LL/2 (LLC1) Lewis lung carcinoma cell line | ECACC | 90020104 | |
| C57BL/6NCrl mice, female, inbred | Charles River | Strain code: 027 | |
| CelCulture, CO2 incubator | Esco Micro | CCL-170B | |
| Corning Matrigel Basement membrane matrix | Merck | CLS354234 | |
| Corning, 384- well spheroid microplates | Merck | CLS3830 | |
| Fetal bovine serum | Merck | F7524 | |
| Gibco, DPBS | Thermo Fisher Scientific | 21600044 | |
| Gramicidin S | Lumobiotics | Custom synthesis | |
| HyClone, DMEM/high glucose | Cytiva | SH30003.04 | |
| IN Cell Analyzer 6500HS, imaging system | Cytiva | 29240358 | |
| Invitrogen, Calcein AM | Thermo Fisher Scientific | C1430 | |
| Isoflurane anesthesia machine | ASA | S/N ASA 1305 | |
| L-glutamine, 200 mM solution | Merck | G7513 | |
| LIKA-surgeon, diode surgery laser | Fotonika plus | – | |
| LMB002 | Lumobiotics | Custom synthesis | |
| Penicillin–Streptomycin, solution stabilized | Merck | P4333 | |
| PhenoPlate, 96-well plates | PerkinElmer | 6055302 | |
| Photometer PCE-LED 20 | PCE Instruments | PCE-LED 20 | |
| Thermo Scientific, Hoechst 33342 | Thermo Fisher Scientific | 62249 | |
| Thermo Scientific, Propidium iodide | Thermo Fisher Scientific | J66764-MC | |
| Trypan blue, 0.4% solution | Merck | T8154 | |
| Trypsin–EDTA, 10 x solution | Merck | T4174 | |
| UltraCruz Cell culture flasks with vented caps, 75 cm2 | Santa Cruz Biotechnology | sc-200263 | |
| UltraCruz, bottle top filters, PES, 0.22 μm | Santa Cruz Biotechnology | sc-360882 | |
| Vydac 218TP, C18 HPLC column (4.6 mm × 250 mm, 5 µm) | Altmann Analytik (Avantor distributor) | GR5103827 |
References
- Fuchter, M. J. On the promise of photopharmacology using photoswitches: a medicinal chemist’s perspective. Journal of Medicinal Chemistry. 63 (20), 11436-11447 (2020).
- Volarić, J., Szymanski, W., Simeth, N. A., Feringa, B. L. Molecular photoswitches in aqueous environments. Chemical Society Reviews. 50, 12377-12449 (2021).
- Paoletti, P., Ellis-Davies, G. C. R., Mourot, A. Optical control of neuronal ion channels and receptors. Nature Reviews Neuroscience. 20, 514-532 (2019).
- Hüll, K., Morstein, J., Trauner, D. In Vivo Photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Ma, X., et al. In vivo photopharmacology with a caged mu opioid receptor agonist drives rapid changes in behavior. Nature Methods. 20, 682-685 (2023).
- Sarabando, S. N., Palmeira, A., Sousa, M. E., Faustino, M. A. F., Monteiro, C. J. P. Photomodulation Approaches to Overcome Antimicrobial Resistance. Pharmaceuticals. 16 (5), 682 (2023).
- Kolarski, D., Szymanski, W., Feringa, B. L., Hirota, T., Hatori, M., Panda, S. Chronophotopharmacology: Methodology for high spatiotemporal control over the circadian rhythm with light. Neuromethods. 186, (2022).
- Babii, O., et al. Peptide drugs for photopharmacology: how much of a safety advantage can be gained by photocontrol. Future Drug Discovery. 2 (1), FDD28 (2020).
- Davis, A. M., Keeling, D. J., Steele, J., Tomkinson, N. P., Tinker, A. C. Components of successful lead generation. Current Topics in Medicinal Chemistry. 5 (4), 421-439 (2005).
- Balani, S. K., Miwa, G. T., Gan, L., Wu, J., Lee, F. W. Strategy of utilizing in vitro and in vivo adme tools for lead optimization and drug candidate selection. Current Topics in Medicinal Chemistry. 5 (11), 1033-1038 (2005).
- Kleijn, A., et al. A Systematic comparison identifies an ATP-based viability assay as most suitable read-out for drug screening in glioma stem-like cells. Stem Cells International. 2016, (2016).
- Rodrigues, J., Heinrich, M. A., Teixeira, L. M., Prakash, J. 3D in vitro model revolution: unveiling tumor-stroma interactions. Trends in Cancer. 7 (3), 249-264 (2021).
- Sittinger, M., et al. Tissue engineering and autologous transplant formation: practical approaches with resorbable biomaterials and new cell culture techniques. Biomaterials. 17 (3), 237-242 (1996).
- Matai, I., Kaur, G., Seyedsalehi, A., McClinton, A., Laurencin, C. T. Progress in 3D bioprinting technology for tissue/organ regenerative engineering. Biomaterials. 226, 119536 (2020).
- Babii, O., et al. Direct photocontrol of peptidomimetics: an alternative to oxygen-dependent photodynamic cancer therapy. Angewandte Chemie International Edition. 55 (18), 5493-5496 (2016).
- De Ridder, K., et al. Novel 3D lung tumor spheroids for oncoimmunological assays. Advanced NanoBiomed Research. 2 (4), 2100124 (2022).
- Pauli, C., et al. Personalized in vitro and in vivo cancer models to guide precision medicine. Cancer Discovery. 7 (5), 462-477 (2017).
- Van Straten, D., Mashayekhi, V., De Bruijn, H. S., Oliveira, S., Robinson, D. J. Oncologic photodynamic therapy: basic principles, current clinical status and future directions. Cancers. 9 (2), 19 (2017).
- Li, X., Kwon, N., Guo, T., Liu, Z., Yoon, J. Innovative strategies for hypoxic-tumor photodynamic therapy. Angewandte Chemie International Edition. 57 (36), 11522-11531 (2018).
- Hull, K., Morstein, J., Trauner, D. In vivo photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Babii, O., et al. Structure-activity relationships of photoswitchable diarylethene-based β-hairpin peptides as membranolytic antimicrobial and anticancer agents. Journal of Medicinal Chemistry. 61 (23), 10793-10813 (2018).
- Heckl, C., Aumiller, M., Rühm, A., Sroka, R., Stepp, H. Fluorescence and treatment light monitoring for interstitial photodynamic therapy. Photochemistry and Photobiology. 96 (2), 388-396 (2020).

