In vitro og in vivo evaluering av fotokontrollerte biologisk aktive forbindelser - potensielle legemiddelkandidater for fotofarmakologi av kreft
Summary
Denne protokollen presenterer et sett med eksperimenter vedtatt for evaluering av fotoswitchable anticancer peptider, som kan brukes i preklinisk screening av slike forbindelser. Dette inkluderer cytotoksisitetsvurdering i 2D- og 3D-cellekulturer, evaluering av fotoisomeriseringseffektivitet ex vivo (modellvev) og in vivo-effekt.
Abstract
Fotokontrollerte, biologisk aktive forbindelser er en fremvoksende klasse av “smarte” legemiddelkandidater. De gir ekstra sikkerhet i systemisk kjemoterapi på grunn av deres presise spatiotemporal aktivering ved å lede et godartet, ikke-ioniserbart lys til et bestemt sted i pasientens kropp. Denne artikkelen presenterer et sett med metoder for å evaluere in vitro-styrken og ex vivo-effektiviteten av fotoaktivering av fotokontrollerte, biologisk aktive forbindelser, samt de vivo-effekten i tidlige stadier av legemiddelutvikling. Metoden brukes på anticancer cytotoksiske peptider, nemlig de diarylethenholdige analogene av et kjent antibiotika, gramicidin S. Forsøkene utføres ved hjelp av 2D (adherente celler) og 3D (sfæroider) cellekulturer av en kreftcellelinje (Lewis lungekarsinom, LLC), levende vevssurrogater (kjøttdeig) og en allograftkreftmodell (subkutan LLC) i immunkompetente mus. Utvelgelsen av de mest effektive forbindelsene og estimering av realistiske fototerapeutiske vinduer utføres via automatisert fluorescensmikroskopi. Fotoaktiveringseffektiviteten ved varierende belysningsregimer bestemmes på forskjellige dybder i et modellvev, og den optimale lysdoseringen påføres i det endelige terapeutiske in vivo-eksperimentet.
Introduction
Fotokontrollerte biologisk aktive forbindelser har dukket opp de siste tiårene som en lovende komponent i trygge kjemoterapier for menneskelige sykdommer og for å spesifikt utrydde ondartede solide svulster1. Disse forbindelsene inneholder reversibelt fotoisomererbare fragmenter (molekylære fotobrytere) og kan veksle mellom inaktive og aktive fotoisomerer ved bestråling med lys av forskjellige bølgelengder.
Sammenlignet med deres ikke-fotokontrollerbare analoger, kan fotokontrollerte legemidler være tryggere fordi de kan systematisk innføres i pasientens kropp i mindre aktive og i hovedsak ikke-toksiske former, og aktiveres deretter av lys bare der det er nødvendig, for eksempel i svulster, sår og sår. Selv om flere spennende demonstrasjoner av slike molekylære legemiddelprototyper finnes i nyere akademiske artikler 2,3,4,5,6,7, eksisterer ikke feltet klinisk fotofarmakologi – en anvendelse av godkjente kombinasjoner av legemiddel / medisinsk utstyr / sykdom – . Fotofarmakologi er ennå i legemiddeloppdagelsesstadiet, og systematiske prekliniske studier er ukjente.
Vi har bare nylig demonstrert in vivo sikkerhetsfordelen for noen fotokontrollerte anticancerpeptider, nemlig analogene til peptidantibiotikumet gramicidin S8. Disse fotokontrollerte derivatene inneholder en diarylethene (DAE) fotobryter, som gjennomgår reversible fotoinduserte transformasjoner mellom de såkalte røde lysgenererte “ringåpne” og UV-genererte “ringlukkede” fotoformene (illustrert i figur 1 for en av derivatene, forbindelsen LMB002).
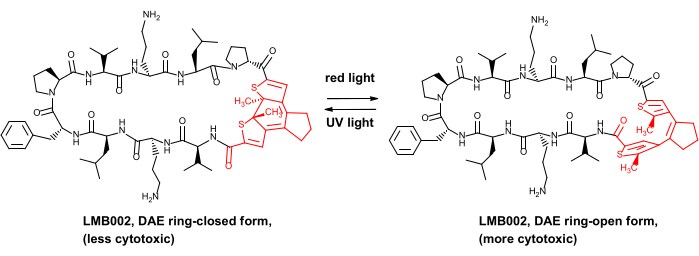
Figur 1: Fotokontrollert cytotoksisk peptid LMB002 og fotoisomerisering. Diarylethenfragmentet er vist i rødt. Forkortelse: DAE = diarylethene. Klikk her for å se en større versjon av denne figuren.
Å finne treff og utføre hit-to-lead-optimalisering krever ofte in vitro og in vivo-screening av passende sammensatte biblioteker 9,10. Her demonstrerer vi en metodikk som er egnet for systematisk høykapasitetsscreening av cytotoksisitet av fotokontrollerte forbindelser. Vi bestemmer også fotoisomeriseringseffektiviteten, estimerer lysdosen i modellvev og evaluerer in vivo-effekten til de best presterende kandidatene. Tilnærmingen er i samsvar med bioetikk og dyrepleiehensyn.
I dette arbeidet modifiseres tradisjonelle prekliniske metoder for å unngå ukontrollert fotoisomerisering av testede forbindelser. Det overordnede målet med å anvende disse modifiserte metodene her er å utvikle en generell strategi som er enkel og rask og gir statistisk signifikante data for pålitelig å sammenligne in vitro-aktiviteter og rasjonalisere de vivo-effektivitetstestingen av fotosvitsjebare forbindelser for blyidentifikasjon og videreutvikling.
Strategien består av tre påfølgende trinn. Det første trinnet innebærer bestemmelse av IC 50 (tilsynelatende50 % cellelevedyktighet) i serielle fortynninger for de aktive og inaktive fotoformene av utvalgte fotokontrollerte biologisk aktive forbindelser ved bruk av todimensjonale (2D, monolag) og tredimensjonale (3D, sfæroid) cellekulturer og konfokal høy gjennomstrømning automatisert fluorescensmikroskopi. Fototerapeutiske vinduer sammenlignes med hensyn til IC50-forskjellen mellom de to fotoformene, og de best presterende kandidatene velges. Det er ingen spesifikk fordel i toksisitetsvurdering ved automatisert mikroskopi og andre cytotoksisitetsscreeningsplattformer (analyser)11; Mer komplekse cellebaserte tumormodeller12 kan enkelt implementeres på dette stadiet.
For forbindelsene som er valgt i trinn 1, er det andre trinnet å realistisk estimere fotovekslingseffektiviteten inne i vevet som en funksjon av dybde fra den bestrålte vevsoverflaten ved å kvantifisere fotovekslingseffektiviteten til de mindre aktive fotoformene i et vevsurrogat ved bruk av UV-detektert høyytelsesvæskekromatografi (HPLC) av bestrålte prøveekstrakter. In vivo kan fotoswitching-effektivitet studeres, men vi foreslår å bruke et enkelt vevsurrogat – hakket svinekjøtt. Vi har testet gyldigheten av denne tilnærmingen. Vi målte konverteringen av våre fotoswitchable forbindelser in vivo på en muskreftmodell og observerte omtrent samme fotokonvertering på en dybde målt i tidligere eksperimenter med mus8. Ethvert egnet alternativt kunstig vev13, 3D bioprintet vev/organ14, biopsimaterialer eller annet unntatt animalsk materiale kan brukes. Imidlertid er dette oppsettet et godt kompromiss, da det er økonomisk, raskt og etisk.
Det tredje trinnet er bestemmelse av in vivo anticancer effekt i en murine cancer modell. Forbindelsene som demonstrerer overlegne egenskaper i in vitro-forsøkene og effektivt fotoswitching på en dybde på minst 1-1,5 cm i modellvevene, er valgt for dette eksperimentet.
Denne protokollen kan brukes på forbindelser som har forskjellige typer fotobrytere, forutsatt at fotoformene deres (eller deres fotostasjonære tilstander, PSS) er stabile i rimelig tid (noen dager eller lenger). Til illustrasjon er en tidligere beskrevet DAE-avledet LMB002 brukt15. LMB002-fotoformene er termisk stabile og kan lagres ved -20 °C i minst ett år uten vesentlig nedbrytning. Lewis lungekarsinom (LLC) celler er valgt for dette in vitro og in vivo demonstrasjon, men ingen restriksjoner pålegges celletype. LLC-celler er adherente, lett dyrkbare i 3D, og brukes til å generere tumoroider (som beskrevet i referansen16). In vivo LLC-celler brukes til å modellere metastatiske prosesser og kan lett generere solide svulster i immunkompetente mus etter subkutan injeksjon. Denne de vivo-metodikken kan brukes universelt på andre kreftmodeller17,18. Den detaljerte implementeringen av denne strategien er beskrevet nedenfor.
Protocol
Representative Results
Discussion
Fotokontrollerte forbindelser er enestående i stoffutvikling; Det er imidlertid ikke etablert metoder for preklinisk og klinisk evaluering. Den nærmeste monoterapianalogen, fotodynamisk terapi (PDT), er behandlingsmodaliteten for klinisk bruk som mange land har tatt i bruk mot kreft og er under utvikling for andre indikasjoner19,20. I likhet med fotofarmakologi er PDT også basert på bruk av lys for å aktivere det bioaktive stoffet (singlet oksygen). Derfor kan noen eksperimentelle metoder som brukes til prekliniske og kliniske studier i PDT, tas i bruk for fotofarmakologi. For eksempel er lyskilder, lysleveringsmetoder og medisinsk utstyr godt utviklet og godkjent for PDT; De kan brukes direkte til evaluering av fotokontrollerte stoffer. Imidlertid har PDT og fotofarmakologi mange forskjeller fra hverandre4, noe som rettferdiggjør behovet for å etablere spesifikke metoder for sistnevnte.
For det første er det ikke-aktiverte stoffet i PDT (oksygen) alltid tilstede i levende vev ved ikke-toksiske konsentrasjoner. I motsetning til dette kan ikke-aktiverte fotokontrollerte biologisk aktive forbindelser ha gjenværende aktivitet og uønsket toksisitet. Derfor bør ideelle fotofarmakologiske legemidler ha minimert biologisk aktivitet i sin administrerte form og må være svært aktive i sin lysgenererte form, det “fototerapeutiske vinduet”21 må være så stort som mulig. Å finne treffet og utføre hit-to-lead optimalisering krever identifisering av egnede forbindelser og screening av relativt store biblioteker, allerede i tidlige stadier av stoffutvikling. Her foreslo vi en automatisert konfokal fluorescerende mikroskopi med høy gjennomstrømning for å identifisere effektive fotobryterforbindelser.
Den valgte metoden for cytotoksisitetsevaluering muliggjør enkel implementering av det mest kritiske kravet – vedlikehold av PSS eller stabiliteten til den synlige-lysfølsomme fotoisomeren. Dette skyldes at lyseksponeringen minimeres ved implementeringen. Derfor, hvis du velger alternative metoder, bør automatiserte foretrekkes. Denne tilnærmingen er pålitelig og informativ. Bruken av 3D-cellekulturer (sfæroider) på dette stadiet gir en helhetlig forståelse av cellens respons på behandlingen i et mer realistisk vevslignende mikromiljø. I tillegg kan verdifull innsikt i forbindelsenes virkningsmekanisme fås ved hjelp av mikroskopi som direkte metode. Den konfokale fluorescerende mikroskopien med riktig fargeprotokoll muliggjør visuell vurdering av morfologien til cellene og sfæroidene; Viktige detaljer om celledød og endringer inne i cellene kan også oppdages.
For det andre krever lett applikasjon et nøye valg av lysdosering. Ved PDT er lett overdose ekstremt skadelig for vev22. Fotofarmakologisk terapi kan være fordelaktig ved overdreven lysbestråling. Den øvre grensen for det aktiverte stoffet er definert av den administrerte dosen av det ikke-aktiverte stoffet og dets farmakokinetikk. Imidlertid er lysdosering fortsatt et problem i fotofarmakologi. Det må utvises forsiktighet for å sikre at bestrålingseffekten og eksponeringstiden ikke er mindre enn behovet for behandlingen. I prinsippet kan genereringen av det aktiverte stoffet overvåkes in vivo. Av bioetiske grunner foreslo vi imidlertid et eksperiment med et modellvev (ferskt kjøttdeig) blandet med den ikke-aktiverte forbindelsen15. Dette eksperimentet er enkelt og kan modifiseres for å bruke forskjellige lyskilder. Det kan også tilpasses for fotofysisk estimering av lysdosering og måling av termiske påvirkninger. Her igjen, ved å bruke modellvev, er lyseksponeringen mulig å minimere, sammenlignet for eksempel med den mer nøyaktige bestemmelsen av fotovekslingseffektivitet under in vivo-forholdene , et alternativ som alltid kan være interessant å vurdere.
Til slutt kan forbindelsene som demonstrerer overlegne egenskaper i in vitro toksisitetsskjermene og effektivt fotoswitcher minst 1-1,5 cm dypt i modellvevet, velges for kostbare, arbeidskrevende og langvarige in vivo-studier . I denne protokollen brukte vi samme cellelinje (LLC) som in vitro-vurderingen for å generere allograftkreftmodellen. Tumorvekstdynamikken, dødeligheten og metastasetallet er parametrene som er mest egnet for å vurdere krefteffekt. Sammenlignet med konvensjonell kjemoterapi, brukes en ekstra faktor i den fotofarmakologiske behandlingen – lyset. Derfor er det nødvendig med to kontrolldyrgrupper: en som bare mottar kjøretøyet og den andre som mottar kjøretøyet og bestrålingen. Dette oppsettet gjør det mulig å evaluere lysets innvirkning på de målte parametrene. I vårt forsøk mottok dyrene i de to eksperimentelle gruppene den ikke-aktiverte forbindelsen, og musens svulster i en gruppe ble bestrålt. Bestrålingsregimet var likt for kontroll- og behandlingsgruppene. Sammenligning med referanse kjemoterapi er ikke nødvendig på dette stadiet fordi hovedformålet med forsøket er å demonstrere den kombinerte effekten av lys og sammensatt applikasjon. De best presterende forbindelsene som viser denne effekten, kan deretter velges for videre studier av deres in vivo-toksisitet og sammenligning med referanseverdier for å ta viktige go-no-go-beslutninger om deres utvikling. Teknisk sett kan in vivo-eksperimentet som vi beskriver, lett tilpasses farmakokinetiske eller farmakodynamiske studier, for eksempel av en forbindelse som allerede er valgt som legemiddelledning.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Forfatterne anerkjenner EU-finansiering av H2020-MSCA-RISE-programmet gjennom PELICO (#690973) og ALISE (#101007256) prosjekter. Dette arbeidet ble støttet av DFG-GRK 2039 (SA, TS og ASU), NACIP programmet til Helmholtz Society (SA og ASU), og VIP + av BMBF (OB og ASU). Vi anerkjenner Dr. Serhii Koniev, Karlsruhe Institute of Technology, som har syntetisert forbindelsen LMB002, renset den og vennlig gitt forbindelsen til studien. Forfatterne takker også Chupryna Maksym som filmet og samlet videoen i Ukraina, og til alle modige forsvarere av Ukraina som gjorde det eksperimentelle arbeidet, skrivingen og filmingen av denne publikasjonen mulig.
Materials
| Agilent 1100 Series capillary LC system | ALSI-Chrom (Agilent distributor) | – | |
| ATCC CRL-1642, LL/2 (LLC1) Lewis lung carcinoma cell line | ECACC | 90020104 | |
| C57BL/6NCrl mice, female, inbred | Charles River | Strain code: 027 | |
| CelCulture, CO2 incubator | Esco Micro | CCL-170B | |
| Corning Matrigel Basement membrane matrix | Merck | CLS354234 | |
| Corning, 384- well spheroid microplates | Merck | CLS3830 | |
| Fetal bovine serum | Merck | F7524 | |
| Gibco, DPBS | Thermo Fisher Scientific | 21600044 | |
| Gramicidin S | Lumobiotics | Custom synthesis | |
| HyClone, DMEM/high glucose | Cytiva | SH30003.04 | |
| IN Cell Analyzer 6500HS, imaging system | Cytiva | 29240358 | |
| Invitrogen, Calcein AM | Thermo Fisher Scientific | C1430 | |
| Isoflurane anesthesia machine | ASA | S/N ASA 1305 | |
| L-glutamine, 200 mM solution | Merck | G7513 | |
| LIKA-surgeon, diode surgery laser | Fotonika plus | – | |
| LMB002 | Lumobiotics | Custom synthesis | |
| Penicillin–Streptomycin, solution stabilized | Merck | P4333 | |
| PhenoPlate, 96-well plates | PerkinElmer | 6055302 | |
| Photometer PCE-LED 20 | PCE Instruments | PCE-LED 20 | |
| Thermo Scientific, Hoechst 33342 | Thermo Fisher Scientific | 62249 | |
| Thermo Scientific, Propidium iodide | Thermo Fisher Scientific | J66764-MC | |
| Trypan blue, 0.4% solution | Merck | T8154 | |
| Trypsin–EDTA, 10 x solution | Merck | T4174 | |
| UltraCruz Cell culture flasks with vented caps, 75 cm2 | Santa Cruz Biotechnology | sc-200263 | |
| UltraCruz, bottle top filters, PES, 0.22 μm | Santa Cruz Biotechnology | sc-360882 | |
| Vydac 218TP, C18 HPLC column (4.6 mm × 250 mm, 5 µm) | Altmann Analytik (Avantor distributor) | GR5103827 |
References
- Fuchter, M. J. On the promise of photopharmacology using photoswitches: a medicinal chemist’s perspective. Journal of Medicinal Chemistry. 63 (20), 11436-11447 (2020).
- Volarić, J., Szymanski, W., Simeth, N. A., Feringa, B. L. Molecular photoswitches in aqueous environments. Chemical Society Reviews. 50, 12377-12449 (2021).
- Paoletti, P., Ellis-Davies, G. C. R., Mourot, A. Optical control of neuronal ion channels and receptors. Nature Reviews Neuroscience. 20, 514-532 (2019).
- Hüll, K., Morstein, J., Trauner, D. In Vivo Photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Ma, X., et al. In vivo photopharmacology with a caged mu opioid receptor agonist drives rapid changes in behavior. Nature Methods. 20, 682-685 (2023).
- Sarabando, S. N., Palmeira, A., Sousa, M. E., Faustino, M. A. F., Monteiro, C. J. P. Photomodulation Approaches to Overcome Antimicrobial Resistance. Pharmaceuticals. 16 (5), 682 (2023).
- Kolarski, D., Szymanski, W., Feringa, B. L., Hirota, T., Hatori, M., Panda, S. Chronophotopharmacology: Methodology for high spatiotemporal control over the circadian rhythm with light. Neuromethods. 186, (2022).
- Babii, O., et al. Peptide drugs for photopharmacology: how much of a safety advantage can be gained by photocontrol. Future Drug Discovery. 2 (1), FDD28 (2020).
- Davis, A. M., Keeling, D. J., Steele, J., Tomkinson, N. P., Tinker, A. C. Components of successful lead generation. Current Topics in Medicinal Chemistry. 5 (4), 421-439 (2005).
- Balani, S. K., Miwa, G. T., Gan, L., Wu, J., Lee, F. W. Strategy of utilizing in vitro and in vivo adme tools for lead optimization and drug candidate selection. Current Topics in Medicinal Chemistry. 5 (11), 1033-1038 (2005).
- Kleijn, A., et al. A Systematic comparison identifies an ATP-based viability assay as most suitable read-out for drug screening in glioma stem-like cells. Stem Cells International. 2016, (2016).
- Rodrigues, J., Heinrich, M. A., Teixeira, L. M., Prakash, J. 3D in vitro model revolution: unveiling tumor-stroma interactions. Trends in Cancer. 7 (3), 249-264 (2021).
- Sittinger, M., et al. Tissue engineering and autologous transplant formation: practical approaches with resorbable biomaterials and new cell culture techniques. Biomaterials. 17 (3), 237-242 (1996).
- Matai, I., Kaur, G., Seyedsalehi, A., McClinton, A., Laurencin, C. T. Progress in 3D bioprinting technology for tissue/organ regenerative engineering. Biomaterials. 226, 119536 (2020).
- Babii, O., et al. Direct photocontrol of peptidomimetics: an alternative to oxygen-dependent photodynamic cancer therapy. Angewandte Chemie International Edition. 55 (18), 5493-5496 (2016).
- De Ridder, K., et al. Novel 3D lung tumor spheroids for oncoimmunological assays. Advanced NanoBiomed Research. 2 (4), 2100124 (2022).
- Pauli, C., et al. Personalized in vitro and in vivo cancer models to guide precision medicine. Cancer Discovery. 7 (5), 462-477 (2017).
- Van Straten, D., Mashayekhi, V., De Bruijn, H. S., Oliveira, S., Robinson, D. J. Oncologic photodynamic therapy: basic principles, current clinical status and future directions. Cancers. 9 (2), 19 (2017).
- Li, X., Kwon, N., Guo, T., Liu, Z., Yoon, J. Innovative strategies for hypoxic-tumor photodynamic therapy. Angewandte Chemie International Edition. 57 (36), 11522-11531 (2018).
- Hull, K., Morstein, J., Trauner, D. In vivo photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Babii, O., et al. Structure-activity relationships of photoswitchable diarylethene-based β-hairpin peptides as membranolytic antimicrobial and anticancer agents. Journal of Medicinal Chemistry. 61 (23), 10793-10813 (2018).
- Heckl, C., Aumiller, M., Rühm, A., Sroka, R., Stepp, H. Fluorescence and treatment light monitoring for interstitial photodynamic therapy. Photochemistry and Photobiology. 96 (2), 388-396 (2020).

