Samtidig vurdering av slektskap, divisjonsnummer og fenotype via flowcytometri for hematopoietiske stam- og stamceller
Summary
Her presenteres en flowcytometribasert teknikk som gjør det mulig å måle antall celledelinger, overflatecellefenotype og cellulær slektskap samtidig. Disse egenskapene kan testes statistisk ved hjelp av et permutasjonsbasert rammeverk.
Abstract
Få teknikker kan vurdere fenotype og skjebne for samme celle samtidig. De fleste av de nåværende protokollene som brukes til å karakterisere fenotype, selv om de er i stand til å generere store datasett, nødvendiggjør ødeleggelsen av cellen av interesse, noe som gjør det umulig å vurdere dens funksjonelle skjebne. Heterogene biologiske differensieringssystemer som hematopoiese er derfor vanskelig å beskrive. Ved å bygge på celledelingssporingsfargestoffer, videreutviklet vi en protokoll for samtidig å bestemme slektskap, divisjonsnummer og differensieringsstatus for mange enkelt hematopoietiske forfedre. Denne protokollen tillater vurdering av ex vivo differensieringspotensialet for murine og humane hematopoietiske progenitorer, isolert fra forskjellige biologiske kilder. Dessuten, siden den er basert på flowcytometri og et begrenset antall reagenser, kan den raskt generere en stor mengde data, på encellenivå, på en relativt billig måte. Vi tilbyr også den analytiske pipelinen for enkeltcelleanalyse, kombinert med et robust statistisk rammeverk. Siden denne protokollen tillater kobling av celledeling og differensiering på enkeltcellenivå, kan den brukes til kvantitativt å vurdere symmetrisk og asymmetrisk skjebneforpliktelse, balansen mellom selvfornyelse og differensiering, og antall divisjoner for en gitt forpliktelsesskjebne. Til sammen kan denne protokollen brukes i eksperimentelle design som tar sikte på å løse de biologiske forskjellene mellom hematopoietiske forfedre, fra et enkeltcelleperspektiv.
Introduction
Det siste tiåret ble preget av den verdensomspennende spredningen av enkeltcellede tilnærminger til cellulær og molekylærbiologi. Etter å ha fulgt i trinnene til enkeltcellegenomikk1,2, er det i dag mulig å studere mange komponenter i en enkelt celle (f.eks. DNA, RNA, proteiner), med nye enkeltcelle-omics-teknikker som spirer hvert år. Disse teknikkene har kastet lys over gamle og nye spørsmål for feltene immunologi, nevrobiologi, onkologi og andre, både ved hjelp av menneskelige og modellorganismeceller3. Ved å fremheve forskjellene mellom individuelle celler, førte enkeltcelle-omics til definisjonen av en ny modell for hematopoiesis, sentrert på heterogeniteten til hematopoietiske stam- og stamceller (HSPCs) og beveget seg bort fra den klassiske modellen for diskrete homogene populasjoner 4,5.
En av de få ulempene ved alle -omics-teknikkene er ødeleggelsen av cellen av interesse, og utelukker muligheten til å vurdere funksjonaliteten. Omvendt gir andre enkeltcellemetoder, som enkeltcelletransplantasjonsanalyse og avstamningssporingsteknologier, en avlesning av funksjonaliteten til forfedrecellen ved å vurdere skjebnen til individuelle celler in vivo 6,7. Avstamningssporingsteknologier innebærer å merke cellen av interesse med en arvelig genetisk7 eller en fluorescerende etikett8,9, slik at skjebnen til flere enkeltceller kan følges samtidig. Imidlertid er karakteriseringen av startcellene vanligvis begrenset til et begrenset antall parametere, for eksempel ekspresjonen av noen få overflateproteiner vurdert ved flowcytometri10. I tillegg krever enkeltcellede avstamningssporingsteknologier møysommelig deteksjon av den cellulære etiketten, vanligvis via DNA / RNA-sekvensering eller bildebehandling. Dette siste punktet begrenser spesielt antall forhold som kan testes i et enkelt eksperiment.
En annen klasse av metoder som brukes til å studere funksjonaliteten til enkeltceller er ex vivo celledyrkingssystemer av enkle HSPCer. Disse gullstandardanalysene er enkle å utføre, og involverer sortering av individuelle celler i cellekulturbeholdere med 96 brønner, og etter kultur karakteriserer celleavkomfenotypen, vanligvis ved flowcytometri eller morfologisk analyse. Disse analysene har for det meste blitt brukt til å karakterisere den langsiktige differensieringen av HSPCer i modne celler, vanligvis etter 2-3 uker med kultur11,12. Alternativt har de blitt brukt til å forsøke å opprettholde og utvide ex vivo HSPCs 13,14,15,16,17,18, med løfte om medisinsk fordel for human stamcelletransplantasjon 19. Til slutt har de blitt brukt til å studere HSPCs tidlige engasjement ved bruk av kortsiktig kultur20, med det lave antallet celler generert i denne kulturen som den viktigste begrensende faktoren. En ulempe med disse forskjellige typer ex vivo-analyser er at de bare delvis reflekterer in vivo-kompleksiteten; Likevel er de en av de sjeldne måtene å studere menneskelig HSPC-differensiering på.
En manglende informasjon fra eksisterende enkeltcellemetoder (enkeltcelle-omikk, avstamningssporing og ex vivo-kultur) er nøyaktig påvisning av celledelinger, en viktig parameter å vurdere når man studerer HSPC-dynamikk21. En enkel måte å vurdere antall divisjoner via flowcytometri er bruk av løselige “proteinfargestoffer”, som 5- (og 6)-karboksyfluoresceindiacetat succinimidylester (CFSE)22. Disse delingsfargestoffene diffunderer inne i cytoplasma av de fargede cellene, og fortynnes med halvparten og overføres til de to dattercellene ved hver celledeling, slik at de kan oppregne opptil 10 divisjoner. Ved å kombinere flere divisjonsfarger er det mulig å frø flere individuelle forfedre i samme brønn, da hvert enkelt fargestoff tillater separasjon av de forskjellige etterkommerne. Dette er prinsippet bak bruken av cellefargestoffer for multiplex klonal og divisjonssporing som først ble introdusert for murine lymfocytter23,24.
Her presenterer vi utviklingen av MultiGen-analysen for bruk med murine og humane HSPCer. Det tillater testing av mange enkeltceller samtidig for deres egenskaper av differensiering, divisjon og slektskap ex vivo. Denne høye gjennomstrømningen, enkel å utføre og billig analyse gjør det mulig å måle den cellulære fenotypen, antall divisjoner som utføres, og cellenes slektskap og klonale forhold til de andre cellene i brønnen, alt på samme tid. Den kan brukes til å kvantitativt vurdere symmetrisk og asymmetrisk skjebneforpliktelse, balansen mellom selvfornyelse og differensiering, og antall divisjoner som er nødvendige for en gitt forpliktelsesskjebne. Protokollen krever en fluorescensaktivert cellesorterer (FACS) og et flowcytometer med en plateleser, pluss utstyret som er nødvendig for å utføre cellekultur. I tillegg til den tekniske protokollen for utførelse av analysen på humane HSPCer, gir vi også det detaljerte analyserammeverket, inkludert statistisk testing som er nødvendig for å vurdere cellulære egenskaper relatert til begrepet cellefamilie25. Denne protokollen har allerede blitt brukt med hell for å beskrive murine HSPC-rommet26,27.
Følgende protokoll bruker magnetisk berikede CD34+-celler som utgangsmateriale28. På denne måten er det mulig å effektivt flekke og isolere humane HSPCer fra forskjellige blodkilder (f.eks. Navlestrengsblod, benmarg, perifert blod). Det er viktig å ikke forkaste CD34-fraksjonen, da den vil bli brukt som en del av protokollen for å angi forskjellige typer eksperimentelle kontroller. De nevnte cellemengdene og volumene kan skaleres opp eller ned, i henhold til eksperimentell arbeidsflyt og nødvendigheter. På samme måte kan protokollen tilpasses studiet av forskjellige typer progenitorer, ganske enkelt ved å modifisere antistoffene som brukes til cellesortering og flowcytometritrinn.
Protocol
Representative Results
Discussion
MultiGen-analysen er en høy gjennomstrømning, enkel å utføre og billig analyse, som har vært medvirkende til å studere lymfocytt 23,24,35 og murine hematopoietiske celler 26,27. Her presenterer vi en ny utvikling av tilnærmingen som gjør det mulig å dechiffrere ex vivo den tidlige fasen av menneskelig HSPC-forpliktelse, på enkeltcellenivå ved hjelp av kortsiktig kultur (figur 6). Encellede ex vivo-kultursystemer brukes vanligvis til å vurdere den langsiktige skjebnen til HSPCer i modne celler, men noen skjebner forekommer tidligere enn andre36, noe som potensielt forstyrrer analysen mot færre skjebner. I tillegg savner disse kultursystemene vanligvis informasjon om divisjoner under skjebneforpliktelsen. De første forpliktelsestrinnene har vist seg å skje så tidlig som i begynnelsen av kulturen, noen ganger uten divisjon26,37, noe som gjør kortsiktig kultur og sporingsdeling avgjørende for å studere tidlig skjebneforpliktelse. Ved samtidig å følge skjebnen, divisjonen og slektskapet, gjør denne analysen det mulig å forstå rollen som den første divisjonen og skjebnebeslutningen i menneskelige HSPCer. Ved hjelp av analysen er det mulig å utlede etter hvor mange divisjoner forpliktelsesprosessen oppstår, balansen mellom selvfornyelse og differensiering for de tidlige forfedrene, og hvordan disse egenskapene arves over generasjoner. Så vidt vi vet, er dette den eneste analysen som tillater denne typen målinger for humane HSPCer, ved encelleoppløsning. I tillegg, ved å bruke forskjellige kombinasjoner av celledelingsfarger, økte vi gjennomstrømningen av analysen, noe som gjør denne analysen til et verdifullt verktøy for å generere store datasett raskt. Fargestoffkombinasjonene tillater å følge flere familier i de samme brønnene, og øker antall celler som er tilgjengelige for analyse i kortsiktig kultur. Antall kombinasjoner kan potensielt økes enda mer, ved tilsetning av andre fargestoffer (f.eks. Gult fargestoff) eller modifisering av forholdet mellom CFSE og CTV. Dette reduserer imidlertid antall andre parametere som kan analyseres.
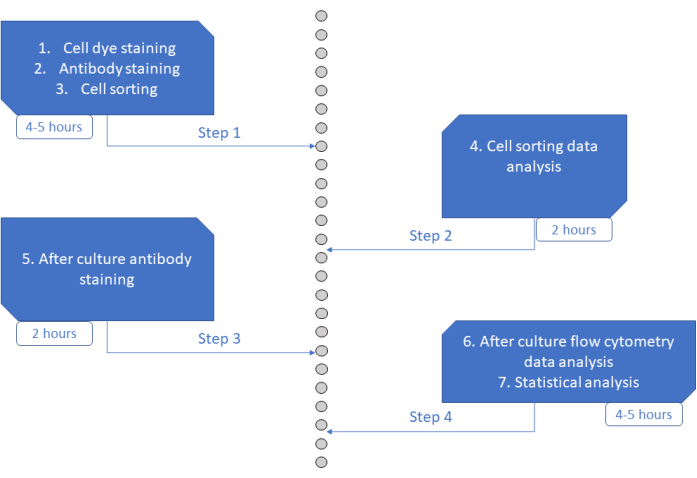
Figur 6: Skjematisk fremstilling av protokollen. Klikk her for å se en større versjon av denne figuren.
For å utføre analysen vellykket, på grunn av det store antallet brønner og det reduserte antall celler som skal analyseres, er det nødvendig å kjøre flowcytometrianalysen på en analysator utstyrt med en plateleser. Den nye generasjonen benkanalysatorer er spesielt tilpasset denne analysen, da de fleste av dem har et mindre dødvolum for å redusere prosentandelen av celletap. Dette garanterer i sin tur en høyere effektivitet i å gjenvinne hele hver brønn, noe som gir en effektivitet estimert i 70% -området26. Estimering av celletap under flowcytometri-oppkjøpet er avgjørende for analysen av hver enkelt familie. For eksempel, forutsatt ingen celledød og teller antall divisjoner, er det mulig å estimere antall celler per hver familie. Likevel er det ønskelig å kjøre noen bekreftende eksperimenter, spesielt i estimering av celledød i de testede kulturforholdene og måling av utvinningsgraden eksperimentelt ved bruk av et definert antall celler.
Et av de avgjørende trinnene i denne protokollen er toppoppdraget. Som allerede nevnt er en toppfordeling av god kvalitet sterkt avhengig av isolering av svært smale topper ved cellesortering. Likevel er det fortsatt vanskelig å tildele riktig antall divisjoner basert unikt på fordelingen. Siden cellesortering og flowcytometrianalyse utføres på to forskjellige maskiner, er det ikke mulig å sammenligne intensiteten til hvert signal direkte, så det kan være vanskelig å vite om den første toppen observert i høyre ende av histogrammet er topp 0 eller topp 1. I denne forbindelse er få løsninger mulige; En måte er å utføre et ortogonalt eksperiment for nøyaktig å måle antall divisjoner utført av disse cellene (f.eks. Levende celleavbildning). En annen mulighet er å bare telle antall celler i brønnen under et invertert lysfeltmikroskop, før du kjører flowcytometrianalysen. Dette vil utlede et gjennomsnittlig antall divisjoner (forutsatt ingen celledød). Endelig er en post-hoc-løsning for toppoppdrag påvisning av et uvanlig antall “umulige familier”; Disse familiene er sammensatt av et større enn mulig antall celler per generasjon (f.eks. Fem celler i generasjon 2, eller to celler i generasjon 1 og en celle i generasjon 2). Muligheten til å ekskludere umulige familier er kodet i det statistiske analysetrinnet, og flagger den umulige familien. Dersom forekomsten av disse feilene er for høy, er det rimelig å anta at topptildelingen må revideres.
I denne protokollen inkluderte vi noen få eksempler på datarepresentasjon og analyse for analysen, da dette har blitt et viktig trinn i generering og tolkning av store datasett38. Det første eksemplet er varmekartet som viser totaliteten av alle analyserte celler, organisert per familie. Dette er et effektivt verktøy for å utforske de generelle egenskapene til dataene og potensielle konklusjoner: er familier sammensatt av flere celletyper eller har de en tendens til å være homogene i sammensetningen? Er familier spredt over flere generasjoner, eller deler de stort sett like mange ganger? Denne utforskende analysen må deretter suppleres med mer spesifikke plott og statistisk testing. Den kan brukes til kvantitativt å vurdere symmetrisk og asymmetrisk skjebneforpliktelse, differensiering uten divisjon, balansen mellom selvfornyelse og differensiering, og antall divisjoner for en gitt forpliktelsesskjebne. Det er grunnleggende, under eksperimentell planlegging, å sette cellekulturlengden i samsvar med typen spørsmål som stilles; For eksempel, for de to første spørsmålene (symmetrisk / asymmetrisk balanse og differensiering uten divisjon), tillater planlegging av svært korte kulturer trinn isolering av et stort antall familier som bare har utført en eller ingen divisjoner i det heletatt 26. Omvendt tillater lengre eksperimenter utforskning av antall divisjoner som kreves for en bestemt celleforpliktelse, da de prøver familier på forskjellige stadier av differensiering. Likevel er denne metoden ikke designet for langsiktige kulturer (2-3 uker), da cellefargestofffortynning ikke er i stand til nøyaktig å spore mer enn syv eller åtte divisjoner22. Som en konsekvens er dette verktøyet for det meste tilpasset for å studere tidlig engasjement av hematopoietiske progenitorer, og er ikke designet for å gjøre robuste konklusjoner om de langsiktige differensieringsegenskapene til disse cellene.
Det statistiske rammeverket ble utviklet spesielt for analyse av denne typen data og basert på begrepet permutasjoner26. Dette var nødvendig på grunn av observasjonen av en familiær avhengighet av celletypefordelingen og på antall utførte divisjoner. Med andre ord, celler som er en del av samme familie er også mer sannsynlig å vise lignende fenotyper og dele seg samme antall ganger. Selv om en grundig analyse ligger utenfor omfanget av dette arbeidet, bør det gitte settet med statistiske tester være tilstrekkelig når man vurderer forskjellige forhold.
Avslutningsvis utgjør denne protokollen et verdifullt verktøy for å vurdere den cellulære dynamikken til hematopoietiske stam- og stamceller ex vivo, på en rask og billig måte. På grunn av sin fleksibilitet og allsidighet med hensyn til tidspunkt, kulturforhold og type HSPCer analysert, tillater det å teste en rekke eksperimentelle forhold. Som en flowcytometribasert analyse kan den implementeres i de fleste laboratorier, og den krever ikke omfattende forkunnskaper, noe som gjør den til en god kandidat for screeninger og piloteksperimenter.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Vi vil gjerne takke medlemmene av Institut Curie Flow Facility for deres hjelp med å sette opp flowcytometri-eksperimentene. Vi ønsker også å anerkjenne bidragene fra de andre medlemmene av Team Perié under flere diskusjoner. Vi takker Dr. Julia Marchingo og Prof. Phil Hodgkin (Walter end Eliza Hall Institute of Medical Research) for å dele sin protokoll for multipleksing av celledelingsfarger på lymfocytter. Vi takker Saint Louis hospital cord blood biobank for å gi de biologiske ressursene som er nødvendige for utviklingen av denne protokollen. Studien ble støttet av et ATIP-Avenir-tilskudd fra CNRS og Bettencourt-Schueller Foundation (til LP), tilskudd fra Labex CelTisPhyBio (ANR-10-LBX-0038) (til LP og AD), Idex Paris-Science-Lettres Program (ANR-10-IDEX-0001-02 PSL) (til LP), Canceropole INCA Emergence (2021-1-EMERG-54b-ICR-1, til LP), og ITMO MIIC-tilskuddet (21CM044, til LP). I tillegg til finansiering fra Det europeiske forskningsrådet (ERC) under EUs Horizon 2020 forsknings- og innovasjonsprogram ERC StG 758170-Microbar (til LP), ble AD støttet av et stipend fra Fondation de France.
Materials
| 1.5 mL polypropylene microcentrifuge tubes | vWR | 87003-294 | |
| 15-mL polypropylene tubes | vWR | 734-0451 | |
| 50-mL polypropylene tubes | vWR | 734-0448 | |
| 96-well U-bottom culture plate | Falcon | 353077 | |
| Anti-human Lin APC | Thermo Fisher | 22-7776-72 | Dilution 1/40 |
| ARIA III | BD | Can be replaced with any FACS sorter able to sort individual cells in 96-wells plate | |
| Carboxyfluorescein succinimidyl ester (CFSE) | Life Technologies | C34570 | |
| Cell Trace Violet (CTV) | Life Technologies | C34571 | |
| Compensation beads | BD | 552843 | |
| Dulbecco’s modified Eagle medium (DMEM) | Life Technologies | 11320033 | |
| Ethylenediaminetetraacetic acid (EDTA) | Thermo Scientific | J62948-36 | Prepare a solution 0.5 M, in sterilised water |
| FC block Fc1.3216 | BD | 564220 | Dilution 1/50 |
| Fetal Bovine Serum (FBS) | Dutscher | S1900-500C | Batch S00CH |
| FlowJo v10.8.1 | BD | ||
| Mouse anti-human CD10 PerCP-5.5, clone HI10a | Biolegend | 312216 | Dilution 1/20 |
| Mouse anti-human CD123 BUV395, clone 7G3 | BD | 564195 | Dilution 1/15 |
| Mouse anti-human CD34 APC-Cy7, clone 581 | Biolegend | 343513 | Dilution 1/40 |
| Mouse anti-human CD38 BV650, clone HB7 | Biolegend | 356620 | Dilution 1/40 |
| Mouse anti-human CD45RA AF700, clone HI100 | BD | 560673 | Dilution 1/20 |
| Mouse anti-human CD45RA PE-Cy7, clone HI100 | BD | 560675 | Dilution 1/20 |
| Mouse anti-human CD90 PE, clone 5E10 | Biolegend | 328110 | Dilution 1/20 |
| Phosphate Buffered Saline (PBS) 1X | Life Technologies | 10010001 | |
| Python | |||
| R | |||
| Sterile 12×75 mm conical polypropylene tubes | Falcon | ||
| ZE5 | Biorad | Can be replaced with any flow cytometry analyzer equipped with a plate reader | |
| Laboratory prepared | |||
| Cell culture media | Depends from the specific experiment. Prepare fresh daily and store at +4 °C until use | ||
| DMEM + 10% FBS | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 50 mL of FBS to 450 mL DMEM | ||
| PBS 1X + EDTA 0.1% | Can be stored in sterile conditions, at room temperature, up to 1 year. To prepare 500 mL, add 3.42 mL of EDTA 0.5 M to 500 mL PBS 1X | ||
| Staining buffer | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 2 mL of EDTA 0.5 M and 1 mL FBS to 500 mL PBS 1X |
References
- Ginhoux, F., Yalin, A., Dutertre, C. A., Amit, I. Single-cell immunology: Past, present, and future. Immunity. 55 (3), 393-404 (2022).
- Ke, M., Elshenawy, B., Sheldon, H., Arora, A., Buffa, F. M. Single cell RNA-sequencing: A powerful yet still challenging technology to study cellular heterogeneity. Bioessays. 44 (11), 2200084 (2022).
- Regev, A., et al. The human cell atlas. Elife. 6, 27041 (2017).
- Laurenti, E., Göttgens, B. From haematopoietic stem cells to complex differentiation landscapes. Nature. 553 (7689), 418-426 (2018).
- Haas, S., Trumpp, A., Milsom, M. D. Causes and consequences of hematopoietic stem cell heterogeneity. Cell Stem Cell. 22 (5), 627-638 (2018).
- Loughran, S. J., Haas, S., Wilkinson, A. C., Klein, A. M., Brand, M. Lineage commitment of hematopoietic stem cells and progenitors: insights from recent single cell and lineage tracing technologies. Experimental Hematology. 88, 1-6 (2020).
- Perié, L., Duffy, K. R. Retracing the in vivo haematopoietic tree using single-cell methods. FEBS Letters. 590 (22), 4068-4083 (2016).
- Yu, V. W. C., et al. Epigenetic memory underlies cell-autonomous heterogeneous behavior of hematopoietic stem cells. Cell. 167 (5), 1310-1322 (2016).
- Ganuza, M., et al. Lifelong haematopoiesis is established by hundreds of precursors throughout mammalian ontogeny. Nature Cell Biology. 19 (10), 1153-1163 (2017).
- Naik, S. H., Schumacher, T. N., Perié, L. Cellular barcoding: A technical appraisal. Experimental Hematology. 42 (8), 598-608 (2014).
- Quek, L., et al. Genetically distinct leukemic stem cells in human CD34 − acute myeloid leukemia are arrested at a hemopoietic precursor-like stage. The Journal of Experimental Medicine. 213 (8), 1513-1535 (2016).
- Karamitros, D., et al. Single-cell analysis reveals the continuum of human lympho-myeloid progenitor cells. Nature Immunology. 19 (1), 85-97 (2018).
- Boitano, A. E., et al. Aryl hydrocarbon receptor antagonists promote the expansion of human hematopoietic stem cells. Science. 329 (5997), 1345-1348 (2010).
- Delaney, C., et al. Notch-mediated expansion of human cord blood progenitor cells capable of rapid myeloid reconstitution. Nature Medicine. 16 (2), 232-236 (2010).
- Fares, I., et al. Cord blood expansion. Pyrimidoindole derivatives are agonists of human hematopoietic stem cell self-renewal. Science. 345 (6203), 1509-1512 (2014).
- Guo, B., Huang, X., Lee, M. R., Lee, S. A., Broxmeyer, H. E. Antagonism of PPAR-γ 3 signaling expands human hematopoietic stem and progenitor cells by enhancing glycolysis. Nature Medicine. 24 (3), 360-367 (2018).
- Vannini, N., et al. The NAD-booster nicotinamide riboside potently stimulates hematopoiesis through increased mitochondrial clearance. Cell Stem Cell. 24 (3), 405-418 (2019).
- Gupta, R., et al. Nov/CCN3 enhances cord blood engraftment by rapidly recruiting latent human stem cell activity. Cell Stem Cell. 26 (4), 527-541 (2020).
- Horwitz, M. E., et al. Omidubicel vs standard myeloablative umbilical cord blood transplantation: results of a phase 3 randomized study. Blood. 138 (16), 1429-1440 (2021).
- Weinreb, C., Rodriguez-Fraticelli, A., Camargo, F. D., Klein, A. M. Lineage tracing on transcriptional landscapes links state to fate during differentiation. Science. 367 (6479), 3381 (2020).
- Loeffler, D., Schroeder, T. Understanding cell fate control by continuous single-cell quantification. Blood. 133 (13), 1406-1414 (2019).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. Journal of Visualized Experiments. (70), e4287 (2012).
- Marchingo, J. M., et al. T-cell stimuli independently sum to regulate an inherited clonal division fate. Nature Communications. 7, 13540 (2016).
- Horton, M. B., et al. Multiplexed division tracking dyes for proliferation-based clonal lineage tracing. Journal of Immunology. 201 (3), 1097-1103 (2018).
- Lehmann, E. L., Romano, J. P., Casella, G. . Testing statistical hypotheses. , 784 (2005).
- Tak, T., et al. HSPCs display within-family homogeneity in differentiation and proliferation despite population heterogeneity. Elife. 10, 360624 (2021).
- Sommerkamp, P., et al. Mouse multipotent progenitor 5 cells are located at the interphase between hematopoietic stem and progenitor cells. Blood. 137 (23), 3218-3224 (2021).
- Kato, K., Radbruch, A. Isolation and characterization of CD34+ hematopoietic stem cells from human peripheral blood by high-gradient magnetic cell sorting. Cytometry. 14 (4), 384-392 (1993).
- Miltenyi, S., Müller, W., Weichel, W., Radbruch, A. High gradient magnetic cell separation with MACS. Cytometry. 11 (2), 231-238 (1990).
- Doulatov, S., et al. Revised map of the human progenitor hierarchy shows the origin of macrophages and dendritic cells in early lymphoid development. Nature Immunology. 11 (7), 585-593 (2010).
- Goardon, N., et al. Coexistence of LMPP-like and GMP-like leukemia stem cells in acute myeloid leukemia. Cancer Cell. 19 (1), 138-152 (2011).
- Laurenti, E., et al. CDK6 levels regulate quiescence exit in human hematopoietic stem cells. Cell Stem Cell. 16 (3), 302-313 (2015).
- Aiuti, A., et al. Lentiviral hematopoietic stem cell gene therapy in patients with Wiskott-Aldrich syndrome. Science. 341 (6148), 1233151 (2013).
- Davison, A. C., Hinkley, D. V. . Bootstrap Methods and their Application. , (1997).
- Horton, M. B., et al. Lineage tracing reveals B cell antibody class switching is stochastic, cell-autonomous, and tuneable. Immunity. 55 (10), 1843-1855 (2022).
- Notta, F., et al. Distinct routes of lineage development reshape the human blood hierarchy across ontogeny. Science. 351 (6269), 2116 (2016).
- Grinenko, T., et al. Hematopoietic stem cells can differentiate into restricted myeloid progenitors before cell division in mice. Nature Communications. 9 (1), 1898 (2018).
- Saeys, Y., Van Gassen, S., Lambrecht, B. N. Computational flow cytometry: Helping to make sense of high-dimensional immunology data. Nature Reviews Immunology. 16 (7), 449-462 (2016).

