Generering av pasientavledede podocytter fra hudbiopsier
Summary
Dette manuskriptet beskriver en to-trinns protokoll for å generere pasientspesifikke podocytter fra dermale fibroblaster via episomal omprogrammering til menneskeinduserte pluripotente stamceller (hiPSCs) og påfølgende differensiering til podocytter.
Abstract
Podocytter er epitelceller som sitter på urinstedet til den glomerulære filtreringsbarrieren som bidrar til glomerulusens selektive filterfunksjon. Mutasjoner i podocyttspesifikke gener kan forårsake fokal segmental glomerulosklerose (FSGS), og podocytter påvirkes også i mange andre primære og sekundære nefropatier. På grunn av deres differensierte natur er primære cellekulturmodeller begrenset for podocytter. Derfor brukes ofte betinget immortaliserte celler. Imidlertid har disse betinget udødeliggjorte podocyttene (ciPodocytter) flere begrensninger: cellene kan dedifferensiere i kultur, spesielt når de når sammenløp, og flere podocyttspesifikke markører er enten bare litt eller ikke uttrykt i det hele tatt. Dette setter spørsmålstegn ved bruken av ciPodocytter og deres anvendelighet for fysiologisk, patofysiologisk og klinisk rekkevidde. Her beskriver vi en protokoll for generering av humane podocytter – inkludert pasientspesifikke podocytter – fra en hudstansebiopsi ved episomal omprogrammering av dermale fibroblaster til hissc og påfølgende differensiering i podocytter. Disse podocyttene ligner in vivo podocytter mye bedre når det gjelder morfologiske egenskaper, som utviklingen av fotprosesser og uttrykket av den podocytspesifikke markøren. Til slutt, men viktigere, opprettholder disse cellene pasientens mutasjoner, noe som resulterer i en forbedret ex vivo-modell for å studere podocyttsykdommer og potensielle terapeutiske stoffer i en individualisert tilnærming.
Introduction
Podocytter er spesialiserte, postmitotiske nyreepitelceller som danner den glomerulære filtreringsbarrieren til nyrene sammen med den glomerulære kjellermembranen (GBM), glomerulære endotelceller og glykokalyx. Fenotypisk består podocytter av en cellekropp og primære, mikrotubulidrevne membranforlengelser, samt sekundære forlengelser kalt fotprosesser 1,2. Den glomerulære filtreringsbarrieren som filtrerer urin fra blodet er bygget av fenestrert endotel, GBM, og en spesialisert type intercellulært kryss som forbinder nærliggende podocytfotprosesser, kalt spaltemembranen til podoctyes3. Under sunne forhold beholdes proteiner større enn albumin fra filtreringsbarrieren på grunn av deres størrelse og ladning4.
Mutasjoner i cytoskjelett- eller podocyttspesifikke gener, samt sirkulerende faktorer som påvirker podocyttsignalveier, er kjent for å indusere podocytt effacement, løsrivelse eller apoptose, noe som resulterer i proteinuri og glomerulær sklerose. Spesielt er cytoskjelettrearrangering, endringer i podocytpolaritet eller skade på fotprosesser med tilhørende tap av spaltekryss avgjørende5. På grunn av deres terminalt differensierte status kan podocytter nesten ikke erstattes etter løsrivelse av GBM. Men hvis podocytter er festet til GBM, kan de fortsatt komme seg fra effacement og reformere interdigitating fotprosesser 6,7,8. Videre forståelse av hendelsene som fører til podocyttskade i ulike glomerulære lidelser kan gi nye terapeutiske mål som vil hjelpe til med å utvikle behandlinger for disse sykdommene. Podocyttskade er et kjennetegn på forskjellige glomerulære sykdommer, inkludert fokal segmental glomerulosklerose (FSGS), diabetisk nefropati, minimal endringssykdom og membranøs glomerulonefropati, som krever pålitelige podocyt ex vivo-modeller for å studere patologiske mekanismer og potensielle behandlingsmetoder for disse sykdommene 9,10. Podocytter kan studeres ex vivo ved klassisk primærcellekultur basert på isolering av glomeruli ved differensialsikting11. På grunn av den terminalt differensierte tilstanden med begrenset spredningskapasitet, bruker de fleste forskere imidlertid mus eller humane ciPodocyttcellelinjer som uttrykker temperaturfølsomme varianter av SV40 stort T-antigen. Alternativt isoleres ciPodocytter fra transgene mus som har SV40 Tag immortaliserende gen 1,12.
CiPodocytter prolifererer ved 33 °C, men går inn i vekststans og begynner å differensiere ved 37 °C13,14. Det må huskes at eksperimentelle data oppnådd med disse cellene skal tolkes med en viss forsiktighet, da cellene genereres ved hjelp av en unaturlig geninnsetting15. Siden disse cellene har et udødeliggjørende gen, endres den cellulære fysiologien på grunn av pågående spredning12. Podocyttcellelinjer generert av denne tilnærmingen har nylig blitt stilt spørsmålstegn ved, da mus-, menneske- og rottekocytter uttrykker mindre enn 5% synaptopodin og nefrin på proteinnivå, samt NPHS1 og NPHS2 på mRNA-nivå sammenlignet med glomerulært uttrykk16. Dessuten uttrykker de fleste podocyttcellelinjer ikke nefrin17,18. Chittiprol et al. beskrev også en signifikant forskjell i cellemotilitet og respons på puromycin og doksorubicin i ciPodocytter16. Podocytter kan bli funnet i urinen etter løsrivelse fra GBM i forskjellige glomerulære sykdommer 19,20,21,22. Levedyktige urinpodocytter kan dyrkes ex vivo i opptil 2-3 uker, men de fleste celler gjennomgår apoptose23,24. Interessant nok finnes podocytter ikke bare i urinen hos pasienter med glomerulær sykdom, men også i urinen til friske personer, mest sannsynlig når de er senescent-again med et begrenset potensial for replikasjon i kultur24. Videre er det urinavledede podocyttallet begrenset, og cellene dedifferensierer i kultur, viser mindre fotprosesser, endrer morfologi, og viktigst av alt har begrenset spredningskapasitet. Ekspresjonen av podocyttspesifikke gener er fraværende, forsvinner i løpet av få uker, eller varierer mellom disse celleklonene. Noen celler som er positive for den podocyttspesifikke markøren, uttrykte samtidig markøren for tubulære epitelceller eller myofibroblaster og mesangialceller, noe som antyder dedifferensiering og/eller transdifferensiering av de dyrkede urinpodocyttene24,25.
Nylig er generering av ciPodocyttcellelinjer avledet fra urinen til pasienter og friske frivillige ved transduksjon med et termofølsomt SV40 stort T-antigen og hTERT beskrevet26. mRNA-ekspresjon for synaptopodin, nestin og CD2-assosiert protein ble påvist, men podocin mRNA var fraværende i alle kloner. I tillegg til problemene med urinpodocytter, inneholder disse cellene også det innsatte immortaliserende genet, noe som resulterer i ulempene diskutert ovenfor.
I motsetning til dette har humane induserte pluripotente stamceller (hiPSCs) en enorm kapasitet til selvfornyelse og differensiering til flere celletyper under passende forhold. Det har tidligere blitt vist at hissc kan tjene som en nesten ubegrenset kilde til podocytter27,28.
Her beskrives en totrinnsprotokoll for å generere pasientspesifikke podocytter fra dermale fibroblaster av hudstansebiopsier med påfølgende episomal omprogrammering til hissc og endelig differensiering til hisc-deriverte podocytter (figur 1).
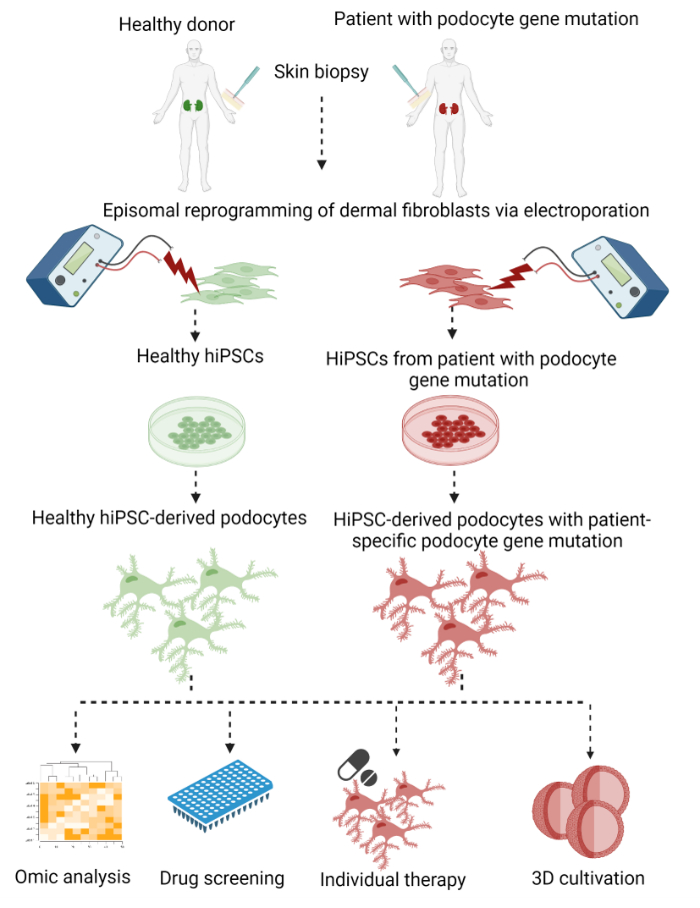
Figur 1: Protokoll for å generere pasientspesifikke hiPSC-deriverte podocytter. Grafisk oversikt over protokollen for å generere pasientspesifikke podocytter fra dermale fibroblaster av en hudbiopsi ved omprogrammering til hisscc og differensiering til podocytter. Klikk her for å se en større versjon av denne figuren.
Som et første skritt ble somatiske dermale fibroblaster vokst ut fra en hudstansebiopsi og omprogrammert til hiPSCs ved hjelp av en integrasjonsfri metode ved elektroporering med plasmider som uttrykker transkripsjonsfaktorene OCT3/4, KLF4, SOX2 og c-MYC 29,30,31. Oppståtte hiPSC-kolonier ble senere valgt og utvidet. Differensiering begynte med induksjon av mesodermal avstamning ved aktivering av WNT-signalveien, etterfulgt av generering av nephron-stamceller som fortsatt var i stand til å spre seg. Til slutt ble cellene differensiert til podocytter. I denne prosedyren modifiserte og kombinerte vi tidligere publiserte protokoller for episomal omprogrammering for generering av hiPSCs av Bang et al.32 og Okita et al.33, samt en protokoll for differensiering av hissc i podocytter av Musah et al.28,34,35.
Faktisk hadde podocytter generert av vår protokoll en fenotype nærmere podocytter in vivo, angående utviklingen av et distinkt nettverk av primære og sekundære fotprosesser og ekspresjonen av podocyttspesifikke markører, som synaptopodin, podocin og nephrin. Ved bruk av hiPSC-avledede podocytter opprettholdes pasientens genetiske bakgrunn under omprogrammering og differensiering. Dette muliggjør pasientspesifikk podocyttsykdomsmodellering og oppdagelse av potensielle terapeutiske stoffer ex vivo i et nesten ubegrenset celleantall. Videre er denne protokollen minimalt invasiv, kostnadseffektiv, etisk akseptabel og kan legge til rette for nye veier for narkotikautvikling.
Protocol
Representative Results
Discussion
Denne cellekulturbaserte protokollen kombinerer episomal omprogrammering av humane dermale fibroblaster til pasientspesifikke hiPSCer og påfølgende differensiering til hiPSC-avledede podocytter. Dette gjør at vi kan studere mutasjonsrelaterte endringer av podocytter fra pasienter med genetisk glomerulær sykdom angående podocyttskade. Protokollen for å omprogrammere dermale fibroblaster med en integrasjonsfri metode ved elektroporering er tilpasset fra det publiserte arbeidet til Bang et al.32 og Okita et al.33. Protokollen for å skille podocytter fra hiPSCs er tilpasset fra den publiserte protokollen fra Musah et al.28,34,35. Det finnes allerede publikasjoner som beskriver genereringen av podocytter fra hiPSCs 27,34,35. Imidlertid er protokollen gitt her optimalisert og billigere med hensyn til differensiering av hissc i podocytter. Sammenlignet med den publiserte protokollen fra Musah et al., testet vi denne protokollen på forskjellige beleggreagenser, som vitronectin, laminin silke-511 og solubilisert kjellermembranmatrise. Konsentrasjonene av vitronectin og laminin silke-511 kunne reduseres til 2,5 μg/ml i stedet for 5 μg/ml 28,34,35. Videre var det mulig å redusere konsentrasjonene av BMP7 og activin A-to svært dyre vekstfaktorer med 50%, fra 100 ng / ml til 50 ng / ml.
Dette muliggjør rimeligere differensiering. Nephrons stamceller fra dag 7 spredte seg fortsatt, og muligheten for frysing ble vist tidligere. Vi utvidet disse cellene etter tining og før endelig differensiering i basisk medium som inneholder Dulbeccos modifiserte Eagle-medium (DMEM) og B27 i flere dager, noe som reduserte kostnadene ytterligere. I tillegg til differensieringstrinnene beskriver denne protokollen utveksten av fibroblaster fra hudbiopsier med påfølgende generering av pasientspesifikke hiPSCer via episomal omprogrammering. Kombinasjonen av disse to metodene muliggjør generering av pasientspesifikke podocytter. Derfor er det gitt en komplett trinnvis protokoll for å generere pasientspesifikke hiPSC-avledede podocytter her som ikke ble beskrevet før i så detalj.
Siden den overordnede protokollen inneholder flere forskjellige celletyper, er det avgjørende å karakterisere de genererte celletypene på forskjellige trinn. Celler er i kultur i lengre tid, så kvalitetskontroll bør utføres ved forskjellige passasjer. Når du arbeider med hiPSCs, er daglig fôring samt overvåking av celleatferd og morfologi nødvendig. Steriliteten til differensieringsmediet må sikres ved filtersterilisering gjennom et 0,2 μm filter. Hele protokollen, fra hudbiopsi til hiPSC-avledede podocytter, tar flere måneder, men det er mulig å fryse cellene på forskjellige stadier av prosessen. Fibroblaster, utvalgte hiPSC-kloner og proliferative nephron-stamceller etter 7 dager i nephronprogenitordifferensieringsmedium kan fryses, og en fungerende cellebank kan genereres.
Selv om hiPSC-deriverte friske podocytter utvikler et distinkt nettverk av primære og sekundære fotprosesser (figur 5A,B) og uttrykker typisk podocyttspesifikk markør (figur 6A-C), er karakteristiske spaltemembraner, sett in vivo, vanskelig å etterligne i klassiske todimensjonale cellekulturmodeller. Videre er intercellkommunikasjon med andre glomerulære celletyper ikke mulig i denne monokulturinnstillingen.
På grunn av deres terminale differensierte tilstand og mangel på spredningskapasitet er det vanskelig å studere podocytter ex vivo. Ved hjelp av betinget immortalisering av primære podocytter er det mulig å overvinne denne begrensningen ved innsetting av en termosensitiv bryter, noe som resulterer i en cellekulturmodell hvor celler prolifererer ved 33 °C og differensierer ved 37 °C13,14. Selv om disse ciPodocytter har høyt potensial for podocyttforskning, er det begrensninger, som mangel på markøruttrykk, dedifferensiert morfologi og manglende dannelse av fotprosesser15,16.
Differensieringen av podocytter fra pasientavledede somatiske celler muliggjør generering og sammenligning av syke podocytter med friske kontrollceller ex vivo. Dette gjør oss i stand til å studere podocyttskader på grunn av mutasjoner i podocyttspesifikke gener. Videre har arbeid med hiPSCs potensialet for å skape tredimensjonale cellekultursykdomsmodeller, eller rettere organoider43,44. Samkultur av hiPSC-avledede podocytter med andre glomerulære celler, som glomerulære endotelceller eller mesangialceller, kan føre til ny innsikt om intercellulær kommunikasjon i helse og glomerulær sykdom.
Videre kan karakterisering og behandling av de pasientspesifikke podocyttene utføres ex vivo i høy gjennomstrømningsanalyse. Den individualiserte tilnærmingen åpner muligheten til å undersøke nye terapeutiske mål for spesifikke mutasjoner og å utføre individualisert medisin i fremtiden.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble finansiert av Interdisciplinary Center for Clinical Research (IZKF) ved Friedrich-Alexander University Erlangen-Nürnberg med stipendnummer M4-IZKF-F009 gitt til Janina Müller-Deile, og av Bundesministerium für Bildung und Forschung (BMBF) under prosjektnavnet STOP-FSGS-Speed Translation-Oriented Progress to Treat FSGS, stipendnummer 01GM2202D gitt til Janina Müller-Deile. Vi takker Annalena Kraus for støtten til å ta SEM-bilder.
Materials
| 0.2 µm sterile filter | Rotilab | P668.1 | for sterilization of differentiation medium |
| all-trans retinoic acid | Stem Cell Technologies | 72262 | supplement for differentiation |
| B27 supplement (50 x), serum free | Gibco | 17504044 | supplement for serum-free differentiation medium |
| BG iMatrix-511 Silk | biogems | RL511S | additional option of extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture |
| Bovine serum albumin (BSA) | Roth | 8076.4 | |
| CELLSTAR Filter Cap Cell Culture Flasks, T75, 250 mL | Greiner bio-one | 82050-856 | cell culture plastics suitable for fibroblast culture |
| CHIR99021 (5 mg) | Sigma-Aldrich | 252917-06-9 | supplement for differentiation |
| Corning Matrigel hESC qualified matrix | Corning | 354277 | additional option of extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture (solubilized basement membrane matrix) |
| countess Cell Counting Chamber Slides | Invitrogen | C10283 | to count cells |
| countess II FL Automated Cell Counter | Invitrogen | to count cells | |
| cryoPure tubes, 2 ml, QuickSeal screw cap, white | Sarstedt | 72380 | cryovials for freezing of cells |
| dimethyl sulfoxide (DMSO) | Roth | A994.1 | for fibroblast freezing medium |
| DMEM/F12 (1:1) (1 x) | Gibco | 11320074 | basic medium for differentiation |
| DMEM/F12 + Glutamax | Gibco | 10565018 | basic medium for fibroblast medium |
| EVOS M5000 Imaging System | Thermo Fisher Scientific | AMF5000 | phase contrast microscope |
| fetal bovine serum premium, inactivated (FCS) | PAN Biotech | P301902 | serum for fibroblast medium, fibroblast freezing medium and podocyte maintenance medium |
| fisherbrand Electroporation Cuvettes Plus, 4 mm gap, 800 µL capacity, sterile | Fisherbrand | FB104 | cuvette used for electroporation/episomal reprogramming of fibroblasts (4mm gap) |
| fluoromount-G Mounting Medium, with DAPI | Invitrogen | 00-4959-52 | mounting medium containing dapi |
| gauge needle (0.6 x 30 mm) | BD Microlance3 | 300700 | for separation of hiPSC colonies into small pieces |
| human Recombinant Activin A Protein | 78001.1 | Stem cell technologies | supplement for differentiation |
| human recombinant bone morphogenetic protein 7 (BMP7) | Peprotech | 120-03P | supplement for differentiation |
| human VEGF-165 Recombinant Protein | Thermo Scientific | PHC9394 | supplement for differentiation |
| insulin-transferrin-selenium (ITS -G) (100 x) | Gibco | 41400045 | supplement for podocyte maintenance medium |
| LB medium | Roth | X964.1 | for sterility test of hiPSC culture |
| lookOut Mycoplasma PCR Detection Kit | Sigma Aldrich | MP0035-1KT | commercial mycoplasma detection kit |
| microscope slides | Diagonal GmbH & Co.KG | 21,102 | |
| microtube 1.5 mL | Sarstedt | 72706400 | |
| mTeSR1 Complete Kit | Stem Cell Technologies | 85850 | basic medium for serum-free hiPSC culture medium |
| nalgene freezing container Mr.Frosty | Roth | AC96.1 | to ensure optimal freezing conditions |
| normal goat serum | abcam | ab 7481 | for preincubation solution and antibody diluent |
| nunc 24 well plates | Thermo Scientific | 142485 | cell culture plastics suitable for hiPSC culture |
| nunc 48 well plates | Thermo Scientific | 152640 | cell culture plastics suitable for hiPSC culture |
| nunc 6 well plates | Thermo Scientific | 140685 | cell culture plastics suitable for hiPSC culture |
| nunc EasYDish Dishes 100 mm | Thermo Scientific | 150466 | cell culture plastics suitable for hiPSC culture |
| nunc MicroWell 96-Well, Nunclon Delta-Treated, Flat-Bottom Microplate | Thermo Scientific | 167008 | cell culture plastics suitable for hiPSC culture |
| nutriFreez D10 Cryopreservation Medium | Sartorius | 05-713-1E | serum-free cryopreservation medium for cryopreservation of hiPSC and nephron progenitor cells |
| Opti-MEM | Gibco | 11058021 | electroporation medium |
| pCXLE-hMLN | Addgene | #27079 | plasmid for episomal reprogramming |
| pCXLE-hOCT3/4 plasmid | Addgene | #27077 | plasmid for episomal reprogramming |
| pCXLE-hSK plasmid | Addgene | #27078 | plasmid for episomal reprogramming |
| penicillin-streptomycin | Sigma-Aldrich | P4333-100ML | to avoid bacterial contamination |
| plastic coverslips | Sarstedt | 83.1840.002 | for immunofluorescent stainings of hiPSCs and hiPSC-derived podocytes |
| ROTI Histofix | Roth | P087.3 | commercial paraformaldehyde (4 %) for fixation of cells |
| RPMI 1640 + L-Glutamine | Gibco | 21875034 | basic medium for podocyte maintenance medium |
| staining chamber StainTray Black lid | Roth | HA51.1 | |
| stemPro Accutase Cell Dissociation Reagent | Gibco | A1110501 | enzymatic cell detachment solution used for dissociation of hiPSCs |
| sterile phosphate buffered saline (PBS) (1 x) | Gibco | 14190094 | used for washing and coating |
| sterile water | Roth | T1432 | |
| syringe without needle 20 mL | BD Plastipak | 300629 | to filter sterilize differentiation medium |
| TC dish 100 mm | Sarstedt | 8,33,902 | sterile cell culture plastics used for cutting the skin biopsy and fibroblast culture |
| TC dish 35 mm | Sarstedt | 8,33,900 | sterile cell culture plastics used for outgrowing fibroblasts from skin biopsy |
| triton X 100 | Roth | 3051.3 | for preincubation solution |
| trypan Blue Stain (0.4 %) for use with the Countess Automated Cell Counter | Invitrogen | T10282 | to count cells |
| trypsin-EDTA (10 x) | Biowest | X0930-100 | dissociation reagent used for fibroblasts and nephron progenitor cells |
| tube 15 mL | Greiner bio-one | 188271-N | |
| tube 50 mL | Greiner bio-one | 227261 | |
| vitronectin ACF | Sartorius | 05-754-0002 | extracellular matrix reagent used in coating solution to coat cell culture plastics suitable for hiPSC culture |
| Y-27632 dihydrochloride (10 mg) | Tocris | 1254 | to avoid apoptosis of hiPSCs during splitting |
| Primary antibodies | |||
| OCT4 | Stem Cell Technologies | 60093.1 | pluripotency marker, dilution 1:200 |
| SSEA-4 | Stem Cell Technologies | 60062FI.1 | pluripotency marker, dilution 1:100 |
| Ki67 | Abcam | ab15580 | proliferation marker, dilution 1:300 |
| synaptopodin | Proteintech | 21064-1-AP | podocyte-specific marker, dilution 1:200 |
| nephrin | Progen | GP-N2 | podocyte-specific marker, dilution 1:25 |
| podocin | proteintech | 20384-1-AP | podocyte-specific marker, dilution 1:100 |
| Secondary antibodies | |||
| goat anti-Guinea Pig IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 555 | Invitrogen | A21435 | secondary anditbody, dilution 1:1000 |
| alexa Fluor 647 Goat Anti-Rabbit SFX Kit, highly cross-adsorbed | Invitrogen | A31634 | secondary anditbody, dilution 1:1000 |
| donkey anti-Rabbit IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 488 | Invitrogen | A21206 | secondary anditbody, dilution 1:1000 |
| goat anti-Mouse IgG (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor 555 | Invitrogen | A21422 | secondary anditbody, dilution 1:1000 |
| goat anti-Mouse IgG (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor 488 | Invitrogen | A11001 | secondary anditbody, dilution 1:1000 |
References
- Mundel, P., et al. Rearrangements of the cytoskeleton and cell contacts induce process formation during differentiation of conditionally immortalized mouse podocyte cell lines. Experimental Cell Research. 236 (1), 248-258 (1997).
- Grgic, I., et al. Imaging of podocyte foot processes by fluorescence microscopy. Journal of the American Society of Nephrology. 23 (5), 785-791 (2012).
- Grahammer, F., Schell, C., Huber, T. B. The podocyte slit diaphragm-from a thin grey line to a complex signalling hub. Nature Reviews Nephrology. 9 (10), 587-598 (2013).
- Deen, W. M., Lazzara, M. J., Myers, B. D. Structural determinants of glomerular permeability. American Journal of Physiology. Renal Physiology. 281 (4), F579-F596 (2001).
- Schell, C., Huber, T. B. The evolving complexity of the podocyte cytoskeleton. Journal of the American Society of Nephrology. 28 (11), 3166-3174 (2017).
- Muller-Deile, J., Schiffer, M. Podocyte directed therapy of nephrotic syndrome-can we bring the inside out. Pediatric Nephrology. 31 (3), 393-405 (2016).
- Boehlke, C., et al. Hantavirus infection with severe proteinuria and podocyte foot-process effacement. American Journal of Kidney Diseases. 64 (3), 452-456 (2014).
- Schiffer, M., et al. Pharmacological targeting of actin-dependent dynamin oligomerization ameliorates chronic kidney disease in diverse animal models. Nature Medicine. 21 (6), 601-609 (2015).
- Kopp, J. B., et al. Podocytopathies. Nature Reviews. Disease Primers. 6 (1), 68 (2020).
- Wiggins, R. C. The spectrum of podocytopathies: a unifying view of glomerular diseases. Kidney International. 71 (12), 1205-1214 (2007).
- Mundel, P., Reiser, J., Kriz, W. Induction of differentiation in cultured rat and human podocytes. Journal of the American Society of Nephrology. 8 (5), 697-705 (1997).
- Jat, P. S., et al. Direct derivation of conditionally immortal cell lines from an H-2Kb-tsA58 transgenic mouse. Proceedings of the National Academy of Sciences. 88 (12), 5096-5100 (1991).
- Saleem, M. A., et al. A conditionally immortalized human podocyte cell line demonstrating nephrin and podocin expression. Journal of the American Society of Nephrology. 13 (3), 630-638 (2002).
- Eto, N., et al. Podocyte protection by darbepoetin: preservation of the cytoskeleton and nephrin expression. Kidney International. 72 (4), 455-463 (2007).
- Krtil, J., Platenik, J., Kazderova, M., Tesar, V., Zima, T. Culture methods of glomerular podocytes. Kidney & Blood Pressure Research. 30 (3), 162-174 (2007).
- Chittiprol, S., Chen, P., Petrovic-Djergovic, D., Eichler, T., Ransom, R. F. Marker expression, behaviors, and responses vary in different lines of conditionally immortalized cultured podocytes. American Journal of Physiology. Renal Physiology. 301 (3), F660-F671 (2011).
- Shih, N. Y., et al. CD2AP localizes to the slit diaphragm and binds to nephrin via a novel C-terminal domain. The American Journal of Pathology. 159 (6), 2303-2308 (2001).
- Yan, K., Khoshnoodi, J., Ruotsalainen, V., Tryggvason, K. N-linked glycosylation is critical for the plasma membrane localization of nephrin. Journal of the American Society of Nephrology. 13 (5), 1385-1389 (2002).
- Sir Elkhatim, R., Li, J. Y., Yong, T. Y., Gleadle, J. M. Dipping your feet in the water: podocytes in urine. Expert Review of Molecular Diagnostics. 14 (4), 423-437 (2014).
- Camici, M. Urinary detection of podocyte injury. Biomedicine & Pharmacotherapy. 61 (5), 245-249 (2007).
- Muller-Deile, J., et al. Overexpression of preeclampsia induced microRNA-26a-5p leads to proteinuria in zebrafish. Scientific Reports. 8 (1), 3621 (2018).
- Schenk, H., et al. Removal of focal segmental glomerulosclerosis (FSGS) factor suPAR using CytoSorb. Journal of Clinical Apheresis. 32 (6), 444-452 (2017).
- Petermann, A., Floege, J. Podocyte damage resulting in podocyturia: a potential diagnostic marker to assess glomerular disease activity. Nephron. Clinical Practice. 106 (2), c61-c66 (2007).
- Vogelmann, S. U., Nelson, W. J., Myers, B. D., Lemley, K. V. Urinary excretion of viable podocytes in health and renal disease. American Journal of Physiology. Renal Physiology. 285 (1), F40-F48 (2003).
- Petermann, A. T., et al. Podocytes that detach in experimental membranous nephropathy are viable. Kidney International. 64 (4), 1222-1231 (2003).
- Sakairi, T., et al. Conditionally immortalized human podocyte cell lines established from urine. American Journal of Physiology. Renal Physiology. 298 (3), F557-F567 (2010).
- Rauch, C., et al. Differentiation of human iPSCs into functional podocytes. PLoS One. 13 (9), e0203869 (2018).
- Musah, S., et al. Mature induced-pluripotent-stem-cell-derived human podocytes reconstitute kidney glomerular-capillary-wall function on a chip. Nature Biomedical Engineering. 1, 0069 (2017).
- Takahashi, K., Okita, K., Nakagawa, M., Yamanaka, S. Induction of pluripotent stem cells from fibroblast cultures. Nature Protocols. 2 (12), 3081-3089 (2007).
- Takahashi, K., Yamanaka, S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell. 126 (4), 663-676 (2006).
- Teshigawara, R., Cho, J., Kameda, M., Tada, T. Mechanism of human somatic reprogramming to iPS cell. Laboratory Investigation. 97 (10), 1152-1157 (2017).
- Bang, J. S., et al. Optimization of episomal reprogramming for generation of human induced pluripotent stem cells from fibroblasts. Animal Cells and Systems. 22 (2), 132-139 (2018).
- Okita, K., et al. A more efficient method to generate integration-free human iPS cells. Nature Methods. 8 (5), 409-412 (2011).
- Musah, S., Dimitrakakis, N., Camacho, D. M., Church, G. M., Ingber, D. E. Directed differentiation of human induced pluripotent stem cells into mature kidney podocytes and establishment of a Glomerulus Chip. Nature Protocols. 13 (7), 1662-1685 (2018).
- Burt, M., Bhattachaya, R., Okafor, A. E., Musah, S. Guided differentiation of mature kidney podocytes from human induced pluripotent stem cells under chemically defined conditions. Journal of Visualized Experiments. (161), e61299 (2020).
- Vangipuram, M., Ting, D., Kim, S., Diaz, R., Schule, B. Skin punch biopsy explant culture for derivation of primary human fibroblasts. Journal of Visualized Experiments. (77), e3779 (2013).
- Hoffding, M. K., Hyttel, P. Ultrastructural visualization of the Mesenchymal-to-Epithelial Transition during reprogramming of human fibroblasts to induced pluripotent stem cells. Stem Cell Research. 14 (1), 39-53 (2015).
- Bharathan, S. P., et al. Systematic evaluation of markers used for the identification of human induced pluripotent stem cells. Biology Open. 6 (1), 100-108 (2017).
- Scholzen, T., Gerdes, J. The Ki-67 protein: from the known and the unknown. Journal of Cellular Physiology. 182 (3), 311-322 (2000).
- Sun, X., Kaufman, P. D. Ki-67: more than a proliferation marker. Chromosoma. 127 (2), 175-186 (2018).
- Vaz, I. M., et al. Chromosomal aberrations after induced pluripotent stem cells reprogramming. Genetics and Molecular Biology. 44 (3), 20200147 (2021).
- Reiser, J., Altintas, M. M. Podocytes. F1000Research. 5, 114 (2016).
- Ohmori, T., et al. Impaired NEPHRIN localization in kidney organoids derived from nephrotic patient iPS cells. Scientific Reports. 11 (1), 3982 (2021).
- Morizane, R., Bonventre, J. V. Generation of nephron progenitor cells and kidney organoids from human pluripotent stem cells. Nature Protocols. 12 (1), 195-207 (2017).

