- 00:00Vue d'ensemble
- 01:28Principles of Soil Nutrient Analysis
- 04:12Extraction of Nutrients
- 06:21Analyzing Samples for Nitrate
- 07:52Analyzing Samples for Phosphate
- 09:16Analyzing Samples for Potassium
- 11:13Applications
- 13:08Summary
Analyse des éléments nutritifs du sol : azote, phosphore et potassium
English
Diviser
Vue d'ensemble
Source : Laboratoires de Margaret Workman et Kimberly Frye – Depaul University
Dans cette expérience, trois macronutriments de sol sont chimiquement extraite, combinée avec des réactifs à base de couleur, puis analysées à l’aide de couleurs pour déterminer la concentration des éléments nutritifs présente dans l’échantillon de sol.
Azote, phosphore et potassium sont les principaux composants des engrais de sol. Ces méthodes isolent chaque élément nutritif du sol dans une solution qui peut être analysée à l’aide de la turbidité et la couleur pour déterminer la concentration des nutriments présents dans l’échantillon de sol. Connaissant la concentration actuelle informe les scientifiques environnementaux d’une carence nutritionnelle ou d’excédent dans les sols utilisés pour soutenir la production végétale et donne également une idée générale dans les cycles biogéochimiques fondamentales d’un écosystème.
Principles
Lorsque chimiquement isolées du sol, éléments nutritifs peuvent être détectés à l’aide de cette technique. Azote et phosphore, trouve généralement sous forme de nitrates et de phosphates, sont extraites avec un extractant chimique qui lie l’élément nutritif d’intérêt. Une fois extrait du sol, chaque élément nutritif est cumulable avec un réactif connu qui provoque la solution nutritive remplacer une couleur de nutriments spécifiques dans une relation linéaire, avec une couleur plus foncée, ce qui indique une concentration accrue d’éléments nutritifs. Pour analyser la concentration de chaque substance nutritive, un réactif chimique serviront à la couleur de chaque échantillon avec une augmentation dans l’intensité de couleur indiquant l’augmentation de la concentration d’éléments nutritifs.
Dans les essais de nitrate élevé et moyen de gamme, cadmium métallique est utilisé pour réduire les nitrates (n °3–) en nitrites (NO2–). Le cadmium est contenu dans l’acheté 5 Nitraver (haute et moyenne gamme) et 6 Nitraver (gamme basse) oreillers de poudre.
PAS3– + Cd + 2 H+ → NO2– + Cd2 + + H2O
Les ions nitrites réagissent ensuite avec l’acide sulfanilique (dans un milieu acide contenu dans la poudre de NitraVer 5) pour former un sel de diazonium intermédiaire. Lorsqu’il est couplé avec l’acide gentisique (également contenue dans les 5 NitraVer), une solution de couleur ambre est formée. Intensité de la couleur de ce composé est directement proportionnelle à la concentration de nitrates de l’échantillon de l’eau et peut être quantifiée en utilisant la boîte de comparateur de couleur nitrate avec un disque de couleur ambre nitrate continue.
Pour le phosphore, le sodium molydate et pyrosulfate de potassium dans la poudre de réactif PhosVer 3 achetée réagissent avec les phosphates solubles réactifs pour former un complexe phospho-molybdate.
H 2 PO 4 – 12 Na2MoO4 + → BP12O403-
Le complexe est ensuite réduit par l’acide ascorbique (également contenue dans PhosVer 3 poudre) pour former une couleur bleu de molybdène. La couleur bleue est quantifiée à l’aide d’une boîte de comparateur de couleur de phosphate avec un disque de couleur bleue continue de phosphate.
Une boîte de comparateur de couleur est utilisée pour cette méthode. Cet outil fonctionne selon des intensités de couleur connue pour chaque concentration entre 0-50 mg/L. Un disque de couleur sur la boîte est tourné jusqu’à ce que la couleur dans les deux fenêtres matches (blancs et échantillons). Une fois que les couleurs correspondent, la concentration en éléments nutritifs (mg/L) s’affichera dans une fenêtre séparée plus faible sur la zone de comparaison de couleur. Ces boîtes sont assez robustes pour être utilisé avec les élèves à tous les niveaux jusqu’à cours introductif et peuvent facilement être transportés dans le cadre d’un sol de champ kit qui peut être utilisée à un emplacement de prélèvement d’échantillons pour tester. Ces méthodes permettent de base nutritive tests en laboratoire en classe sans nécessiter de coûteux pièces d’équipement qui n’est peut-être pas disponible. Pour assurer l’exactitude d’essai, les nitrates et les phosphates des solutions standards peuvent être utilisées à la place un échantillon dans les procédures avant de voyager au terrain ou au début de l’analyse des échantillons de sol en laboratoire.
Dans les tests de potassium, les ions de potassium combinent avec tétraphénylborate de sodium contenue dans la poudre de réactif de Potassium 3 achetée pour former de tétraphénylborate de potassium, un précipité blanc. Le précipité reste en suspension dans les échantillons, causant une augmentation de la turbidité.
AUCUN3– + Cd + 2 H+ ne NaB (C6H5)4 + K+ → Ko (C6H5)4 Na+
Une jauge de mesure de potassium est utilisée pour quantifier la quantité de turbidité qui est convertie à la concentration de potassium. La jauge d’huile a un point noir sur une extrémité qui est placée dans l’échantillon jusqu’à ce que le point n’est donc plus visible à travers le précipité blanc. La jauge est progressivement marquée pour indiquer une échelle de visibilité qui est ensuite convertie en concentration de potassium avec un tableau de conversion. Cette méthode est une procédure peu coûteuse avec équipement minimal qui peut être transporté vers un site d’échantillonnage en plein air et assez robuste pour être utilisé avec les étudiants de tout niveau jusqu’à cours introductif.
Procédure
Résultats
Each nutrient analysis will result in a concentration reported in mg/L.
Nitrate and Phosphate concentrations will be determined with the color comparator boxes and display the result in the window.

Figure 1. Example color disks for nitrate (left) and phosphate (right) color comparator boxes. Color intensities are on the outer edge of the disks and nutrient concentration (mg/L) are on the inner edge of the disks.
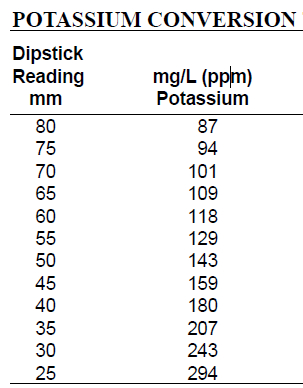
Table 1. Potassium Conversion Table used to convert dipstick potassium reading into mg/L. Locate the dipstick reading on the left column and record the corresponding mg/L concentration on the right column.
| Nitrogen | Phosphorus | Potassium | |
| Nutrient level range in ppm | |||
| Low | 0-15 | 0-25 | 0-60 |
| Medium | 15-30 | 25-50 | 60-100 |
| High | 30+ | 50+ | 100+ |
Table 2. Table of nutrient ranges arranged by categories.
Applications and Summary
Determining the nutrient concentrations for nitrate, phosphates, and potassium can reveal how a soil is functioning in regards to its intended use and how nutrients are cycling through a soil. A nutrient test provides a report of average nutrient concentration (mg/L) for all nutrients tested. In an agricultural setting, knowing the concentration of nutrients can help food producers know when to add fertilizer, how much to add, and which nutrients need supplemented and in what amount. Consistently high nitrogen soils, for instance, would be good for growing nitrogen-demanding crops such as soy and corn. High nitrogen levels are also particularly useful for non-flowering plants because nitrogen is required for any green part of plants. High nitrogen levels can suppress flowering however, if they remain higher than phosphorus levels. Phosphorus controls flowering in plants and is important to any plant production involving flowering or fruiting plants and phosphorus is often added to soils or directly to plants before and during flowering and fruiting life-cycle stages to increase agricultural yields in larger crop size and increased amounts of fruit production per plant. Potassium is involved in catalyzing many chemical reactions required to support plant life including drought tolerance and moisture regulation. Low potassium soils will likely need to be irrigated if soil amendment is not possible. Nutrient concentration can also inform of nutrient deficiencies or surpluses that can be detrimental to plant growth. If a nutrient is too high, amendments can be performed to reduce a surplus, such as adding mulch or tilling the soil. If nutrients are too low to support plant production, fertilization can be used to add nutrients in an amount needed for a specific crop. Low nutrient soil may also have more applicable uses to land managers for recreational or developed (paved surfaces or building construction) spaces.
Transcription
Soil nutrient analyses can be carried out to extract three major soil macronutrients, nitrogen, phosphorus, and potassium, and combine them with color-based reagents to determine their concentration.
Nitrogen, phosphorus, and potassium are major components of soil fertilizer. Knowing their concentration in soils can inform environmental scientists of nutrient deficiency or surplus in soils used to support plant production, and provide a general insight into the basic biogeochemical cycles of an ecosystem.
Soil nutrient analysis can be carried out using chemicals to bind the macronutrient of interest. For nitrogen or phosphorus, reagents are added which react to the presence of the specific macronutrient and produce colored products. Potassium concentration is determined by forming precipitates in an amount proportional to potassium concentration.
These methods are simple, inexpensive, require minimal equipment, and can be carried out in a field setting if desired. This video will illustrate the techniques used to extract and quantify these common soil macronutrients.
To begin analysis, macronutrients are first extracted from collected soil samples. Nitrogen is extracted using calcium sulfate; phosphorus and potassium are extracted using Mehlich 2 solution, a solution of acetic acid, ammonium chloride, hydrochloric acid, hydrofluoric acid, and demineralized water.Boundmacronutrients present in suspension can then be separated from the remaining solid soil components by vacuum filtration.
Once macronutrients have been extracted, their concentration can be determined. For nitrogen, cadmium metal is used to reduce nitrates to nitrites. This cadmium is present in pre-packaged pillows that are added to the soil filtrate. The nitrite ions react with sulfanilic acid to form diazonium salt. This couples with gentisic acid and an amber solution is formed.
For phosphorus, sodium molybdate reacts with the soluble reactive phosphate to form a phospho-molybdate complex. This is then reduced by ascorbic acid to form a molybdenum blue color.
The color intensity of both solutions is proportional to the nutrient concentration. Color comparator boxes are used for analysis of nitrate and phosphate. Samples are compared to a blank, and the color disk is turned until both viewing windows match. The corresponding nutrient concentration in mg/L will be displayed in a separate window. The color intensity of both solutions is proportional to the nutrient concentration.
To quantify potassium, the ions from the soil filtrate combine with sodium tetraphenylborate to form potassium tetraphenylborate, a white precipitate. The precipitate remains in suspension, causing an increase in turbidity.
A potassium dipstick is used to quantify turbidity caused by the precipitate. The dipstick is placed in the sample and lowered until the black dot at the end is no longer visible. The stick is incrementally marked, and readings on this scale can be converted to potassium concentration using a conversion chart.
Now that we are familiar with the principles behind extraction and quantification of soil macronutrients, let’s take a look at how the procedures are carried out in the laboratory.
Once the soil samples have been collected, correctly transported, and stored, they can be brought into the laboratory for analysis, beginning with the nitrogen extraction. First, turn on the balance, set a weigh boat on top, and tare.
Using a spatula, weigh out 10 g of dried, sieved soil sample and transfer to a labeled 100-mL beaker. Next, weigh 0.1 g of calcium sulfate and transfer it to the beaker.
Measure out 20 mL of deionized water with a graduated cylinder and transfer to the beaker. Thoroughly mix the contents of the beaker with a stirring rod. Repeat these additions for each test soil sample. Secure samples on a tabletop shaker and agitate for 1 min.
To begin extraction of phosphorus and potassium from the soils, use a spatula to weigh out 2 g of dried, sieved soil sample, and transfer to a labeled 100-mL beaker. With a graduated cylinder, measure 20 mL of Mehlich 2 soil extractant and transfer to the beaker. Thoroughly mix the contents of the beaker with a stir rod. Secure samples on a tabletop shaker and agitate for 5 min. After extraction, all three nutrient sample sets should be vacuum filtered using a vacuum flask and Büchner funnel.
First, turn on the vacuum jet and slowly pour the soil extract solution into the funnel. Extract should drain from the funnel, into the flask. Pour the filtrate into a clean, labeled 50-mL beaker. Remove the funnel, discard filter paper, and rinse funnel and flask with deionized water. Use an air jet to dry the funnel and flask.
Now the nutrient samples have been filtered, content analysis can begin. For each nutrient test, begin by labeling a color viewing tube with an “S”, for sample. Label a second with a “B” for blank.
Thoroughly rinse both color viewing tubes with deionized water, then shake to remove the remaining rinse water. Add the sample extract to a depth of ¼ inch in the color viewing tube marked “S”. Cap the tube with a rubber stopper and shake for 3 s, then discard the solution.
Next, add the sample extract to both tubes until the meniscus is even with the 5-mL mark on the tubes, at the bottom of the frosted area. Add the contents of one nitrogen reagent pillow to the tube marked “S”. Cap and shake the tube vigorously for 1 min. Immediately place both tubes into the comparator, with tube “B” in the outside hole, and tube “S” on the inside. Leave for 5 min.
Hold the comparator up to a light source and rotate the disc until the color in the window for tube “B” matches that in the window for tube “S”. Record the concentration value displayed in the lower window of the color comparator box.
Samples can also be analyzed for phosphate content using the color comparator. Using a dropper, add 2.5 mL of the filtered phosphorus sample extract to a 25 mL graduated cylinder. Add deionized water to the 25 mL mark, cap with a stopper, and invert to mix. Add the diluted sample extract to about ¼ inch deep in the color viewing tube marked “S” to rinse the tube. Cap with a rubber stopper, and shake for a few seconds before discarding the solution.
Into both tubes, add the sample extract until the meniscus is even with the 5 mL mark. Add the contents of one phosphorus reagent pillow to the “S” tube, cap, and shake vigorously for 1 min. Immediately place the color tubes into the color comparator, with the blank tube in the outside hole, and the sample tube in the inside hole. Leave for 3 min. Hold the comparator up to a light source, and rotate the disc until the window for tube “B” matches the color in the window for tube “S”. Record the value displayed in the window.
Finally, samples can be analyzed for potassium content. Using a dropper, add 3 mL of potassium sample extract to a 25 mL cylinder. Add deionized water to the 21 mL mark on the cylinder, cap firmly with a rubber stopper, and invert. Next, add one potassium 2 reagent pillow to the cylinder. Add 3 mL of an alkaline EDTA solution to the cylinder, cap with a rubber stopper, and invert several times to mix. Let the solution stand for 3 min. Add the contents of one potassium reagent pillow, cap the cylinder and shake vigorously for 10 s. Allow the solution to stand for 3 min as a white turbidity develops.
Looking straight down into the cylinder, slowly insert the potassium dipstick vertically into the solution until the black dot is no longer visible from above. Hold the dipstick in position and rotate the cylinder to view the scale. Record the number on the dipstick scale where the surface of the sample meets the dipstick. Refer to the potassium conversion table to determine the concentration of samples in mg/L. Locate the dipstick reading in the left hand column, and record the corresponding mg/L concentration reported in the right hand column.
Once concentrations are obtained, a table of nutrient ranges can be used to assess sample quality and determine whether sampled soil needs nutrient amendment, and if so, how much. Nutrient amendment can be carried out by application of specific fertilizers.
The ability to analyze the soil nutrient composition of soils has a wide variety of applications, with potential implications for human populations or agricultural ecosystems.
Different crop plants will have different potential nutrient requirements for optimal growing. For example, high nitrogen levels are needed for growing nitrogen-demanding crops, such as soy and corn. High levels of phosphorus can stimulate and enhance flower or fruit production. The ability to measure soil nutrient composition in an intended crop growing area can therefore allow farmers or land managers to supplement the soil with necessary nutrients to grow their intended crop successfully.
The composition of soil can also have implications for its ability to retain water, which can in turn influence its ability to support different flora or fauna. For example, low potassium soils have poor drought tolerance, and may require nutrient amendment, by fertilization of the soil with appropriate amounts of the missing nutrient. Alternatively, irrigation may be necessary to grow any plants that do not display high drought tolerance.
Soil composition and nutrient quality can also help inform land managers to designate appropriate land-use. In areas where the soil has poor nutrient quality, that would require heavy modification or supplementation to grow crop plants, setting aside land for development of buildings or structures may be more appropriate. Alternatively, areas with ideal composition for intended crop growing can be earmarked and set aside, protected from development.
You’ve just watched JoVE’s introduction to Soil Nutrient Analysis. You should now understand the importance of soil macronutrients, how to extract them from soils, and how to determine their concentrations. Thanks for watching!




