DNA metylering: Bisulphite Modifikasjon og analyse
Summary
Gullstandarden for DNA metylering analyse er genomisk sekvensering av bisulphite konvertert DNA. Denne metoden tar fordel av den økte følsomheten av cytosin, sammenlignet med 5-methylcytosine (5-MEC) til bisulphite deaminering henhold sure forhold. Unmethylated cytosines kan skilles fra denaturert cytosines etter PCR forsterkning av målet genomisk DNA.
Abstract
Epigenetikk beskriver arvelige endringer i gen-funksjon som oppstår uavhengig av DNA-sekvensen. Den molekylære grunnlaget for epigenetic genregulering er komplisert, men i hovedsak innebærer endringer av DNA selv eller proteiner som DNA kollegaer. Den dominerende epigenetic modifikasjon av DNA i mammalske genomer er metylering av cytosin nukleotider (5-MEC). DNA metylering gir instruksjon til genuttrykk maskiner om hvor og når genet skal uttrykkes. Den primære mål sekvens for DNA metylering i pattedyr er 5'-CpG-3 'dinucleotides (Figur 1). CpG dinucleotides er ikke jevnt fordelt i hele genomet, men er konsentrert i regioner av repetitive genomisk sekvenser og CpG "øyer" vanligvis forbindes med genet prosjektpartnere (figur 1). DNA metylering mønstre etableres tidlig i utviklingen, moduleres under vev spesifikke differensiering og forstyrret i mange sykdommer, inkludert kreft. Til understand den biologiske rolle DNA metylering og dens rolle i menneskelig sykdom, presis, effektiv og reproduserbare metoder er nødvendig for å oppdage og kvantifisere individuell 5-MeCs.
Denne protokollen for bisulphite konvertering er "gullstandarden" for DNA metylering analyse og enklere identifisering og kvantifisering av DNA metylering ved singel nukleotid oppløsning. Kjemien til cytosin deaminering av natrium bisulphite involverer tre trinn (figur 2). (1) sulfonert: Tilsetning av bisulphite til 5-6 doble bindingen av cytosin (2) hydrolic deaminering: hydrolytisk deaminering av den resulterende cytosin-bisulphite derivatet å gi en uracil-bisulphite derivat (3) Alkali Desulphonation: Fjerning av sulphonate gruppe ved en lutbehandling å gi uracil. Bisulphite deaminates fortrinnsvis cytosin til uracil i enkeltrom strandet DNA, mens 5-MEC er refraktær til bisulphite-mediert deaminering. Ved PCR forsterkning, er uracil forsterkessom tymin mens 5-MEC rester forbli som cytosines, slik denaturert CpGs skal skilles fra unmethylated CpGs ved tilstedeværelsen av en cytosin "C" versus tymin "T" rester under sekvensering.
DNA modifisering av bisulphite konvertering er en veletablert protokoll som kan utnyttes for mange metoder for DNA metylering analyse. Siden påvisning av 5-MEC ved bisulphite konvertering ble først demonstrert av Frommer et al. 1 og Clark et al. 2, metoder basert rundt bisulphite konvertering av genomisk DNA står for majoriteten av nye data om DNA metylering. Ulike metoder for post PCR-analyse kan benyttes, avhengig av graden av spesifisitet og oppløsning av metylering nødvendig. Kloning og sekvensering er fortsatt den mest lett tilgjengelig metode som kan gi single nukleotid oppløsning for metylering over DNA-molekylet.
Protocol
Discussion
DNA metylering analyse av genomisk sekvensering av bisulphite konvertert DNA er et veletablert og allsidig metode som muliggjør identifisering og kvantifisering av DNA metylering ved singel nukleotid oppløsning. Men avhengig bisulphite konvertering og påfølgende analyse på premisset om at DNA har blitt fullt konvertert med hver unmethylated cytosin blir deaminated til uracil og bare denaturert cytosines gjenværende un-reaktiv. Hvis konverteringen er ufullstendig, kan problemer oppstå med analyse siden uomvendte unmethylated cytosines kan feilaktig tolkes som denaturert cytosines. Bisulphite konvertering kan være optimalisert på ulike stadier for å maksimere andelen av konverteringen. For DNA å være fullt konvertert det først skal være singel strandet slik at cytosin rester blir utsatt for bisulphite ioner. Det første trinnet, DNA denaturering, er kritisk og kan være kilde til ufullstendig konvertering hvis DNA er ikke fullt denaturert. For å sikreat DNA er fullt denaturert det er viktig at reaksjonen parametere inkludert fjerning av alle assosiert protein, passende salt konsentrasjon, inkubasjonstemperatur og tid er egnet til å opprettholde DNA i single strandet konformasjon. Det er viktig å bruke friske 3M NaOH og å tillate tilstrekkelig inkubasjonstid. Hvis DNA er motstand denaturering, kan enkelte modifikasjoner til protokollen inkludert forlenge inkubasjonstiden til 30 minutter eller fragmentering av DNA før denaturering lette DNA denaturering. I tillegg kan enkelt strandet DNA (ssDNA) re-anneal å doble DNA (dsDNA) under bisulphite konverteringen reaksjon. Gjennomføring av reaksjonen ved høyere temperatur (90-95 ° C) enten periodevis eller kontinuerlig under bisulphite reaksjonen kan hjelpe vedlikehold av ssDNA. Det er imidlertid viktig å være klar over at DNA fornedrelse er sterkt akselerert på disse høyere temperaturer. Ulike reagenser kan også legges til forstyrre re-annealing av the DNA-strenger, som for eksempel urea.
Konsentrasjonen av DNA og dens kvalitet kan også påvirke effektiviteten av bisulphite reaksjonen og ultimate PCR yield. DNA nedbrytning er en begrensning av bisulphite konvertering protokollen. Den kjemiske behandlingen av DNA introduserer forskjellige tråd pauser i ssDNA og noen av de tøffe forholdene er nødvendig for fullstendig bisulphite konvertering inkludert høy bisulphite konsentrasjon, lang inkubasjonstider kan akselerere DNA degradering. Under standard reaksjonen forholdene beskrevet, er DNA degradering ikke et vanlig problem, men hvis protokoll modifikasjoner er innført, slik som for sekvenser som er refraktære til omvendelse, for DNA maler som er degradert eller av dårlig kvalitet som FFPE prøvene, da DNA-degradering kan bli en betydelig begrensning.
Formalinfikserte, parafin embedded (FFPE) og degradert DNA-prøver kan være effektivt bisulphite konvertert og forsterket bruke denne protokollenMen modifikasjoner for å sikre at DNA ikke er ytterligere degradert blir rådet. Bruk av en transportør RNA som t-RNA anbefales. Også glykogen kan legges som en transportør når DNA konsentrasjonen er lav (<200 ng). Fordi DNA isolert fra FFPE vev allerede er fragmentert og ytterligere fragmentering finner sted under deaminering, må man sørge for å minimere ytterligere degradering. Ikke fragment DNA ytterligere før denaturering og begrense inkubasjonstiden for bisulphite reaksjonen til 4 timer. Design amplicons ikke større enn 300 bp på grunn av fragmentert DNA.
En annen faktor som kan påvirke PCR amplifisering at bisulphite konvertering av unmethylated cytosines reduserer kompleksiteten i DNA-malen. Følgende primer designen protokoll beskrevet i pkt. 4.1, økt primer lengde og nestede PCR kan alle bidra til å øke spesifisitet og PCR yield.
Endelig er siden DNA-malen endret under bisulphITE konvertering, forsterkning bias kan være en bekymring. Sikre at proporsjonal PCR forsterkning av denaturert og unmethylated maler er merket med en kontroll 50/50 M / U DNA blanding, som beskrevet i protokollen, se Figur 3. Også sørge for at forsterkning av bare konvertert maler er oppstått bruker HpaIII begrensning enzym og gel elektroforese (figur 3). PCR-forholdene må være optimalisert ved å variere temperatur og / eller magnesium konsentrasjon eller forlenge forlengelse tid. Noen maler synes å være spesielt problematisk og primer posisjon må kanskje justeres eller degenererte primere må benyttes.
Neste generasjons sekvensering teknikker er i rask utvikling for å oppnå et lignende vedtak om å bisulphite genomisk sekvensering, og tredje generasjon eneste molekyl sekvensering har potensial for å tillate analyse av både primær DNA og metylering uten behov for bisulphite sekvensering. Men utbredt tilgjengelighet og specificity av disse teknikkene er fortsatt litt tid borte. Bisulphite genomisk sekvensering er gullstandarden i metylering analyse og er en robust protokoll. Metoden har kommet til punktet der felles problemer og begrensninger har blitt løst, og søknadene har ekspandert fra individ genet analyser til høy gjennomstrømming og hele genomet analyse beskrevet av Clark et al. 2006 4. Feilsøking retningslinjer og ytterligere anbefalinger er beskrevet i Tabell 1. Det foreslås at den optimale tilnærmingen er å begynne med følge standard protokollen og bare introdusere modifikasjon hvis og når et problem oppstår.
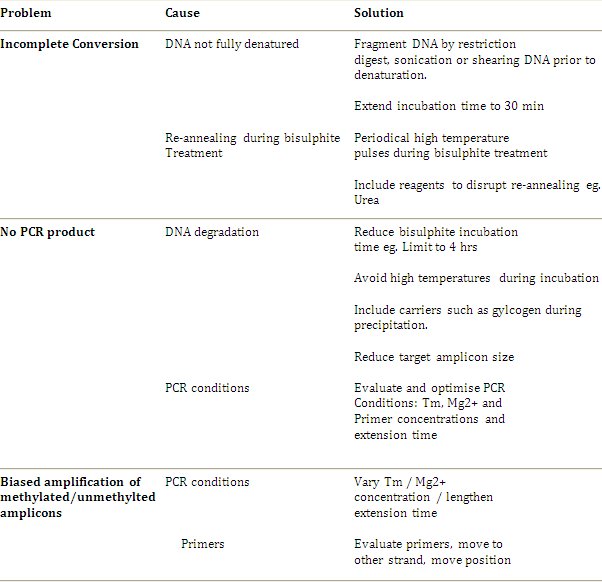
Tabell 1. Feilsøking Retningslinjer
Divulgazioni
The authors have nothing to disclose.
Materials
- Sodium Metabisulphite (Ajax Finechem)
- Hydroquinone (Merck)
- Wizard DNA-clean-up system (Promega)
Riferimenti
- Frommer, M. A genomic sequencing protocol that yields a positive display of 5-methylcytosine residues in individual DNA strands. Proc. Natl. Acad. Sci. U. S. A. 89, 1827-1831 (1992).
- Clark, S. J. High sensitivity mapping of methylated cytosines. Nucleic. Acids. Res. 22, 2990-2997 (1994).
- Grunau, C., Clark, S. J., Rosenthal, A. Bisulfite genomic sequencing: systematic investigation of critical experimental parameters. Nucleic. Acids. Res. 29, E65-E65 (2001).
- Clark, S. J. DNA methylation: bisulphite modification and analysis. Nat. Protoc. 1, 2353-2364 (2006).

