Interna och Observation av fluorescerande Biomolekyler i levande mikroorganismer via elektroporation
Summary
Studies of biomolecules in vivo are crucial for understanding molecular function in a biological context. Here we describe a novel method allowing the internalization of fluorescent biomolecules, such as DNA or proteins, into living microorganisms. Analysis of in vivo data recorded by fluorescence microscopy is also presented and discussed.
Abstract
The ability to study biomolecules in vivo is crucial for understanding their function in a biological context. One powerful approach involves fusing molecules of interest to fluorescent proteins such as GFP to study their expression, localization and function. However, GFP and its derivatives are significantly larger and less photostable than organic fluorophores generally used for in vitro experiments, and this can limit the scope of investigation.
We recently introduced a straightforward, versatile and high-throughput method based on electroporation, allowing the internalization of biomolecules labeled with organic fluorophores into living microorganisms. Here we describe how to use electroporation to internalize labeled DNA fragments or proteins into Escherichia coli and Saccharomyces cerevisiæ, how to quantify the number of internalized molecules using fluorescence microscopy, and how to quantify the viability of electroporated cells. Data can be acquired at the single-cell or single-molecule level using fluorescence or FRET. The possibility of internalizing non-labeled molecules that trigger a physiological observable response in vivo is also presented. Finally, strategies of optimization of the protocol for specific biological systems are discussed.
Introduction
De flesta fluorescens studier inuti levande celler är beroende av proteinfusioner med fluorescerande proteiner (fps), såsom GFP 1. Dessa fluorescerande taggar tillåter studier av antal kopior, spridningsbild eller lokalisering av proteiner involverade i processer såsom genuttryck eller membrantransport 2-7. Ramprogrammen erbjuder hög märkning specificitet, enkel implementering, och finns i en stor inventering av varianter med olika fotofysikaliska och kemiska egenskaper en. Emellertid organiska fluoroforer förblir det främsta valet för in vitro-försök på grund av deras större fotostabilitet (upp till 100-faldigt mer stabil än FPS) 8,9, liten storlek (upp till 100-faldigt mindre volym än FPS) och enkel intramolekylär märkning (huvudsakligen genom användningen av cysteinrester). Alla dessa faktorer är särskilt viktiga för enda molekyl fluorescens och FRET studerar 10.
Flera internametoder Combining fördelarna med ekologisk märkning och in vivo upptäckt har införts under det senaste decenniet; Men sådana metoder antingen använda relativt stora polypeptider taggar (t.ex. TMP, Halo, eller 20 kDa SNAP taggar) 11-14, kräver användning av onaturliga aminosyror 15, eller är begränsade till stora, singel-membran eukaryota celler (t.ex.. , skrapa lastning, spruta lastning, mikroinjektion) 16-19.
Detta protokoll beskriver en roman, enkel och hög genomströmning metod som kopplar fördelarna med ekologiska fluoroforer med in vivo observation interna. Att utveckla denna teknik, vi anpassat elektroporering förfarande som vanligen används för att transformera celler med plasmid DNA 20,21 för att ladda mikroorganismer, såsom E. coli eller S. cerevisiae med ekologiskt märkta biomolekyler. Protokollet består av fyra enkla steg: inkubation av celler med märkta biomolekyler,elektroporering, cellåtervinning, och cell tvättning för att avlägsna icke-interna biomolekyler. Här presenterar vi denna elektroporation protokoll, liksom cell imaging och dataanalysprocesser för att studera cellbaserad och enda molekyl fluorescens och FRET signaler.
Elektroporation bygger på avlossa en högspännings elektriskt fält över en låg jonstyrka cellsuspension att bilda transienta membran porer genom vilka biomolekyler kan komma in celler (Figur 1) 20,21. Precis som med transformation av bakterier eller jäst med plasmid DNA, celler måste vara beredd före elektroporering att säkerställa deras electrocompetency. Detta förfarande, som består av flera tvättningssteg med vatten, ökar membranpermeabiliteten och sänker jonstyrkan av cell lösning för att undvika Ijusbågsbildning i elektroporationskyvett. I detta protokoll kan celler framställas som beskrivs nedan (Se PROTOKOLL: 1,1) eller köpas från kommersiella leverantörs.
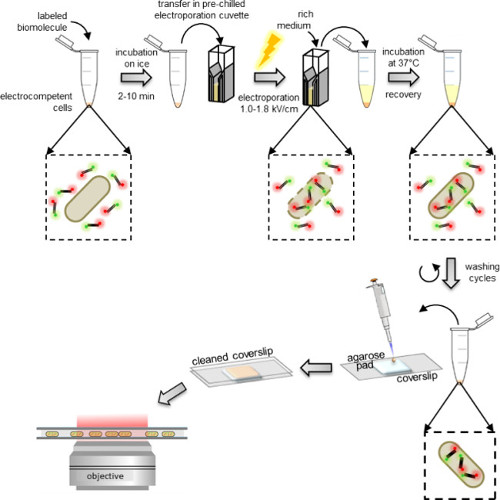
Figur 1: Schematisk bild av internaprotokollet Från vänster till höger:. Lägga till några mikroliter märkta biomolekyler till portion av elektroceller (dubbelt märkt DNA-fragment och bakterier i detta exempel); inkubera 1-10 min på is och överför till en pre-kyld elektroporeringskyvett; electroporate och sedan lägga 0,5-1 ml rikt medium till cellerna direkt efter; inkubera vid 37 ° C (eller den temperatur som krävs av organismen, t.ex., 29 ° C för jäst) för att låta cellerna återhämta sig; utföra fem tvättsteg för att avlägsna eventuella överskott icke-interna märkta molekyler; suspendera den slutliga pelleten i 100-200 pl PBS-buffert och pipett 10 ìl på en agaros pad; täcka kudden med en rengjord täck och bild på ett fluorescensmikroskop (i brett fält läge eller HILO-läge).
Medan DNA interna är enkel (Figur 2), försiktighetsåtgärder måste vidtas vid interna märkta proteiner med hjälp elektroporering. Först kanske beståndet urval av ekologiskt märkta proteinet fortfarande innehålla en liten andel av fritt färgämne. Fria färgmolekyler är mycket mindre än proteiner och kan därför intern företrädesvis. För att säkerställa att de allra flesta av de observerade interna fluorescerande molekyler motsvarar proteinet av intresse, bör den initiala proteinprovet innehåller mindre än ~ 2% fri färgämne (Figur 5) 22. Överskottet av icke-internaliserade märkta proteinerna kan även fastna på det yttre cellmembranet efter elektroporering; detta fenomen är protein specifikt och måste kontrolleras för varje nytt protein. Vi föreslår flera alternativ som tillåter avlägsnandet av icke-interna proteiner från den laddade cellprov (Se PROTOKOLL: 3.3.3).
Slutligen celler återsuspenderas i en liten volym av fosfatbuffert och pipetterades på en agaros pad, möjliggör deras avbildning på ett fluorescensmikroskop. Immobilisering på agaros kuddar är en enkee och effektivt sätt att avbilda celler på ett täck utan att skada deras integritet. Dynan bör innehålla en låg fluorescens odlingsmedium.
Cell imaging kan utföras antingen i Vidvinkel, total inre reflektion fluorescens (TIRF) eller använda HILO (Mycket benäget och Laminerade Optisk Sheet) mikroskopi. I HILO konfigurationen, tränger laserstrålen djupare i provet än i TIRF, ännu inte belysa hela provet som för widefield, som tillåter en större signal-till-brusförhållandet 23. Beroende på lasereffekten och tidsupplösning som används, kan interna biomolekyler räknas (med hjälp av stegvis-fotoblekning analys, figur 3), lokaliserad eller spåras 24-28. Internalisering av dubbelt märkta konstruktioner med en FRET-par av fluoroforer medger kvantifiering av FRET både encelliga eller enda molekyl nivåer (Figur 6).
Olika parametrar kan varierasberoende på den önskade utgången och det biologiska systemet studeras. Först, kan mängden internaliserad material per cell avstämmas genom att ändra koncentrationen av märkta biomolekyler sattes till cellerna före elektroporering (Figur 2). Elektroporation fältstyrkan kommer också att påverka både laddningseffektivitet och cellviabilitet; som väntat, medan lasteffektivitets ökar med ökande fältstyrka, livskraft elektroporerade celler minskar (Figur 4A). Båda parametrar kan kvantifieras genom registrering andelen belastade och delande celler efter elektroporering. Denna livskraft analys i kombination med fluorescens avbildning bekräftas även den observation av interna biomolekyler i levande celler och tillåta ständig kontroll över flera generationer (Figur 4B).
Sammanfattningsvis ger detta protokoll internalisering av fluorescerande DNA och proteinmolekyler iE. coli eller S. cerevisiae 26. Individuella molekyler märkta med organiska fluoroforer kan spåras med hög Spatiotemporal upplösning för tidsskalor en storleksordning längre än FPS. Slutligen är denna metod är förenlig med widefield, TIRF och konfokal upptäckt, liksom pulsade exciteringssystem, såsom ALEX (alternerande laserexcitation 28,29).
Protocol
Representative Results
Discussion
Många parametrar kan varieras under cell elektroporering och datainsamling, beroende på det biologiska systemet av intresse och den exakta arten av experimentet (cellnivå eller enda molekyl analys). Till exempel, när electroporating DNA i bakterier, 0,25-5 pmol märkta dsDNA-fragment leder till en låg interna effektivitet, för att direkt enda molekyl detektering (dvs., Utan behov av fotoblekning i förväg). Över 5 pmol dsDNA, celler tenderar att vara tungt lastad, en regim bättre lämpad för encelliga analys. Alla märkta DNA: n bör också vara tidigare gelrenades för att avlägsna varje spår av fritt färgämne (icke-reagerade fluorofor) från DNA-stamlösningen. Dessutom potentiella problem med DNA nedbrytning, särskilt för smFRET experiment, kan åtgärdas med hjälp av DNA-molekyler med onaturliga nukleinsyror eller motiv som skyddar exonukleas-tillgängliga terminaler såsom hårnålsslingor.
En annan adjustable parameter i elektroporering är fältstyrkan appliceras under elektroporering. Låg fältstyrka (~ 1 kV / cm) kommer att leda till en låg laddningseffektivitet lämplig för enda molekyl studier. Högre fältstyrkor (upp till 1,8 kV / cm) ökar lasteffektiviteten; Men det finns ett omvänt samband mellan fältstyrka och cellviabiliteten efter elektroporering (se figur 4). För referens, en normal fältstyrka används för bakterier och jäst elektroporation är ~ 1,5 kV / cm. Tidskonstanten, som representerar längden på detta förfall, är en bekväm parameter att följa, eftersom de ständiga droppar tids så fort något överslag fenomen inträffar i kyvetten. Under normala inställningar, bör tidskonstanten vara större än 4 ms; lägre värden kommer att leda till låg lasteffektivitet eller ens icke-lastade skadade celler. De flesta electroporators erbjuda andra frihetsgrader (t.ex. "pulstrunke" eller "puls form"), som kan modifieras för att ställa bådecellbelastning och viabilitet. Vi tillämpade denna metod för att både bakterier och jäst, men liknande förfaranden bör också göra det möjligt att internalisering av märkta biomolekyler i däggdjursceller med hjälp av lämpliga inställningar elektroporator eftersom deras membran är faktiskt mindre komplex (singel lipidbiskiktet) och eftersom elektroporering har redan använts med sådana celler 21.
När interna märkta proteinerna, behöver all fritt färgämne som skall avlägsnas från det märkta proteinet stamlösningen före elektroporering. Fria färgämnesmolekyler, på grund av sin mindre storlek, kan intern företrädesvis över proteiner av intresse, och är svåra att skilja under dataanalys (trots deras förväntade snabbare diffusion). Som en guide, för ett urval av ekologiskt märkta proteinet vara lämpliga för elektroporering, bör mängden återstående fria färgämne vara under 2% (detekteras med hjälp av fluorescerande scanning av ett SDS-PAGE) 22. Denna process är särskilt viktig,som vissa molekyler kan hålla sig till de yttre membranen hos electroporated bakterier eller jäst. I detta sammanhang bör det negativa kontrollprovet visar fluorescensintensiteten per cell klart lägre än elektroporerade celler, helst så låg som den autofluorescens nivån tomma celler (celler som inte har varit inkuberade med eventuella fluorescerande biomolekyler heller elektroporerade, Figur 2).
Som med dsDNA, är internaeffektiviteten av märkta proteiner kopplade till mängden biomolekyler till cellerna före elektroporering. Men andra parametrar, såsom storlek och laddning, spela en roll i interna. Små proteiner uppvisar höga interna effektivitet, medan större proteiner (upp till 98 kDa) kan framgångsrikt intern men med lägre effektivitet (Figur 5) 26. Den isoelektriska punkten av proteinet, potentiella interaktioner med cellmembranet och andra fysikalisk-kemiska parametrar ocksåinflytande cellbelastning under elektroporering. Som ett resultat, användarna behöver för att optimera experiment för sitt eget system, att veta att en hög initial koncentration av märkt protein (> 50 ^ M) kommer att ge den bästa chansen för framgångsrik lastning. Elektroporation erbjuder också ett nytt verktyg för att störa och analysera cellulär funktion genom att införa proteiner och andra biomolekyler i celler (antingen märkta eller omärkta). T7 RNA-polymeras experiment (figur 5C) närvarande ett sådant exempel på ett experiment där vi kan införa en biomolekyl som kan förändra genuttryck in vivo med användning av elektroporering.
När du utför enda molekyl fluorescens experiment, är TIR belysning brukar gynnas framför andra belysningslägen som det erbjuder det bästa signal-brus-förhållandet med endast spännande fluoroforer inom en tunn sektion ovanför täckytan (~ 100 nm). Men imaging märkta biomolekyler diffunderar inuti levande mikroorganismer kan relägget djupare belysning (upp till 0,8 | im för E. coli). Djupare belysning uppnås i Hilo läge, samtidigt som en hög signal-brus-förhållande. Å andra sidan, är brett fält avbildning särskilt viktigt för stegvis fotoblekning analys, där användaren uppskatta antalet interna molekyler genom fotoblekning en hel laddad cell med hög lasereffekt och dividera den initiala cellfluorescensintensitet med det enhetsintensitet produceras av en enda molekyl (enda fotoblekning steg, fig 3). Widefield bildbehandling krävs också för långsiktig molekylen spårning för att lokalisera de diffunderar molekylerna av intresse, även om deras banor täcker hela cellvolymen.
I detta protokoll presenterar vi hur elektroporering, en standardteknik för biologer och biokemister för att leverera nukleinsyror i celler, utgör en enkel metod för att leverera fluorescerande biomolekyler i olika celltyper. Thär ny, och erbjuder hög kapacitet teknik ett unikt verktyg för att observera märkta molekyler i sin ursprungliga miljö. I tillägg finns biomolekyler märkta med fluoroforer täcker ett brett spektrum av våglängder, elektroporering kan leverera molekyler modifierade med många kemiska grupper, såsom onaturliga nukleotider och aminosyror, metallkelatorer, tvärbindningsmedel, och placering i bur grupper. Om det biologiska systemet av intresse är inte avgörande för cellutveckling, kan den gen som kodar för målproteinet också tas bort (eller knackat ned), se till att proteinerna observerats efter interna representerar alla (eller de flesta) av den intracellulära proteinpoolen . I huvudsak kan elektroporering "transplantation" flexibiliteten i in vitro biokonjugaten in i levande celler och därmed gynna insatser inom syntetisk biologi, systembiologi och in vivo enda molekyl upptäckt.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
We thank Stephan Uphoff for discussions.
R.C. was supported by Linacre College, Oxford University. A.P. was supported by the German Academic Exchange Service (DAAD), the German National Academic Foundation and EPSRC. M.S. was supported by the Wellcome Trust. A.N.K. was supported by a UK BBSRC grant (BB/H01795X/1), and a European Research Council Starter grant (261227).
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| ElectroMax DH5-alpha Comptent cells | Invitrogen | 11319-019 | or any other commercial or lab-mage electrocompetant bacteria or yeast. |
| EZ Rich Defined Madia | Teknova | M2105 | low fluorescence rich media |
| MicroPulser Electroporation Apparatus | Biorad | 165-2100 | or any classical electroporator for microorganism transformation |
| Certified Molecular Biology agarose | Biorad | 161-3100 | low fluorescence agarose for agarose pad |
| Microscope coverslips No 1.5 thickness | Menzel | BB024060SC | remove background particles by heating slides in furnace at 500 °C for 1h |
| Single-molecule fluorescence microscope | Home-built | described in REFs | |
| Localization software | Custom-written, available online | MATLAB and C++ software package that can be adapted for localization analysis. | |
| Tracking software | Available online | MATLAB implementation by Blair and Dufresne. |
Riferimenti
- Tsien, R. Y. The green fluorescent protein. Annu Rev Biochem. 67, 509-544 (1998).
- Leake, M. C., et al. Stoichiometry and turnover in single, functioning membrane protein complexes. Nature. 443, 355-358 (2006).
- Taniguchi, Y., Kawakami, M. Application of HaloTag protein to covalent immobilization of recombinant proteins for single molecule force spectroscopy. Langmuir. 26, 10433-10436 (2010).
- Xie, X. S., Choi, P. J., Li, G. W., Lee, N. K., Lia, G. Single-molecule approach to molecular biology in living bacterial cells. Annual review of biophysics. 37, 417-444 (2008).
- Lee, J. H., et al. Highly multiplexed subcellular RNA sequencing in situ. Science. 343, 1360-1363 (2014).
- Miesenbock, G., De Angelis, D. A., Rothman, J. E. Visualizing secretion and synaptic transmission with pH-sensitive green fluorescent proteins. Nature. 394, 192-195 (1998).
- Sauer, M. Localization microscopy coming of age: from concepts to biological impact. J Cell Sci. 126, 3505-3513 (2013).
- Dempsey, G. T., Vaughan, J. C., Hao Chen, K., Zhuang, X. Evaluation of fluorophores for optimal performance in localizationbased super-resolution imaging. Nat Meth. 8, 1027-1041 (2011).
- Shaner, N. C., Steinbach, P. A., Tsien, R. Y. A guide to choosing fluorescent proteins. Nat Meth. 2, 905-909 (2005).
- Landgraf, D., Okumus, B., Chien, P., Baker, T. A., Paulsson, J. Segregation of molecules at cell division reveals native protein localization. Nat. Methods. 9, 480-482 (2012).
- Jaitin, D. A., et al. Massively Parallel Single-Cell RNA-Seq for Marker-Free Decomposition of Tissues into Cell Types. Science. 343, 776-779 (2014).
- Aldridge, S., et al. AHT-ChIP-seq: a completely automated robotic protocol for high-throughput chromatin immunoprecipitation. Genome Biol. 14, R124 (2013).
- Keppler, A., et al. A general method for the covalent labeling of fusion proteins with small molecules in vivo. Nat Biotechnol. 21, 86-89 (2003).
- Wombacher, R., et al. Live-cell super-resolution imaging with trimethoprim conjugates. Nat. Methods. 7, 717-719 (2010).
- Zhang, Z., et al. A new strategy for the site-specific modification of proteins in vivo. Biochimica. 42, 6735-6746 (2003).
- McNeil, P. L., Murphy, R. F., Lanni, F., Taylor, D. L. A method for incorporating macromolecules into adherent cells. J Cell Biol. 98, 1556-1564 (1984).
- Clarke, M. S., McNeil, P. L. Syringe loading introduces macromolecules into living mammalian cell cytosol. J Cell Sci. 102, 533-541 (1992).
- Sakon, J. J., Weninger, K. R. Detecting the conformation of individual proteins in live cells. Nat. Methods. 7, 203-205 (2010).
- Taylor, L. S. Electromagnetic syringe. IEEE Trans. Biomed. Eng. 25, 303-304 (1978).
- Dower, W. J., Miller, J. F., Ragsdale, C. W. High efficiency transformation of E. coli by high voltage electroporation. Nucleic Acids Res. 16, 6127-6145 (1988).
- Neumann, E., Schaefer-Ridder, M., Wang, Y., Hofschneider, P. H. Gene transfer into mouse lyoma cells by electroporation in high electric fields. EMBO J. 1, 841-845 (1982).
- Sustarsic, M., et al. Optimized delivery of fluorescently labeled proteins in live bacteria using electroporation. Histochem Cell Biol. , (2014).
- Tokunaga, M., Imamoto, N., Sakata-Sogawa, K. Highly inclined thin illumination enables clear single-molecule imaging in cells. Nat. Methods. 5, 159-161 (2008).
- Sinha, A., et al. A cascade of DNA-binding proteins for sexual commitment and development in Plasmodium. Nature. 000, 1-5 (2014).
- English, B. P., et al. Single-molecule investigations of the stringent response machinery in living bacterial cells. Proc Natl Acad Sci U S A. 108, E365-E373 (2011).
- Crawford, R., et al. Long-lived intracellular single-molecule fluorescence using electroporated molecules. Biophys J. 105, 2439-2450 (2013).
- Uphoff, S., Reyes-Lamothe, R., Garza de Leon, F., Sherratt, D. J., Kapanidis, A. N. Single-molecule DNA repair in live bacteria. Proc Natl Acad Sci U S A. 110, 8063-8068 (2013).
- Uphoff, S., Sherratt, D. J., Kapanidis, A. N. Visualizing Protein-DNA Interactions in Live Bacterial Cells Using Photoactivated Single-molecule Tracking. J Vis Exp. , (2014).
- Hohlbein, J., Gryte, K., Heilemann, M., Kapanidis, A. N. Surfing on a new wave of single-molecule fluorescence methods. Phys Biol. 7, 031001 (2010).
- Xie, X. S., Yu, J., Yang, W. Y. Perspective – Living cells as test tubes. Science. 312, 228-230 (2006).
- Santoso, Y., et al. Conformational transitions in DNA polymerase I revealed by single-molecule FRET. Proc Natl Acad Sci U S A. 107, 715-720 (2010).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature communications. 4, 2131 (2013).

