A Human-maskin-grensesnitt Integrering rimelige sensorer med en nevromuskulær elektrisk stimulering System for Post-takts Balance Rehabilitering
Summary
A novel low-cost human-machine interface for interactive post-stroke balance rehabilitation system is presented in this article. The system integrates off-the-shelf low-cost sensors towards volitionally driven electrotherapy paradigm. The proof-of-concept software interface is demonstrated on healthy volunteers.
Abstract
Et hjerneslag oppstår når en arterie frakter blod fra hjertet til et område i hjernen brister eller en blodpropp hindrer blodstrømmen til hjernen og dermed hindre levering av oksygen og næringsstoffer. Omtrent halvparten av de slagrammede sitter igjen med en viss grad av uførhet. Innovative metoder for restorative neurorehabilitation er sterkt behov for å redusere langsiktig uførhet. Muligheten av nervesystemet å omorganisere sin struktur, funksjon og tilkoblinger som et svar på indre eller ytre stimuli kalles nevroplastisitet. Neuroplasticity er involvert i post-takts funksjonsforstyrrelser, men også i rehabilitering. Fordelaktig neuroplastic endringer kan gjøres lettere med ikke-invasiv elektroterapi, slik som nevromuskulær elektrisk stimulering (NMES) og sensoriske elektrisk stimulering (SES). Nmes innebærer koordinert elektrisk stimulering av motoriske nerver og muskler for å aktivere dem med kontinuerlige korte pulser av elektrisk strøm mens SES involves stimulering av sensoriske nerver med elektrisk strøm som resulterer i opplevelser som varierer fra knapt lesbar til svært ubehagelig. Her kan aktiv kortikal deltakelse i rehabiliterings prosedyrer forenkles ved å kjøre non-invasiv elektro med biosignals (electromyogram (EMG), elektroencefalogram (EEG), electrooculogram (EOG)) som representerer samtidig aktiv persepsjon og vilje innsats. For å oppnå dette på en ressursfattige omgivelser, for eksempel i lav- og mellominntektsland, presenterer vi en rimelig menneske-maskin-grensesnitt (HMI) ved å utnytte de siste fremskritt i off-the-sokkel videospill sensorteknologi. I denne artikkelen diskuterer vi open-source programvare grensesnitt som integrerer lavkost off-the-sokkel sensorer for visuell-auditive biofeedback med ikke-invasiv elektro å bistå postural kontroll under balanse rehabilitering. Vi demonstrere proof-of-concept på friske frivillige.
Introduction
En episode av nevrologisk dysfunksjon forårsaket av fokus cerebral, spinal eller retinal infarkt kalles hjerneslag 1. Hjerneslag er et globalt helseproblem og fjerde største årsaken til uførhet på verdensbasis en. I land som India og Kina, de to mest folkerike land i verden, er nevrologisk funksjonshemming på grunn av slag å bli stemplet som skjult epidemi to. En av de vanligste medisinske komplikasjoner etter et slag er fall med en rapportert forekomst på opp til 73% i det første året etter slag tre. Post-takts fall den er multifaktoriell og omfatter både rygg og supraspinal faktorer som balanse og visuospatial forsømmelse 4. En gjennomgang av Geurts og kolleger 5 identifiserte 1) multi-retnings nedsatt maksimal vekt forskyvning på tobent stående, 2) lav hastighet, 3) retnings upresishet, og 4) små amplituder av single og sykliske sub-maksimal frontal plan vektskiftninger som balansen faktorer for fall risk. Den påfølgende innvirkning på dagliglivets aktiviteter kan være betydelig siden tidligere arbeider har vist at balansen er knyttet til ambulerende evne og selvstendighet i brutto motorisk funksjon 5, 6. Videre Geurts og kolleger 5 antydet at supraspinal multisensorisk integrering (og muskel koordinering 7) i tillegg til muskelstyrke er avgjørende for balansen utvinning som mangler i dagens protokoller. Mot multisensorisk integrasjon, vår hypotese 8 på volitionally drevet non-invasiv elektro (nmes / SES) er at dette adaptiv atferd kan formes og tilrettelagt av moduler aktiv oppfatning av sanseinntrykk i løpet nmes / SES-assistert bevegelse av benet slik at hjernen kan innlemme denne tilbakemeldingen til påfølgende bevegelsen utgang ved å rekruttere alternative motorveier 9, om nødvendig.
For å oppnå volitionally drevet nmes / SES-assistert balansetrening i en ressurs-Dårlig innstilling, ble en rimelig menneske-maskin-grensesnitt (HMI) som er utviklet ved å utnytte tilgjengelige åpen kildekode programvare og nylige fremskritt i off-the-sokkel videospill sensorteknologi for visuell-auditiv biofeedback. Nmes innebærer koordinert elektrisk stimulering av nerver og muskler som har vist seg å forbedre muskelstyrke og redusere spastisitet 10. Dessuten innebærer SES stimulering av sensoriske nerver med elektrisk strøm for å fremkalle følelser der foreløpige publiserte arbeider 11 viste at subsensory stimulering brukes over tibialis anterior musklene alene er effektivt i å dempe postural svai. Her vil HMI muliggjøre sensoriske-motor integrering under interaktiv post-takts balanse terapi hvor volitionally drevet nmes / SES for ankelen muskler vil fungere som en muskel forsterker (med nmes) samt forbedre afferent tilbakemeldinger (med SES) til bistå sunne ankel strategier 12,13,14 å opprettholde oppreist holdning under postural svaier. Dette erbasert på hypotesen presenteres i Dutta et al. 8 at økt corticospinal eksitabilitet av relevante ankel muskler skjer gjennom non-invasiv elektro kan låne til en forbedret supraspinal modulering av ankelen stivhet. Faktisk har tidligere arbeid vist at nmes / SES frembringer varige endringer i corticospinal eksitabilitet, muligens som et resultat av co-aktiverende motor og sensoriske fibre 15,16. Videre Khaslavskaia og Sinkjaer 17 viste i mennesker at samtidig motor kortikal kjøretur til stede på tidspunktet for nmes / SES forbedret motor kortikal eksitabilitet. Derfor kan volitionally drevet nmes / SES indusere kortsiktige neuroplasticity i spinal reflekser (f.eks gjensidig Ia hemming 17) hvor corticospinal nevroner som prosjektet via synkende veier til en gitt motoneuron basseng kan hemme antagonistiske motoneuron bassenget via Ia-hemmende interneurons i mennesker 18, som vist i figur 1, i retning av en operant kondisjone paradigmet (se Dutta et al. 8).
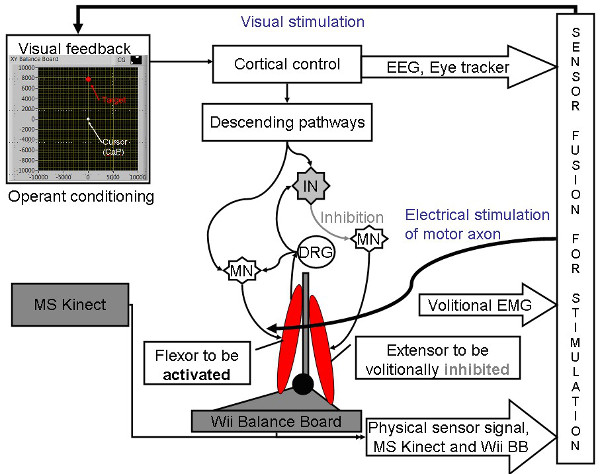
Figur 1: Konseptet (. Detaljer på Dutta et al 21) underliggende interaktivt menneske-maskin-grensesnitt (HMI) for å drive trykksenteret (CoP) markøren til spolt mål å forbedre ankelen muskel koordinering henhold volitionally drevet nevromuskulær elektrisk stimulering (NMES) -assisted visuomotor balanse terapi EEG. elektroencefalografi, MN: α-motoneuron, IN: Ia-hemmende interneuron, EMG: electromyogram, DRG: dorsal root ganglion. Gjengitt fra 8 og 37. Klikk her for å se en større versjon av dette tallet.
Den Antero-posterior (AP) forskyvninger i sentrum av masse (COM) utføresved ankel plantarflexors (slik som mediale gastrocnemius og soleus muskler) og dorsiflexors (for eksempel den fremre tibiale muskel), mens Karakter-laterale (ML) forskyvninger er utført av ankel invertors (for eksempel den fremre tibiale muskel) og evertors (for eksempel peroneus longus og brevis muskler). Derfor slagrelaterte ankel svekkelser inkludert svakhet av ankelen dorsiflexor muskler og økt spastisitet i ankelen plantarflexor muskler føre til nedsatt postural kontroll. Her kan agility treningsprogrammer 6 utnyttes i en virtuell virkelighet (VR) basert spillplattform som utfordrer dynamisk balanse hvor oppgaver er gradvis økt i vanskeligheter som kan være mer effektivt enn statisk stretching / vekt-skiftende treningsprogram for å forebygge fall 6. For eksempel kan fagene utføre volitionally drevet nmes / SES assistert AP og ML forskyvninger under en dynamisk visuomotor balanse oppgave hvor vanskelighetsgraden kan økes gradvis til Ameliorate post-takts ankel-spesifikke kontrollproblemer i vekt skiftende løpet tobent stående. Mot volitionally drevet nmes / SES assistert balanse terapi i en ressursfattige omgivelser, presenterer vi en rimelig HMI for Mobile Brain / Body Imaging (MOBI) 19, mot visuelle auditive biofeedback som også kan benyttes til datainnsamling fra lav- lige sensorer for offline data leting i MoBILAB (se Ojeda et al. 20).
Protocol
Representative Results
Discussion
En enkel å bruke, klinisk gyldig rimelig verktøy for bevegelse og balanse terapi vil være et paradigmeskifte for neurorehabilitation i en lav-ressurs innstilling. Det er sannsynlig å ha en svært høy samfunnsmessig betydning siden nevrologiske lidelser som slag vil dramatisk øke i fremtiden på grunn av aldring verdens befolkning to. Det er derfor et stort behov for å utnytte cyber fysiske systemer hvor evnen til å tilpasse, overvåke og støtte nevro-rehabilitering på eksterne nettsteder har nylig b…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Forskning utført innenfor rammen av Joint målrettede programmet i informasjons- og kommunikasjonsvitenskap og teknologi – ICST, støttet av CNRS, INRIA, og DST under CEFIPRA paraply. Forfatterne ønsker å takke støtte av studenter, spesielt Rahima Sidiboulenouar, Rishabh Sehgal, og Gorish Aggarwal, mot utviklingen av den eksperimentelle oppsettet.
Materials
| NMES stimulator | Vivaltis, France | PhenixUSBNeo | NMES stimulator cum EMG sensor (Figure 2b) |
| Balance Board | Nintendo, USA | Wii Balance Board | Balance Board (Figure 2b) |
| Motion Capture | Microsoft, USA | XBOX-360 Kinect | Motion Capture (Figure 2b) |
| Eye Tracker | Eye Tribe | The Eye Tribe | SmartEye Tracker (Figure 2a) |
| EEG Data Acquisition System | Emotiv, Australia | Emotiv Neuroheadset | Wireless EEG headset (Figure 2b) |
| EEG passive electrode | Olimex | EEG-PE | EEG passive electrode for EOG and references (6 in number)(Figure 2b) |
| EEG active electrode | Olimex | EEG-AE | EEG active electrode (10 in number)(Figure 2b) |
| Computer with PC monitor | Dell | Data processing and visual feedback (Figure 2) | |
| Softwares, EMG electrodes, NMES electrodes, and cables |
Riferimenti
- Sacco, R. L., Kasner, S. E. An updated definition of stroke for the 21st century: a statement for healthcare professionals from the American Heart Association/American Stroke Association. Stroke; a journal of cerebral circulation. 44 (7), 2064-2089 (2013).
- Das, A., Botticello, A. L., Wylie, G. R., Radhakrishnan, K. Neurologic Disability: A Hidden Epidemic for India. Neurology. 79 (21), 2146-2147 (2012).
- Verheyden, G. S. A. F., Weerdesteyn, V. Interventions for preventing falls in people after stroke. The Cochrane database of systematic reviews. 5, 008728 (2013).
- Campbell, G. B., Matthews, J. T. An integrative review of factors associated with falls during post-stroke rehabilitation. Journal of Nursing Scholarship: An Official Publication of Sigma Theta Tau International Honor Society of Nursing / Sigma Theta Tau. 42, 395-404 (2010).
- Geurts, A. C. H., de Haart, M., van Nes, I. J. W., Duysens, J. A review of standing balance recovery from stroke. Gait & posture. 22, 267-281 (2005).
- Marigold, D. S., Eng, J. J., Dawson, A. S., Inglis, J. T., Harris, J. E., Gylfadóttir, S. Exercise leads to faster postural reflexes, improved balance and mobility, and fewer falls in older persons with chronic stroke. Journal of the American Geriatrics Society. 53, 416-423 (2005).
- Mansfield, A., Mochizuki, G., Inness, E. L., McIlroy, W. E. Clinical correlates of between-limb synchronization of standing balance control and falls during inpatient stroke rehabilitation. Neurorehabilitation and neural repair. 26, 627-635 (2012).
- Dutta, A., Lahiri, U., Das, A., Nitsche, M. A., Guiraud, D. Post-stroke balance rehabilitation under multi-level electrotherapy: a conceptual review. Neuroprosthetics. 8, 403 (2014).
- Agnes Roby-Brami, S. F. Reaching and Grasping Strategies in Hemiparetic Patients. Human Kinetics Journals. , (2010).
- Sabut, S. K., Sikdar, C., Kumar, R., Mahadevappa, M. Functional electrical stimulation of dorsiflexor muscle: effects on dorsiflexor strength, plantarflexor spasticity, and motor recovery in stroke patients. NeuroRehabilitation. 29, 393-400 (2011).
- Magalhães, F. H., Kohn, A. F. Effectiveness of electrical noise in reducing postural sway: a comparison between imperceptible stimulation applied to the anterior and to the posterior leg muscles. European Journal of Applied Physiology. 114, 1129-1141 (2014).
- Hwang, S., Tae, K., Sohn, R., Kim, J., Son, J., Kim, Y. The balance recovery mechanisms against unexpected forward perturbation. Annals of biomedical engineering. 37, 1629-1637 (2009).
- Gatev, P., Thomas, S., Kepple, T., Hallett, M. Feedforward ankle strategy of balance during quiet stance in adults. The Journal of physiology. 514, 915-928 (1999).
- Cofre Lizama, E. L., Pijnappels, M., Reeves, N. P., Verschueren, S. M. P., van Dieën, J. H. Can explicit visual feedback of postural sway efface the effects of sensory manipulations on mediolateral balance performance. Journal of Neurophysiology. , (2015).
- Knash, M. E., Kido, A., Gorassini, M., Chan, K. M., Stein, R. B. Electrical stimulation of the human common peroneal nerve elicits lasting facilitation of cortical motor-evoked potentials. Experimental brain research. 153, 366-377 (2003).
- Dinse, H. R., Tegenthoff, M. Evoking plasticity through sensory stimulation: Implications for learning and rehabilitation. The Journal of neuroscience: the official journal of the Society for Neuroscience. 6, 11-20 (2015).
- Khaslavskaia, S., Sinkjaer, T. Motor cortex excitability following repetitive electrical stimulation of the common peroneal nerve depends on the voluntary drive. Experimental brain research. 162, 497-502 (2005).
- Perez, M. A., Field-Fote, E. C., Floeter, M. K. Patterned sensory stimulation induces plasticity in reciprocal ia inhibition in humans. The Journal of neuroscience: the official journal of the Society for Neuroscience. 23, 2014-2018 (2003).
- Makeig, S. Mind Monitoring via Mobile Brain-Body Imaging. Foundations of Augmented Cognition. Neuroergonomics and Operational. , 749-758 (2009).
- Ojeda, A., Bigdely-Shamlo, N., Makeig, S. MoBILAB: an open source toolbox for analysis and visualization of mobile brain/body imaging data. Frontiers in Human Neuroscience. 8, 121 (2014).
- Dutta, A., Chugh, S., Banerjee, A., Dutta, A. Point-of-care-testing of standing posture with Wii balance board and microsoft kinect during transcranial direct current stimulation: A feasibility study. NeuroRehabilitation. 34, 789-798 (2014).
- Nataraj, R. . Feedback Control Of Standing Balance Using Functional Neuromuscular Stimulation Following Spinal Cord Injury. , (2011).
- Dutta, A., Paulus, W., Nitsche, A., M, Translational Methods for Non-Invasive Electrical Stimulation to Facilitate Gait Rehabilitation Following Stroke – The Future Directions. Neuroscience and Biomedical Engineering. 1, 22-33 (2013).
- Banerjee, A., Khattar, B., Dutta, A. A Low-Cost Biofeedback System for Electromyogram-Triggered Functional Electrical Stimulation Therapy: An Indo-German Feasibility Study. ISRN Stroke. 2014, e827453 (2014).
- Kerkhoff, G., Reinhart, S., Ziegler, W., Artinger, F., Marquardt, C., Keller, I. Smooth pursuit eye movement training promotes recovery from auditory and visual neglect: a randomized controlled study. Neurorehabilitation and Neural Repair. 27, 789-798 (2013).
- Carl, J. R., Gellman, R. S. Human smooth pursuit: stimulus-dependent responses. Journal of Neurophysiology. 57, 1446-1463 (1987).
- Clark, R. A., Bryant, A. L., Pua, Y., McCrory, P., Bennell, K., Hunt, M. Validity and reliability of the Nintendo Wii Balance Board for assessment of standing balance. Gait & posture. 31, 307-310 (2010).
- Clark, R. A., Pua, Y. -. H. Validity of the Microsoft Kinect for assessment of postural control. Gait & posture. 36, 372-377 (2012).
- Khattar, B., Banerjee, A., Reddi, R., Dutta, A. Feasibility of Functional Electrical Stimulation-Assisted Neurorehabilitation following Stroke in India: A Case Series. Case Reports in Neurological Medicine. 2012, e830873 (2012).
- Sailer, U., Flanagan, J. R., Johansson, R. S. Eye-hand coordination during learning of a novel visuomotor task. The Journal of neuroscience: the official journal of the Society for Neuroscience. 25, 8833-8842 (2005).
- Herr, H., Popovic, M. Angular momentum in human walking. The Journal of Experimental Biology. 211, 467-481 (2008).
- Taub, E., Morris, D. M. Constraint-induced movement therapy to enhance recovery after stroke. Current atherosclerosis reports. 3, 279-286 (2001).
- Kasten, E., Wuest, S., Sabel, B. A. Residual vision in transition zones in patients with cerebral blindness. Journal of Clinical and Experimental Neuropsychology. 20, 581-598 (1998).
- Marshall, S. P. Identifying Cognitive State from Eye Metrics. Aviation, Space, and Environmental Medicine. 78, 165-175 (2007).
- Weerdesteyn, V., de Niet, M., van Duijnhoven, H. J. R., Geurts, A. C. H. Falls in individuals with stroke. Journal of Rehabilitation Research and Development. 45, 1195-1213 (2008).
- Stinear, C. M., Barber, P. A., Petoe, M., Anwar, S., Byblow, W. D. The PREP algorithm predicts potential for upper limb recovery after stroke. Brain: A Journal of Neurology. 135 ((Pt 8)), 2527-2535 (2012).
- Dutta, A., Lahiri, D., Kumar, U., Das, A., Padma, M. V. Post-stroke engagement-sensitive balance rehabilitation under an adaptive multi-level electrotherapy: clinical hypothesis and computational framework. Neuroscience and Biomedical Engineering. 2 (2), 68-80 (2015).

