Samtidig Vurdering af cardiomyocyte DNA Synthesis og Ploidi: En metode til at hjælpe Kvantificering af cardiomyocyte Regeneration og Omsætning
Summary
Quantification of cardiomyocyte turnover is challenging. The protocol described here makes an important contribution to this challenge by enabling accurate and sensitive quantification of neo-cardiomyocyte nuclei generation and nuclei ploidy.
Abstract
Selv om det er accepteret, at hjertet har en begrænset potentiale til at regenerere cardiomyocytter følgende skade, og at lave niveauer af cardiomyocyte omsætning forekomme under normal aldring, kvantificering af disse hændelser er fortsat udfordrende. Dette er til dels på grund af sjældenhed af processen og det forhold, at flere cellulære kilder bidrager til myocardial vedligeholdelse. Desuden DNA dobbeltarbejde inden cardiomyocytter ofte fører til en polyploid cardiomyocyte og kun sjældent fører til nye cardiomyocytter ved celledeling. For nøjagtigt kvantificere cardiomyocyte diskrimination omsætning mellem disse processer er afgørende. Protokollen beskrevet her beskæftiger langsigtet nukleosid mærkning for at mærke alle kerner, der er opstået som følge af DNA-replikation og cardiomyocyte kerner identificeret ved at udnytte kerner isolation og efterfølgende PCM1 immunolabeling. Tilsammen tillader nøjagtig og følsom identifikation af nucleosid mærkning af cardiomyocyte kerner befolkning. Endvidere 4 ', 6-diamidino-2-phenylindol mærkning og analyse af kerner ploidi, muliggør diskriminering af neo-cardiomyocyte kerner fra kerner, der har inkorporeret nukleosid under polyploidization. Selv om denne metode ikke kan kontrollere for cardiomyocyte binucleation, det giver mulighed for en hurtig og robust kvantificering af neo-cardiomyocyte kerner, mens der tegner sig for polyploidization. Denne metode har en række downstream-applikationer, herunder vurdere de potentielle lægemidler at øge cardiomyocyte regenerering eller undersøgelse af virkningerne af hjertesygdom på cardiomyocyte omsætning og ploidi. Denne teknik er også kompatibel med yderligere downstream immunohistologiske teknikker, der muliggør kvantificering af nukleosid iblanding i alle kardiale celletyper.
Introduction
I de senere år har der været en ophobning af beviser udfordrer den antagelse, at hjertet er en terminalt differentieret, post-mitotisk orgel 1,2. Men kvantificering af cardiomyocyte omsætning og regenerering er stadig udfordrende.
Vanskelighederne i præcist at identificere sjældne cardiomyocyte generation ved hjælp af standard immunhistokemiske teknikker er godt rapporteres 3. Hertil kommer, at cellulære kilde cardiomyocyte generation fortsat usikker med beviser for bidrag fra cardiomyocyte spredning samt ved stamcelle differentiering 4-6. Derfor er brugen af slægt opsporing modeller, som kræver kendskab til cardiomyocyte stamfader fænotype er umuligt og kvantificering af proliferation i en enkelt population, herunder cardiomyocytter, er uhensigtsmæssig. Desuden en cardiomyocyte har potentiale til endoreplication uden karyokinesis (hvilket resulterer i en polyploid bildiomyocyte) eller karyokinesis i fravær af cytokinesen (hvilket resulterer i en binucleated cardiomyocyte) 7,8. Den nøjagtige kvantificering af cardiomyocyte omsætning afhænger af evnen til at skelne mellem disse hændelser og ægte neo-cardiomyocyte generation. Dette skaber unikke komplikationer, fordi DNA-replikation og ekspression af cyclin-afhængige kinaser i cardiomyocytter ikke udelukkende vise sandt celledeling 9,10.
For at hjælpe med kvantificering af neo-cardiomyocyte generation, har vi kombineret en etableret kerner isolation teknik, og immunologisk mærkning af pericentriolar materiale 1 (PCM1) for cardiomyocyte kerner identifikation som beskrevet af Bergmann et al. 7,11 med nye metoder til langsigtet DNA-mærkning og ploidi-analyse. PCM-1 er en centrosom protein, der akkumulerer ved nukleare overflade af differentierede, ikke-cykling myocytter. Tidligere undersøgelser har vist, at antistoffer modPCM-1 specifikt mærke cardiomyocyte kerner 7,11 og som sådan PCM1 er blevet brugt af en række uafhængige grupper at identificere cardiomyocytter 1,12,13. Derudover har vi vist, at PCM1 ekspression kort til genetisk mærkede cardiomyocyte kerner i TnT-Cre transgene musemodel 14 (Supplerende figur 1).
Protokollen beskrevet her muliggør nøjagtig og følsom identifikation af neo cardiomyocyte kerner generation i mus hjertet, uanset de cellulære oprindelse (figur 1A og B), mens der samtidig er mulighed nukleosid mærkning grund polyploidization fra analysen (figur 1C og D). Selv om denne metode ikke kan kontrollere for cardiomyocyte binucleation, det giver mulighed for en hurtig og robust kvantificering af neo-cardiomyocyte kerner, der er nødvendige for den nøjagtig kvantificering af cardiomyocyte omsætning. Endvideredet giver en hurtig screening redskab til at vurdere mulige ændringer i dynamikken i cardiomyocyte generation.
Mens DNA-mærkning omfatter normalt 5-brom-2'-deoxyuridin (BrdU) som thymidin-analog, der er beskrevet her protokollen bruger en 5-ethynyl-2'-deoxyuridin (edu) baseret assay som den kræver færre bearbejdningstrin for en hurtigere gennemløb og kræver ikke denaturering af DNA'et for immuno-detektion, hvilket gør den forenelig med andre immunfarvning protokoller og derved øge de potentielle efterfølgende anvendelser af fremgangsmåden.
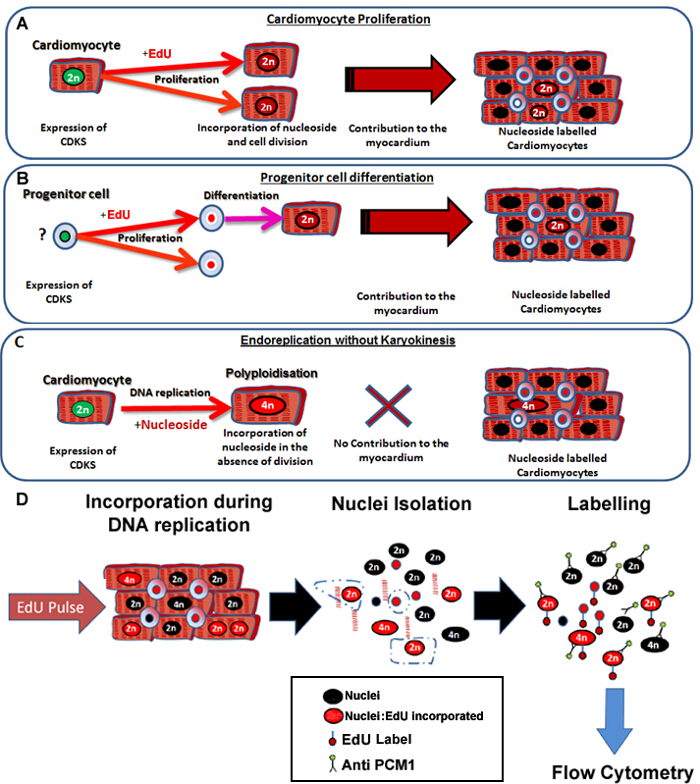
Figur 1: Kontinuerlig pulsering med Edu etiketter neo-cardiomyocytter uanset deres forfædre. (A) edu inkorporeres i DNA'et i cardiomyocytter under celledelingen. Proliferation i cardiomyocyte befolkningen vil Result i en stigning i, eller udskiftning af cardiomyocytter og derfor produktive DNA-syntese (bidrager til væv vedligeholdelse og reparation). (B) edu inkorporeres i DNA'et i kardiale progenitorceller under celledeling. Dette vil blive tilbageholdt i cellen under differentiering til cardiomyocyte afstamning. Denne stamcelledifferentiering vil også resultere i en stigning i antallet af cardiomyocytter og bidrager derfor til væv vedligeholdelse og reparation. (C) cardiomyocytter har potentiale til at undergå "uproduktive" DNA-replikation resulterer i øget cardiomyocyte ploidi, som er forbundet med cardiomyocythypertrofi og myocardial remodeling, men erstatter ikke mistede cardiomyocytter. Processen med polyploidization afviger fra binucleation da det resulterer i en cardiomyocyte med en enkelt kerne, der indeholder fire eller flere sæt af to homologe kromosomer (> 2 N). (D) Efter en kontinuerlig kerner pUlse, denne protokol beskriver kerner isolering og identifikation af de cardiomyocyte kerner ved PCM1 udtryk for at tillade kvantificering af både cardiomyocyte ploidi og Edu inkorporering. PCM1 udtryk og Edu inkorporering detekteres ved anvendelse af flowcytometri. Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
For præcist at kvantificere cardiomyocyte omsætning og regenerering analyser må skelne mellem sandt cardiomyocyte generation og uproduktive DNA division. Mange undersøgelser fortsat blot ignorere disse uproduktive begivenheder, kvantificere cardiomyocyte spredning udelukkende via ekspression af cyclin kinesis og cellecyklus markører. Til dato en enkelt metode, der tillader præcis kvantificering af cardiomyocyte omsætning samtidig med at kontrollere for disse uproduktive begivenheder forbliver hentydninger. Navnlig er det fortsat vanskeligt at forklare cardiomyocyte polyploidization som bidrager med op til ~ 65% af cardiomyocyte DNA-replikation 13. Derfor at bistå med nøjagtig kvantificering af cardiomyocyte generation har vi udviklet en protokol, der tillader den robuste kvantificering af satserne for neo cardiomyocyte kerner samtidig udelukke DNA-replikation, der resulterer i øget ploidi. Selv om denne protokol ikke kan forskelsbehandling mellem neo-cardiomyocyte slægtertion og cardiomyocyte bi-kimdannelse, kan den bruges hurtigt og præcist at beregne den øvre grænse (der tegner sig for ploidi) af cardiomyocyte generation. Denne protokol giver derfor et screeningsværktøj til at vurdere mulige ændringer i satserne for cardiomyocyte generation og polyploidization i sygdomsmodeller eller at vurdere den potentielle effektivitet lægemidler. Når ændringer i hastigheden af neo-cardiomyocyte kerner generation, identificeres ved hjælp af denne protokol efterfølgende studier kan anvendes til at konstatere, om denne på grund af ændringer i cardiomyocyte generation af cardiomyocyte nukleering nummer, som beskrevet tidligere 2,13,17,18. Disse omfatter anvendelsen af histologiske kvantificering cardiomyocyte kernedannende dynamik under pulsen periode eller analyser af vævssnit opnået fra Edu pulserende dyr i at sammenligne Edu inkorporering i mononukleære og flerkernede cardiomyocyte befolkninger.
På grund af de lave niveauer af cardiomyocyte omsætning denneprotokollen bruger multiple injektioner af edu over en periode på 7 dage. Dette giver også mulighed for "jagter" af alle potentielle cellulære kilder til cardiomyocyte generation og tillader kvantificering af kumulativ cardiomyocyte kerner generation løbet af denne periode. Afhængigt af undersøgelsen, kan denne tidsramme justeres efter de forudsagte niveauer for cardiomyocyte generation. Til nøjagtig kvantificering af edu inkorporering i cardiomyocyte kerner, er det bydende nødvendigt, at der ikke er nogen ikke-specifik mærkning af kernerne med det sekundære antistof anvendes til påvisning PCM-1 reaktivitet. Det ville derfor være fornuftigt at foretage yderligere sekundære antistoftitrering eksperimenter for at optimere dette aspekt af protokollen, især hvis en anden medlemsstat end den sekundære antistof foreslået i denne protokol skal bruges. Protokollen beskrevet her anvender PCM-1 ekspression til at identificere cardiomyocyte kerner. Mens dette er en etableret cardiomyocyte markering, kan alternative markører anvendes til at valideredata; disse omfatter antistoffer specifikke for cardiac troponin T, som er blevet identificeret som delvis lokaliseret i cardiomyocyte kerner 1. Ligeledes kan alternative nukleare lokaliserede proteiner bruges til at identificere og kvantificere Edu indarbejdet i andre end de cardiomyocytter kerner befolkninger. Det er vigtigt, at alle cardiomyocyte kerner, der aktivt undergår mitose er udelukket fra analysen, som skæbnen for denne DNA-syntese er ukendt og kan resultere i enten celledeling eller øget ploidi. PCM1 adskilles under M-fasen af cellens cyklus derfor cardiomyocytter undergår mitose vil ikke identificeres ved PCM1 ekspression. Desuden bør alle kerner i S-fasen af cellecyklussen udelukkes fra efterfølgende analyse. Dette kan opnås ved gating alle kerner med en DAPI intensitet over 2N befolkningen, herunder dem med en DAPI intensitet mellem 2N og 4N populationer.
Selv om det er i stigende gradaccepteret, at hjertet har kapacitet til at erstatte cardiomyocytter under normal ældning og efter akut skade, kilden og graden af dette potentiale forbliver kontroversiel. Desuden har forskellige satser for cardiomyocyte omsætning er rapporteret 1,7,20-22. Dette kan til dels skyldes vanskelighederne med præcist at identificere og kvantificere neo-cardiomyocyte generation 19. Til dato de fleste undersøgelser har påberåbt kun på brugen af histologisk analyse og identificering af cardiomyocytter via ekspressionen af cytoplasmatiske proteiner, herunder proteiner af sarkomeret, til kvantificering af cardiomyocyte omsætning og fornyelse 2,4,23,24. Anvendelsen af disse metoder til påvisning af ekspression af proliferationsmarkører, eller som demonstreret her, kan inkorporeringen af thymidinanaloger let resultere i fejlagtig identifikation af andre kardiale celletyper som cardiomyocytter. Mens anvendelsen af 3D konfokal billeddannelse kan bidrage til at afhjælpe disse problemer thESE metoder er dyre og tidskrævende. Interessant, den her beskrevne protokol demonstrerer neo-cardiomyocyte kerner generation sker med en hastighed på 0,17% pr uge. Dette er i overensstemmelse med andre flowcytometri baserede undersøgelser, der påviser ugentlige omsætning på op til 0,13% 5. Selv om det er fristende at ekstrapolere årlige omsætning satser baseret på disse data, som i tidligere undersøgelser 2,5,25,26, dette er uhensigtsmæssigt, da satserne for omsætningen er dynamiske løbet levetid af et dyr 13.
Denne metode har en række potentielle anvendelser, herunder at vurdere de potentielle lægemidler at øge cardiomyocyte regenerering eller undersøgelse af virkningerne af hjertesygdom på cardiomyocyte omsætning og satserne for cardiomyocyte polyploidization.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
This work was supported by the British Heart Foundation, project grant PG/13/69/30454.
Materials
| 0.32 M sucrose | Sigma | 84100 | |
| 10 mM Tris-HCl (pH = 8) | Sigma | T3253 | |
| 5 mM CaCl2 | Sigma | c5086 | |
| 5 mM magnesium acetate | sigma | M-5661 | |
| 2.0 mM EDTA | Sigma | E5134 | |
| 0.5 mM EGTA | Sigma | 63779 | |
| 1 mM DTT | Sigma | D0632 | |
| 70 mM KCl | Sigma | P9541 | |
| 10 mM MgCl2 | Sigma | M8266 | |
| 1.5 mM spermine | Sigma | 85590 | |
| Isotype rabbit IgG- ChIP Grade | abcam | abc7415 | |
| Rabbit anti-PCM-1 antibody | Sigma | HPA023374 | |
| Alexa Fluor 488 F(ab')2 Fragment of Goat Anti-Rabbit IgG (H+L) Antibody | Life technologies | A-11070 | |
| cell strainers 70 μm and 100μm | Fisher scientific | 11597522, 11517532 | |
| Glass dounce (40 ml) and pestle large clearance | Sigma | D9188-1SET | |
| EdU (5-ethynyl-2’-deoxyuridine) | Life technologies | A10044 | |
| Click-iT Plus EdU Alexa Fluor 647 Flow Cytometry Assay Kit | Life technologies | C10634 | This kit inlcudes reagents required for section, EdU reaction buffer, EdU fixative, saponin-based permeabilization solution and the reagents required for the EdU labelling cocktail. |
| CyStain DNA 2 step kit, | Sysmex Partec | 05 5005 | This kit inlcudes reagents required for DAPI labelling (DNA staining solution) |
| Probe homogeniser e.g. TissueRuptor | Qiagen | 9001273 | |
| TissueRuptor Disposable Probes | Qiagen | 990890 | |
| ultracentrifuge | Sorvall | ||
| Facscanto II | BD Biosciences | ||
| Ultracentrifuge Tube, Thinwall, Polypropylene. 38.5 mL, 25 x 89 mm | Beckman Coulter | 326823 | |
| Bovine serum albumin | Sigma | A2153 |
Riferimenti
- Bergmann, O., et al. Evidence for cardiomyocyte renewal in humans. Science. 324, 98-102 (2009).
- Senyo, S. E., et al. Mammalian heart renewal by pre-existing cardiomyocytes. Nature. 493, 433-436 (2013).
- Soonpaa, M. H., Rubart, M., Field, L. J. Challenges measuring cardiomyocyte renewal. Biochim Biophys Acta. 1833, 799-803 (2013).
- Loffredo, F. S., Steinhauser, M. L., Gannon, J., Lee, R. T. Bone marrow-derived cell therapy stimulates endogenous cardiomyocyte progenitors and promotes cardiac repair. Cell Stem Cell. 8, 389-398 (2011).
- Malliaras, K., et al. Cardiomyocyte proliferation and progenitor cell recruitment underlie therapeutic regeneration after myocardial infarction in the adult mouse heart. EMBO Mol Med. 5, 191-209 (2013).
- Hsieh, P. C., et al. Evidence from a genetic fate-mapping study that stem cells refresh adult mammalian cardiomyocytes after injury. Nat Med. 13, 970-974 (2007).
- Bergmann, O., et al. Identification of cardiomyocyte nuclei and assessment of ploidy for the analysis of cell turnover. Exp Cell Res. 317, 188-194 (2011).
- Herget, G. W., Neuburger, M., Plagwitz, R., Adler, C. P. DNA content, ploidy level and number of nuclei in the human heart after myocardial infarction. Cardiovasc Res. 36, 45-51 (1997).
- Scholzen, T., Gerdes, J. The Ki-67 protein: from the known and the unknown. J Cell Physiol. 182, 311-322 (2000).
- Carmena, M., Earnshaw, W. C. The cellular geography of aurora kinases. Nat Rev Mol Cell Biol. 4, 842-854 (2003).
- Bergmann, O., Jovinge, S. Isolation of Cardiomyocyte Nuclei from Post-mortem Tissue. J. Vis. Exp. , e4205 (2012).
- Gilsbach, R., et al. Dynamic DNA methylation orchestrates cardiomyocyte development, maturation and disease. Nat Commun. 5, 5288 (2014).
- Richardson, G., Laval, S., Owens, W. A. Cardiomyocyte regeneration in the mdx mouse model of non-ischemic cardiomyopathy. Stem Cells Dev. , (2015).
- Jiao, K., et al. An essential role of Bmp4 in the atrioventricular septation of the mouse heart. Genes Dev. 17, 2362-2367 (2003).
- Bergmann, O., et al. Cardiomyocyte renewal in humans. Circ Res. 110, e17-e18 (2012).
- Prigge, J. R., et al. Nuclear double-fluorescent reporter for in vivo and ex vivo analyses of biological transitions in mouse nuclei. Mamm Genome. , (2013).
- Naqvi, N., et al. A proliferative burst during preadolescence establishes the final cardiomyocyte number. Cell. 157, 795-807 (2014).
- Liu, Z., Yue, S., Chen, X., Kubin, T., Braun, T. Regulation of cardiomyocyte polyploidy and multinucleation by CyclinG1. Circ Res. 106, 1498-1506 (2010).
- Ang, K. L., et al. Limitations of conventional approaches to identify myocyte nuclei in histologic sections of the heart. Am J Physiol Cell Physiol. 298, C1603-C1609 (2010).
- Kajstura, J., et al. Myocyte turnover in the aging human heart. Circ Res. 107, 1374-1386 (2010).
- Kajstura, J., et al. Cardiomyogenesis in the adult human heart. Circ Res. 107, 305-315 (2010).
- Walsh, S., Ponten, A., Fleischmann, B. K., Jovinge, S. Cardiomyocyte cell cycle control and growth estimation in vivo–an analysis based on cardiomyocyte nuclei. Cardiovasc Res. 86, 365-373 (2010).
- Anversa, P., Leri, A., Kajstura, J. Cardiac regeneration. J Am Coll Cardiol. 47, 1769-1776 (2006).
- Gonzalez-Valdes, I., et al. Bmi1 limits dilated cardiomyopathy and heart failure by inhibiting cardiac senescence. Nat Commun. 6, 6473 (2015).
- Kimura, W., et al. Hypoxia fate mapping identifies cycling cardiomyocytes in the adult heart. Nature. 523, 226-230 (2015).
- Soonpaa, M. H., Field, L. J. Assessment of cardiomyocyte DNA synthesis in normal and injured adult mouse hearts. Am J Physiol. 272, H220-H226 (1997).

