Samtidig Vurdering av kardiomyocytt DNA syntese og ploidiundersøkelse: En metode for å hjelpe Kvantifisering av kardiomyocytt Regeneration og Omsetning
Summary
Quantification of cardiomyocyte turnover is challenging. The protocol described here makes an important contribution to this challenge by enabling accurate and sensitive quantification of neo-cardiomyocyte nuclei generation and nuclei ploidy.
Abstract
Selv om det er akseptert at hjertet har et begrenset potensial til å regenerere cardiomyocytes etter skade og at lave nivåer av kardiomyocytt omsetning oppstår under normal aldring, forblir kvantifisering av disse hendelsene utfordrende. Dette er delvis på grunn av sjeldenhet av prosessen og det faktum at flere cellulære kilder bidra til hjerteinfarkt vedlikehold. Videre er DNA-duplisering i kardiomyocytter fører ofte til en polyploid kardiomyocytt og bare sjelden fører til nye kardiomyocytter med celledeling. For nøyaktig å kvantifisere kardiomyocytt omsetning diskriminering mellom disse prosessene er avgjørende. Protokollen er beskrevet her anvender langtids nukleosid merking for å merke alle kjerner som har oppstått som et resultat av DNA-replikasjon og cardiomyocyte kjerner som er identifisert ved å benytte kjerner isolering og påfølgende PCM1 immunolabeling. Sammen dette gjør det mulig nøyaktig og følsom identifikasjon av nukleosidet merking av cardiomyocyte kjerner befolkningen. Videre, 4 ', 6-diamidino-2-fenylindol merking og analyse av kjerner ploiditet, muliggjør diskriminering av neo-cardiomyocyte kjerner fra kjerner som har innarbeidet i løpet av nukleosid Polyploidisering. Selv om denne metoden ikke kan kontrollere for kardiomyocytt binucleation, gir det en rask og robust kvantifisering av neo-kardiomyocytt kjerner mens regnskap for Polyploidisering. Denne metoden har en rekke nedstrøms applikasjoner, inkludert vurdering av potensielle therapeutics å forbedre kardiomyocytt regenerering eller undersøke effekten av hjertesykdom på kardiomyocytt omsetning og ploiditet. Denne teknikken er også kompatibelt med flere nedstrøms immunohistologiske teknikker, slik at kvantifisering av nukleosid inkorporering i alle hjertecelletyper.
Introduction
I de senere årene har det vært en opphopning av bevis utfordrer antakelsen at hjertet er et terminalt differensiert, post-mitotisk organ 1,2. Men kvantifisering av kardiomyocytt omsetning og regenerering er fortsatt utfordrende.
Vanskelighetene i nøyaktig identifisering av sjeldne kardiomyocytt generasjon ved hjelp av standard immunhistokjemiske teknikker er vel rapportert tre. I tillegg er usikkert med bevis for bidrag fra kardiomyocytt spredning samt av stamcelle differensiering 4-6 cellekilde kardiomyocytt generasjon. Derfor er umulig og kvantifisering av proliferasjon i en enkelt populasjon, inkludert kardiomyocytter bruk av avstamning sporing modeller som krever kjennskap til kardiomyocytt stamfar fenotype, er upassende. Videre er en kardiomyocytt har potensial for endoreplication uten karyokinesis (noe som resulterer i en polyploid bildiomyocyte) eller karyokinesis i fravær av cytokinese (noe som resulterer i en binucleated kardiomyocytt) 7,8. Den nøyaktig kvantifisering av kardiomyocytt omsetningen er avhengig av evnen til å skille mellom disse hendelsene og sann neo-kardiomyocytt generasjon. Dette skaper unike komplikasjoner fordi DNA replikasjon og uttrykk for cyclin-avhengige kinaser i cardiomyocytes ikke utelukkende demonstrere sann celledeling 9,10.
For å bistå i kvantifisering av neo-kardiomyocytt generasjon, har vi kombinert en etablert kjerner isolasjon teknikk, og immunologisk merking av pericentriolar materiale 1 (PCM1) for cardiomyocyte kjerner identifisering som beskrevet av Bergmann et al. 7,11 med nye metoder for langsiktig DNA merking og ploiditetsanalysen. PCM-1 er en sentrosomen protein som akkumuleres ved kjernekraft overflaten av differensierte, ikke-sykling muskelceller. Tidligere studier har vist at antistoffer motPCM-en spesifikt merke cardiomyocyte kjerner 7,11 og som sådan PCM1 har blitt brukt av en rekke uavhengige grupper for å identifisere cardiomyocytes 1,12,13. I tillegg har vi vist at PCM1 uttrykk tilordner til genetisk merkede cardiomyocyte kjernene i TnT-CRE transgen musemodell 14 (Supplementary figur 1).
Protokollen er beskrevet her gjør det mulig nøyaktig og følsom identifikasjon av neo kardiomyocytt kjerner generering i mus hjertet, uavhengig av de cellulære opprinnelse (figur 1A og B) samtidig med unntak av nukleosid-merking på grunn Polyploidisering fra analysen (figur 1C og D). Selv om denne metoden ikke kan kontrollere for kardiomyocytt binucleation, gir det en rask og robust kvantifisering av neo-kardiomyocytt kjerner som er nødvendig for nøyaktig kvantifisering av kardiomyocytt omsetning. Dessuten,det gir en rask screening verktøy for å vurdere potensielle endringer i dynamikken i kardiomyocytt generasjon.
Selv om DNA-merking involverer vanligvis 5-brom-2'-deoksyuridin (BrdU) som tymidinanalog, protokollen beskrevet her anvender en 5-etynyl-2'-deoksyuridin (EDU) basert assay som det krever færre prosesstrinn for en hurtigere gjennomstrømning og som ikke krever denaturering av DNA for immuno-deteksjon, slik at det er kompatibelt med andre immunfarging protokoller og dermed øke den potensielle nedstrøms anvendelser av fremgangsmåten.
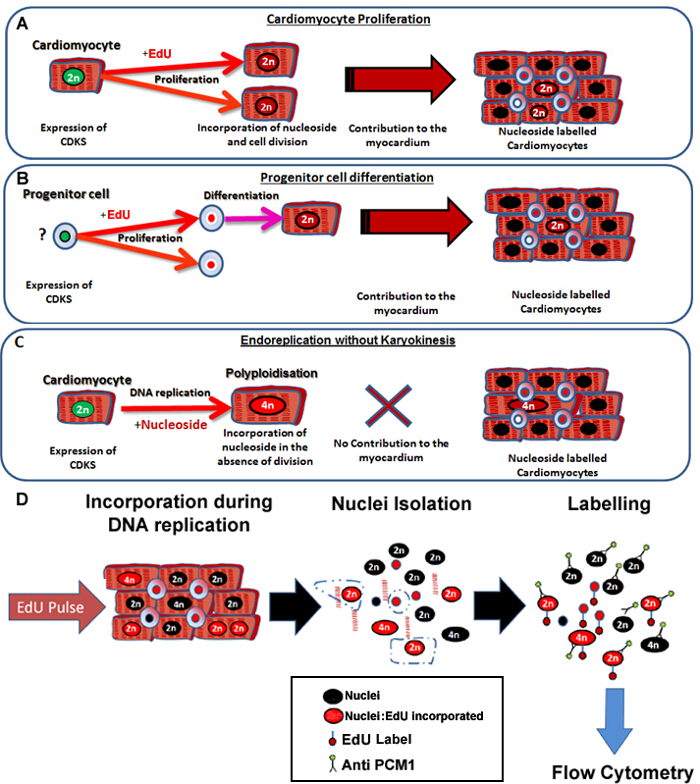
Figur 1: Kontinuerlig pulserende med Edu etiketter neo-cardiomyocytes uavhengig av deres forfedre. (A) EDU er innlemmet i DNA av kardiomyocytter under celledeling. Spredning i kardiomyocytt befolkningen vil Result i en økning i, eller erstatning av kardiomyocytter og er således produktivt DNA-syntese (bidrar til vev vedlikehold og reparasjon). (B) EDU er innlemmet i DNA av hjerte progenitorceller under celledeling. Dette vil bli holdt tilbake i cellen under differensiering til kardiomyocytt avstamning. Dette stamcelledifferensiering vil også resultere i en økning i antallet av kardiomyocytter og bidrar derfor til vev vedlikehold og reparasjon. (C) kardiomyocytter har potensial til å gjennomgå "ikke-produktiv" DNA-replikasjon som resulterer i økt kardiomyocytt ploiditet, som er forbundet med kardiomyocytt hypertrofi og myokardial remodellering, men ikke erstatte tapte kardiomyocytter. Prosessen med Polyploidisering forskjellig fra binucleation som det resulterer i et kardiomyocytt med en enkelt kjerne som inneholder fire eller flere sett av to homologe kromosomer (> 2N). (D) Ved å følge en kontinuerlig kjerner pUlse, beskriver denne protokollen kjerner isolering og identifisering av cardiomyocyte kjerner av PCM1 uttrykk for å tillate kvantifisering av både kardiomyocytt ploidiresultat og Edu innlemmelse. PCM1 uttrykk og Edu innlemmelse oppdaget ved hjelp av flowcytometri. Klikk her for å se en større versjon av dette tallet.
Protocol
Representative Results
Discussion
For nøyaktig kvantifisere kardiomyocytt omsetning og regenerering analyser må skille mellom sant kardiomyocytt generasjon og nonproductive DNA divisjon. Mange studier fortsette å bare ignorere disse nonproductive hendelser, kvantifisere kardiomyocytt spredning utelukkende via uttrykk for cyclin kinesis og cellesyklus markører. Å date en enkel metode som gjør det mulig for nøyaktig kvantifisering av kardiomyocytt omsetningen mens kontrollere for disse nonproductive hendelsene forblir banneord. Spesielt er det fortsatt vanskelig å gjøre rede for kardiomyocytt Polyploidisering som bidrar opp til ~ 65% av kardiomyocytt DNA-replikasjon 13. Derfor å bistå i nøyaktig kvantifisering av kardiomyocytt generasjon har vi utviklet en protokoll som gjør det robust kvantifisering av satsene for neo cardiomyocyte kjerner samtidig utelukke DNA replikasjon som resulterer i økt ploidiresultat. Selv om denne protokollen kan ikke diskriminering mellom neo-kardiomyocytt slektersjon og kardiomyocytt bi-kjernedannelse, kan den brukes til raskt og nøyaktig å beregne den øvre grense (regnskap for ploiditet) av kardiomyocytt generasjon. Denne protokollen gir derfor et screeningverktøy for å vurdere potensielle endringer i satsene for kardiomyocytt generasjon og Polyploidisering i sykdomsmodeller eller for å vurdere potensialet effektiviteten av behandlingsformer. Når endringer i frekvensen av neo-kardiomyocytt kjerner generasjon er identifisert ved hjelp av denne protokollen påfølgende studier kan anvendes for å fastslå om denne på grunn av endringer i kardiomyocytt generering av kardiomyocytt kjernedannelse tall, slik det er beskrevet tidligere 2,13,17,18. Disse inkluderer bruk av histologiske kvantifisering cardiomyocyte kjerne dynamikk under pulsperioden eller analyser av vevssnitt hentet fra Edu pulserte dyr i å sammenligne Edu innlemmelse i mononukleærerte og multinucleated cardiomyocyte populasjoner.
På grunn av de lave nivåer av kardiomyocytt omsetning detteprotokollen bruker flere injeksjoner av Edu over en 7 dagers periode. Dette gjør også "jage" av alle mulige cellulære kilder kardiomyocytt generasjon og tillater kvantifisering av kumulative kardiomyocytt kjerner generasjon i løpet av denne tidsperioden. Avhengig av studien, kan dette tidsrommet tilpasses den anslåtte nivåer av kardiomyocytt generasjon. For nøyaktig kvantifisering av edu-inkorporering i cardiomyocyte kjerner, er det viktig at det ikke er noen ikke-spesifikk merking av kjerner med det sekundære antistoff som brukes til å detektere PCM-1 reaktivitet. Det ville derfor være aktuelt å foreta flere sekundære antistoff titrering eksperimenter for å optimalisere dette aspektet av protokollen, særlig hvis et sekundært antistoff enn det som foreslås i denne protokollen som skal benyttes. Protokollen er beskrevet her bruker PCM-1 uttrykk for å identifisere cardiomyocyte kjerner. Selv om dette er en etablert kardiomyocytt markør, kan alternative markører brukes til å valideredata; disse inkluderer antistoffer som er spesifikke for hjerte troponin T som er blitt identifisert som delvis lokalisert i cardiomyocyte kjerner 1. På lignende måte kan alternative nukleære lokaliserte proteiner anvendes for å identifisere og kvantifisere EDU innlemmelse i andre enn den til kardiomyocytter kjerner populasjoner. Det er viktig at alle cardiomyocyte kjerner som er aktivt som gjennomgår mitose er ekskludert fra analysen, som skjebnen til denne DNA-syntese er ukjent og kan resultere i enten celledeling eller økt ploiditet. PCM1 demonteres i M-fasen av cellesyklusen derfor kardiomyocytter som gjennomgår mitose vil ikke bli identifisert ved PCM1 uttrykk. I tillegg bør alle kjerner i S-fasen av cellesyklus bli ekskludert fra etterfølgende analyse. Dette kan oppnås ved å portstyre ut alle kjerner med en DAPI intensitet over den 2N populasjonen inkludert de med en DAPI intensitet mellom 2N og 4N populasjoner.
Selv om det blir stadigakseptert at hjertet har kapasitet til å erstatte cardiomyocytes under normal aldring og etter akutt skade, kilden og graden av dette potensialet er fortsatt kontroversielt. I tillegg har ulike priser av kardiomyocytt omsetning rapportert 1,7,20-22. Dette kan være delvis på grunn av vanskelighetene med nøyaktig identifisering og kvantifisering av neo-kardiomyocytt generasjon 19. Fram til i dag de fleste studier har støttet seg bare på bruk av histologisk analyse og identifikasjon av kardiomyocytter via ekspresjon av cytoplasmiske proteiner, inkludert proteiner av sarcomere, for kvantifisering av kardiomyocytt omsetning og fornyelse 2,4,23,24. Bruken av disse fremgangsmåter for å påvise ekspresjon av spredning markører, eller som vist her, kan inkorporering av tymidinanaloger lett resultere i feilidentifisering av andre hjertecelletyper som kardiomyocytter. Mens bruken av 3D-konfokalt avbildnings kan bidra til å lindre disse problemene thESE metoder er kostbare og tidkrevende. Interessant, protokollen beskrevet her demonstrerer neo-cardiomyocyte kjerner generering forekommer ved en hastighet på 0,17% pr uke. Dette er konsistent med andre flowcytometri basert studier som viser ukentlige omsetning på opptil 0,13% 5. Selv om det er fristende å ekstrapolere årlig omsetning priser basert på disse dataene, som i tidligere studier 2,5,25,26, dette er upassende som prisene i omsetning er dynamiske under levetiden til et dyr 13.
Denne metoden har en rekke potensielle bruksområder, inkludert vurdering av potensielle therapeutics å forbedre kardiomyocytt regenerering eller undersøke effekten av hjertesykdom på kardiomyocytt omsetning og priser av kardiomyocytt Polyploidisering.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
This work was supported by the British Heart Foundation, project grant PG/13/69/30454.
Materials
| 0.32 M sucrose | Sigma | 84100 | |
| 10 mM Tris-HCl (pH = 8) | Sigma | T3253 | |
| 5 mM CaCl2 | Sigma | c5086 | |
| 5 mM magnesium acetate | sigma | M-5661 | |
| 2.0 mM EDTA | Sigma | E5134 | |
| 0.5 mM EGTA | Sigma | 63779 | |
| 1 mM DTT | Sigma | D0632 | |
| 70 mM KCl | Sigma | P9541 | |
| 10 mM MgCl2 | Sigma | M8266 | |
| 1.5 mM spermine | Sigma | 85590 | |
| Isotype rabbit IgG- ChIP Grade | abcam | abc7415 | |
| Rabbit anti-PCM-1 antibody | Sigma | HPA023374 | |
| Alexa Fluor 488 F(ab')2 Fragment of Goat Anti-Rabbit IgG (H+L) Antibody | Life technologies | A-11070 | |
| cell strainers 70 μm and 100μm | Fisher scientific | 11597522, 11517532 | |
| Glass dounce (40 ml) and pestle large clearance | Sigma | D9188-1SET | |
| EdU (5-ethynyl-2’-deoxyuridine) | Life technologies | A10044 | |
| Click-iT Plus EdU Alexa Fluor 647 Flow Cytometry Assay Kit | Life technologies | C10634 | This kit inlcudes reagents required for section, EdU reaction buffer, EdU fixative, saponin-based permeabilization solution and the reagents required for the EdU labelling cocktail. |
| CyStain DNA 2 step kit, | Sysmex Partec | 05 5005 | This kit inlcudes reagents required for DAPI labelling (DNA staining solution) |
| Probe homogeniser e.g. TissueRuptor | Qiagen | 9001273 | |
| TissueRuptor Disposable Probes | Qiagen | 990890 | |
| ultracentrifuge | Sorvall | ||
| Facscanto II | BD Biosciences | ||
| Ultracentrifuge Tube, Thinwall, Polypropylene. 38.5 mL, 25 x 89 mm | Beckman Coulter | 326823 | |
| Bovine serum albumin | Sigma | A2153 |
Riferimenti
- Bergmann, O., et al. Evidence for cardiomyocyte renewal in humans. Science. 324, 98-102 (2009).
- Senyo, S. E., et al. Mammalian heart renewal by pre-existing cardiomyocytes. Nature. 493, 433-436 (2013).
- Soonpaa, M. H., Rubart, M., Field, L. J. Challenges measuring cardiomyocyte renewal. Biochim Biophys Acta. 1833, 799-803 (2013).
- Loffredo, F. S., Steinhauser, M. L., Gannon, J., Lee, R. T. Bone marrow-derived cell therapy stimulates endogenous cardiomyocyte progenitors and promotes cardiac repair. Cell Stem Cell. 8, 389-398 (2011).
- Malliaras, K., et al. Cardiomyocyte proliferation and progenitor cell recruitment underlie therapeutic regeneration after myocardial infarction in the adult mouse heart. EMBO Mol Med. 5, 191-209 (2013).
- Hsieh, P. C., et al. Evidence from a genetic fate-mapping study that stem cells refresh adult mammalian cardiomyocytes after injury. Nat Med. 13, 970-974 (2007).
- Bergmann, O., et al. Identification of cardiomyocyte nuclei and assessment of ploidy for the analysis of cell turnover. Exp Cell Res. 317, 188-194 (2011).
- Herget, G. W., Neuburger, M., Plagwitz, R., Adler, C. P. DNA content, ploidy level and number of nuclei in the human heart after myocardial infarction. Cardiovasc Res. 36, 45-51 (1997).
- Scholzen, T., Gerdes, J. The Ki-67 protein: from the known and the unknown. J Cell Physiol. 182, 311-322 (2000).
- Carmena, M., Earnshaw, W. C. The cellular geography of aurora kinases. Nat Rev Mol Cell Biol. 4, 842-854 (2003).
- Bergmann, O., Jovinge, S. Isolation of Cardiomyocyte Nuclei from Post-mortem Tissue. J. Vis. Exp. , e4205 (2012).
- Gilsbach, R., et al. Dynamic DNA methylation orchestrates cardiomyocyte development, maturation and disease. Nat Commun. 5, 5288 (2014).
- Richardson, G., Laval, S., Owens, W. A. Cardiomyocyte regeneration in the mdx mouse model of non-ischemic cardiomyopathy. Stem Cells Dev. , (2015).
- Jiao, K., et al. An essential role of Bmp4 in the atrioventricular septation of the mouse heart. Genes Dev. 17, 2362-2367 (2003).
- Bergmann, O., et al. Cardiomyocyte renewal in humans. Circ Res. 110, e17-e18 (2012).
- Prigge, J. R., et al. Nuclear double-fluorescent reporter for in vivo and ex vivo analyses of biological transitions in mouse nuclei. Mamm Genome. , (2013).
- Naqvi, N., et al. A proliferative burst during preadolescence establishes the final cardiomyocyte number. Cell. 157, 795-807 (2014).
- Liu, Z., Yue, S., Chen, X., Kubin, T., Braun, T. Regulation of cardiomyocyte polyploidy and multinucleation by CyclinG1. Circ Res. 106, 1498-1506 (2010).
- Ang, K. L., et al. Limitations of conventional approaches to identify myocyte nuclei in histologic sections of the heart. Am J Physiol Cell Physiol. 298, C1603-C1609 (2010).
- Kajstura, J., et al. Myocyte turnover in the aging human heart. Circ Res. 107, 1374-1386 (2010).
- Kajstura, J., et al. Cardiomyogenesis in the adult human heart. Circ Res. 107, 305-315 (2010).
- Walsh, S., Ponten, A., Fleischmann, B. K., Jovinge, S. Cardiomyocyte cell cycle control and growth estimation in vivo–an analysis based on cardiomyocyte nuclei. Cardiovasc Res. 86, 365-373 (2010).
- Anversa, P., Leri, A., Kajstura, J. Cardiac regeneration. J Am Coll Cardiol. 47, 1769-1776 (2006).
- Gonzalez-Valdes, I., et al. Bmi1 limits dilated cardiomyopathy and heart failure by inhibiting cardiac senescence. Nat Commun. 6, 6473 (2015).
- Kimura, W., et al. Hypoxia fate mapping identifies cycling cardiomyocytes in the adult heart. Nature. 523, 226-230 (2015).
- Soonpaa, M. H., Field, L. J. Assessment of cardiomyocyte DNA synthesis in normal and injured adult mouse hearts. Am J Physiol. 272, H220-H226 (1997).

