تسلسل عميق متحيز من الحمض النووي الريبي الفيروسات من العينات السريرية
Summary
This protocol describes a rapid and broadly applicable method for unbiased RNA-sequencing of viral samples from human clinical isolates.
Abstract
نحن هنا الخطوط العريضة لجيل القادم من بروتوكول تسلسل الحمض النووي الريبي التي تمكن دي نوفو المجالس ومكالمات البديل داخل مجموعة من العوامل الوراثية الفيروسية التي تم جمعها من مصادر السريرية والبيولوجية. هذه الطريقة غير منحازة والعالمي. ويستخدم البادئات العشوائية لتخليق [كدنا ولا يتطلب أي معرفة مسبقة من المحتوى تسلسل الفيروسي. قبل بناء المكتبة، يتم استخدام انتقائي الهضم أساس H-ريبونوكلياز في استنزاف غير المرغوب فيها RNA – بما في ذلك بولي (RA) الناقل والحمض النووي الريبي الريباسي – من عينة الحمض النووي الريبي الفيروسية. نضوب انتقائية يحسن كلا من جودة البيانات وعدد فريدة من نوعها يقرأ في المكتبات RNA تسلسل الفيروسية. وعلاوة على ذلك، يتم استخدام الخطوة "tagmentation" القائم على ترانسبوزاز في البروتوكول كما أنه يقلل من العام وقت البناء المكتبة. وقد مكن بروتوكول تسلسل عميق السريع لأكثر من 600 لاسا وفيروس إيبولا العينات بما في ذلك مجموعات من كل الدم والأنسجة المعزولة وغير قابلة للتطبيق على نطاق واسع لدراسات الجينوم الميكروبية الأخرى.
Introduction
الجيل القادم التسلسل الفيروسات من مصادر السريرية يمكن أن تبلغ نقل وبائيات الأمراض، فضلا عن المساعدة في دعم رواية التشخيص، وتطوير اللقاحات العلاجية. وقد سمح التوليف [كدنا باستخدام بادئات عشوائية للكشف والتجمع من الجينوم من المتباينة، وشارك في إصابة أو حتى الفيروسات الجديدة 1،2. كما هو الحال مع أساليب مشاركات أخرى، والملوثات غير المرغوب فيها وتشغل العديد من التسلسل يقرأ ويؤثر سلبا على نتائج التسلسل. المضيف وبولي (RA) RNA الناقل والملوثات الموجودة في العديد من مجموعات عينة الفيروسية الحالية.
يصف بروتوكول وسيلة فعالة وفعالة من حيث التكلفة لجينوم الفيروس تسلسل الحمض النووي الريبي عميقة على أساس غير متحيز الحمض النووي الريبي مجموع وما يليها. طريقة يستخدم لريبونوكلياز H نضوب انتقائية الخطوة 3 لإزالة المضيف الريباسي غير المرغوب فيها وRNA الناقل. نضوب انتقائية يثري المحتوى الفيروسي (الشكل 1) ويحسن الجودة الشاملة من تسلسل البيانات(الشكل 2) من العينات السريرية. وعلاوة على ذلك، يتم تطبيق tagmentation إلى البروتوكول كما أنه يقلل بشكل ملحوظ وقت البناء المكتبة. وقد استخدمت هذه الأساليب لتوليد بسرعة مجموعات كبيرة من البيانات من الايبولا وحمى لاسا جينوم فيروس 2،4،5، ويمكن استخدامها لدراسة مجموعة واسعة من فيروسات الحمض النووي الريبي. وأخيرا، فإن النهج لا يقتصر على عينات الإنسان؛ وقد تجلى فائدة نضوب انتقائية في عينات الأنسجة التي تم جمعها من القوارض المصابة لاسا ونماذج المرض الرئيسيات غير البشرية 5،6.
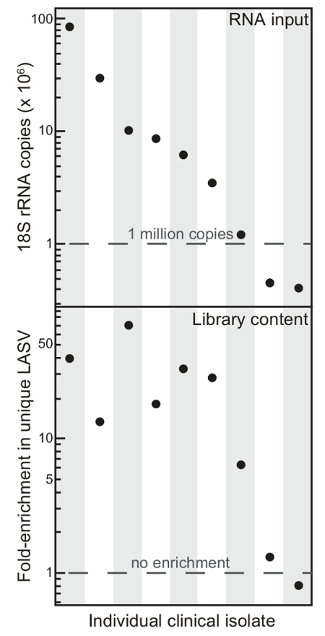
يعكس الشكل 1. إجمالي RNA المحتوى إثراء لاسا الفيروسات المحتوى عن طريق الانتقائية استنفاد ابتداء المضمون العام (RNA المدخلات) وإثراء فريد فيروس حمى لاسا (LASV) يقرأ (محتوى مكتبة) عند نضوب الريباسي من تسعة العزلات السريرية المختلفة. تم تعديل هذا الرقم من 6 <em>. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
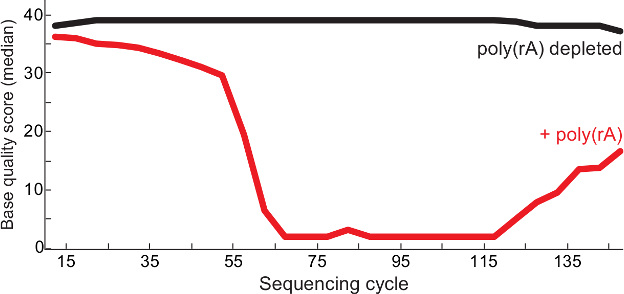
الشكل 2. العالي الجودة تسلسل بعد الناقل RNA نضوب. الصفات قاعدة الوسيطة في دورة تسلسل بولي (RA) -contaminated المكتبات اسا فيروس (الأحمر) والسيطرة (أي الناقل لوحظ في مكتبة، أسود) من تقرير QC 13. من القراءة (1) وقراءة 2 من نهاية يقترن يقرأ يتم دمج في ملف BAM مكتبة وتعرض عشرات الجودة في كل قاعدة. تم تعديل هذا الرقم من 6. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
والفيروسي RNA وما يليها تفاصيل بروتوكول إنشاء المكتبات مباشرة من استخراجRNA جمعها من العينات السريرية والبيولوجية. لضمان السلامة الشخصية، ينبغي المعطل جميع عينات مصل الدم والبلازما والأنسجة الفيروسية في مخازن مناسبة قبل استخراج الحمض النووي الريبي. في بعض التعطيل واستخراج مجموعات، يتم تضمين الناقل بولي (RA) RNA. سيتم إزالة هذا خلال ريبونوكلياز H خطوة نضوب انتقائية الأولية. واستنادا إلى الشفاء الكامل، وتركيز المتوقع من الحمض النووي الريبي الناقل هو 100 نانوغرام / ميكرولتر. في البروتوكول، ويستخدم 110 نانوغرام / ميكرولتر بنسبة ضئيلة DT RNA (تركيز الناقل 1.1x) للنضوب. إذا بولي (RA) الناقل غير موجود في العينة، لا ينبغي أن تضاف بعد ذلك بنسبة ضئيلة (DT) قبل نضوب.
تم تصميم بروتوكول التالية لمدة 24 ردود الفعل في شكل لوحة PCR (ما يصل الى 250 حجم ميكرولتر). وذكرت إصدار سابق من هذا البروتوكول في Matranga، وآخرون. 6.
Protocol
Representative Results
Discussion
النهج المبين تمكن قوية وعالمية، والتسلسل السريع، وكان يستخدم لتسلسل فيروس إيبولا خلال 2،4 2014 انتشار المرض. وذلك بربط نضوب انتقائية والتوليف [كدنا مع بناء مكتبة tagmentation، تم تخفيض الوقت عملية الشامل التي كتبها ~ 2 أيام من وسائل محول ربط السابقة. وفي الآونة الأخيرة، كان يعمل هذا البروتوكول من قبل المتعاونين الدوليين وغيرهم مع نجاحا كبيرا 15،16 وسيتم نشر إلى مختبرات في غرب أفريقيا لدعم البحوث والدراسات القائمة على علم الجينوم المحلية وتشخيص 17.
بروتوكول الموصوفة هنا يستخدم البادئات العشوائية لإعداد كدنا] للمكتبات الحمض النووي الريبي وما يليها الفيروسية. على عكس النهج RNA وما يليها الفيروسية السابقة، أنه لا يتطلب أي معرفة مسبقة من تسلسل البيانات أو تفصيلا وتستغرق وقتا طويلا التصميم التمهيدي للفيروس أو كليد محددة. ويمكن تطبيق هذا الأسلوب على أي عينة الحمض النووي الريبي الفيروسية. على سبيل المثال، كان يستخدم لتوليد محتوى الفيروسي من كل من الايبولاوعينات لاسا 6. ويمكن أيضا أن تستخدم بروتوكول لtranscriptomic المضيف، مشاريع التسلسل metagenomic واكتشاف الممرض 1.
ويستهدف خطوة حاسمة للبروتوكول ريبونوكلياز H الهضم، والإنتاجية العالية، وطريقة منخفضة التكلفة لإزالة الناقل غير المرغوب فيها والجيش الملكي النيبالي المضيف من العينات الفيروسية. الخطوة نضوب انتقائية للبروتوكول يستخدم العديد من المكونات، ويتطلب مهارة ودقة. ينبغي أن تؤخذ الوقت الاضافي والرعاية أثناء الإعداد الأولي.
حيث أن معظم مصل الدم والبلازما العينات السريرية غالبا ما يكون قليلا جدا مادة الحمض النووي والتلوث وفقدان العينة شائعة. لتجنب هذه المشاكل، يجب توخي الحذر خاصة عند استخدام هذا البروتوكول. أولا، RNA هو عرضة للتدهور. وبالتالي كل المناطق يجب أن تكون نظيفة وخالية من nucleases. ثانيا، لتحديد عينات مناسبة للاستخدام في هذا البروتوكول، المقايسات QRT-PCR RNA لكلا المضيف وفيروس ينبغي أن تستخدم لتقدير 5،6 </suص>. عند المقارنة بين المدخلات يرقى مع نتائج التسلسل من البروتوكول، والنجاح التسلسل (أي جيل من بيانات كافية لتجميع الفيروسي الكامل) المترابطة مع العينات التي تحتوي على ما لا يقل عن 100 خريج الحمض النووي الريبي مجموع و1،000 نسخة من الفيروس. وينبغي تجنب الثالث، والتعرض للمصادر البيئية من الأحماض النووية. يتم البروتوكول المذكورة هنا في مجلس الوزراء للسلامة الأحيائية لاحتياطات السلامة والحد من الملوثات البيئية. وعلاوة على ذلك، لدينا مجموعة والآخرون يلاحظون أن الإنزيمات التجارية قد تكون مصدرا آخر للتلوث الأحماض النووية البكتيرية في عينات المدخلات المنخفضة 6،18. استخدام مساحة عمل نظيفة (على سبيل المثال، PCR غطاء محرك السيارة، ومجلس الوزراء للسلامة الأحيائية) والضوابط السلبية (على سبيل المثال، الماء أو عازلة) سوف تساعد على التخفيف من وتتبع التلوث، على التوالي. للعينات مع <100 خريج من الحمض النووي الريبي مجموع، بولي فقط (RA) RNA الناقل، وليس الريباسي، ينبغي المنضب لضمان تحقيق نتائج التسلسل عالية الجودة مع الحد من فقدان المواد. للغايةعينات المدخلات المنخفضة، قد تكون أساليب كدنا] التضخيم أكثر ملاءمة 19، على الرغم من بولي (RA) الناقل يجب إزالة قبل تركيب كدنا].
استنزاف المضيف الريباسي يثري المحتوى الفيروسي في المكتبات التسلسل وينطبق على مجموعات عينة مختلفة بما في ذلك المصل أو البلازما، وأنواع متعددة من الأنسجة من القوارض والرئيسيات غير البشرية 5،6. في الكائنات غير البشرية، يقرأ محاذاة إلى 28S الريباسي بقيت بعد نضوب، مما يشير إلى 28S الريباسي أقل محفوظ بين البشر والأنواع الأخرى 6،20. عند استخدام هذا الأسلوب مع العزلات غير البشرية، قد يكون من الضروري لتكملة مع oligos الحمض النووي مكملة لتسلسل الريباسي المتباينة لل3،21 المضيف المحدد.
منذ البروتوكول هو غير متحيز، الفيروسية يقرأ قد لا تمثل سوى جزء صغير من المحتوى الكلي للمكتبة. على الرغم من أن الريباسي هو النوع الأكثر وفرة من الحمض النووي الريبي المضيفة وفقط نسبة صغيرة من الريباسي يقرأ (0؛ 1٪) وجدت بعد نضوب انتقائية، وجميع RNA المضيفة الأخرى (على سبيل المثال، مرنا) تبقى بعد نضوب وقد تكون مسؤولة عن يقرأ العديد من تسلسل من العينة. لذلك "الإفراط" (أي oversequencing) مكتبات فردية مطلوب من أجل الحصول على ما يكفي من التغطية للمكالمات التجمع والبديل الفيروسية. لدراستنا، ونحن نحاول تسلسل ~ 20 مليون يقرأ في عينة لدينا ما يكفي من العمق لتحليل الفيروسي المتغيرات الجيني وما يرتبط بها فضلا عن المحتوى metagenomic 2،5. لدراسات اكتشاف metagenomic والممرض، من المهم أن نلاحظ أن تتم إزالة تلويث الحمض النووي المضيف الدناز الهضم. لذلك قد تفقد الفيروسات ومسببات الأمراض الأخرى التي تحتوي على جينوم الحمض النووي خلال هذه العملية، ولكن قد لا يزال تكون متسلسلة وسيطة الحمض النووي الريبي.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
This work has been funded in part with Federal funds from the National Institutes of Health, Office of Director, Innovator (No.: DP2OD06514) (PCS) and from the National Institute of Allergy and Infectious Diseases, National Institutes of Health, Department of Health and Human Services, under Contracts (No:HHSN272200900018C, HHSN272200900049C and U19AI110818).
Materials
| 96-Well PCR Plates | VWR | 47743-953 | |
| Strips of Eight Caps | VWR | 47745-512 | |
| Nuclease-free water | Ambion | AM9937 | 50 ml bottle |
| TURBO DNase | Ambion | AM2238 | post RNA extraction step, 2 U/µL, buffer included |
| PCR cycler | any PCR cyclers | ||
| Agencourt RNAClean XP SPRI beads | Beckman Coulter Genomics | A63987 | beads for RNA cleanup |
| Real Time qPCR system | any system | ||
| DynaMag-96 Side Skirted Magnet | Invitrogen | 12027 | |
| 70% Ethanol | prepare fresh | ||
| qRT-PCR primers | IDT DNA | see Table 2 | |
| 5M NaCl | Ambion | AM9760G | |
| 1M Tris-HCl pH 7.4 | Sigma | T2663-1L | |
| 1M Tris-HCl pH 7.5 | Invitrogen | 15567-027 | |
| 1M MgCl2 | Ambion | AM9530G | |
| Linear acrylamide | Ambion | AM9520 | |
| DNA oligos covering entire rRNA region | IDT DNA | see Table 3, order lab-ready at 100 µM | |
| Oligo (dT) | IDT DNA | 40 nt long, desalted | |
| Hybridase Thermostable RNase H | Epicentre | H39100 | |
| RNase-free DNase Kit | Qiagen | 79254 | post selective depletion step |
| SUPERase-In RNase Inhibitor | Ambion | AM2694 | |
| Random Primers | Invitrogen | 48190-011 | mostly hexamers |
| 10 mM dNTP mix | New England Biolabs | N0447L | |
| SuperScript III Reverse Transcriptase | Invitrogen | 18080-093 | with first-strand buffer, DTT |
| Air Incubator | any air incubator cyclers | ||
| NEBNext Second Strand Synthesis (dNTP-free) Reaction Buffer | New England Biolabs | B6117S | 10x |
| E. coli DNA Ligase | New England Biolabs | M0205L | 10 U/μl |
| E. coli DNA Polymerase I | New England Biolabs | M0209L | 10 U/μl |
| E. coli RNase H | New England Biolabs | M0297L | 2 U/μl |
| 0.5M EDTA | Ambion | AM9261 | |
| Agencourt AMPure XP SPRI beads | Beckman Coulter Genomics | A63881 | beads for DNA cleanup |
| Elution Buffer | Qiagen | 10 mM Tris HCl, pH 8.5 | |
| Quant-iT dsDNA HS Assay Kit | Invitrogen | Q32854 | |
| Qubit fluorometer | Invitrogen | Q32857 | |
| Nextera XT DNA Sample Prep Kit | Illumina | FC-131-1096 | |
| Nextera XT DNA Index Kit | Illumina | FC-131-1001 | |
| Tapestation 2200 | Agilent | G2965AA | |
| High Sensitivity D1000 reagents | Agilent | 5067-5585 | |
| High Sensitivity D1000 ScreenTape | Agilent | 5067-5584 | |
| BioAnalyzer 2100 | Agilent | G2939AA | |
| High Sensitivity DNA reagents | Agilent | 5067-4626 | |
| Library Quantification Complete kit (Universal) | Kapa Biosystems | KK4824 | alternative to tapestation, bioanalyzer for library quantification |
Riferimenti
- Stremlau, M. H., et al. Discovery of novel rhabdoviruses in the blood of healthy individuals from West Africa. PLoS Negl Trop Dis. 9, e0003631 (2015).
- Gire, S. K., et al. Genomic surveillance elucidates Ebola virus origin and transmission during the 2014 outbreak. Science. 345, 1369-1372 (2014).
- Morlan, J. D., Qu, K., Sinicropi, D. V. Selective depletion of rRNA enables whole transcriptome profiling of archival fixed tissue. PLoS One. 7, e42882 (2012).
- Park, D. J., et al. Ebola Virus Epidemiology, Transmission, and Evolution during Seven Months in Sierra Leone. Cell. 161, 1516-1526 (2015).
- Andersen, K. G., et al. Clinical Sequencing Uncovers Origins and Evolution of Lassa Virus. Cell. 162, 738-750 (2015).
- Matranga, C. B., et al. Enhanced methods for unbiased deep sequencing of Lassa and Ebola RNA viruses from clinical and biological samples. Genome Biol. 15, 519 (2014).
- Tang, F., et al. RNA-Seq analysis to capture the transcriptome landscape of a single cell. Nat Protoc. 5, 516-535 (2010).
- Jiang, L., et al. Synthetic spike-in standards for RNA-seq experiments. Genome Res. 21, 1543-1551 (2011).
- . Kapa Biosystems Available from: https://www.kapabiosystems.com/product-applications/products/next-generation-sequencing-2/library-quantification/ (2015)
- . Illumina Technologies Available from: https://support.illumina.com/content/dam/illumina-support/documents/documentation/system_documentation/miseq/preparing-libraries-for-sequencing-on-miseq-15039740-d.pdf (2015)
- Kircher, M., Sawyer, S., Meyer, M. Double indexing overcomes inaccuracies in multiplex sequencing on the Illumina platform. Nucleic Acids Res. 40, 3 (2012).
- Trombley, A. R., et al. Comprehensive panel of real-time TaqMan polymerase chain reaction assays for detection and absolute quantification of filoviruses, arenaviruses, and New World hantaviruses. Am J Trop Med Hyg. 82, 954-960 (2010).
- Hu, Y., et al. Serial high-resolution analysis of blood virome and host cytokines expression profile of a patient with fatal H7N9 infection by massively parallel RNA sequencing. Clin Microbiol Infect. 21, 713 (2015).
- Simon-Loriere, E., et al. Distinct lineages of Ebola virus in Guinea during the 2014 West African epidemic. Nature. 524, 102-104 (2015).
- Folarin, O. A., Happi, A. N., Happi, C. T. Empowering African genomics for infectious disease control. Genome Biol. 15, 515 (2014).
- Blainey, P. C., Quake, S. R. Digital MDA for enumeration of total nucleic acid contamination. Nucleic Acids Res. 39, 19 (2011).
- Malboeuf, C. M., et al. Complete viral RNA genome sequencing of ultra-low copy samples by sequence-independent amplification. Nucleic Acids Res. 41, 13 (2013).
- Gonzalez, I. L., Sylvester, J. E., Smith, T. F., Stambolian, D., Schmickel, R. D. Ribosomal RNA gene sequences and hominoid phylogeny. Mol Biol Evol. 7, 203-219 (1990).
- Adiconis, X., et al. Comparative analysis of RNA sequencing methods for degraded or low-input samples. Nat Methods. 10, 623-629 (2013).

