Comparação de tabaco métodos de remoção de células hospedeiras de proteínas por descascamento plantas intactas ou por tratamento térmico de extratos
Summary
Três métodos de precipitação de calor são apresentados de forma eficaz que remova mais do que 90% de proteínas da célula hospedeira (HCPs) a partir de tabaco extrai antes de qualquer outro passo de purificação. A planta HCPs agregar irreversivelmente a temperaturas superiores a 60 ° C.
Abstract
As plantas que não só fornecem alimentos, rações e matérias-primas para os seres humanos, mas também foram desenvolvidos como um sistema económico para a produção de proteínas biofarmacêuticos, tais como anticorpos, vacinas candidatas e enzimas. Estes devem ser purificada a partir da biomassa da planta, mas etapas de cromatografia são prejudicados pelas concentrações elevadas de proteínas da célula hospedeira (HCPs) em extractos de plantas. No entanto, a maioria dos profissionais de saúde agregar irreversivelmente a temperaturas superiores a 60 ° C facilitam a purificação posterior da proteína alvo. Aqui, são apresentados três métodos para conseguir a precipitação de calor de profissionais de saúde do tabaco em folhas, quer intactos ou extractos. O branqueamento de folhas intactas podem ser facilmente incorporados nos processos existentes, mas pode ter um impacto negativo sobre as etapas de filtração subsequentes. O oposto é verdadeiro para a precipitação de calor de extratos de folhas em um vaso agitado, o que pode melhorar o desempenho das operações a jusante embora com grandes mudanças no design de equipamento de processo, tais comogeometria homogeneizador. Por fim, uma configuração de permutador de calor está bem caracterizada em termos de condições de transferência de calor e fácil à escala, mas a limpeza pode ser difícil e pode haver um impacto negativo sobre a capacidade do filtro. A abordagem de design-de-experiências pode ser utilizada para identificar os parâmetros de processo mais importantes que afectam a remoção de HCP e recuperação do produto. Isto facilita a aplicação de cada método em outras plataformas de expressão e na identificação de o método mais adequado para uma dada estratégia de purificação.
Introduction
Modernos sistemas de saúde dependem cada vez mais proteínas biofarmacêuticas 1. Produzindo estas proteínas em plantas é vantajoso devido à carga patógeno baixo e escalabilidade maior em comparação com os sistemas de expressão convencionais 2-4. No entanto, o processamento a jusante (DSP) de produtos farmacêuticos derivados de plantas pode ser um desafio, porque os procedimentos de extração disruptivas resultar em uma carga de partículas de alta, com turbidez superior a 5.000 unidades nefelométrico de turbidez (NTUs) e proteína da célula hospedeira (HCP) concentrações muitas vezes superior a 95 % [m / m] 5,6.
Processos de clarificação elaborados são necessários para remover as partículas dispersas 7-9, mas o equipamento de cromatografia é menos dispendioso para operar em modo de ligação e-eluem durante a recuperação inicial do produto, se houver um passo anterior para a remoção eficiente dos profissionais de saúde 10,11. Isto pode ser conseguido quer por precipitação da proteína alvo usando flocculformigas 12 ou baixo pH 13,14, bem como fazendo com que os profissionais de saúde para agregar. A agregação selectiva da ribulose-1,5-bifosfato-carboxilase / oxigenase (RuBisCO), a HCP mais abundante nas plantas verdes, tais como o tabaco (Nicotiana tabacum), pode ser promovida através da adição de polietilenoglicol 15, mas isso é caro e incompatível com grande fabricação -scale. O tratamento térmico tem sido demonstrado para desnaturar e precipitar mais de 95% dos profissionais de saúde do tabaco, enquanto vacinas candidatas contra a malária proteína, tais como Vax8 permanecer estável na solução 16-18.
Três diferentes abordagens foram usadas para conseguir a precipitação induzida pelo calor de profissionais de saúde do tabaco: (i) de branqueamento, isto é, a imersão das folhas intactas no estado líquido quente, (ii) uma temperatura controlada agitada recipiente, e (iii) um permutador de calor ( A Figura 1) 16. Para as folhas intactas, o branqueamento conseguida a precipitação rápida e eficiente dos profissionais de saúde e também foi fácilampliar e compatível com processos de fabricação em grande escala existentes que incluem um passo inicial para lavar a biomassa vegetal 19. Em contraste, vasos de temperatura controlada já estão disponíveis em alguns processos e pode ser utilizado para o tratamento térmico de extractos de plantas 20, mas a sua escalabilidade e taxa de transferência de energia são limitados porque a razão de superfície para volume dos tanques é progressivamente reduzida e torna-se inadequada em escala processo. Um permutador de calor é uma alternativa tecnicamente bem definido para aquecida vasos agitados mas requer um fornecimento abundante de meios de aquecimento e arrefecimento, por exemplo, de vapor e de água fria, assim como uma taxa de fluxo volumétrica rigidamente controlado, que é adaptada à geometria do permutador de calor e propriedades de mídia, por exemplo., a capacidade de calor específico. Este artigo mostra como todos os três métodos podem ser usados para a precipitação induzida pelo calor de tabaco, os profissionais de saúde e os profissionais de saúde da planta em geral. A criação e funcionamento de each método em um ambiente de laboratório pode ser usado para avaliar a sua aptidão para processos de grande escala. O grande desafio é identificar modelos de escala para baixo adequados e condições de funcionamento para cada operação que se parecem com os dispositivos e condições utilizadas durante a fabricação em escala processo. Os dados aqui apresentados referem-se a experiências conduzidas com plantas de tabaco transgénicas que expressam a vacina candidata malária Vax8 e proteína fluorescente DsRed 16, mas o método também tem sido aplicada com sucesso a N. benthamiana plantas que expressam transitoriamente outras proteínas biofarmacêuticas 21.
Um projeto-de-experimentos (DOE) aproximar 22 pode facilitar o desenvolvimento de processos, e floculantes 23 também pode ser benéfico, neste contexto, como descrito anteriormente 8. A principal diferença entre o branqueamento, reservatórios aquecidos e permutadores de calor é que o branqueamento é aplicado a folhas intactas no início do processo ao passo que o OTdela são aplicados aos extractos de plantas (Figura 1).
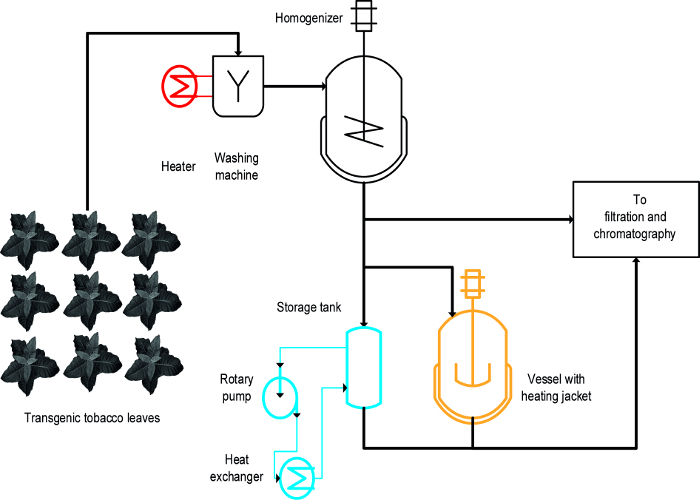
Figura 1:. Esquema de Fluxo do Processo Ilustrando a implementação de três métodos diferentes para Tobacco HCP Calor Precipitation O material vegetal é lavado e homogeneizadas antes de clarificação e purificação. O equipamento para a etapa de branqueamento (vermelho) podem ser facilmente adicionados à maquinaria existente. Em contraste, usando um recipiente com agitação (laranja) e, especialmente, um permutador de calor (azul) requer um ou vários dispositivos e tubos adicionais. Por favor clique aqui para ver uma versão maior desta figura.
Protocol
Representative Results
Discussion
Os três métodos de precipitação acima descritos calor pode remover eficazmente os profissionais de saúde do tabaco antes de qualquer passo de purificação cromatográfica 16,17. Eles complementam outras estratégias que visam aumentar a pureza inicial do produto, por exemplo, gutação 29, 30 ou rhizosecretion centrífuga extracção 31,32, todos os quais são limitados para as proteínas secretadas. No entanto, os métodos baseados em calor só pode ser utiliza…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
We would like to acknowledge Dr. Thomas Rademacher, Alexander Boes and Veronique Beiß for providing the transgenic tobacco seeds, and Ibrahim Al Amedi for cultivating the tobacco plants. The authors wish to thank Dr. Richard M. Twyman for editorial assistance as well as Güven Edgü for providing the MSP1-19 reference. This work was funded in part by the European Research Council Advanced Grant ”Future-Pharma”, proposal number 269110, the Fraunhofer-Zukunftsstiftung (Fraunhofer Future Foundation) and Fraunhofer-Gesellschaft Internal Programs under Grant No. Attract 125-600164.
Materials
| 2100P Portable Turbidimeter | Hach | 4650000 | Turbidimeter |
| Amine Coupling Kit | GE Healthcare | BR100050 | SPR chip coupling kit |
| Autoclaving basket | Nalgene | 6917-0230 | Basket for leaf blanching |
| Biacore T200 | GE Healthcare | 28-9750-01 | SPR device |
| Bio Cell Analyser BCA 003 R&D with 3D ORM | Sequip | n.a. | Particle size analyzer |
| Blender | Waring | 800EG | Blender |
| BP-410 | Furh | 2632410001 | Bag filter |
| Centrifuge 5415D | Eppendorf | 5424 000.410 | Centrifuge |
| Centrifuge tube 15 mL | Labomedic | 2017106 | Reaction tube |
| Centrifuge tube 50 mL self-standing | Labomedic | 1110504 | Reaction tube |
| CM5 chip | GE Healthcare | BR100012 | Chip for SPR measurements |
| Cuvette 10x10x45 | Sarsted | 67.754 | Cuvette for Zetasizer Nano ZS |
| Design-Expert(R) 8 | Stat-Ease, Inc. | n.a. | DoE software |
| Disodium phosphate | Carl Roth GmbH | 4984.3 | Media component |
| Ferty 2 Mega | Kammlott | 5.220072 | Fertilizer |
| Forma -86C ULT freezer | ThermoFisher | 88400 | Freezer |
| Greenhouse | n.a. | n.a. | For plant cultivation |
| Grodan Rockwool Cubes 10x10cm | Grodan | 102446 | Rockwool block |
| Twentey-loop heat exchanger (4.8 m length) | n.a. (custom design) | n.a. | Heat exchanger |
| HEPES | Carl Roth GmbH | 9105.3 | Media component |
| K200P 60D | Pall | 5302303 | Depth filter layer |
| KS50P 60D | Pall | B12486 | Depth filter layer |
| Lauda E300 | Lauda Dr Wobser GmbH | Z90010 | Water bath thermostat |
| L/S 24 | Masterflex | SN-06508-24 | Tubing |
| mAb 5.2 | American Type Culture Collection | HB-9148 | Vax8 specific antibody |
| Masterflex L/S | Masterflex | HV-77921-75 | Peristaltic pump |
| Miracloth | Labomedic | 475855-1R | Filter cloth |
| MultiLine Multi 3410 IDS | WTW | WTW_2020 | pH meter / conductivity meter |
| Osram cool white 36 W | Osram | 4930440 | Light source |
| Phytotron | Ilka Zell | n.a. | For plant cultivation |
| Sodium disulfit | Carl Roth GmbH | 8554.1 | Media component |
| Sodium chloride | Carl Roth GmbH | P029.2 | Media component |
| Stainless-steel vessel; 0.7-kg 2.0-L; height 180 mm; diameter 120 mm | n.a. (custom design) | n.a. | Container for heat precipitation |
| Synergy HT | BioTek | SIAFRT | Fluorescence and spectrometric plate reader |
| VelaPad 60 | Pall | VP60G03KNH4 | Filter housing |
| Zetasizer Nano ZS | Malvern | ZEN3600 | DLS particle size distribution measurement |
| Zetasizer Software v7.11 | Malvern | n.a. | Software to operate the Zetasizer Nano ZS device |
Riferimenti
- PhRMA. . 2013 Report: Medicines in Development – Biologics. , (2013).
- Buyel, J. F. Process development strategies in plant molecular farming. Curr. Pharm. Biotechnol. 16, 966-982 (2015).
- Stoger, E., Fischer, R., Moloney, M., Ma, J. K. C. Plant molecular pharming for the treatment of chronic and infectious diseases. Annu. Rev. Plant Biol. 65, 743-768 (2014).
- Melnik, S., Stoger, E. Green factories for biopharmaceuticals. Curr. Med. Chem. 20, 1038-1046 (2013).
- Buyel, J. F., Twyman, R. M., Fischer, R. Extraction and downstream processing of plant-derived recombinant proteins. Biotechnol. Adv. 33, 902-913 (2015).
- Wilken, L. R., Nikolov, Z. L. Recovery and purification of plant-made recombinant proteins. Biotechnol. Adv. 30, 419-433 (2012).
- Buyel, J. F., Fischer, R. Scale-down models to optimize a filter train for the downstream purification of recombinant pharmaceutical proteins produced in tobacco leaves. Biotechnol. J. 9, 415-425 (2014).
- Buyel, J. F., Fischer, R. Flocculation increases the efficacy of depth filtration during the downstream processing of recombinant pharmaceutical proteins produced in tobacco. Plant Biotechnol. J. 12, 240-252 (2014).
- Buyel, J. F., Opdensteinen, P., Fischer, R. Cellulose-based filter aids increase the capacity of depth filters during the downstream processing of plant-derived biopharmaceutical proteins. Biotechnol. J. 10, 584-591 (2014).
- Buyel, J. F., Fischer, R. Generic chromatography-based purification strategies accelerate the development of downstream processes for biopharmaceutical proteins produced in plants. Biotechnol. J. 9, 566-577 (2014).
- Buyel, J. F., Woo, J. A., Cramer, S. M., Fischer, R. The use of quantitative structure-activity relationship models to develop optimized processes for the removal of tobacco host cell proteins during biopharmaceutical production. J. Chromatogr. A. 1322, 18-28 (2013).
- Holler, C., Vaughan, D., Zhang, C. M. Polyethyleneimine precipitation versus anion exchange chromatography in fractionating recombinant beta-glucuronidase from transgenic tobacco extract. J. Chromatogr. A. 1142, 98-105 (2007).
- Buyel, J. F., Fischer, R. Downstream processing of biopharmaceutical proteins produced in plants: the pros and cons of flocculants. Bioengineered. 5, 138-142 (2014).
- Hassan, S., van Dolleweerd, C. J., Ioakeimidis, F., Keshavarz-Moore, E., Ma, J. K. Considerations for extraction of monoclonal antibodies targeted to different subcellular compartments in transgenic tobacco plants. Plant Biotechnol. J. 6, 733-748 (2008).
- Arfi, Z. A., Drossard, J., Hellwig, S., Fischer, R., Buyel, J. F. Polyclonal antibodies can effectively detect tobacco host cell proteins after RuBisCO depletion and endotoxin removal. Biotechnol. J. , (2015).
- Buyel, J. F., Gruchow, H. M., Boes, A., Fischer, R. Rational design of a host cell protein heat precipitation step simplifies the subsequent purification of recombinant proteins from tobacco. Biochem. Eng. J. 88, 162-170 (2014).
- Buyel, J. F., Fischer, R. A juice extractor can simplify the downstream processing of plant-derived biopharmaceutical proteins compared to blade-based homogenizers. Process Biochem. 50, 859-866 (2014).
- Beiss, V., et al. Heat-precipitation allows the efficient purification of a functional plant-derived malaria transmission-blocking vaccine candidate fusion protein. Biotechnol. Bioeng. 112, 1297-1305 (2015).
- Ma, J. K., et al. Regulatory approval and a first-in-human phase I clinical trial of a monoclonal antibody produced in transgenic tobacco plants. Plant Biotechnol. J. 13, 1106-1120 (2015).
- Mahajan, P. V., Caleb, O. J., Singh, Z., Watkins, C. B., Geyer, M. Postharvest treatments of fresh produce. Philos T R Soc A. 372, (2014).
- Menzel, S., et al. Optimized blanching reduces the host cell protein content and substantially enhances the recovery and stability of two plant derived malaria vaccine candidates. Front. Plant Sci. , (2015).
- Buyel, J. F., Fischer, R. Characterization of complex systems using the design of experiments approach: transient protein expression in tobacco as a case study. J. Vis. Exp. , e51216 (2014).
- Buyel, J. F. Procedure to evaluate the efficiency of flocculants for the removal of dispersed particles from plant extracts. J. Vis. Exp. , e53940 (2016).
- Simonian, M. H., Smith, J. A. Spectrophotometric and colorimetric determination of protein concentration. Curr. Protoc. Mol. Biol. 76, (2006).
- Buyel, J. F., Kaever, T., Buyel, J. J., Fischer, R. Predictive models for the accumulation of a fluorescent marker protein in tobacco leaves according to the promoter/5’UTR combination. Biotechnol. Bioeng. 110, 471-482 (2013).
- Piliarik, M., Vaisocherova, H., Homola, J. Surface plasmon resonance biosensing. Methods Mol. Biol. 503, 65-88 (2009).
- Kim, T. D., Ryu, H. J., Cho, H. I., Yang, C. H., Kim, J. Thermal behavior of proteins: Heat-resistant proteins and their heat-induced secondary structural changes. Biochemistry-Us. 39, 14839-14846 (2000).
- Kwon, S., Jung, Y., Lim, D. Proteomic analysis of heat-stable proteins in Escherichia coli. Bmb Rep. 41, 108-111 (2008).
- Komarnytsky, S., Borisjuk, N. V., Borisjuk, L. G., Alam, M. Z., Raskin, I. Production of recombinant proteins in tobacco guttation fluid. Plant Physiol. 124, 927-933 (2000).
- Drake, P. M. W., et al. Development of rhizosecretion as a production system for recombinant proteins from hydroponic cultivated tobacco. FASEB J. 23, 3581-3589 (2009).
- Turpen, T. H. Tobacco mosaic virus and the virescence of biotechnology. Philos. Trans. R. Soc. Lond., Ser. B: Biol. Sci. 354, 665-673 (1999).
- Kingsbury, N. J., McDonald, K. A. Quantitative Evaluation of E1 Endoglucanase Recovery from Tobacco Leaves Using the Vacuum Infiltration-Centrifugation Method. Biomed. Res. Int. , (2014).
- Buyel, J. F. Numeric simulation can be used to predict heat transfer during the blanching of leaves and intact. Biochem. Eng. J. , (2015).
- Mandal, M. K., Fischer, R., Schillberg, S., Schiermeyer, A. Inhibition of protease activity by antisense RNA improves recombinant protein production in Nicotiana tabacum cv. Bright Yellow 2 (BY-2) suspension cells. Biotechnol. J. 9, 1065-1073 (2014).
- Welty, J. R., Wicks, C. E., Wilson, R. E. . Fundamentals of momentum, heat, and mass transfer. , (1976).
- Lowe, D., et al. Aggregation, stability, and formulation of human antibody therapeutics. Advances in protein chemistry and structural biology. 84, 41-61 (2011).
- Gong, R., et al. Engineered human antibody constant domains with increased stability. J. Biol. Chem. 284, 14203-14210 (2009).
- Rouet, R., Lowe, D., Christ, D. Stability engineering of the human antibody repertoire. FEBS Lett. 588, 269-277 (2014).
- Stabel, J. R., Lambertz, A. Efficacy of pasteurization conditions for the inactivation of Mycobacterium avium subsp paratuberculosis in milk. J. Food Prot. 67, 2719-2726 (2004).
- Wichers, H., Mills, C., Wichers, H., Hoffmann-Sommergruber, K. Ch. 12. Managing Allergens in Food. , 336 (2006).
- Davis, P. J., Williams, S. C. Protein modification by thermal processing. Allergy. 53, 102-105 (1998).
- Dubois, M. F., Hovanessian, A. G., Bensaude, O. Heat-shock-induced denaturation of proteins. Characterization of the insolubilization of the interferon-induced p68 kinase. J. Biol. Chem. 266, 9707-9711 (1991).

