Sammenligning av Tobakks Host Cell Protein fjerning Metoder ved Blanche Intakte Planter eller ved varmebehandling av ekstrakter
Summary
Tre varme utfellingsmetoder er presentert som effektivt fjerner mer enn 90% av vertscelleproteiner (HCPs) fra tobakksekstrakter før en hvilken som helst annen rensetrinn. Anlegget HCPs irreversibelt å aggregere ved temperaturer over 60 ° C.
Abstract
Planter gir ikke bare mat, fôr og råvarer for mennesker, men har også blitt utviklet som et økonomisk produksjonssystem for biofarmasøytisk proteiner, slik som antistoffer, vaksinekandidater og enzymer. Disse må renses fra plantebiomasse men kromatografiske trinn blir hindret av de høye konsentrasjonene av vertscelleproteiner (HCPs) i planteekstrakter. Men de fleste HCPs irreversibelt å aggregere ved temperaturer over 60 ° C som letter etterfølgende rensing av målproteinet. Her er tre metoder presenteres for å oppnå varme utfelling av tobakk Helsepersonell i enten intakte blader eller ekstrakter. Blanche av intakte bladene kan enkelt bli innlemmet i eksisterende prosesser, men kan ha en negativ innvirkning på etterfølgende filtreringstrinn. Det motsatte er tilfelle for varme utfelling av blad ekstrakter i en rørt fartøy, som kan forbedre ytelsen til nedstrømsvirksomheten riktignok med store endringer i prosessutstyr design, for eksempelhomogenisator geometri. Til slutt blir en varmeveksler oppsett godt karakterisert med hensyn til varmeoverføringsbetingelser og lett å skala, men rengjøring kan være vanskelig og det kan være en negativ innvirkning på filterkapasitet. Utformingen-of-eksperimenter tilnærming kan brukes til å identifisere de mest relevante prosessparametre som påvirker HCP fjerning og produktgjenvinning. Dette letter anvendelsen av hver metode i andre uttrykk plattformer og identifisering av den mest egnede metode for et gitt rensestrategi.
Introduction
Moderne helsevesen stadig avhenge biofarmasøytisk proteiner 1. Fremstilling av disse proteiner i planter er fordelaktig på grunn av den lave patogen byrde og større skalerbarhet forhold til konvensjonelle ekspresjonssystemer 2-4. Imidlertid kan nedstrømsprosessering (DSP) av plante-avledet legemidler være utfordrende fordi forstyrrende ekstraksjonsmetoder resultere i en høy partikkel belastning, med turbidities stiger 5000 nefelometriske turbiditetsenheter (NTUs), og vertscelleprotein (HCP) konsentrasjoner ofte overstiger 95 % [m / m] 5,6.
Forseggjort avklarings prosedyrer er nødvendig for å fjerne dispergerte partikler 7-9, men kromatografi utstyr er mindre kostbart å operere i binde-og-elute modus under innledende produktgjenvinningen hvis det er et tidligere trinn for effektiv fjerning av HCPs 10,11. Dette kan oppnås enten ved utfelling av målproteinet ved hjelp flocculmaur 12 eller lav pH 13,14, samt ved forårsaker Helsepersonell å aggregere. Den selektive aggregering av ribulose-1,5-bisfosfat-karboksylase / oksygenase (RUBISCO), det mest tallrike HCP i grønne planter som tobakk (Nicotiana tabacum) kan fremmes ved tilsetning av polyetylenglykol 15, men dette er kostbart og uforenlig med stor -skala produksjon. Varmebehandling har vist seg å denaturere og presipitere mer enn 95% av tobakks HCPs, mens protein malaria vaksinekandidater som Vax8 forbli stabil i oppløsning 16-18.
Tre forskjellige metoder ble brukt for å oppnå den varmeinduserte utfelling av tobakks HCPs: (i) blanchering, dvs. nedsenking av intakte blader i varm væske, (ii) en temperaturkontrollert omrørt beholder, og (iii) en varmeveksler ( Figur 1) 16. For intakte blader, forvelling oppnås rask og effektiv utfelling av Helsepersonell og var også lettå skalere opp og kompatibel med eksisterende storskala produksjonsprosesser som inkluderer et første skritt for å vaske anlegget biomasse 19. I motsetning til dette temperaturstyrt fartøy er allerede tilgjengelig i noen prosesser og kan anvendes for varmebehandling av plante-ekstrakter 20, men deres skalerbarhet og energioverføring hastighet er begrenset, fordi den overflate-til-volum-forholdet av tankene er gradvis redusert og blir uegnet i prosessen skala. En varmeveksler er en teknisk veldefinert alternativ til å varmes opp omrørt fartøy, men krever en rikelig tilførsel av varme- og kjølemedier, for eksempel damp og kaldt vann, samt en kontrollert volumetrisk strømningshastighet som er tilpasset til varmeveksleren geometri og media egenskaper, f.eks., den spesifikke varmekapasitet. Denne artikkelen viser hvordan alle tre fremgangsmåter kan anvendes for varmeinduserte utfelling av tobakk HCPs, og plante HCPs generelt. Etablering og drift av EACh fremgangsmåte i et laboratorium kan brukes til å vurdere om de er egnet for større skala prosesser. Den store utfordringen er å identifisere tilstrekkelig skala-down modeller og driftsforhold for hver operasjon som ligner enhetene og betingelsene som brukes under prosessen-skala produksjon. Dataene presentert her viser til eksperimenter utført med transgene tobakksplanter som uttrykker det malaria vaksine kandidat Vax8 og fluorescerende protein DsRed 16, men fremgangsmåten er også blitt brukt til N. benthamiana planter forbigående uttrykker andre biofarmasøytisk proteiner 21.
En design-of-eksperimenter (DoE) nærmer 22 kan forenkle prosessutvikling, og flokulanter 23 kan også være nyttig i denne sammenheng som tidligere beskrevet åtte. Hovedforskjellen mellom blanche, oppvarmede beholdere og varmevekslere er at blanche påtrykkes intakte bladene tidlig i prosessen, mens othennes tilføres planteekstrakter (figur 1).
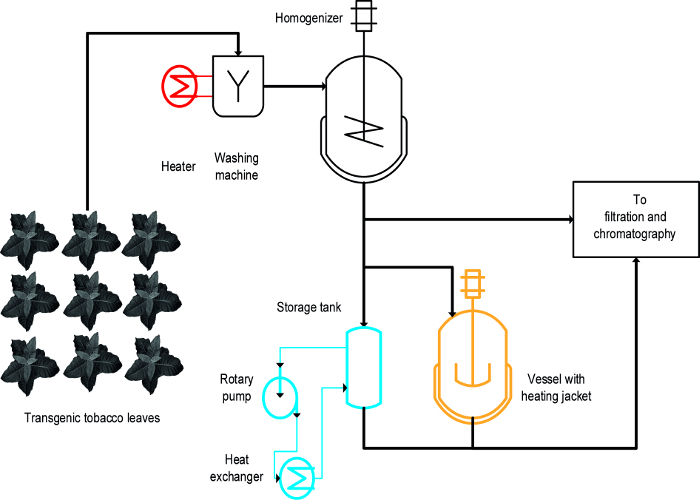
Figur 1:. Process Flow skjema som illustrerer gjennomføring av tre ulike metoder for Tobacco HCP Heat Nedbør Plantematerialet blir vasket og homogenisert før avklaring og rensing. Utstyr for forvellingstrinn (rød) lett kan legges til eksisterende maskineri. I motsetning til ved hjelp av en rørt fartøy (oransje) og spesielt en varmeveksler (blå) krever en eller flere andre enheter og rør. Klikk her for å se en større versjon av dette tallet.
Protocol
Representative Results
Discussion
De tre metoder for varme nedbør beskrevet ovenfor effektivt kan fjerne tobakk Helsepersonell før noen kromatografisk rensetrinn 16,17. De utfyller andre strategier som tar sikte på å øke første produktet renhet, f.eks guttation 29, rhizosecretion 30 eller sentrifugal utvinning 31,32, som alle er begrenset til utskilte proteiner. Imidlertid kan de varmebaserte metoder bare brukes på en meningsfull måte dersom målet proteinet som skal renses kan tåle den minst…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
We would like to acknowledge Dr. Thomas Rademacher, Alexander Boes and Veronique Beiß for providing the transgenic tobacco seeds, and Ibrahim Al Amedi for cultivating the tobacco plants. The authors wish to thank Dr. Richard M. Twyman for editorial assistance as well as Güven Edgü for providing the MSP1-19 reference. This work was funded in part by the European Research Council Advanced Grant ”Future-Pharma”, proposal number 269110, the Fraunhofer-Zukunftsstiftung (Fraunhofer Future Foundation) and Fraunhofer-Gesellschaft Internal Programs under Grant No. Attract 125-600164.
Materials
| 2100P Portable Turbidimeter | Hach | 4650000 | Turbidimeter |
| Amine Coupling Kit | GE Healthcare | BR100050 | SPR chip coupling kit |
| Autoclaving basket | Nalgene | 6917-0230 | Basket for leaf blanching |
| Biacore T200 | GE Healthcare | 28-9750-01 | SPR device |
| Bio Cell Analyser BCA 003 R&D with 3D ORM | Sequip | n.a. | Particle size analyzer |
| Blender | Waring | 800EG | Blender |
| BP-410 | Furh | 2632410001 | Bag filter |
| Centrifuge 5415D | Eppendorf | 5424 000.410 | Centrifuge |
| Centrifuge tube 15 mL | Labomedic | 2017106 | Reaction tube |
| Centrifuge tube 50 mL self-standing | Labomedic | 1110504 | Reaction tube |
| CM5 chip | GE Healthcare | BR100012 | Chip for SPR measurements |
| Cuvette 10x10x45 | Sarsted | 67.754 | Cuvette for Zetasizer Nano ZS |
| Design-Expert(R) 8 | Stat-Ease, Inc. | n.a. | DoE software |
| Disodium phosphate | Carl Roth GmbH | 4984.3 | Media component |
| Ferty 2 Mega | Kammlott | 5.220072 | Fertilizer |
| Forma -86C ULT freezer | ThermoFisher | 88400 | Freezer |
| Greenhouse | n.a. | n.a. | For plant cultivation |
| Grodan Rockwool Cubes 10x10cm | Grodan | 102446 | Rockwool block |
| Twentey-loop heat exchanger (4.8 m length) | n.a. (custom design) | n.a. | Heat exchanger |
| HEPES | Carl Roth GmbH | 9105.3 | Media component |
| K200P 60D | Pall | 5302303 | Depth filter layer |
| KS50P 60D | Pall | B12486 | Depth filter layer |
| Lauda E300 | Lauda Dr Wobser GmbH | Z90010 | Water bath thermostat |
| L/S 24 | Masterflex | SN-06508-24 | Tubing |
| mAb 5.2 | American Type Culture Collection | HB-9148 | Vax8 specific antibody |
| Masterflex L/S | Masterflex | HV-77921-75 | Peristaltic pump |
| Miracloth | Labomedic | 475855-1R | Filter cloth |
| MultiLine Multi 3410 IDS | WTW | WTW_2020 | pH meter / conductivity meter |
| Osram cool white 36 W | Osram | 4930440 | Light source |
| Phytotron | Ilka Zell | n.a. | For plant cultivation |
| Sodium disulfit | Carl Roth GmbH | 8554.1 | Media component |
| Sodium chloride | Carl Roth GmbH | P029.2 | Media component |
| Stainless-steel vessel; 0.7-kg 2.0-L; height 180 mm; diameter 120 mm | n.a. (custom design) | n.a. | Container for heat precipitation |
| Synergy HT | BioTek | SIAFRT | Fluorescence and spectrometric plate reader |
| VelaPad 60 | Pall | VP60G03KNH4 | Filter housing |
| Zetasizer Nano ZS | Malvern | ZEN3600 | DLS particle size distribution measurement |
| Zetasizer Software v7.11 | Malvern | n.a. | Software to operate the Zetasizer Nano ZS device |
Riferimenti
- PhRMA. . 2013 Report: Medicines in Development – Biologics. , (2013).
- Buyel, J. F. Process development strategies in plant molecular farming. Curr. Pharm. Biotechnol. 16, 966-982 (2015).
- Stoger, E., Fischer, R., Moloney, M., Ma, J. K. C. Plant molecular pharming for the treatment of chronic and infectious diseases. Annu. Rev. Plant Biol. 65, 743-768 (2014).
- Melnik, S., Stoger, E. Green factories for biopharmaceuticals. Curr. Med. Chem. 20, 1038-1046 (2013).
- Buyel, J. F., Twyman, R. M., Fischer, R. Extraction and downstream processing of plant-derived recombinant proteins. Biotechnol. Adv. 33, 902-913 (2015).
- Wilken, L. R., Nikolov, Z. L. Recovery and purification of plant-made recombinant proteins. Biotechnol. Adv. 30, 419-433 (2012).
- Buyel, J. F., Fischer, R. Scale-down models to optimize a filter train for the downstream purification of recombinant pharmaceutical proteins produced in tobacco leaves. Biotechnol. J. 9, 415-425 (2014).
- Buyel, J. F., Fischer, R. Flocculation increases the efficacy of depth filtration during the downstream processing of recombinant pharmaceutical proteins produced in tobacco. Plant Biotechnol. J. 12, 240-252 (2014).
- Buyel, J. F., Opdensteinen, P., Fischer, R. Cellulose-based filter aids increase the capacity of depth filters during the downstream processing of plant-derived biopharmaceutical proteins. Biotechnol. J. 10, 584-591 (2014).
- Buyel, J. F., Fischer, R. Generic chromatography-based purification strategies accelerate the development of downstream processes for biopharmaceutical proteins produced in plants. Biotechnol. J. 9, 566-577 (2014).
- Buyel, J. F., Woo, J. A., Cramer, S. M., Fischer, R. The use of quantitative structure-activity relationship models to develop optimized processes for the removal of tobacco host cell proteins during biopharmaceutical production. J. Chromatogr. A. 1322, 18-28 (2013).
- Holler, C., Vaughan, D., Zhang, C. M. Polyethyleneimine precipitation versus anion exchange chromatography in fractionating recombinant beta-glucuronidase from transgenic tobacco extract. J. Chromatogr. A. 1142, 98-105 (2007).
- Buyel, J. F., Fischer, R. Downstream processing of biopharmaceutical proteins produced in plants: the pros and cons of flocculants. Bioengineered. 5, 138-142 (2014).
- Hassan, S., van Dolleweerd, C. J., Ioakeimidis, F., Keshavarz-Moore, E., Ma, J. K. Considerations for extraction of monoclonal antibodies targeted to different subcellular compartments in transgenic tobacco plants. Plant Biotechnol. J. 6, 733-748 (2008).
- Arfi, Z. A., Drossard, J., Hellwig, S., Fischer, R., Buyel, J. F. Polyclonal antibodies can effectively detect tobacco host cell proteins after RuBisCO depletion and endotoxin removal. Biotechnol. J. , (2015).
- Buyel, J. F., Gruchow, H. M., Boes, A., Fischer, R. Rational design of a host cell protein heat precipitation step simplifies the subsequent purification of recombinant proteins from tobacco. Biochem. Eng. J. 88, 162-170 (2014).
- Buyel, J. F., Fischer, R. A juice extractor can simplify the downstream processing of plant-derived biopharmaceutical proteins compared to blade-based homogenizers. Process Biochem. 50, 859-866 (2014).
- Beiss, V., et al. Heat-precipitation allows the efficient purification of a functional plant-derived malaria transmission-blocking vaccine candidate fusion protein. Biotechnol. Bioeng. 112, 1297-1305 (2015).
- Ma, J. K., et al. Regulatory approval and a first-in-human phase I clinical trial of a monoclonal antibody produced in transgenic tobacco plants. Plant Biotechnol. J. 13, 1106-1120 (2015).
- Mahajan, P. V., Caleb, O. J., Singh, Z., Watkins, C. B., Geyer, M. Postharvest treatments of fresh produce. Philos T R Soc A. 372, (2014).
- Menzel, S., et al. Optimized blanching reduces the host cell protein content and substantially enhances the recovery and stability of two plant derived malaria vaccine candidates. Front. Plant Sci. , (2015).
- Buyel, J. F., Fischer, R. Characterization of complex systems using the design of experiments approach: transient protein expression in tobacco as a case study. J. Vis. Exp. , e51216 (2014).
- Buyel, J. F. Procedure to evaluate the efficiency of flocculants for the removal of dispersed particles from plant extracts. J. Vis. Exp. , e53940 (2016).
- Simonian, M. H., Smith, J. A. Spectrophotometric and colorimetric determination of protein concentration. Curr. Protoc. Mol. Biol. 76, (2006).
- Buyel, J. F., Kaever, T., Buyel, J. J., Fischer, R. Predictive models for the accumulation of a fluorescent marker protein in tobacco leaves according to the promoter/5’UTR combination. Biotechnol. Bioeng. 110, 471-482 (2013).
- Piliarik, M., Vaisocherova, H., Homola, J. Surface plasmon resonance biosensing. Methods Mol. Biol. 503, 65-88 (2009).
- Kim, T. D., Ryu, H. J., Cho, H. I., Yang, C. H., Kim, J. Thermal behavior of proteins: Heat-resistant proteins and their heat-induced secondary structural changes. Biochemistry-Us. 39, 14839-14846 (2000).
- Kwon, S., Jung, Y., Lim, D. Proteomic analysis of heat-stable proteins in Escherichia coli. Bmb Rep. 41, 108-111 (2008).
- Komarnytsky, S., Borisjuk, N. V., Borisjuk, L. G., Alam, M. Z., Raskin, I. Production of recombinant proteins in tobacco guttation fluid. Plant Physiol. 124, 927-933 (2000).
- Drake, P. M. W., et al. Development of rhizosecretion as a production system for recombinant proteins from hydroponic cultivated tobacco. FASEB J. 23, 3581-3589 (2009).
- Turpen, T. H. Tobacco mosaic virus and the virescence of biotechnology. Philos. Trans. R. Soc. Lond., Ser. B: Biol. Sci. 354, 665-673 (1999).
- Kingsbury, N. J., McDonald, K. A. Quantitative Evaluation of E1 Endoglucanase Recovery from Tobacco Leaves Using the Vacuum Infiltration-Centrifugation Method. Biomed. Res. Int. , (2014).
- Buyel, J. F. Numeric simulation can be used to predict heat transfer during the blanching of leaves and intact. Biochem. Eng. J. , (2015).
- Mandal, M. K., Fischer, R., Schillberg, S., Schiermeyer, A. Inhibition of protease activity by antisense RNA improves recombinant protein production in Nicotiana tabacum cv. Bright Yellow 2 (BY-2) suspension cells. Biotechnol. J. 9, 1065-1073 (2014).
- Welty, J. R., Wicks, C. E., Wilson, R. E. . Fundamentals of momentum, heat, and mass transfer. , (1976).
- Lowe, D., et al. Aggregation, stability, and formulation of human antibody therapeutics. Advances in protein chemistry and structural biology. 84, 41-61 (2011).
- Gong, R., et al. Engineered human antibody constant domains with increased stability. J. Biol. Chem. 284, 14203-14210 (2009).
- Rouet, R., Lowe, D., Christ, D. Stability engineering of the human antibody repertoire. FEBS Lett. 588, 269-277 (2014).
- Stabel, J. R., Lambertz, A. Efficacy of pasteurization conditions for the inactivation of Mycobacterium avium subsp paratuberculosis in milk. J. Food Prot. 67, 2719-2726 (2004).
- Wichers, H., Mills, C., Wichers, H., Hoffmann-Sommergruber, K. Ch. 12. Managing Allergens in Food. , 336 (2006).
- Davis, P. J., Williams, S. C. Protein modification by thermal processing. Allergy. 53, 102-105 (1998).
- Dubois, M. F., Hovanessian, A. G., Bensaude, O. Heat-shock-induced denaturation of proteins. Characterization of the insolubilization of the interferon-induced p68 kinase. J. Biol. Chem. 266, 9707-9711 (1991).

