La préparation et les propriétés des Thermo-réversiblement réticulé Rubber Chemistry Via Diels-Alder
Summary
A simple two-step approach involving rubber modification and cross-linking yields fully reworkable, elastic rubber products.
Abstract
Procédé pour l'utilisation de la chimie de Diels-Alder thermo-réversible comme outil de réticulation pour le caoutchouc est démontrée. Dans ce travail, un caoutchouc éthylène-propylène commercial, greffé avec de l'anhydride maléique, est thermo-réticulation réversible en deux étapes. Les groupements anhydride en attente sont d'abord modifiées par furfurylamine pour greffer des groupes furanne au squelette du caoutchouc. Ces groupes furanne pendants sont ensuite réticulés avec un bis-maléimide par l'intermédiaire d'une réaction de couplage de Diels-Alder. Les deux réactions peuvent être réalisées dans un large éventail de conditions expérimentales et peuvent être facilement appliquées sur une grande échelle. Les propriétés matérielles des Diels-Alder caoutchoucs réticulés résultants sont similaires à un copolymère éthylène / propylène / caoutchouc de diène (EPDM) référence de peroxyde durci. Les liaisons transversales se brisent à des températures élevées (> 150 ° C) par la réaction de rétro-Diels-Alder et peuvent être réformées par recuit thermique à des températures plus basses (50-70 ° C). Réversibilité du système a été prouvé with spectroscopie infrarouge, des essais de solubilité et les propriétés mécaniques. La recyclabilité du matériau a également été montré d'une manière pratique, à savoir, en coupant un échantillon réticulé en petites parties et la compression leur moulage dans de nouveaux échantillons présentant des propriétés mécaniques comparables, ce qui est impossible pour les caoutchoucs classiquement réticulés.
Introduction
Soufre vulcanisation et le peroxyde durcissement sont actuellement les principales techniques de réticulation industrielles dans l'industrie du caoutchouc, ce qui donne des liaisons croisées chimiques irréversibles qui empêchent le retraitement à l' état fondu. 1, 2 A ' du berceau au berceau' approche de recycler les caoutchoucs réticulés nécessite un matériau comporte des caoutchoucs semblables à réticulés en permanence à des conditions de service, tout en ayant la capacité de traitement et de recyclage complet d'une matière thermoplastique à haute température. Une approche pour atteindre une telle recyclabilité utilise les réseaux caoutchouteux avec des liaisons transversales réversibles qui répondent à un stimulus externe, comme la température (plus réalisables du point de vue des futures applications industrielles). 3-5 La formation de ces liaisons transversales relativement faible services des températures est nécessaire pour une bonne tenue mécanique du caoutchouc, tandis que leur clivage à des températures élevées (similaires à la température de traitement de la non-réticulé composé d'origine) permet de recyclage du matériau.
Certains matériaux spécifiques peuvent être réversiblement réticulé en utilisant des réseaux dits covalentes dynamiques par des réactions de polycondensation 6 ou par ce qu'on appelle la topologie du réseau réversible gel via des réactions de trans – estérification. 9/7 L'inconvénient de ces méthodes réside dans la nécessité de concevoir et la synthèse de nouveaux polymères plutôt que de modifier, de caoutchoucs commerciaux existants qui ont déjà les propriétés souhaitées. Les techniques de thermo-réversible réticuler les caoutchoucs comprennent la liaison hydrogène, des interactions ioniques et de liaison covalente telle que par réarrangements disulfure thermo-activé. 10-13 Récemment, thermoréversible de réticulation par l' intermédiaire de Diels-Alder (DA) de la chimie a été développée. 14 chimie -21 DA peut être appliquée à une large gamme de polymères et représente un choix populaire, d' autant plus que la réaction DA permet une cinétique relativement rapide et des conditions réactionnelles douces. 17, 22-24 ThLes températures de couplage faible eir et de haute découplage font furane et d' excellents candidats maléimide pour un polymère réversible de réticulation. 18-20, 25-28
Le but de ce travail est de fournir un procédé pour l'utilisation du DA de la chimie comme un outil de réticulation thermo-réversible pour un produit en caoutchouc industriel (figure 1). 5 En premier lieu , la réactivité des élastomères d'hydrocarbures saturés, tels que l' éthylène / des caoutchoucs de propylène (EPM) doit être augmentée. Un exemple pertinent commercialement qui facilite tel est le greffage radicalaire peroxyde initiée par de l' anhydride maléique (MA) 29-34 En second lieu , un groupe furanne peut être greffé sur un caoutchouc EPM à maléate en insérant furfurylamine (FFA) dans l'anhydride pendant. pour former un imide. 35, 36 Enfin, les groupements furane qui sont ainsi fixés au squelette en caoutchouc peut alors participer à la chimie DA thermo-réversible comme diène riche en électrons. 25 37 l'électron-poou le bis-maléimide (BM) est un diénophile convenant pour cette réaction de reticulation. 19, 26, 38
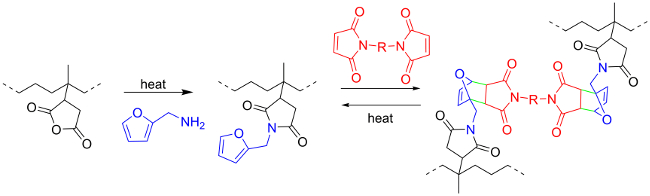
Figure 1. Schéma réactionnel. Greffage Furan et bismaléimide réticulation de EPM-g-MA caoutchouc (réimprimé avec la permission de 5). S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Protocol
Representative Results
Discussion
Un caoutchouc EPM-g-MA commerciale était thermo-réversible réticulé dans une approche simple en deux étapes. Le caoutchouc maléaté a été modifié avec la FFA pour greffer des groupes furanne sur le squelette du caoutchouc. Les furannes en attente résultant montrent la réactivité comme diènes de Diels-Alder. Un BM aliphatique est utilisé comme agent de reticulation, ce qui entraîne un pont thermo-réversible entre deux groupements furane. Les deux réactions ont réussi avec de bonnes conversions (> 80%…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
This research forms part of the research program of the Dutch Polymer Institute, project #749.
Materials
| ENB-EPDM | LANXESS Elastomers B.V. | Keltan 8550C | |
| EPM-g-MA | LANXESS Elastomers B.V. | Keltan DE5005 | Vacuum oven for one hour at 175 °C |
| furfurylamine | Sigma-Aldrich | F20009 | Freshly distillated before use |
| di-dodecylamine | Sigma-Aldrich | 36784 | |
| maleic anhydride | Sigma-Aldrich | M0357 | |
| octadecyl-1-(3,5-di-tert.-butyl-4-hydroxyphenyl)propionate | Sigma-Aldrich | 367079 | |
| bis(tert.-butylperoxy-iso-propyl) benzene | Sigma-Aldrich | 531685 | |
| tetrahydrofuran | Sigma-Aldrich | 401757 | |
| decalin | Sigma-Aldrich | 294772 | |
| acetone | Sigma-Aldrich | 320110 |
Riferimenti
- Myhre, M., MacKillop, D. A. Rubber recycling. Rubber Chem Technol. 75 (3), 429-474 (2002).
- Baranwal, K. C., Stephens, H. L. . Basic Elastomer Technology. , (2001).
- Such, G. K., Johnston, A. P. R., Liang, K., Caruso, F. Synthesis and functionalization of nanoengineered materials using click chemistry. Prog Polym Sci. 37 (7), 985-1003 (2012).
- Kloxin, C. J., Scott, T. F., Adzima, B. J., Bowman, C. N. Covalent Adaptable Networks (CANS): A Unique Paradigm in Cross-Linked Polymers. Macromol. 43 (6), 2643-2653 (2010).
- Polgar, L. M., van Duin, M., Broekhuis, A. A., Picchioni, F. The use of Diels-Alder chemistry for thermo-reversible cross-linking of rubbers: the next step towards recycling of rubber products. Macromol. 48 (19), 7096-7105 (2015).
- Garcia, J. M., et al. Recyclable, strong thermosets and organogels via paraformaldehyde condensation with diamines. Sci. 344 (6185), 732-735 (2014).
- Montarnal, D., Capelot, M., Tournilhac, F., Leibler, L. Silica-like malleable materials from permanent organic networks. Sci. 334 (6058), 965-968 (2011).
- Capelot, M., Montarnal, D., Tournilhac, F., Leibler, L. Metal-catalyzed transesterification for healing and assembling of thermosets. J Am Chem Soc. 134 (18), 7664-7667 (2012).
- Cordier, P., Tournilhac, F., Soulie-Ziakovic, C., Leibler, L. Self-healing and thermoreversible rubber from supramolecular assembly. Nature. 451 (7181), 977-980 (2008).
- Imbernon, L., Oikonomou, E. K., Norvez, S., Leibler, L. Chemically crosslinked yet reprocessable epoxidized natural rubber via thermo-activated disulfide rearrangements. Polym Chem. 6 (23), 4271-4278 (2015).
- Van der Mee, M. A. J., Goossens, J. G. P., van Duin, M. Thermoreversible cross-linking of maleated ethylene/propylene copolymers with diamines and amino-alcohols. Polym. 49 (5), 1239-1248 (2008).
- Van der Mee, M. A. J., Goossens, J. G. P., Van Duin, M. Thermoreversible covalent crosslinking of maleated ethylene/propylene copolymers with diols. J Polym Sci A-Polym Chem. 46 (5), 1810-1825 (2008).
- Das, A., et al. Ionic modification turns commercial rubber into a self-healing material. Acs Appl Mater Interf. 7 (37), 20623-20630 (2015).
- Gandini, A. The furan/maleimide Diels-Alder reaction: A versatile click-unclick tool in macromolecular synthesis. Prog Polym Sci. 38 (1), 1-29 (2013).
- Toncelli, C., De Reus, D. C., Picchioni, F., Broekhuis, A. A. Properties of reversible Diels-Alder furan/maleimide polymer networks as function of crosslink density. Macromol Chem Phys. 213 (2), 157-165 (2012).
- Tian, Q., Rong, M. Z., Zhang, M. Q., Yuan, Y. C. Synthesis and characterization of epoxy with improved thermal remendability based on Diels-Alder reaction. Polym Int. 59 (10), 1339-1345 (2010).
- Franc, G., Kakkar, A. K. Diels-Alder “click” chemistry in designing dendritic macromolecules. Chem-a Eur J. 15 (23), 5630-5639 (2009).
- Goiti, E., Huglin, M. B., Rego, J. M. Thermal breakdown by the retro Diels-Alder reaction of crosslinking in poly[styrene-co-(furfuryl methacrylate). Macromol Rapid Comm. 24 (11), 692-696 (2003).
- Gheneim, R., Perez-Berumen, C., Gandini, A. Diels-Alder reactions with novel polymeric dienes and dienophiles: Synthesis of reversibly cross-linked elastomers. Macromol. 35 (19), 7246-7253 (2002).
- Moustafa, M. M. A. R., Gillies, E. R. Rubber functionalization by Diels-Alder chemistry: from cross-linking to multifunctional graft copolymer synthesis. Macromol. 46 (15), 6024-6030 (2013).
- Scheltjens, G., Diaz, M. M., Brancart, J., Van Assche, G., Van Mele, B. A self-healing polymer network based on reversible covalent bonding. React Funct Polym. 73 (2), 413-420 (2013).
- Gandini, A., Silvestre, A. J. D., Coelho, D. Reversible click chemistry at the service of macromolecular materials. Polym Chem. 2 (8), 1713-1719 (2011).
- Nandivada, H., Jiang, X., Lahann, J. Click chemistry: Versatility and control in the hands of materials scientists. Adv Mater. 19 (17), 2197-2208 (2007).
- Chen, X. X., et al. A thermally re-mendable cross-linked polymeric material. Sci. 295 (5560), 1698-1702 (2002).
- Laita, H., Boufi, S., Gandini, A. The application of the Diels-Alder reaction to polymers bearing furan moieties .1. Reactions with maleimides. Eur Polym J. 33 (8), 1203-1211 (1997).
- Gandini, A., Coelho, D., Silvestre, A. J. D. Reversible click chemistry at the service of macromolecular materials. Part 1: Kinetics of the Diels-Alder reaction applied to furan-maleimide model compounds and linear polymerizations. Eur Polym J. 44 (12), 4029-4036 (2008).
- Ax, J., Wenz, G. Thermoreversible networks by Diels-Alder Reaction of cellulose furoates with bismaleimides. Macromol Chem Phys. 213 (2), 182-186 (2012).
- Canary, S. A., Stevens, M. P. Thermally reversible cross-linking of polystyrene via the furan-maleimide Diels-Alder reaction. J Polym Sci A-Polym Chem. 30 (8), 1755-1760 (1992).
- Burlett, D. J., Lindt, J. T. Reactive processing of rubbers. Rubber Chem Technol. 66 (3), 411-434 (1993).
- Saelao, J., Phinyocheep, P. Influence of styrene on grafting efficiency of maleic anhydride onto natural rubber. J Appl Polym Sci. 95 (1), 28-38 (2005).
- Guldogan, Y., Egri, S., Rzaev, Z. M. O., Piskin, E. Comparison of maleic anhydride grafting onto powder and granular polypropylene in the melt by reactive extrusion. J Appl Polym Sci. 92 (6), 3675-3684 (2004).
- Van Duin, M. Grafting of polyolefins with maleic anhydride: Alchemy or technology. Macromol Symp. 202, 1-10 (2003).
- Barra, G. M. O., Crespo, J. S., Bertolino, J. R., Soldi, V., Pires, A. T. N. Maleic anhydride grafting on EPDM: Qualitative and quantitative determination. J Braz Chem Soc. 10 (1), 31-34 (1999).
- Oostenbrink, A. J., Gaymans, R. J. Maleic-anhydride grafting on epdm rubber in the melt. Polym. 33 (14), 3086-3088 (1992).
- Schmidt, U., Zschoche, S., Werner, C. Modification of poly(octadecene-alt-maleic anhydride) films by reaction with functional amines. J Appl Polym Sci. 87 (8), 1255-1266 (2003).
- Vermeesch, I., Groeninckx, G. Chemical modification of poly(styrene-co-maleic anhydride) with primary N-alkylamines by reactive extrusion. J Appl Polym Sci. 53 (10), 1365-1373 (1994).
- Zhang, Y., Broekhuis, A. A., Picchioni, F. Thermally self-healing polymeric materials: the next step to recycling thermoset polymers. Macromol. 42 (6), 1906-1912 (2009).
- Gousse, C., Gandini, A., Hodge, P. Application of the Diels-Alder reaction to polymers bearing furan moieties. 2. Diels-Alder and retro-Diels-Alder reactions involving furan rings in some styrene copolymers. Macromol. 31 (2), (1998).
- Mikroyannidis, J. A. Synthesis and Diels-Alder polymerization of furfurylidene and furfuryl-substituted maleamic acids. J Polym Sci A-Polym Chem. 30 (1), 125-132 (1992).
- Kossmehl, G., Nagel, H., Pahl, A. Cross-linking reactions on polyamides by bis- and tris(maleimide)s. Angew Makromol Chem. 227 (1), 139-157 (1995).
- Liu, X., et al. Kinetic study of Diels-Alder reaction involving in maleimide-furan compounds and linear polyurethane. Polym Bull. 70 (8), 2319-2335 (2013).
- Stamboliyska, B. A., Binev, Y. I., Radomirska, V. B., Tsenov, J. A., Juchnovski, I. N. IR spectra and structure of 2,5-pyrrolidinedione (succinimide) and of its nitranion: experimental and ab initio MO studies. J Molec Struct. 516 (2-3), 237-245 (2000).
- Sombatsompop, N., Kumnuantip, C. Rheology, cure characteristics, physical and mechanical properties of tire tread reclaimed rubber/natural rubber compounds. J Appl Polym Sci. 87 (10), 1723-1731 (2003).
- Kim, J. K., Lee, S. H. New technology of crumb rubber compounding for recycling of waste tires. J Appl Polym Sci. 78 (8), 1573-1577 (2000).
- Dikland, H. G., van Duin, A. Miscibility of EPM-EPDM blends. Rubber Chem Technol. 76 (2), 495-506 (2003).
- Klots, T. D., Chirico, R. D., Steele, W. V. Complete vapor-phase assignment for the fundamental vibrations of furan, pyrrole and thiophene. Spectrochim Acta A-Mol Biomol Spectr. 50 (4), 765-795 (1994).
- Litvinov, V. M., Barendswaard, W., van Duin, M. The density of chemical crosslinks and chain entanglements in unfilled EPDM vulcanizates as studied with low resolution, solid state 1H-NMR. Rubber Chem Technol. 71 (1), 105-118 (1998).
- Orza, R. A., Magusin, P. C. M. M., Litvinov, V. M., van Duin, M., Michels, M. A. J. Solid-state 1H-NMR study on chemical cross-links, chain entanglements, and network heterogeneity in peroxide-cured EPDM rubbers. Macromol. 40 (25), 8999-9008 (2007).
- Henssler, J. T., Matzger, A. J. Regiochemical effects of furan substitution on the electronic properties and solid-state structure of partial fused-ring oligothiophenes. J Org Chem. 77 (20), 9298-9303 (2012).
- Hofmann, W. . Rubber Technology Handbook. , (1989).
- Chen, Y., Xu, C. Stress-strain behaviors and crosslinked networks Studies of natural rubber-zinc dimethacrylate composites. J Macromol Sci B-Phys. 51 (7), 1384-1400 (2012).
- Pritchard, R. H., Terentjev, E. M. Swelling and de-swelling of gels under external elastic deformation. Polym. 54 (26), 6954-6960 (2013).
- Tizard, G. A., Dillard, D. A., Norris, A. W., Shephard, N. Development of a high precision method to characterize Poisson’s ratios of encapsulant gels using a flat disk configuration. Exp Mech. 52 (9), 1397-1405 (2012).
- Dijkhuis, K. A. J., Babu, I., Lopulissa, J. S., Noordermeer, J. W. M., Dierkes, W. K. A mechanistic approach to EPDM devulcanization. Rubber Chem. Technol. 81 (2), 865-880 (2008).
- Sutanto, P., Picchioni, E., Janssen, L. P. B. M., Dijkhuis, K. A. J., Dierkes, W. K., Noordermeer, J. W. M. State of the art: Recycling of EPDM rubber vulcanizates. Int Polym Proc. 21 (2), (2006).

