Udvikling og Identifikation af en roman underpopulation af human neutrofil-afledte Giant fagocytter<em> In vitro</em
Summary
Vi beskriver her en fremgangsmåde til opnåelse og identifikation af en nyligt karakteriseret subpopulation af neutrofil-afledte giant fagocytter. Disse celler udvikler i kultur fra friske humane blodneutrofiler, og er kendetegnet ved fagocytose, autophagy, uhyre stor størrelse, og forlænget levetid. Denne metode er væsentlig for yderligere at undersøge dette unikke neutrofil-afledte subpopulation.
Abstract
Neutrofiler (PMN) er bedst kendt for deres fagocytiske funktioner mod invaderende patogener og mikroorganismer. De har den korteste halveringstid blandt leukocytter og i deres ikke-aktiveret tilstand er konstitutivt forpligtet til apoptose. Når rekrutteret til inflammatoriske steder at løse inflammation, de producerer en vifte af cytotoksiske molekyler med potente antimikrobielle drab. Men når disse kraftfulde cytotoksiske molekyler frigives på en ukontrolleret måde, de kan skade omkringliggende væv. I de senere år er dog neutrofil alsidighed i stigende grad dokumenteret, ved at demonstrere plasticitet og immunregulerende funktioner. Vi har for nylig identificeret en ny neutrofil-afledt subpopulation, som udvikler spontant i standard dyrkningsbetingelser uden tilsætning af cytokiner / vækstfaktorer, såsom granulocyt koloni-stimulerende faktor (GM-CSF) / interleukin (IL) -4. Deres fagocytiske evner neutrofile rester generelt bidrage til at øge deresstørrelse uhyre; derfor blev de betegnet gigantiske fagocytter (Gφ). I modsætning til neutrofiler, er Gφ længe levet i kultur. De udtrykker klyngen af differentiering (CD) neutrofile markører CD66b / CD63 / CD15 / CD11 / myeloperoxidase (MPO) / neutrofilelastase (NE), og er blottet for monocytlinjen markører CD14 / CD16 / CD163 og dendritiske CD1c / CD141 markører . De har også take-up latex og zymosan og svare ved oxidativ burst til stimulering med opsoniseret-zymosan og PMA. Gφ udtrykker også scavenger receptorer CD68 / CD36, og i modsætning til neutrofiler, internaliserer oxideret-low density lipoprotein (oxLDL). I modsætning friske neutrofiler, eller dyrkede monocytter, de reagerer på oxLDL optagelse af øgede reaktive oxygenarter (ROS) produktion. Derudover disse fagocytter indeholder mikrotubulus-associeret protein-1 lette kæde 3B (LC3B) overtrukne vakuoler, hvilket indikerer aktiveringen af autofagi. Ved anvendelse af specifikke inhibitorer er det klart, at både fagocytose og autofagi er prerequisites for deres udvikling og sandsynligvis NADPH oxidase afhængig ROS. Vi beskriver her en metode til fremstilling af denne nye delpopulation af langlivet, neutrofil-afledte fagocytceller i kultur, deres identifikation og deres aktuelt kendte karakteristika. Denne protokol er afgørende for opnåelse og karakterisering Gφ for yderligere at undersøge deres betydning og funktion.
Introduction
Polymorfonukleære neutrofiler (PMN) udgør den største befolkning af leukocytter i blodet, der tjener som den første linje i forsvaret mod invaderende patogener ved at producere en bred vifte af cytotoksiske molekyler. Den traditionelle opfattelse har længe været, at af blod cirkulerer, kortlivet, professionelle fagocytter, som er de første til at ankomme til akutte inflammatoriske steder til at bekæmpe infektioner og støtte i clearance af patogener og skadelige partikler. 1 I deres ikke-aktiveret tilstand, neutrofiler er konstitutivt engageret i apoptose. Når du overfører fra blodet til inflammatoriske steder, neutrofiler gennemgår aktivering til at løse inflammation. De fagocytere og dræbe invaderende mikroorganismer, ved at producere en bred vifte af cytotoksiske molekyler som reaktive ilt arter (ROS), lytiske enzymer såsom neutrofilelastase (NE) og cathepsiner med potent mikrobicid aktivitet. For at fælde patogener, neutrofiler også frigive ekstracellulære fælder (NET), Der består af nukleare kromatin tråde indeholder antibakterielle peptider og forskellige lytiske enzymer. Dog kan ukontrolleret udslip af disse cytotoksiske molekyler fra neutrofiler også forevige inflammatoriske reaktioner og fremkalde skader på omgivende væv. 2 Derfor er en effektiv clearance af apoptotiske neutrofiler af makrofager (MO) og dendritiske celler (DC) er afgørende for at løse inflammation. 3, 4, 5, 6
I de senere år er der imidlertid er det blevet mere og mere klart, at neutrofiler er alsidige celler, hvis funktioner går langt ud over fagocytose og patogen drab. 6, 7 Ved undergår priming eller aktivering, er neutrofil plasticitet langsomt ved at vinde opmærksomhed. For eksempel bakterier og mycobakterier udfordret neutrofiler blev vist tiludskiller interleukin (IL) -10 og styre den inflammatoriske reaktion, hvilket antyder tilstedeværelsen af immuno-regulatoriske responser. 8 Post-mitotiske neutrofiler blev vist til trans-differentiere til MO-lignende celler, eller DC-lignende celler ved fordøjelse og præsentere antigen fragmenter, når de behandles med cytokiner og vækstfaktorer, 9, 10 således, betjener en kritisk rolle i integrationen af medfødte og adaptive reaktioner. 3, 6 Aktivering af vækstfaktorer fremmet engulfment af apoptotiske neutrofiler eller cellerester derved lette clearance af vragdele på inflammatoriske steder og løsningen af inflammation, 3, 9 især når MO / DC clearance system er utilstrækkelig eller overvældet, 11, 12 tyder potentielle "selvregulering" for at hjælpe reløse det inflammatoriske respons. Dette, idet apoptose er en form for reguleret selv-dødsfald, som kan inhibere ekstracellulær frigivelse af cytotoksiske forbindelser og dermed forhindre skade på omgivende væv. 6
Langvarig overlevelse er en anden funktion af neutrofil aktivering og blev påvist ved behandling med forskellige vært afledte faktorer såsom granulocytkolonistimulerende faktor (G-CSF), granulocyt-makrofag koloni-stimulerende faktor (GM-CSF), inflammatoriske cytokiner, såsom interferon ( IFN) -γ, tumornekrosefaktor (TNF) -a og / eller patogen afledte produkter, hvori der tages neutrofiler til at modulere deres overlevelse respons. 6 Faktisk neutrofil overlevelse er en forudsætning for dets plasticitet og var forbundet med dens evne til at udføre fagocytose. 6, 13 Følgelig blev det også vist at associere med fænotypiske og funktionelle ændringer, som DEPENded på opreguleret genekspression ved at inducere syntese af nye proteiner involveret i neutrofil levetid forlængelse, og formindsket apoptose. 10
I modsætning til neutrofiler, som er kortvarig og konstitutivt gennemgår apoptose i kultur, eller de cytokiner / vækstfaktorer-aktiverede neutrofiler, der er beskrevet ovenfor, som har forlænget levetid, har vi for nylig identificeret en ny, lille delpopulation af neutrofiler, der udvikler spontant i langvarig standard kultur betingelser fra frisk isolerede humane blodneutrofiler uden eksternt tilsætning cytokiner eller vækstfaktorer. 14 Disse neutrofil-afledte celler, som ikke var beskrevet før i litteraturen blev betegnet giant fagocytter (Gφ). Den Gφ har udvidet levetid i kultur, de er fuldt udviklet inden for 5-7 dage, og er kendetegnet ved unikke morfologiske træk, fænotypiske udtryk og funktioner. De er voldsomt forstørret på grund af autophagocytosis af døde neutrofile rester, vakuoliserede, og indeholder phagolysosomes. Den Gφ udtrykke specifikke neutrofile granula markør – cluster of differentiation (CD) 66b, de azurofile granuler markører – CD63 og myeloperoxidase (MPO) og yderligere neutrofile markører, såsom CD11, NE, CD15, de NADPH oxidase subunits gp91- phOx og p22 phOx og autophagy markør -LC3BII. 14, 15 Funktionelt de aktivt take-up latexkugler og zymosan partikler, og generere ROS i afhængighed zymosan og phorbol-12-myristat-13-acetat (PMA) stimulation. Interessant, i modsætning til friske neutrofiler, Gφ også intensivt udtrykke scavenger receptorer CD68 og CD36, take-up oxideret low density lipoprotein (oxLDL), og generere ROS i respons på stimulering med oxLDL. Derudover Gφ er blottet for de monocytiske afstamning markører CD14, CD16 og CD163 eller de dendritiske markører CD1c og CD141. Desuden PHAgocytosis og autophagy og sandsynligvis funktionelle NADPH oxidase er forudsætninger for deres udvikling. Dette eftersom, fagocytose-inhibitor cytochalsin B, den autofagi inhibitorer 3-methyladenin (3-MA) og bafilomycin (BafA1) og NADPH oxidase inhibitor – diphenylen iodonium (DPI) – forhindrede deres udvikling. Derudover monocytter / neutrofiler co-kulturer samt udsættelse for intermitterende hypoxi hæmmet deres udvikling, mens neutrofil tilpasning til vedvarende hypoxi var tydelig. 14,15 Deres foreslåede udvikling i kultur er illustreret i figur 1 .Den protokol i nærværende dokument beskriver trin for trin forberedelse af Gφ fra frisk isoleret cirkulerende humant blod neutrofiler, deres udvikling, identifikation og nogle grundlæggende karakteristika. Denne protokol kan bruges til at undersøge og afsløre det brede spektrum og roller disse nyligt beskrevet og spændende neutrofil-afledt Gφ for at characterize deres betydning og deres potentielle funktioner.
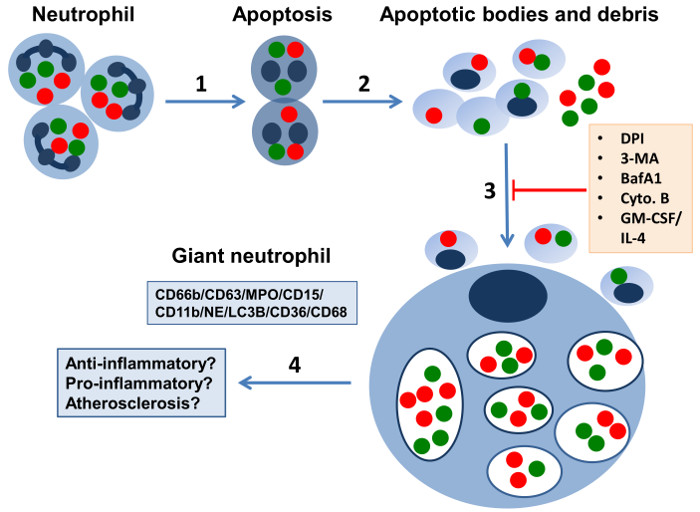
Figur 1: Skematisk repræsentation kæmpeceller Udvikling i 7 Day Neutrocyt kulturer. Det foreslås, at der på inflammatoriske steder (1) neutrofiler undergår apoptotisk celledød, og (2) release-membran-omkranset fragmenter indeholdende nukleart affald, granulat (grønne og røde prikker) og andre subcellulære bestanddele, som udløser autofagi mekanismer. (3) Giant fagocytter (Gφ) udvikle sig i langsigtede neutrofile kulturer blottet for cytokiner eller vækstfaktorer ved internalisere apoptotiske organer og neutrofil vragrester, samtidig med at funktionelle NADPH oxidase.They er kendetegnet ved forskellige neutrofil CD66b + / CD63 + / MPO + / CD15 + / CD11 + / NE markører, store fagosomer omslutter granulater og cellerester, og scavenger receptorer CD36 og CD68. Gb1; er for det meste mononukleære celler, i stand til at internalisere også forskellige partikler og oxideret LDL og generere ROS. Membranerne af celleblærerne påfyldning Gφ indeholder LC3B (markeret med mørkeblå), en markør for autophagosomal membran, hvilket tyder på en streng sammenhæng mellem autofagi og kæmpe fagocyt formation. Gφ ikke udvikler i medium indeholdende GM-CSF / IL-4. Også hæmmere såsom NADPH oxidase inhibitor – diphenylen iodonium (DPI), de autofagi hæmmere 3-methyladenin (3-MA) og bafilomycin (BafA1) og fagocytose inhibitor cytochalasin B (. Cyto B) afskaffe deres dannelse. (4) Potentielle Gφ funktioner i vivo kan omfatte anti eller pro-inflammatoriske egenskaber og deltagelse i aterosklerotiske processer (dette tal er baseret på vores resultater 14, 15 og blev ændret fra den medfølgende Leder af Berton 20). Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Kæmpe fagocytter (Gφ) er en ny defineret subpopulation af neutrofil-afledte celler, der udtrykker grundlæggende og specifikke neutrofile markører såsom CD66b / CD15 / CD63 / MPO / NE. Denne type af neutrofil-afledt fagocyt blev ikke beskrevet i litteraturen før. I modsætning til neutrofiler, der er kortvarige og gennemgår apoptose, Gφ er Annexin-V-negative og vise udvidet levetid. Men ligesom neutrofiler, Gφ internalisere også partikler og producere NADPH oxidase-afhængige ROS som reaktion på disse partikler og PMA. Men for at deres evner internalisere oxLDL og dermed til at producere ROS er unikke funktioner i Gφ. 14
En række faktorer viste sig at påvirke deres udvikling i kultur. Manglen på eksterne cytokiner eller vækstfaktorer i vækstmediet er afgørende (specifikt GM-CSF / IL-4). Men neutrofiler migration mod IL-8 viste sig en diskriminerende faktor mellem dem, der devstak ind Gφ og dem, der ikke gjorde. Også, internalisering af affald som følge af apoptotiske neutrofiler, ekspressionen af autofagi proteiner (LC3B) og funktionelle NADPH oxidase, blev alle vist at være afgørende for deres udvikling, da deres inhibering forhindrede Gφ dannelse (figur 1). Tilsyneladende, udviklingen af disse kæmpeceller skyldes neutrofiler adskiller sig fra den, der karakteriserer kæmpecelledannelse i monocyt / makrofag afstamning. Den sidstnævnte form multi-nukleeret kæmpeceller forbundet med forskellige kroniske inflammatoriske sygdomme, 20, 21 henviser til den neutrofile Gφ her beskrevne udvikles gennem autophagocytosis, ved at opsluge celle rester og forblive hovedsagelig mono-nukleeret hele deres udvikling, 14 (sjældent men nogle gange et sekund kerne kan observeres). Desuden er en række kontroller etableret deres neutrofil oprindelse: (1) EXPREssion af de specifikke neutropilic markører og fravær af dendritiske og monocytlinjen markører, (2) deres hæmmet udvikling i monocytter / PMN co-kulturer, (3) deres forskellige bevægelsesmønstre i kultur fra makrofager (som det fremgår af levende celler og tid -lapse mikroskopi), 14 (4) deres lys tilslutning til plast retter og (5) deres udvikling fra ren CD15 + / CD14 – PMN erhvervet ved flowcytometri.
Nogle af de funktioner, der in vitro kan give os fingerpeg om deres potentielle funktioner in vivo. For eksempel at evner Gφ forbruge store mængder af neutrofile granula og debris, tilstedeværelsen af store vakuoler, og ekspressionen LC3B – en autofagi protein, som bidrager til at mindske inflammation gennem regulatoriske interaktioner med medfødte immunsystem signalveje, 22 – som alle support scavenging evner. Som sådan, Også disse resultater viser, at Gφ måske fungerer på inflammatoriske steder, hvor MO / DC-system er utilstrækkeligt, eller overvældet, og dermed bidrage til løsningen af inflammation. Dette begreb kan være understøttet af det faktum, at Gφ udvikling i blandede monocyt / neutrofile kulturer hæmmes. 14 Også da Gφ udtrykker oxLDL scavenger receptorer (CD36, CD68), internalisere oxLDL, og producere ROS som svar på det, kan indikere, at de er involveret i aterosklerotiske processer til at løse inflammation. Da Gφ udviklede kun fra neutrofiler, der migrerede mod IL-8 og neutrofiler 'transmigration tværs endotel monolag mod IL-8 repræsenterer neutrofil rekruttering til akutte inflammatoriske steder, dette fund også kan støtte anti-inflammatoriske funktioner. Omvendt kan udførelsen af Gφ i visse inflammatoriske tilstande at de kan påtage granula bestanddele og ROS dermed bidrage til prsamstemmende inflammation og vævsskader. 20 Men samlet, deres autophagic evner indikerer, at Gφ sandsynligvis er involveret i faldende den inflammatoriske respons i stedet forevige det.
Interessant har vi for nylig identificeret tilstedeværelsen af Gφ i humane aterosklerotiske plaques. (som forberedelse). Men et stort antal spørgsmål mangler at blive bragt i orden. For eksempel er Gφ pro- eller anti-inflammatorisk? Hvad er de faktorer, som bestemmer deres dannelse og funktion in vitro eller in vivo? Hvilke specifikke neutrofile delpopulation er deres forløber celle, der letter deres udvikling i Gφ? Er de forbundet med visse patologier og hvilke? Kollektivt, udgør interessante spørgsmål med hensyn til deres oprindelse og potentielle funktioner.
Men kritiske trin og faldgruber i protokollen bør holdes for øje. Et afgørende skridt i udviklingen af Gφ is dyrkning af de rene neutrofiler i medium blottet for cytokiner, vækstfaktorer eller antibiotika. En anden afgørende skridt er at udelukke, at Gφ udvikle sig fra forurenende monocytter og at fastslå neutrofile oprindelse Gφ. Således efter blod separation ved diskontinuerlig gradient, neutrofilerne blev yderligere udsat for et yderligere trin med oprensning ved flowcytometri under anvendelse af granulocyt gating og CD15 + / CD14 – markører. Den udviklede Gφ opnået fra neutrofiler, der blev yderligere oprenset ved flowcytometri adskillelse afveg ikke fra dem, der ikke blev udsat for dette trin i oprensningen. Derfor er de fleste af eksperimenterne blev udført uden flowcytometri oprensningstrin skyldes ekstra celletab. Notatet i nogle sjældne tilfælde nogle eosinofile blev noteret i kultur. Deres størrelse forblev uændret i hele kulturen periode. Vi bør også bemærke, at selv om der er en række metoderfor neutrofil adskillelse fra humant blod, den her beskrevne metode er den eneste metode vi ansat, og derfor kan vi ikke sammenligne Gφ udvikling af andre tilgængelige metoder til neutrofil adskillelse.
En stor faldgrube i efterforskningen Gφ skyldes den manglende evne til at opnå et tilstrækkeligt antal ren Gφ population egnet til forskellige biokemiske analyser. Det er dybest set umuligt i de betingelser, blev gennemført vores eksperimenter. Første, udbyttet af Gφ er lav. Fra 1,0 x 10 6 PMN seedet omkring 100-200 Gφ udvikle sig efter syv dage i kultur, afhængigt af bloddonor. For det andet, er det dybest set svært i øjeblikket at adskille udviklede Gφ i kultur fra den resterende neutrofile vragrester i skålen. Disse begrænsninger har gjort det næsten umuligt at analysere cellerne ved biokemiske eller molekylærbiologiske metoder. Derfor er denne protokol fokuseres ved at beskrive Gφ identifikation og funktion ved hjælp af lysog konfokal mikroskopi. Deres morfologisk transformation fra neutrofiler ind Gφ i kultur blev også fulgt af levende celler og tid bortfalder mikroskopi. 14 Tilsyneladende kan der være behov meget større mængder blod for at gennemføre biokemiske eller molekylærbiologiske metoder og overvinde det lave udbytte opnået og adskillelse af den levedygtige Gφ fra neutrofiler 'vragrester i skålen.
Sammenfattende har vi for nylig beskrevet for første gang udviklingen af Gφ i kultur, en subpopulation af langlivede fagocytter af neutrofil oprindelse. Derfor er dette den eneste metode øjeblikket er til rådighed til at opnå Gφ i kultur, selv om de to store begrænsninger ovennævnte bør overvindes (det lave udbytte af Gφ opnået i kultur og den manglende evne til at adskille den fremkaldte Gφ fra neutrofil debris i kulturen fad). Alligevel deres forberedelse og identifikation, præsenteres i denne protokol, er essential for forskere interesseret i inflammatoriske responser og neutrofil biologi og plasticitet, for yderligere at undersøge den potentielle betydning og funktion Gφ.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Forfatterne takker Dr. Edith Suss-Toby for hendes uvurderlige hjælp med konfokale mikroskopi studier. Denne undersøgelse blev støttet af Ministeriet for Indvandring Absorption og Udvalget for planlægning og budgettering i Rådet for Videregående Uddannelse inden for rammerne af den Kamea programmet (LD og AP). Vi har også takker støtte fra Research Fellow fra Lady Davis Foundation ph.d.-forskning Fellowship (OR).
Materials
| Sterile scalp vein set (21GX3/4) | Bio Diagnostics Ltd. | # 20080312 | A strile needle for venipancture |
| VACUETTE HOLDEX Single-Use Holder PP | Greiner Bio-One | # 450263 | For securing during venipuncture |
| VACUETTE Tube K3E K3EDTA (16×100/9 ml) | Greiner Bio-One | # 455036 | Sterile tube for blood collection |
| Nunclon MultiDish (24 wellx1ml) | Thermo Scientific | # 142475 | |
| Polypropylene conical centrifuge tube (50 ml) | Greiner Bio-One | # E14103PJ | |
| Transwell-24 well (transmigration assay) | Corning | # CA-3415 | Polycarbonate membrane, 6.5 mm diameter, 3 μm pores) |
| RPMI-1640 medium | BioIndustries | # 01-100-1A | Do not add antibiotics |
| EA.hy926 (ATCC CRL2922) | BioIndustries | # CRL-2922 | |
| ATCC-formulated Dulbecco’s Modified Eagle’s Medium | BioIndustries | # 302002 | complete growth medium |
| Polysucrose – Histopaque1119 | Sigma-Aldrich | # 1119-1 | Tissue culture grade |
| Polysucrose – Histopaque1077 | Sigma-Aldrich | # 1077-1 | Tissue culture grade |
| Phosphate buffered saline (PBS) – ion free | BioIndustries | # 02-023-1A | Cell biology and molecular biology grade |
| Heat inactivated Fetal calf serum (HI-FCS) | BioIndustries | # 04-121-1B | Cell biology grade or tissue culture grade, low LPS |
| NaCl | Sigma | # S3014 | Molecular biology grade, suitable for cell culture |
| Paraformaldehyde, 16% | Electron Microscopy Sciences | # 15710 | Cell bology grade or tissue culture grade (only 16% PFA) |
| Triton X-100 | Sigma-Aldrich | # 9002-93-1 | Molecular biology grade |
| Normal Goat Serum | BioIndustries | # 04-009-1 | Cell biology and molecular biology grade |
| Trypan blue | BioIndustries | # 031021B | Tissue culture grade |
| May-Grünwald | Sigma-Aldrich | # MG500 | Cell biology grade-(procedure No GS-10) |
| Giemsa stain Kit | Sigma | # 48900 | Cell biololgy grade-(procedure No GS-10) |
| Fibronectin | BioIndustries | # 03090105 | |
| Human Interleukin-8 (CXCL8) | PeproTech | # 200-08-5 | |
| Anti-CD14 (clone 5A3B11B5) | Santa Cruz Biotechnologies | # sc-58951 | Mouse IgG2b; expressed by monocytes |
| Anti-CD63 (clone MX-49.129.5) | Santa Cruz Biotechnologies | # sc-5275 | Mouse IgG1; expressed by neutrophils |
| Anti-CD66b (clone 80H3) | AbD Serotec | # MCA216 | Mouse IgG1; expressed by neutrophils |
| Anti-CD1c (BDCA-1) (clone AD5-8E7) | MACS Miltenyi Biotec | # 130-090-695 | Mouse IgG2a; expressed by dendritic cells |
| Anti-CD15 (clone MY-1) | Abcam | # ab754 | Mouse IgM; expressed by neutrophils |
| Anti-Cytochrome b-245 Light Chain (p22-phox) (clone 44.1) | BioLegend | # 650001 | Mouse IgG2a; to recognize neutrophil NADPH oxidase complex |
| Anti-CD68 | Protein Tech | # 16192-1-AP | Rabbit IgG; to recognize oxLDL scavenger receptor |
| Anti-LC3B | Sigma | # L7543 | Rabbit IgG |
| Anti-Myeloperoxidase | Abcam | # ab45977 | Rabbit IgG |
| Anti-Neutrophil elastase | Calbiochem | # 481001 | Rabbit IgG |
| Anti-NOX2 (gp91-phox) | Abcam | # ab131083 | Rabbit IgG |
| Anti-CD36 (SR-B3) | Novus Biologicals | # NB400-144 | Rabbit IgG |
| Purified Mouse IgG1, κ Isotype Control (clone MG1-45) | BioLegend | # 401401 | Antibody used as isotype control |
| Purified Mouse IgG2a, κ Isotype Control (clone MOPC-173) | BioLegend | # 400263 | Antibody used as isotype control |
| Normal rabbit IgG | Santa Cruz Biotechnologies | # sc-2027 | Antibody used as isotype control |
| CF488A Goat Anti-Rabbit IgG (H+L) | Biotium | # 20012 | Anti-Rabbit IgG with the green fluorescent dye CF488A |
| CF647 Goat Anti-Rabbit IgG (H+L) | Biotium | # 20043 | Anti-Rabbit IgG with the red fluorescent dye CF647 |
| CF488A Goat Anti-Mouse IgG (H+L) | Biotium | # 20010 | Anti-Mouse IgG with the green fluorescent dye CF488A |
| CF647 Goat Anti-Mouse IgG (H+L) | Biotium | # 20040 | Anti-Mouse IgG with the red fluorescent dye CF647 |
| Fluorescent Mounting Medium with DAPI | Vectashield H-1000; Vector Lab Inc. | # E19-18 | Nuclear staining |
| Confocal laser scanning microscope (LSM 700) | Carl Zeiss | Ser.# 3523000380 | Plan Apo x40 immersion oil objective |
| Zeiss CLSM software (ZEN 2010) | Carl Zeiss MicroImaging GmbH | version 6.0 | For colocalization analysis |
| ImageJ software | Wayne Rasband, NIH, USA | version 1.49k | For determination of cell areas and fluorescence intensity |
| Light microscope (Axiovert 25) | Carl Zeiss | Ser.# 201060153 | Examination of cells in culture |
| Centrifuge (Megafuge 1.0 R) | Heraeus Instruments | # D-37520 | Cells separation from blood; cytospins preparation |
| Inverted fluorescent microscope (Zeiss Axio Observer Z.1) | Carl Zeiss | Ser.# 3834001470 | Demonstration of giant phagocytes development |
| Temperature-controlled incubation system (Cube&Box) | Life Imaging Services | Temperature control system for microscopes | |
| High resolution digital CCD camera (AxioCam HRm) | Carl Zeiss | Ser.# 117090279 | For capturing high-contrast image data from an examined cell objects |
Riferimenti
- Borregaard, N. Neutrophils, from marrow to microbes. Immunity. 33, 657-670 (2010).
- Silva, M. T., Correia-Neves, M. Neutrophils and macrophages: the main partners of phagocyte cell systems. Front. Immunol. 3, 174 (2012).
- Cowburn, A. S., Condliffe, A. M., Farahi, N., Summers, C., Chilvers, E. R. Advances in neutrophil biology: clinical implications. Chest. 134, 606-612 (2008).
- Duffin, R., Leitch, A. E., Fox, S., Haslett, C., Rossi, A. G. Targeting granulocyte apoptosis: mechanisms, models, and therapies. Immunol. Rev. 236, 28-40 (2010).
- Silva, M. T. Macrophage phagocytosis of neutrophils at inflammatory/infectious foci: a cooperative mechanism in the control of infection and infectious inflammation. J. Leukoc. Biol. 89, 675-683 (2011).
- Witko-Sarsat, V., Pederzoli-Ribeil, M., Hirsch, E., Sozzani, S., Cassatella, M. A. Regulating neutrophil apoptosis: new players enter the game. Trends Immunol. 32, 117-124 (2011).
- Cassatella, M. A., Locati, M., Mantovani, A. Never underestimate the power of a neutrophil. Immunity. 31, 698-700 (2009).
- Zhang, X., Majlessi, L., Deriaud, E., Leclerc, C., Lo-Man, R. Coactivation of Syk kinase and MyD88 adaptor protein pathways by bacteria promotes regulatory properties of neutrophils. Immunity. 31, 761-771 (2009).
- Araki, H., et al. Reprogramming of human postmitotic neutrophils into macrophages by growth factors. Blood. 103, 2973-2980 (2004).
- Iking-Konert, C., et al. Up-regulation of the dendritic cell marker CD83 on polymorphonuclear neutrophils (PMN): divergent expression in acute bacterial infections and chronic inflammatory disease. Clin. Exp. Immunol. 130, 501-508 (2002).
- Rydell-Tormanen, K., Uller, L., Erjefalt, J. S. Neutrophil cannibalism–a back up when the macrophage clearance system is insufficient. Resp. Res. 7, 143 (2006).
- Esmann, L., et al. Phagocytosis of apoptotic cells by neutrophil granulocytes: diminished proinflammatory neutrophil functions in the presence of apoptotic cells. J. Immunol. 184, 391-400 (2010).
- Nordenfelt, P., Tapper, H. Phagosome dynamics during phagocytosis by neutrophils. J. Leukoc. Biol. 90, 271-284 (2011).
- Dyugovskaya, L., Berger, S., Polyakov, A., Lavie, L. The development of giant phagocytes in long-term neutrophil cultures. J. Leukoc. Biol. 96, 511-521 (2014).
- Dyugovskaya, L., Berger, S., Polyakov, A., Lavie, P., Lavie, L. Intermittent Hypoxia Affects the Spontaneous Differentiation In Vitro of Human Neutrophils into Long-Lived Giant Phatocytes. Oxid. Med. Cell. Longev. , 9636937 (2016).
- Mihalache, C. C., et al. Inflammation-associated autophagy-related programmed necrotic death of human neutrophils characterized by organelle fusion events. J. Immunol. 186, 6532-6542 (2011).
- Manders, E. M. M., Verbeek, F. J., Aten, J. A. Measurement of Colocalization of Objects in Dual-Color Confocal Images. J. Microsc. 169, 375-382 (1993).
- Matsushima, H., et al. Neutrophil differentiation into a unique hybrid population exhibiting dual phenotype and functionality of neutrophils and dendritic cells. Blood. 121, 1677-1689 (2013).
- Oehler, L., et al. Neutrophil granulocyte-committed cells can be driven to acquire dendritic cell characteristics. J. Exp. Med. 187, 1019-1028 (1998).
- Berton, G. Editorial: Gigantism: a new way to prolong neutrophil life. J. Leukoc. Biol. 96, 505-506 (2014).
- Milde, R., et al. Multinucleated Giant Cells Are Specialized for Complement-Mediated Phagocytosis and Large Target Destruction. Cell. Rep. 13, 1937-1948 (2015).
- Deretic, V., Saitoh, T., Akira, S. Autophagy in infection, inflammation and immunity. Nat. Rev. Immunol. 13, 722-737 (2013).

