Utveckling och identifieringen av en ny underpopulation av humant neutrofilt härrörande Giant fagocyter<em> In Vitro</em
Summary
Vi beskriver här en metod för att erhålla och identifiera en nyligen tecknas subpopulation av neutrofil-härlett jätte fagocyter. Dessa celler utvecklas i odling från färska humana blod neutrofiler, och kännetecknas av fagocytos, autophagy, oerhört stora, och förlängd livslängd. Denna metod är viktigt att ytterligare undersöka denna unika neutrofil-härlett subpopulation.
Abstract
Neutrofiler (PMN) är mest känd för sina fagocytiska funktioner mot invaderande patogener och mikroorganismer. De har den kortaste halveringstiden bland leukocyter och deras icke-aktiverade tillståndet är konstitutivt åtagit sig att apoptos. När rekryteras till inflammatoriska ställen att lösa inflammation, de producerar en rad cytotoxiska molekyler med potent antimikrobiell dödande. Men när dessa kraftfulla cytotoxiska molekyler frigörs på ett okontrollerat sätt de kan skada omgivande vävnader. Under de senaste åren dock är neutrofila mångsidighet allt bevisas genom att visa plasticitet och immunfunktioner. Vi har nyligen identifierat en ny neutrofil-härlett subpopulation, som utvecklar spontant i standardodlingsförhållanden utan tillsats av cytokiner / tillväxtfaktorer såsom granulocyt-kolonistimulerande faktor (GM-CSF) / interleukin (IL) -4. Deras fagocytiska förmågor neutrofila rester i stor utsträckning bidra till att öka derasstorlek oerhört; därför de kallades jätte fagocyter (Gφ). Till skillnad från neutrofiler, är Gφ långlivade i kultur. De uttrycker kluster av differentiering (CD) neutrofila markörer CD66b / CD63 / CD15 / CD11b / myeloperoxidas (MPO) / neutrofilelastas (NE), och saknar den monocytiska härstamning markörer CD14 / CD16 / CD163 och de dendritiska CD1c / CD141 markörer . De tar också upp latex och zymosan och svara genom oxidativ burst stimulering med opsoniserad-zymosan och PMA. Gφ uttrycker också renhållare receptorer CD68 / CD36, och till skillnad från neutrofiler, internalisera oxiderat-lågdensitetslipoprotein (oxLDL). Till skillnad från färska neutrofiler, eller odlade monocyter, de svarar på oxLDL upptag av ökade reaktiva syreradikaler (ROS) produktion. Dessutom dessa fagocyter innehåller mikrotubuli-associerat protein-1 lätta kedjan 3B (LC3B) belagda vakuoler, vilket indikerar aktivering av autophagy. Användning av specifika hämmare är det uppenbart att både fagocytos och autophagy är prerequisites för deras utveckling och sannolikt NADPH-oxidas beroende ROS. Vi beskriver här en metod för framställning av denna nya subpopulation av långlivade, neutrofiler härrörande fagocytiska celler i odling, identifiering och deras närvarande kända egenskaper. Detta protokoll är en förutsättning för att erhålla och karakterisera Gφ för att ytterligare undersöka deras betydelse och funktioner.
Introduction
Polymorfonukleära neutrofiler (PMN) utgör den största populationen av leukocyter i blodet, som fungerar som den första försvarslinjen mot invaderande patogener genom att producera ett brett spektrum av cytotoxiska molekyler. Den traditionella synen har länge varit att cirkulerande blod, kortlivad, professionella fagocyter, som är de första att anlända till akuta inflammatoriska platser för att bekämpa infektioner och stöd i avslutandet av patogener och skadliga partiklar. 1 I sin icke-aktiverade tillstånd, neutrofiler är konstitutivt engagerade i apoptos. När du migrerar från blodet till inflammationsställen, neutrofiler genomgå aktivering för att lösa inflammation. De fagocytera och döda invaderande mikroorganismer, genom att producera en rad cytotoxiska molekyler som reaktiva syreföreningar (ROS), lytiska enzymer såsom neutrofilelastas (NE) och katepsiner med potent mikrobicid aktivitet. För att fånga patogener, neutrofiler frisläpper också extracellulära fällor (NET) Som består av kärn kromatin trådar som innehåller antibakteriella peptider och olika lytiska enzymer. Emellertid kan okontrollerat utsläpp av dessa cytotoxiska molekyler från neutrofiler också föreviga inflammatoriska svar och framkalla skador på omgivande vävnader. 2 Därför är en effektiv clearance av apoptotiska neutrofiler genom makrofager (M O) och dendritiska celler (DC) avgörande för att lösa inflammation. 3, 4, 5, 6
Under de senaste åren har det dock blivit allt tydligare att neutrofiler är mycket mångsidiga celler, vars funktioner går långt utöver fagocytos och patogen dödande. 6, 7 genom att genomgå priming eller aktivering är neutrofila plasticitet gradvis att få uppmärksamhet. Till exempel, bakterier och svamp utmanade neutrofiler visade sigutsöndrar interleukin (IL) -10 och kontrollera den inflammatoriska responsen, vilket tyder på förekomsten av immunreglerande svar. 8 Post-mitotiska neutrofiler visade sig trans differentiera till M O-liknande celler, eller DC-liknande celler genom att smälta och presentera antigen fragment vid behandling med cytokiner och tillväxtfaktorer, 9, 10 således, som betjänar en kritisk roll för att integrera medfödda och adaptiva svar. 3, 6 Aktivering av tillväxtfaktorer främjas omvälvning av apoptotiska neutrofiler eller cellrester, och därmed underlätta clearance av skräp vid inflammationsställen och upplösningen av inflammation, 3, 9 särskilt när M O / DC klareringssystem är otillräcklig eller överväldigad, 11, 12 vilket tyder på potential "självreglering" för att hjälpa relösa det inflammatoriska svaret. Detta eftersom apoptos är en form av reglerad själv död, som kan hämma extracellulär frisättning av cytotoxiska föreningar och sålunda förhindra skada på omgivande vävnader. 6
Förlängd överlevnad är en annan funktion av neutrofil aktivering och påvisades genom behandling med olika värd härledda faktorer såsom granulocyt-kolonistimulerande faktor (G-CSF), granulocyt-makrofag-kolonistimulerande faktor (GM-CSF), inflammatoriska cytokiner såsom interferon ( IFN) -γ, tumörnekrosfaktor (TNF) -a och / eller patogena framställda produkter, alltså, så neutrofiler att modulera deras överlevnad svar. 6 I själva verket är neutrofila överlevnad en förutsättning för dess plasticitet och i samband med dess förmåga att utföra fagocytos. 6, 13 Följaktligen var det också visat sig associera med fenotypiska och funktionella förändringar som depended på uppregleras genuttryck genom att inducera syntes av nya proteiner involverade i neutrofil livslängd förlängning, och minskade apoptos. 10
Till skillnad från neutrofiler som är kortlivade och konstitutivt genomgår apoptos i odling, eller cytokiner / tillväxtfaktorer-aktiverade neutrofiler, som beskrivits ovan, som har förlängda livslängden, har vi nyligen identifierat en ny, liten subpopulation av neutrofiler som utvecklar spontant i långvarig standardodlings villkor från nyligen isolerade humana blod neutrofiler utan externt lägga cytokiner eller tillväxtfaktorer. 14 Dessa neutrofil-härledda celler, som inte beskrivits tidigare i litteraturen benämndes jätte fagocyter (Gφ). Den Gφ har förlängt livslängden i kultur, är de fullt utvecklade inom 5-7 dagar, och kännetecknas av unika morfologiska egenskaper, fenotypiska uttrycket och funktioner. De är kraftigt förstorade på grund av autophagocytosis av döda neutrofiler lämningar, vakuoliserade och innehåller phagolysosomes. Den Gφ uttrycker specifika neutrofila granuler markör – kluster av differentiering (CD) 66b, de azurofila granuler markörerna – CD63 och myeloperoxidas (MPO) och ytterligare neutrofiler markörer såsom CD11b, NE, CD15, de NADPH-oxidas subenheter gp91- phOx och p22- phOx och autophagy markör -LC3BII. 14, 15 Funktionellt de aktivt ta upp latexpärlor och zymosan partiklar och genererar ROS som svar på zymosan och forbol-12-myristat 13-acetat (PMA) stimulering. Intressant, till skillnad från färska neutrofiler, Gφ också intensivt uttrycka renhållare receptorer CD68 och CD36, ta upp oxiderat lågdensitetslipoprotein (oxLDL), och generera ROS som svar på stimulering med oxLDL. Dessutom Gφ saknar de monocytiska härstamning markörer CD14, CD16 och CD163 eller dendritiska markörer CD1c och CD141. Dessutom phagocytosis och autophagy och sannolikt funktionellt NADPH-oxidas är en förutsättning för deras utveckling. Detta eftersom, fagocytos-hämmaren cytochalsin B, den Autophagy inhibitorer 3-metyladenin (3-MA) och bafilomycin (BafA1) och NADPH-oxidas-hämmare – difenylen jodonium (DPI) – förhindrade deras utveckling. Dessutom, monocyter / neutrofiler samodlingar samt exponering för intermittent hypoxi hindras deras utveckling, medan neutrofila anpassning till ihållande hypoxi var uppenbar. 14,15 Deras föreslagna utvecklingen i kultur illustreras i figur 1 .Den protokoll i detta dokument beskriver steg för steg framställningen av Gφ från nyligen isolerade cirkulerande humana blod neutrofiler, deras utveckling, identifiering och vissa grundläggande egenskaper. Detta protokoll kan användas för att ytterligare undersöka och avslöja det breda spektrum och rollerna för dessa nyligen beskrivits och spännande neutrofil-härlett Gφ för att characterize deras betydelse och deras potentiella funktioner.
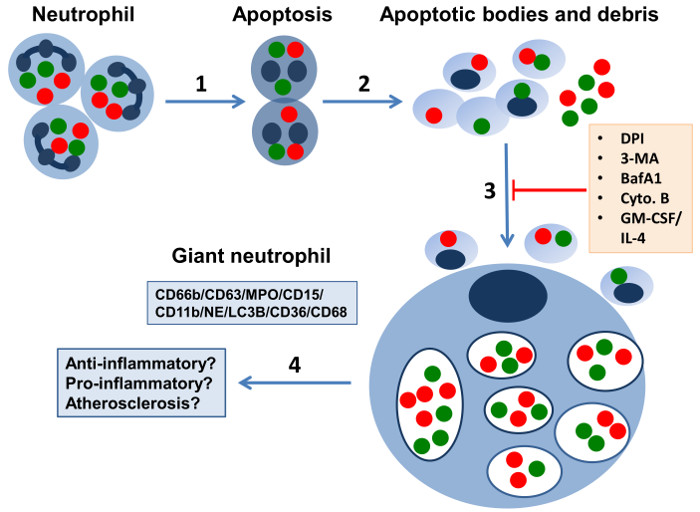
Figur 1: Schematisk representation av jätteceller utveckling 7 Dag neutrofila kulturer. Det föreslås att vid inflammatoriska ställen (1) neutrofiler genomgå apoptotisk celldöd, och (2) frigörmembran inringade fragment innehållande kärn skräp, granulat (gröna och röda prickar) och andra subcellulära komponenter som utlöser Autophagy mekanismer. (3) Jätte fagocyter (Gφ) utvecklas på lång sikt neutrofila kulturer saknar cytokiner eller tillväxtfaktorer från internalisera apoptotiska kroppar och neutrofila skräp, samtidigt som funktionella NADPH oxidase.They kännetecknas av olika neutrofilt CD66b + / CD63 + / MPO + / CD15 + / CD11b + / NE markörer, stora fagosomer omsluter granuler och cellrester, och asätare receptorer CD36 och CD68. gb1; är oftast mononukleära celler, som kan internalisera också olika partiklar och oxiderat LDL och generera ROS. Membranen i vakuoler fyllnings Gφ innehåller LC3B (markerat med mörkblå), en markör av autophagosomal membran, vilket antyder ett strikt samband mellan autophagy och jätte fagocyt bildning. Gφ utvecklar inte i medium innehållande GM-CSF / IL-4. Även inhibitorer såsom NADPH-oxidas-hämmare – difenylen jodonium (DPI), de Autophagy hämmare 3-metyladenin (3-MA) och bafilomycin (BafA1) och fagocytos hämmaren cytochalasin B (. Cyto B) avskaffa deras bildning. (4) Potentiella Gφ funktioner in vivo kan omfatta anti- eller pro-inflammatoriska egenskaper och deltagande i aterosklerotiska processer (denna siffra är baserad på våra resultat 14, 15 och ändrades från medföljande Ledare av BErton 20). Klicka här för att se en större version av denna siffra.
Protocol
Representative Results
Discussion
Giant fagocyter (Gφ) är en nyligen definierade subpopulation av neutrofila-härledda celler som uttrycker grundläggande och specifika neutrofila markörer såsom CD66b / CD15 / CD63 / MPO / NE. Denna typ av neutrofil-härlett fagocyt var inte beskrivits i litteraturen tidigare. Till skillnad från neutrofiler som är kortlivade och genomgår apoptos, Gφ är Annexin-V-negativa och visa utökad livslängd. Men som neutrofiler, Gφ internalisera även partiklar och producera NADPH-oxidas-beroende ROS som svar på dessa partiklar och PMA. Men för att deras förmåga internalisera OxLDL och därmed producera ROS är unika egenskaper Gφ. 14
Ett antal faktorer har visat sig påverka utvecklingen i kultur. Bristen på externa cytokiner eller tillväxtfaktorer i tillväxtmediet är väsentlig (specifikt GM-CSF / IL-4). Men neutrofiler migration mot IL-8 visat sig vara en diskriminerande faktor mellan dem som devrymt in Gφ och de som inte gjorde det. Även internalisering av skräp som härrör från apoptotiska neutrofiler, ett uttryck för Autophagy proteiner (LC3B) och funktionella NADPH-oxidas, var alla visat sig vara nödvändigt för deras utveckling, eftersom deras hämning hindrade Gφ bildning (Figur 1). Tydligen, utvecklingen av dessa jätteceller som härrör från neutrofiler skiljer sig från det som kännetecknar jättecellbildning i monocyt / makrofag-härkomst. Den senare formen flerkärnjätteceller i samband med olika kroniska inflammatoriska sjukdomar, 20, 21, medan den neutrofila Gφ beskrivs här utvecklas via autophagocytosis, genom att uppsluka cellrester och förblir oftast monokärnbildas hela deras utveckling, 14 (sällan men ibland en andra kärna kan observeras). Dessutom har ett antal kontroller etablerat sin neutrofil ursprung: (1) expression av de specifika neutropilic markörer och frånvaro av dendritiska och monocytisk härstamningsmarkörer, (2) deras hämmas utveckling i monocyter / PMN co-kulturer, (3) deras olika rörelsemönster i kultur från makrofager (vilket framgår av levande cell imaging och tid -lapse mikroskopi), 14 (4) deras ljus vidhäftning till plastskålar och (5) deras utveckling från ren CD15 + / CD14 – PMN förvärvats av flödescytometri.
Några av de funktioner som anges in vitro kan ge oss ledtrådar till deras potentiella funktioner in vivo. Till exempel, att förmågan hos Gφ konsumerar stora mängder av neutrofila granuler och skräp, förekomsten av stora vakuoler, och uttrycket LC3B – en autophagy protein som bidrar till att minska inflammation genom reglerings interaktioner med medfödda immunsignalvägar, 22 – som alla stödavlägsnande förmågor. Som sådanDessa fynd tyder också på att Gφ kan fungera på inflammatoriska platser där M O / DC-systemet är otillräcklig eller överväldigad, och på så sätt bidra till att lösa inflammation. Detta begrepp kan stödjas av det faktum att Gφ utveckling i blandade monocyt / neutrofila kulturer hämmas. 14 också, med tanke på att Gφ uttrycka oxLDL renhållare receptorer (CD36, CD68), internalisera oxLDL och producera ROS som svar på det, kan tyda på att de är inblandade i aterosklerotiska processer för att lösa inflammation. Eftersom Gφ utvecklade endast från neutrofiler som migrerade mot IL-8 och neutrofiler "trans över endotelceller monolager mot IL-8 representerar neutrofil rekrytering till akuta inflammatoriska ställen, detta fynd även kan stödja antiinflammatoriska funktioner. Omvänt kan utförandet av Gφ i vissa inflammatoriska tillstånd gör det möjligt för dem att fullgöra granulat beståndsdelar och ROS därmed bidra till perkonsekvent inflammation och vävnadsskada. 20 Men totalt sett, deras autophagic förmåga tyder på att Gφ sannolikt inblandade i fallande den inflammatoriska responsen snarare än permanenta den.
Intressant har vi nyligen identifierat närvaron av Gφ i humana aterosklerotiska plack. (i förberedelse). Men ett stort antal frågor återstår att redas ut. Till exempel, är Gφ pro- eller anti-inflammatoriskt? Vilka är de faktorer som bestämmer deras bildning och funktion in vitro eller in vivo? Vilken specifik neutrofilt subpopulation är deras föregångare cell som underlättar deras utveckling i Gφ? Är de i samband med vissa sjukdomar och som? Tillsammans utgör intressanta frågor om deras ursprung och potentiella funktioner.
Men kritiska steg och fallgropar i protokollet bör hållas i åtanke. Ett kritiskt steg i utvecklingen av Gφ is odling av rena neutrofiler i medium som saknar cytokiner, tillväxtfaktorer eller antibiotika. En annan avgörande steg är att utesluta att Gφ utvecklas från kontaminerande monocyter och fastställa neutrofila ursprung Gφ. Alltså, efter blodseparation genom diskontinuerlig gradient, neutrofilerna rades vidare utsattes för ett ytterligare steg med rening genom flödescytometri med användning av granulocyt gating och CD15 + / CD14 – markörer. Den utvecklade Gφ erhållen från neutrofiler som renades vidare genom flödescytometri separation skilde sig inte från de som inte utsattes för detta reningssteg. Därför är de flesta av de experiment utfördes utan flödescytometri reningssteg på grund av ytterligare cellförlust. Notera i vissa sällsynta fall vissa eosinofiler noterades i kultur. Deras storlek oförändrad under hela odlingsperioden. Vi bör också notera att även om det finns ett antal metoderför neutrofila separation från humant blod, den metod som beskrivs här är det enda sättet vi anställda och därför kan vi inte jämföra Gφ utveckling av andra tillgängliga metoder för neutrofila separation.
En stor fallgrop att utreda Gφ resultat av oförmågan att få tillräckligt antal ren Gφ befolkning som lämpar sig för olika biokemiska analyser. Det är i princip omöjligt under de förhållanden våra experiment genomfördes. För det första är utbytet av Gφ låg. Från 1,0 x 10 6 PMN såddes cirka 100-200 Gφ utvecklas efter sju dagar i kultur, beroende på blodgivare. För det andra är det i princip svårt just nu att separera utvecklade Gφ i kultur från den återstående neutrofila skräp i skålen. Dessa begränsningar har gjort det praktiskt taget omöjligt att analysera cellerna genom biokemiska eller molekylärbiologiska metoder. Därför är detta protokoll fokuserar på att beskriva Gφ identifiering och funktion med hjälp av ljusoch konfokalmikroskopi. Deras morfologiska omvandling från neutrofiler till Gφ i kultur följdes också av levande cell imaging och time lapse mikroskopi. 14 Uppenbarligen kan mycket större blodvolymer behövs för att genomföra biokemiska eller molekylärbiologiska metoder och övervinna det låga utbytet erhållits och separera livskraftig Gφ från neutrofiler "skräp i skålen.
Sammanfattningsvis har vi nyligen beskrevs för första gången utvecklingen av Gφ i kultur, en subpopulation av långlivade fagocyter av neutrofila ursprung. Därför är detta den enda metoden för närvarande finns tillgängliga för att erhålla Gφ i odling, även om de två stora begränsningar som nämnts ovan bör övervinnas (det låga utbytet av Gφ erhållen i kultur och oförmågan att separera den utvecklade Gφ från neutrofil skräp i kulturen maträtt). Ändå deras framställning och identifiering, som presenteras i detta protokoll, är essential för forskare som är intresserade av inflammatoriska svar och neutrofila biologi och plasticitet, i syfte att ytterligare undersöka den potentiella betydelsen och funktioner Gφ.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Författarna tackar Dr Edith Suss-Toby för hennes ovärderlig hjälp med konfokalmikroskopi studierna. Denna studie stöddes av ministeriet för invandring Absorption och utskottet för planering och budgetering av rådet för högre utbildning inom ramen för den Kamea programmet (LD och AP). Vi har också tacksamt erkänna stöd av Research Fellow från Lady Davis Foundation Post-Doctoral Research Fellowship (OR).
Materials
| Sterile scalp vein set (21GX3/4) | Bio Diagnostics Ltd. | # 20080312 | A strile needle for venipancture |
| VACUETTE HOLDEX Single-Use Holder PP | Greiner Bio-One | # 450263 | For securing during venipuncture |
| VACUETTE Tube K3E K3EDTA (16×100/9 ml) | Greiner Bio-One | # 455036 | Sterile tube for blood collection |
| Nunclon MultiDish (24 wellx1ml) | Thermo Scientific | # 142475 | |
| Polypropylene conical centrifuge tube (50 ml) | Greiner Bio-One | # E14103PJ | |
| Transwell-24 well (transmigration assay) | Corning | # CA-3415 | Polycarbonate membrane, 6.5 mm diameter, 3 μm pores) |
| RPMI-1640 medium | BioIndustries | # 01-100-1A | Do not add antibiotics |
| EA.hy926 (ATCC CRL2922) | BioIndustries | # CRL-2922 | |
| ATCC-formulated Dulbecco’s Modified Eagle’s Medium | BioIndustries | # 302002 | complete growth medium |
| Polysucrose – Histopaque1119 | Sigma-Aldrich | # 1119-1 | Tissue culture grade |
| Polysucrose – Histopaque1077 | Sigma-Aldrich | # 1077-1 | Tissue culture grade |
| Phosphate buffered saline (PBS) – ion free | BioIndustries | # 02-023-1A | Cell biology and molecular biology grade |
| Heat inactivated Fetal calf serum (HI-FCS) | BioIndustries | # 04-121-1B | Cell biology grade or tissue culture grade, low LPS |
| NaCl | Sigma | # S3014 | Molecular biology grade, suitable for cell culture |
| Paraformaldehyde, 16% | Electron Microscopy Sciences | # 15710 | Cell bology grade or tissue culture grade (only 16% PFA) |
| Triton X-100 | Sigma-Aldrich | # 9002-93-1 | Molecular biology grade |
| Normal Goat Serum | BioIndustries | # 04-009-1 | Cell biology and molecular biology grade |
| Trypan blue | BioIndustries | # 031021B | Tissue culture grade |
| May-Grünwald | Sigma-Aldrich | # MG500 | Cell biology grade-(procedure No GS-10) |
| Giemsa stain Kit | Sigma | # 48900 | Cell biololgy grade-(procedure No GS-10) |
| Fibronectin | BioIndustries | # 03090105 | |
| Human Interleukin-8 (CXCL8) | PeproTech | # 200-08-5 | |
| Anti-CD14 (clone 5A3B11B5) | Santa Cruz Biotechnologies | # sc-58951 | Mouse IgG2b; expressed by monocytes |
| Anti-CD63 (clone MX-49.129.5) | Santa Cruz Biotechnologies | # sc-5275 | Mouse IgG1; expressed by neutrophils |
| Anti-CD66b (clone 80H3) | AbD Serotec | # MCA216 | Mouse IgG1; expressed by neutrophils |
| Anti-CD1c (BDCA-1) (clone AD5-8E7) | MACS Miltenyi Biotec | # 130-090-695 | Mouse IgG2a; expressed by dendritic cells |
| Anti-CD15 (clone MY-1) | Abcam | # ab754 | Mouse IgM; expressed by neutrophils |
| Anti-Cytochrome b-245 Light Chain (p22-phox) (clone 44.1) | BioLegend | # 650001 | Mouse IgG2a; to recognize neutrophil NADPH oxidase complex |
| Anti-CD68 | Protein Tech | # 16192-1-AP | Rabbit IgG; to recognize oxLDL scavenger receptor |
| Anti-LC3B | Sigma | # L7543 | Rabbit IgG |
| Anti-Myeloperoxidase | Abcam | # ab45977 | Rabbit IgG |
| Anti-Neutrophil elastase | Calbiochem | # 481001 | Rabbit IgG |
| Anti-NOX2 (gp91-phox) | Abcam | # ab131083 | Rabbit IgG |
| Anti-CD36 (SR-B3) | Novus Biologicals | # NB400-144 | Rabbit IgG |
| Purified Mouse IgG1, κ Isotype Control (clone MG1-45) | BioLegend | # 401401 | Antibody used as isotype control |
| Purified Mouse IgG2a, κ Isotype Control (clone MOPC-173) | BioLegend | # 400263 | Antibody used as isotype control |
| Normal rabbit IgG | Santa Cruz Biotechnologies | # sc-2027 | Antibody used as isotype control |
| CF488A Goat Anti-Rabbit IgG (H+L) | Biotium | # 20012 | Anti-Rabbit IgG with the green fluorescent dye CF488A |
| CF647 Goat Anti-Rabbit IgG (H+L) | Biotium | # 20043 | Anti-Rabbit IgG with the red fluorescent dye CF647 |
| CF488A Goat Anti-Mouse IgG (H+L) | Biotium | # 20010 | Anti-Mouse IgG with the green fluorescent dye CF488A |
| CF647 Goat Anti-Mouse IgG (H+L) | Biotium | # 20040 | Anti-Mouse IgG with the red fluorescent dye CF647 |
| Fluorescent Mounting Medium with DAPI | Vectashield H-1000; Vector Lab Inc. | # E19-18 | Nuclear staining |
| Confocal laser scanning microscope (LSM 700) | Carl Zeiss | Ser.# 3523000380 | Plan Apo x40 immersion oil objective |
| Zeiss CLSM software (ZEN 2010) | Carl Zeiss MicroImaging GmbH | version 6.0 | For colocalization analysis |
| ImageJ software | Wayne Rasband, NIH, USA | version 1.49k | For determination of cell areas and fluorescence intensity |
| Light microscope (Axiovert 25) | Carl Zeiss | Ser.# 201060153 | Examination of cells in culture |
| Centrifuge (Megafuge 1.0 R) | Heraeus Instruments | # D-37520 | Cells separation from blood; cytospins preparation |
| Inverted fluorescent microscope (Zeiss Axio Observer Z.1) | Carl Zeiss | Ser.# 3834001470 | Demonstration of giant phagocytes development |
| Temperature-controlled incubation system (Cube&Box) | Life Imaging Services | Temperature control system for microscopes | |
| High resolution digital CCD camera (AxioCam HRm) | Carl Zeiss | Ser.# 117090279 | For capturing high-contrast image data from an examined cell objects |
Riferimenti
- Borregaard, N. Neutrophils, from marrow to microbes. Immunity. 33, 657-670 (2010).
- Silva, M. T., Correia-Neves, M. Neutrophils and macrophages: the main partners of phagocyte cell systems. Front. Immunol. 3, 174 (2012).
- Cowburn, A. S., Condliffe, A. M., Farahi, N., Summers, C., Chilvers, E. R. Advances in neutrophil biology: clinical implications. Chest. 134, 606-612 (2008).
- Duffin, R., Leitch, A. E., Fox, S., Haslett, C., Rossi, A. G. Targeting granulocyte apoptosis: mechanisms, models, and therapies. Immunol. Rev. 236, 28-40 (2010).
- Silva, M. T. Macrophage phagocytosis of neutrophils at inflammatory/infectious foci: a cooperative mechanism in the control of infection and infectious inflammation. J. Leukoc. Biol. 89, 675-683 (2011).
- Witko-Sarsat, V., Pederzoli-Ribeil, M., Hirsch, E., Sozzani, S., Cassatella, M. A. Regulating neutrophil apoptosis: new players enter the game. Trends Immunol. 32, 117-124 (2011).
- Cassatella, M. A., Locati, M., Mantovani, A. Never underestimate the power of a neutrophil. Immunity. 31, 698-700 (2009).
- Zhang, X., Majlessi, L., Deriaud, E., Leclerc, C., Lo-Man, R. Coactivation of Syk kinase and MyD88 adaptor protein pathways by bacteria promotes regulatory properties of neutrophils. Immunity. 31, 761-771 (2009).
- Araki, H., et al. Reprogramming of human postmitotic neutrophils into macrophages by growth factors. Blood. 103, 2973-2980 (2004).
- Iking-Konert, C., et al. Up-regulation of the dendritic cell marker CD83 on polymorphonuclear neutrophils (PMN): divergent expression in acute bacterial infections and chronic inflammatory disease. Clin. Exp. Immunol. 130, 501-508 (2002).
- Rydell-Tormanen, K., Uller, L., Erjefalt, J. S. Neutrophil cannibalism–a back up when the macrophage clearance system is insufficient. Resp. Res. 7, 143 (2006).
- Esmann, L., et al. Phagocytosis of apoptotic cells by neutrophil granulocytes: diminished proinflammatory neutrophil functions in the presence of apoptotic cells. J. Immunol. 184, 391-400 (2010).
- Nordenfelt, P., Tapper, H. Phagosome dynamics during phagocytosis by neutrophils. J. Leukoc. Biol. 90, 271-284 (2011).
- Dyugovskaya, L., Berger, S., Polyakov, A., Lavie, L. The development of giant phagocytes in long-term neutrophil cultures. J. Leukoc. Biol. 96, 511-521 (2014).
- Dyugovskaya, L., Berger, S., Polyakov, A., Lavie, P., Lavie, L. Intermittent Hypoxia Affects the Spontaneous Differentiation In Vitro of Human Neutrophils into Long-Lived Giant Phatocytes. Oxid. Med. Cell. Longev. , 9636937 (2016).
- Mihalache, C. C., et al. Inflammation-associated autophagy-related programmed necrotic death of human neutrophils characterized by organelle fusion events. J. Immunol. 186, 6532-6542 (2011).
- Manders, E. M. M., Verbeek, F. J., Aten, J. A. Measurement of Colocalization of Objects in Dual-Color Confocal Images. J. Microsc. 169, 375-382 (1993).
- Matsushima, H., et al. Neutrophil differentiation into a unique hybrid population exhibiting dual phenotype and functionality of neutrophils and dendritic cells. Blood. 121, 1677-1689 (2013).
- Oehler, L., et al. Neutrophil granulocyte-committed cells can be driven to acquire dendritic cell characteristics. J. Exp. Med. 187, 1019-1028 (1998).
- Berton, G. Editorial: Gigantism: a new way to prolong neutrophil life. J. Leukoc. Biol. 96, 505-506 (2014).
- Milde, R., et al. Multinucleated Giant Cells Are Specialized for Complement-Mediated Phagocytosis and Large Target Destruction. Cell. Rep. 13, 1937-1948 (2015).
- Deretic, V., Saitoh, T., Akira, S. Autophagy in infection, inflammation and immunity. Nat. Rev. Immunol. 13, 722-737 (2013).

