Magnetisk Levitation Sammen med Portable Imaging and Analysis for sykdomsdiagnostikk
Summary
We present a magnetic levitation technique coupled with automated imaging and analysis in both a smartphone-compatible device and a device with embedded imaging and processing. This is applied to measure the density distribution of cells with two demonstrated biomedical applications: sickle cell disease diagnosis and separating white and red blood cells.
Abstract
Currently, many clinical diagnostic procedures are complex, costly, inefficient, and inaccessible to a large population in the world. The requirements for specialized equipment and trained personnel require that many diagnostic tests be performed at remote, centralized clinical laboratories. Magnetic levitation is a simple yet powerful technique and can be applied to levitate cells, which are suspended in a paramagnetic solution and placed in a magnetic field, at a position determined by equilibrium between a magnetic force and a buoyancy force. Here, we present a versatile platform technology designed for point-of-care diagnostics which uses magnetic levitation coupled to microscopic imaging and automated analysis to determine the density distribution of a patient’s cells as a useful diagnostic indicator. We present two platforms operating on this principle: (i) a smartphone-compatible version of the technology, where the built-in smartphone camera is used to image cells in the magnetic field and a smartphone application processes the images and to measures the density distribution of the cells and (ii) a self-contained version where a camera board is used to capture images and an embedded processing unit with attached thin-film-transistor (TFT) screen measures and displays the results. Demonstrated applications include: (i) measuring the altered distribution of a cell population with a disease phenotype compared to a healthy phenotype, which is applied to sickle cell disease diagnosis, and (ii) separation of different cell types based on their characteristic densities, which is applied to separate white blood cells from red blood cells for white blood cell cytometry. These applications, as well as future extensions of the essential density-based measurements enabled by this portable, user-friendly platform technology, will significantly enhance disease diagnostic capabilities at the point of care.
Introduction
Her presenterer vi en teknologiplattform og en teknikk som bruker magnetisk levitasjon kombinert med automatisert bildebehandling og analyse for å analysere tettheten utdeling av pasientens celler som en indikator for sykdom. Denne allsidige metode for tetthetsbaserte cytometrisk analyse kan til slutt bli anvendt på en rekke sykdomsdiagnostikk. Men for å være kompatibel med point-of-care testing og bruk i utviklingsland, må teknikken tilfredsstille krav til lav pris, bærbarhet og brukervennlighet. Anordningen og elektroder må være lett oppnådd ved en lav kostnad. Prøven forberedelse må være enkel, bør analysen automatiseres med minimale krav til brukerundersøkelser eller tolkning, og resultatene skal returneres raskt. Videre må enheten være kompakt og bærbar å være nyttig i kliniske settinger samt utviklingsland. Derfor har vi utviklet et apparat og metode å bruke magnetisk levitasjon i point-of-care-kompatibel teknologi ved kobling automatisert bildebehandling og bildeanalyse for å returnere resultater vedrørende tetthet distribusjon av en befolkning på pasientens celler.
Point-of-care-teknologi tilbyr en bemerkelsesverdig fordel over aktuelle kliniske laboratorium testprosedyrer. Dagens teknologi er for dyrt til å være eid av en kliniker eller for kompliserte til å utføres av medisinsk personale. Mange av disse prosedyrene krever arbeidsintensive protokoller som må utføres av en tekniker. Av disse grunner, er pasientprøver slik som blod eller urin vanligvis oppsamlet i legekontoret deretter overført til en fjerntliggende, sentralisert testlaboratorium for klinisk testing, som kan ta flere dager for legen å motta resultatene av testen. Dette kan føre til forsinkelser eller komplikasjoner i løpet av behandlingen i noen tilfeller gjør denne testingen svært kostbare og ineffektive (forårsaker en økonomisk byrde på forsikrings betalere), og videre gjør mangediagnostikk utilgjengelige i lav ressursinnstillingene og utviklingsland.
Her presenterer vi en magnetisk levitasjon teknikk kombinert med automatisert bildebehandling og analyse både i en enhet med innebygd bildebehandling og behandling (figur 1) og en smarttelefon-kompatibel enhet (figur 2). Disse magnetiske levitasjon-baserte enheter representerer et bredt anvendelig plattform-teknologi som har potensiale til å bli brukt på en rekke forskjellige medisinske diagnostiske anvendelser. De magnetiske levitasjon tilnærming funksjoner basert på en likevekt mellom to krefter: en magnetisk kraft og en oppdriftskraft en, to, tre. Når en partikkel er opphengt i en paramagnetisk medium og satt inn i et magnetisk felt som genereres av to magneter med like poler vendende mot hverandre, en magnetisk kraft virker på partikkelen i retning mot midtlinjen mellom de to magnet ets. Oppdriftskraften er forårsaket av den relative tetthet av partikkelen i forhold til det suspenderende medium og er oppover i tilfelle av partikler mindre tette enn mediet og nedover når det gjelder partikler som er tyngre enn det omgivende medium. Basert på disse to kreftene, vil partiklene nå en likevekt levitasjon posisjon i feltet som balanserer disse to styrker; denne stilling er direkte relatert til tettheten av partikkelen, med tettere partikler Levitating lavere i felten enn mindre tette partikler. En bildemodul, enten en innebygd kamera smarttelefon 4, 5, 6 eller uavhengige optiske komponenter som er utstyrt med en forstørrelseslinse 7, 8, blir brukt til å visualisere posisjonen til partiklene. Bildebehandling, enten gjennom en smarttelefon program 4, 5,= "xref"> 6 eller en innkapslet behandlingsenhet 7, 8, behandler deretter de fangede bilder for å kvantifisere den romlige distribusjon, og derfor tetthetsfordelingen av befolkningen. For å analysere større prøver (slik som de med bare noen få partikler av interesse per milliliter, kan strømning være integrert direkte i anordningen slik at partiklene er levitert og analysert som de passerer gjennom bilde region (fig 2).
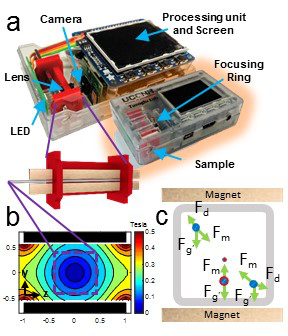
Figur 1: Selvforsynt Magnetic Levitation Platform. (A) Compact magnetisk levitasjon enheter, inkludert en magnetisk fokus modul, bilde komponenter (en light-emitting diode (LED), en optisk linse, og et kamera detektor), og en behandlingsenhet med en skjerm. (B) Magnetisk feltstyrke i cross-delen av området mellom magnetene hvor prøven settes inn. Feltstyrken er størst ved overflaten av magnetene og nærmer seg null ved midtlinjen mellom dem. (C) Partikler, slik som celler, i løpet av de magnetiske felterfaring flere krefter: en magnetisk kraft (F m) mot senterlinjen mellom magnetismen, med størrelse varierende på grunnlag av posisjonen av partikkelen; en gravitasjonskraft (F g ') som er avhengig av partikkeltettheten i forhold til den av suspensjonsmediet, og en dragkraft (F d) motstand mot den partikkelbevegelse. Gjengitt med tillatelse fra Yenilmez, et al. 8 Klikk her for å se en større versjon av dette tallet.
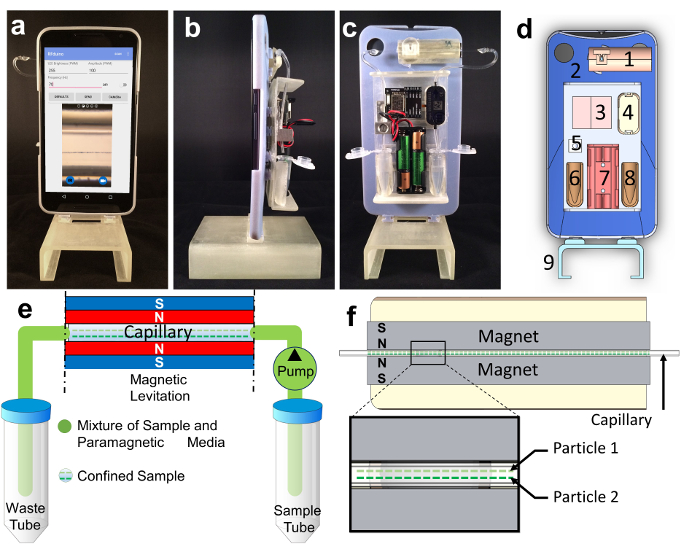
figure 2: Smartphone-kompatibel Flow-assistert Magnetic Levitation Platform. (A – c) Front (a), side (b), og tilbake (c) visninger av magnetisk levitasjon enhet (d) Komponentene i enheten inkluderer: 1) Magnetic levitasjon modul, inkludert permanente magneter, et forstørrelsesglass, og en LED og lys diffuser, 2) smartphone case, 3) elektronikk, inkludert en mikrokontroller, pumpe driver, og Bluetooth-mottaker, 4) micro-pumpeholder, 5) justerbar åpning, 6) avfall rørholder, 7) batteriholder, 8 ) prøve holder, 9) dual-purpose stativ og lokk. (E) Strømnings skjematisk, som viser pumping av prøven gjennom det magnetiske felt. (F) Tverrsnitt av den magnetiske levitasjon modulen, og viser hvordan partikler av ulik tetthet justeres etter hvert som de blir pumpet gjennom feltet; mindre tette partikler, for eksempel Particle 1, vil stabilisere seg på et høyere levitasjon høyde tHan tettere partikler, for eksempel Particle 2. Gjengitt med tillatelse fra Amin, et al. 1 Klikk her for å se en større versjon av dette tallet.
Minimumskravene for bruk av prøven for tetthetsfordeling analyse i dette systemet er muligheten til å oppnå en suspensjon av celler eller partikler større enn ca fem mikrometer og mindre enn ca 250 mikrometer i størrelse (for bildebehandling og bildebehandling) og dens kompatibilitet med blanding i en oppløsning av et paramagnetisk løsning slik som den gadobutrol anvendt her. For sykdomsdiagnostikk, kompatible programmer innbefatter de hvori (i) celler av interesse i seg selv ha en endret densitet når de bærer en sykdom sammenlignet med friske kontroller, (ii) en tetthetsendring kan induseres i cellen ved tilsetning av et reagens eller noen alternativ behandling av et kort icubation tid, eller (iii) forskjellige celletyper er identifisert i en enkelt prøve og i seg selv (eller via noen behandling) har unike karakteristiske tettheter.
Sigdcelleanemi er en genetisk forstyrrelse som forårsaker en mutert form av hemoglobin, HbS, som skal fremstilles i en persons røde blodceller (RBC), noe som kan resultere i intermitterende vaso-okklusive hendelser og kronisk hemolytisk anemi 9. Det er diagnostisert ved hjelp av enten hemoglobin isoelektrisk fokusering, væskekromatografi (HPLC) fraksjonering, eller hemoglobin elektroforese som er svært nøyaktige, men må utføres i et laboratorium klinisk testing fordi de ikke er kompatible med point-of-care innstillinger. Løselighet og papirbaserte tester for sigdcelleanemi har vært foreslått, men generelt krever subjektive bruker tolkning og bekreftende testing. Her bruker vi en tetthet basert tilnærming for å identifisere sigd RBC, som oppnår en høyere tetthet enn RBCs fra folk uten sigdcelleanemi. Mekanismen involverer polymerisasjon av den muterte formen av hemoglobin, HbS, noe som fører til RBC dehydrering i sigdcelleanemi RBC-er i henhold til deoxygenated betingelser 10, 11, 12, 13.
Denne tetthet-baserte fremgangsmåten kan også anvendes for å separere celler av forskjellige typer på grunnlag av densitet: hvite blodceller (WBC) og RBC-7. WBCs er generelt ansvarlig for å bekjempe infeksjoner i kroppen. WBC-cytometri kan brukes til å kvantifisere antallet av disse celler i blodet og tjener som et nyttig diagnoseverktøy. WBC teller høyere enn normalt (generelt ansett mer enn 11.000 celler per mL) kan tyde på infeksjon, immunsystem lidelser, eller leukemi. WBC teller under normalområdet (rundt 3500 celler per mL) kan være forårsaket av autoimmune lidelser eller Conditioner som skader benmargen. Til forskjell fra alternative teknologier, blir prosessen presentert her ikke stole på lyse av de røde blodceller eller flekker for å identifisere WBC. Dette celle-basert test dro fordel av de unike iboende tettheter av de to celletyper for å utføre separasjon, som den WBC populasjonstettheten er blitt rapportert å være lavere enn den for RBC befolkningen som tidligere er beregnet ved hjelp av tetthetsgradient-sentrifugering 2, 3.
Sammenlignet med alternative testing på avsidesliggende steder, er denne testen hurtig, med enkel prøvepreparering (figur 3), separering av celler i innretningen i løpet av 10 – 15 min, og automatisert bildeanalyse, og som krever mindre enn 1 min. På denne måte kan anordningen returnerer resultater raskt for å bedre informere medisinske avgjørelser, tillate behandling som skal administreres umiddelbart for å lindre fysisk og psykisk smerte, og redusere risikoen for komplikasjoner associrerte med en forsinkelse i medisinsk behandling. Denne teknikken kan utføres på stedet enten i kliniske settinger på grunn av enkel prøveopparbeidelse og automatisert bildebehandling og analyse som returnerer et resultat med minimal brukerundersøkelser eller tolkning. På grunn av bruken av en enkel tilnærming ved hjelp av permanente magneter for prøveanalyser og bruk av enten en smarttelefon eller enkle elektriske komponenter for bildebehandling og bildebehandling, enheten samt pr-test kostnadene er minimal i forhold til noen sofistikerte testprosedyrer.
Protocol
Representative Results
Discussion
Kritiske trinn i protokollen
Kritiske faktorer i denne prosess er riktig justering av magnetene. Hvis magnetene komme ut av stilling eller separert mer enn normalt i enheten, kan det påvirke resultatet. For å kontrollere for denne feil eller andre i prosessen, en tetthet styrt partikkel, for eksempel polystyren-mikrokuler, kan brukes til periodisk å kontrollere for endringer over tid. Videre er levitasjon tid viktig for å tillate cellene å nå likevekt. For røde blodceller, er tilstrekkelig til å tillate a…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
The authors would like to acknowledge Dr. Matthew Heeney of Boston Children’s Hospital/Dana-Farber Cancer Institute and Dr. Farzana Pashankar of Yale-New Haven Hospital for providing sickle cell patient samples. The authors would like to thank Chu H. Yu and Ashwini Joshi for their assistance in testing these samples and compiling the data.
S.T. acknowledges the American Heart Association Scientist Development Grant (15SDG25080056) and the University of Connecticut Research Excellence Program award for financial support of this research. S.K. acknowledges that this material is based upon work supported by the National Science Foundation Graduate Research Fellowship (DGE-1247393).
Materials
| Gadavist (Bayer) | Jefferson Medical and Imaging | 2068062 | Gadavist contains 1M gadobutrol, a chelate of gadolinium. We purchased 2 mL vials with 15/ca. |
| Square glass microcapillary tubes | Vitrocom | 8270 | 50 mm length is sufficient |
| Sodium metabisulfite | Sigma-Aldrich | S9000 | Chemical formula: Na2S2O5 |
| Leica Microsystems Critoseal tube sealant | Fisher Scientific | 02-676-20 | |
| Hank's Balanced Salt Solution | Sigma-Aldrich | H9269 SIGMA | |
| Trypsin-EDTA | Sigma-Aldrich | T4049 | Or other reagent as recommended for the cell type used |
| MICROLET 2 Adjustable Lancing Device | Walgreens | 246567 | Any lancing device is acceptable when used according to biosafety protocols |
| Microlet Lancets | Walgreens | 667474 | Must be dispoable and not reused |
| Hausser Bright-Line Phase Hemacytometer | Fisher Scientific | 02-671-6 | Or any preferred method for cell counting |
| ACK Lysing Buffer | ThermoFisher | A1049201 |
Riferimenti
- Tasoglu, S., Khoory, J., Tekin, H., Thomas, C., Karnoub, A., Ghiran, I., Demirci, U. Levitational Image Cytometry with Temporal Resolution. Advanced Materials. 27 (26), 3901-3908 (2015).
- Tasoglu, S., Yu, C. H., Liadudanskaya, V., Guven, S., Migliaresi, C., Demirci, U. Magnetic Levitational Assembly for Living Material Fabrication. Advanced Healthcare Materials. 4 (10), 1469-1476 (2015).
- Tasoglu, S., Yu, C. H., Gungordu, H. I., Guven, S., Vural, T., Demirci, U. Guided and magnetic self-assembly of magnetoceptive gels. Nature Communications. 5, 4702 (2014).
- Amin, R., Knowlton, S., Yenilmez, B., Hart, A., Joshi, A., Tasoglu, S. Smart-phone Attachable, Flow-Assisted Magnetic Focusing Device. RSC Advances. 6, 93922-93931 (2016).
- Knowlton, S. M., Sencan, I., Aytar, Y., Khoory, J., Heeney, M. M., Ghiran, I. C., Tasoglu, S. Sickle Cell Detection Using a Smartphone. Sci Rep. 5, 15022 (2015).
- Knowlton, S., Yu, C. H., Jain, N., Ghiran, I. C., Tasoglu, S. Smart-Phone Based Magnetic Levitation for Measuring Densities. PLoS One. 10 (8), e0134400 (2015).
- Yenilmez, B., Knowlton, S., Tasoglu, S. Self-Contained Handheld Magnetic Platform for Point of Care Cytometry in Biological Samples . Advanced Materials Technologies. 1, 1600144 (2016).
- Yenilmez, B., Knowlton, S., Yu, C. H., Heeney, M., Tasoglu, S. Label-Free Sickle Cell Disease Diagnosis Using a Low-Cost, Handheld Platform. Adv Mat Tech. 1 (5), 1600100 (2016).
- Bender, M. A., Douthitt Seibel, G., Pagon, R. A., et al. . GeneReviews. , (1993).
- Kaul, D. K., Fabry, M. E., Windisch, P., Baez, S., Nagel, R. L. Erythrocytes in sickle cell anemia are heterogeneous in their rheological and hemodynamic characteristics. J Clin Invest. 72 (1), 22-31 (1983).
- Joiner, C. H. Gardos pathway to sickle cell therapies?. Blood. 111 (8), 3918-3919 (2008).
- Finch, J. T., Perutz, M. F., Bertles, J. F., Döbler, J. Structure of Sickled Erythrocytes and of Sickle-Cell Hemoglobin Fibers. Proc Natl Acad Sci. 70 (3), 718-722 (1973).
- Lew, V. L., Etzion, Z., Bookchin, R. M. Dehydration response of sickle cells to sickling-induced Ca(++) permeabilization. Blood. 99 (7), 2578-2585 (2002).
- Ernst, D. J. . NCCLS Procedures for the Collection of Diagnostic Blood Specimens by Venipuncture: Approved Standard-Sixth Addition. 27 (26), (2007).

