在小鼠胚胎干细胞结构功能研究使用重组酶介导的盒式交换
Summary
蛋白质常含有可发挥不同的细胞功能多个域。基因敲除(KO)不考虑这个功能的多样性。这里,我们报告在KO胚胎干细胞的重组介导的盒式交换(RMCE)系的结构 – 功能的方法,其允许各种功能结构域或蛋白质的变体的分子清扫。
Abstract
在小鼠胚胎或胚胎干细胞(mESCs)基因工程允许对于给定的蛋白质的功能的研究。蛋白质是细胞的工作母机和经常由多个功能性结构域,其可以通过翻译后修饰的影响的。整个蛋白在有条件的或组成型敲除(KO)小鼠的耗尽不考虑这一功能多样性和调节。先前报道的mESC的线和衍生的小鼠模型,其中停靠位点FLPE重组介导的盒式交换(RMCE)插入所述ROSA26(R26)基因座内,被。在这里,我们在结构与功能的办法,允许多域蛋白质的不同功能的分子解剖报告。为此,RMCE兼容小鼠必须用基因敲除小鼠杂交,然后RMCE兼容KO mESCs必须隔离。接着,推定救援构建体的面板可以被引入到经由RMCE targeti的R26轨迹NG。所述救援候选的cDNA可以使用重组克隆的靶向载体的RMCE位点之间很容易地插入。接着,KO mESCs被转染的化合物,连同FLPE重组酶表达质粒靶向载体。 RMCE重新激活在ROSA26停放地点的启动子的新霉素抗性基因,并允许正确的靶向事件的选择。以这种方式,获得接近100%的高效率的定位,从而允许在一个半高通量的方式多个推定的救援构建体的插入。最后,R26驱动救援构建体的多个可以针对其营救在亲本KO mESCs观察到表型的能力进行测试。我们目前在P120连环蛋白(p120ctn各)使用内胚层分化的胚状体(EB)的表型读数KO mESCs一个验证的原理结构与功能的研究。这种方法使重要领域的确定,假定下游途径,与疾病相关的点背后对于给定的蛋白质KO表型的突变。
Introduction
据估计,哺乳动物的基因组包含约20000个蛋白质编码基因。选择性剪接和翻译后修饰进一步增加蛋白质的剧目。蛋白具有模块化结构1和通常包含多个相互作用结构域,其允许其招募不同的蛋白质复合物以及它们在多种细胞过程2的参与。一个例子是所谓的p120ctn各多功能蛋白。 p120ctn各由Ctnnd1基因编码,并且由通过N端和C端区域侧接的大型中央犰狳重复结构域。的p120ctn各犰狳域结合经典钙黏着蛋白,其参与细胞 – 细胞粘着的高度保守的近膜结构域,但它也结合所述转录阻遏Kaiso。 p120ctn各的N-末端结构域具有不同的激酶,磷酸酶,小RhoGTPases,和微管相关p相互作用roteins 3。有趣的是,作为选择性剪接的结果,可以从四个备选起始密码子4产生同种型p120ctn各。亚型p120ctn各1A是最长的,因为它是从最-5' 翻译起始密码子,并含有全长N-末端片段。在同种型中p120ctn各3和4所示,该N端片段部分和完全,分别删除。了解蛋白质(或蛋白质亚型)和他们的域名在不同的细胞功能的确切作用仍然是一个挑战。
基因靶向mESCs使蛋白质功能的研究,通过相应基因的基因缺失和发育的重要疾病相关的基因和通路的识别已经广泛贡献。这一突破在反向遗传学在mESC的分离和基因靶向的领域的发展的结果,由于同源重组5 </s了>。同源重组是在其中的DNA片段的双链(DS)DNA断裂后两个相似或相同的核酸部分之间交换的过程。通常情况下,HR是低效的,因为双链DNA断裂是罕见的。最近,同源定向基因靶向的效率可以使用位点特异性核酸酶6,7被增加,但不幸的是,这些都是容易脱靶效应8。一个更可靠的技术,以使基因靶向是RMCE,这是基于位点特异性重组系统,如酶Cre / loxP位或FLPE / FRT。 loxP和FRT序列在噬菌体P1被发现和酿酒酵母 ,分别和由34个碱基对,包括确定该网站的取向的不对称8bp的序列。在另一方面,中,定向例如,DNA拉伸内的两个loxP位将决定两侧装接loxP DNA是否变得切除或I在的Cre介导的重组9 nversed。此外,Cre重组酶也可以诱导易位如果两个站点位于不同染色体上。 RMCE采用异种重组位不交叉反应和嵌入在一个基因位点的优势。在包含由相同的异种位点侧翼的DNA片段的供体质粒的存在,重组酶将插入该DNA片段成因为双同时易位( 图1)的RMCE兼容基因组基因座。在这里,只有正确RMCE靶向克隆可以使药物抗性由于对传入向量的启动子,恢复了“俘获”无启动子的新霉素抗性基因(neo R)存在于所述对接单元的R26基因组( 图1) 10,11。这导致了非常高的靶向效率,通常接近100%11,</ SUP> 12。总之,基于RMCE靶向效率高,可用于结构 – 功能研究;但是,它需要一个预先设计的基因组位点。
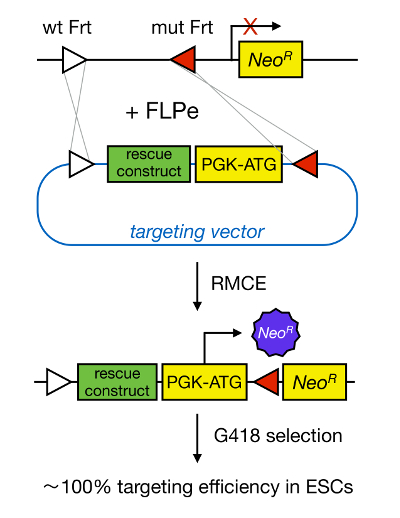
图1. RMCE介导的靶向示意图。 RMCE允许DNA片段从进入靶向载体至限定基因组基因座的交换如果两个怀有2个异种FRT位点(由白色和红色三角形描绘)。此外,工程化基因组基因座包含一个启动子和截短的新霉素抗性(NEO R)基因。通过在进入的DNA片段提供启动子和起始密码子,只有正确的重组事件恢复新霉素抗性,从而导致高的定位效率。 请点击此处查看T的放大版他的身影。
在mESCs基因组工程允许RMCE兼容小鼠的产生。在1981年,两组成功地从胚泡的内细胞团(ICM)捕获多能细胞,并且在培养13 和 14保持它们。 mESCs是能够自我更新和分化成所有类型的胚胎和成年细胞,包括生殖细胞谱系。因此,在基因靶向mESCs通过组成型或条件(使用酶Cre / loxP系统)KO小鼠的发展,使反向遗传学研究。然而,分离的小鼠ES细胞中的经典方法是非常低效的。几个重大的改进已大大增加成功率,用于导出mESC的线,包括使用限定的血清替代(SR)培养基中15的,含有SR和胎牛血清(FBS)16 mESC的介质之间交替,并且使用药理的逻辑化合物如pluripotin或2I 17。 Pluripotin,小合成分子,允许mESCs的未分化状态在不存在白血病抑制因子(LIF)和小鼠胚胎成纤维细胞(MEF中)18传播。最后,已经显示,mESCs可以以非常高的效率(接近100%)时的SR / FBS培养基交替协议与LIF和pluripotin 19,20组合来分离。这些协议使能随后用于结构 – 功能研究RMCE兼容KO mESCs的有效隔离。
本文描述了使一个以确定负责特定细胞过程的蛋白中的关键的结构域或残基的方法。为此,先进的技术,实现高效mESC的隔离,靶向载体组件和mESC的目标管道是创建天。与蛋白同种型,结构域突变体,和下游效应物,例如,大板可以在KO mESCs被引入并可以针对其营救体外 KO表型的能力进行评估。
Protocol
Representative Results
Discussion
我们mESC的隔离方法是用户友好,不需要高深的技能或设备,如囊胚显微外科。因此,这种技术是相当大的比重,科学界的访问。任何人只要有基本的细胞培养经验可以传播ICM长出,并建立mESCs线。然而,囊胚的冲洗和处理需要一些练习。甲口移液管用于传递胚泡,由微量移,微量吸管保持器,管道和抽吸嘴件28的。微量可以通过加热巴斯德吸管的部分最好为几秒钟,从火焰中除?…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
我们感谢金科D'HONT,康斯登范Rockeghem,娜塔莉Farla,凯利·莱米尔和RIET德Rycke的出色的技术支持。我们也感谢EEF Parthoens,Evelien凡Hamme的,和阿曼达·戈卡尔弗斯从炎症研究中心的生物成像核心设施为他们提供专家援助。我们承认为有价值的讨论我们的研究小组的成员。这项工作是由比利时科学政策支持(Belspo校际景点虫眼 – 奖IAPⅦ-07 DevRepair; https://devrepair.be),由伊丽莎白女王医学基金会,比利时(GSKE 2008年至2010年; HTTP:// WWW .fmre-gske.be),以及比利时根特大学(http://www.ugent.be/en/ghentuniv)的协同研究行动(GOA 01G01908)。 SG是法兰德斯研究基金(FWO-V)的博士后研究员。
Materials
| ROSALUC Mice | made in house | frozen sperm available upon request | |
| R26-iPSC mice | made in house | frozen sperm available upon request | |
| Vessel probe | Fine Science Tools | 10160-13 | to check for copulation plugs |
| M2 medium | Sigma-Aldrich | M7167 | make aliquots and store at -20°C |
| Fine forceps (Dumont #5 Standard tip Student forceps) | Fine Science Tools | 11251-10 | spray with 70% EtOH before use (do not autoclave) |
| 23G needles | Fine-ject | 8697 | |
| 1-ml syringes | Soft-ject | 6680 | |
| 60-mm bacterial grade plates (for flushing) | Gosselin | BB60-01 | |
| Mouth pipette | made in house | see discussion | |
| Mouse embryonic fibroblasts (MEFs, TgN (DR4)1 Jae strain) | ATTC | SCRC-1045 | |
| TgN (DR4)1 Jae mice | The Jackson Laboratory | 3208 | |
| Mitomycin C | Sigma-Aldrich | M0503 | |
| Phosphate buffered saline (PBS) without calcium or magnesium | Gibco | 14190-094 | |
| Tg(DR4)1Jae/J mice | JAX | 3208 | mice that contain four drug-selectable genes and DR4 MEFS confers resistance to neomycin, puromycin, hygromycin and 6-thioguanine |
| 0.1% Gelatin | Sigma-Aldrich | G1393 | Dissolve 0.5 g in 500 ml distilled water, autoclave and store at 4°C. |
| Trypsin (0.25%) | Gibco | 25200-056 | |
| 2 μM pluripotin | Cayman Chemical | 10009557 | |
| pRMCE-DV1 | BCCM/LMBP collection | LMBP 08870 | public available from the BCCM/LMBP collection (http://bccm.belspo.be) |
| cre-excised pRMCE-DV1 | BCCM/LMBP collection | LMBP 08195 | public available from the BCCM/LMBP collection (http://bccm.belspo.be) |
| pCAG-FlpE-IRES-Puro-pA | Addgene | 20733 | |
| heat-shock competent DH5α bacteria | made in house | ||
| Gateway pDONR221 vector | Thermo Fisher | 12536-017 | contains kanamycin-resistance gene |
| BP clonase II mix | Thermo Fisher | 11789-020 | |
| LR clonase II mix | Thermo Fisher | 11791-020 | |
| Luria Broth (LB) | |||
| Ampicillin | |||
| Applied Biosystems 3730XL DNA Analyzer | Thermo Fisher | 3730XL | |
| G418 | Thermo Fisher | 11811-023 | |
| Lipofectamine 2000 transfection reagent | Thermo Fisher | 11668027 | |
| Lipofectamine LTX transfection reagent | Thermo Fisher | 15338100 | |
| Effectene transfection reagent | Qiagen | 301425 | |
| GATEWAY pENTR 1A vector | Thermo Fisher | A10462 | recombination-compatible vector |
| mouse monoclonal anti-p120ctn antibody | BD Transduction Laboratories | 610134 | |
| mouse monoclonal anti-Ecadherin antibody | BD Transduction Laboratories | 610181 | |
| General equipment: | |||
| Sterile dissection tools | fine scissors and forceps for dissecting the uterus | ||
| Sterile pipettes: 5 ml, 10 ml and 25 ml | |||
| 15-ml and 50-ml conical centrifuge tubes | |||
| 96-well culture plates V-shaped bottom and flat bottom) | |||
| Culture dishes: 24 wells, 12 wells and 6 wells | |||
| Multichannel pipettes (to pipette 30, 50, 100 and 200 μl) | |||
| Sterile multichannel reservoirs | |||
| Access to a laminar air flow | |||
| Access to an incubator at 37°C with 5% CO2 | |||
| Access to an inverted microscope | |||
| Access to a bench-top centrifuge | |||
| Access to a stereo microscope with transmitted-light | |||
| Culture media: | |||
| MEF Medium: | stored at 4°C; warm 30 min at 37°C before use | ||
| Dulbecco’s modified Eagle’s medium (DMEM) | Gibco | 41965-062 | |
| 10% fetal bovine serum (FBS) | Sigma-Aldrich | F-7524 | |
| L-glutamine (2 mM) | Gibco | 25030-024 | |
| Sodium pyruvate (0.4 mM) | Gibco | 11360-039 | |
| penicillin (100 U/ml) | Gibco | 15140-122 | |
| streptomycin (100 µg/ml) | Gibco | 15140-122 | |
| SR-based mESC medium: | stored at 4°C; warm 30 min at 37°C before use | ||
| DMEM/F12 | Gibco | 31330-038 | mixed in a 1:1 ratio |
| 15% knock-out serum replacement (SR ) | Gibco | 10828–028 | |
| L-glutamine (2 mM) | Gibco | 25030-024 | |
| 0.1 mM non-essential amino acids | Gibco | 11140-050 | |
| penicillin (100 U/ml) | Gibco | 15140-122 | |
| streptomycin (100 µg/ml) | Gibco | 15140-122 | |
| β-mercaptoethanol (0.1 mM) | Sigma-Aldrich | M 3148 | |
| 2,000 U/ml recombinant mouse LIF | (IRC/VIB Protein Service facility) | ||
| FBS-based mESC medium (similar to SR-based mESC medium): | stored at 4°C; warm 30 min at 37°C before use | ||
| Knockout DMEM | Gibco | 10829-018 | |
| 15% FBS | Hyclone | SH30070.03E | |
| Differention Medium | stored at 4°C; warm 30 min at 37°C before use | ||
| Iscove's Modified Dulbecco's Medium (IMDM) | Gibco | 21980-032 | |
| 15% FBS | Hyclone | SH30070.03E | |
| 5% CD Hybridoma Medium(1x) liquid | Gibco | 11279-023 | |
| 2 mM L-glutamine | Gibco | 25030-024 | |
| 0.4 mM 1-thioglycerol | Sigma-Aldrich | M-6145 | |
| 50 μg/ml ascorbic acid | Sigma-Aldrich | A-4544 | |
| penicillin (100 U/ml) | Gibco | 15140-122 | |
| streptomycin (100 µg/ml) | Gibco | 15140-122 | |
| 2i | |||
| 1 μM Erk inhibitor PD0325901 | Axon Medchem | Axon 1408 | |
| 3 μM Gsk3 inhibitor CHIR99021 | Axon Medchem | Axon 1386 |
Riferimenti
- Gul, I. S., Hulpiau, P., Saeys, Y., van Roy, F. Metazoan evolution of the armadillo repeat superfamily. Cell Mol Life Sci. , (2016).
- Valenta, T., Hausmann, G., Basler, K. The many faces and functions of beta-catenin. EMBO J. 31, 2714-2736 (2012).
- Pieters, T., van Hengel, J., van Roy, F. Functions of p120ctn in development and disease. Front Biosci. 17, 760-783 (2012).
- Keirsebilck, A., et al. Molecular cloning of the human p120ctn catenin gene (CTNND1): Expression of multiple alternatively spliced isoforms. Genomics. 50, 129-146 (1998).
- Capecchi, M. R. Gene targeting in mice: functional analysis of the mammalian genome for the twenty-first century. Nat Rev Genet. 6, 507-512 (2005).
- Wang, H., et al. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell. 153, 910-918 (2013).
- Yang, H., et al. One-step generation of mice carrying reporter and conditional alleles by CRISPR/Cas-mediated genome engineering. Cell. 154, 1370-1379 (2013).
- Fu, Y., et al. High-frequency off-target mutagenesis induced by CRISPR-Cas nucleases in human cells. Nat Biotechnol. 31, 822-826 (2013).
- Branda, C. S., Dymecki, S. M. Talking about a revolution: The impact of site-specific recombinases on genetic analyses in mice. Dev Cell. 6, 7-28 (2004).
- Sandhu, U., et al. Strict control of transgene expression in a mouse model for sensitive biological applications based on RMCE compatible ES cells. Nucleic Acids Res. 39, 1 (2010).
- Haenebalcke, L., et al. Efficient ROSA26-based conditional and/or inducible transgenesis using RMCE-compatible F1 hybrid mouse embryonic stem cells. Stem Cell Rev. 9, 774-785 (2013).
- Pieters, T., et al. p120 Catenin-Mediated Stabilization of E-Cadherin Is Essential for Primitive Endoderm Specification. PLoS Genet. 12, e1006243 (2016).
- Evans, M. J., Kaufman, M. H. Establishment in culture of pluripotential cells from mouse embryos. Nature. 292, 154-156 (1981).
- Martin, G. R. Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells. Proc Natl Acad Sci U S A. 78, 7634-7638 (1981).
- Cheng, J., Dutra, A., Takesono, A., Garrett-Beal, L., Schwartzberg, P. L. Improved generation of C57BL/6J mouse embryonic stem cells in a defined serum-free media. Genesis. 39, 100-104 (2004).
- Bryja, V., et al. An efficient method for the derivation of mouse embryonic stem cells. Stem Cells. 24, 844-849 (2006).
- Ying, Q. L., et al. The ground state of embryonic stem cell self-renewal. Nature. 453, 519-523 (2008).
- Chen, S., et al. Self-renewal of embryonic stem cells by a small molecule. Proc Natl Acad Sci U S A. 103, 17266-17271 (2006).
- Pieters, T., et al. Efficient and User-Friendly Pluripotin-based Derivation of Mouse Embryonic Stem Cells. Stem Cell Rev. 8, (2012).
- Yang, W., et al. Pluripotin combined with leukemia inhibitory factor greatly promotes the derivation of embryonic stem cell lines from refractory strains. Stem Cells. 27, 383-389 (2009).
- Haenebalcke, L., et al. The ROSA26-iPSC Mouse: A Conditional, Inducible, and Exchangeable Resource for Studying Cellular (De)Differentiation. Cell Rep. 3, (2013).
- Tucker, K. L., Wang, Y., Dausman, J., Jaenisch, R. A transgenic mouse strain expressing four drug-selectable marker genes. Nucleic Acids Res. 25, 3745-3746 (1997).
- Nyabi, O., et al. Efficient mouse transgenesis using Gateway-compatible ROSA26 locus targeting vectors and F1 hybrid ES cells. Nucleic Acids Res. 37, 55 (2009).
- Katzen, F. Gateway((R)) recombinational cloning: a biological operating system. Expert Opin Drug Discov. 2, 571-589 (2007).
- Schaft, J., Ashery-Padan, R., vander Hoeven, F., Gruss, P., Stewart, A. F. Efficient FLP recombination in mouse ES cells and oocytes. Genesis. 31, 6-10 (2001).
- Spencer, H. L., et al. E-cadherin inhibits cell surface localization of the pro-migratory 5T4 oncofetal antigen in mouse embryonic stem cells. Mol Biol Cell. 18, 2838-2851 (2007).
- Stryjewska, A., et al. Zeb2 Regulates Cell Fate at the Exit from Epiblast State in Mouse Embryonic Stem Cells. Stem Cells. , (2016).
- Nagy, A., Gertsenstein, M., Vintersten, K., Behringer, R. . Manipulating the mouse embryo: A laboratory manual. , (2003).
- van den Berghe, V., et al. Directed migration of cortical interneurons depends on the cell-autonomous action of Sip1. Neuron. 77, 70-82 (2013).
- Li, J., et al. The EMT transcription factor Zeb2 controls adult murine hematopoietic differentiation by regulating cytokine signaling. Blood. , (2016).

