Modellering Hurtig-scanning cyklisk voltammetri data fra elektrostimulerede data om dopaminneurotransmission ved hjælp af QNsim1.0
Summary
Hurtig-scanning cyklisk voltammetri kan overvåge in vivo dopamin neurotransmission i forbindelse med stoffer, sygdom og andre eksperimentelle manipulationer. Dette arbejde beskriver implementeringen af QNsim1.0, en software til modellering af elektrisk stimulerede dopaminresponser ifølge den kvantitative neurobiologiske model for at kvantificere estimater for dopaminfrigivelse og genoptagelsesdynamik.
Abstract
Centrale dopaminerge (DAergic) veje har en vigtig rolle i en lang række funktioner, såsom opmærksomhed, motivation og bevægelse. Dopamin (DA) er impliceret i sygdomme og lidelser, herunder opmærksomhedsunderskud hyperaktivitetsforstyrrelse, Parkinsons sygdom og traumatisk hjerneskade. DA neurotransmission og metoderne til at studere det er derfor af stor videnskabelig interesse. In vivo hurtigscanning cyklisk voltammetri (FSCV) er en metode, der muliggør selektiv overvågning af DA koncentrationsændringer med fin temporal og rumlig opløsning. Denne teknik anvendes almindeligvis i forbindelse med elektriske stimuleringer af stigende DAerg-veje til styring af impulsstrømmen af dopamin-neurotransmission. Selvom det stimulerede DA-neurotransmissionsparadigme kan producere robuste DA-reaktioner med klare morfologier, hvilket gør dem modtagelige for kinetisk analyse, er der stadig meget debat om, hvordan man kan fortolke svarene med hensyn til deres DA-frigivelse og clearanCe komponenter. For at løse dette problem blev en kvantitativ neurobiologisk (QN) ramme for stimuleret DA-neurotransmission for nylig udviklet til realistisk at modellere dynamikken i DA-frigivelse og genoptagelse i løbet af et stimuleret DA-respons. Grundlaget for denne model er baseret på eksperimentelle data fra stimuleret DA neurotransmission og på principper for neurotransmission vedtaget fra forskellige forskningslinjer. QN-modellen implementerer 12 parametre relateret til stimuleret DA-frigivelse og genoptagelsesdynamik til model DA-reaktioner. Dette arbejde beskriver hvordan man simulerer DA-svar ved hjælp af QNsim1.0 og også detaljerede principper, der er blevet implementeret for systematisk at skelne for ændringer i den stimulerede dopaminfrigivelse og genoptagelsesdynamik.
Introduction
Dopamin (DA) neurotransmission spiller en afgørende rolle i forskellige kognitive og adfærdsmæssige funktioner, og dets dysfunktion er impliceret i flere almindelige sygdomme og lidelser. Som sådan er det kritisk at udvikle nøjagtige metoder til kvantitativt at studere DA-neurotransmission in vivo for at vurdere, hvordan DA-neurotransmission ændres i sammenhæng med sygdomsmodeller og lægemiddelfarmakologi. Hurtig-scanning cyklisk voltammetri (FSCV) giver mulighed for overvågning in vivo DA-neurotransmission med fin rumlig og tidsmæssig opløsning. Selv om det er muligt at overvåge fysiologisk DA-neurotransmission i våde, fritt bevæger sig dyr, kan den elektriske stimulering af stigende dopaminerge veje i bedøvede dyr frembringe robuste DA-reaktioner, som er acceptable for den forbedrede kinetiske analyse af DA-neurotransmission.
Elektrisk stimulerede DA-reaktioner afspejler et dynamisk samspil mellem DA-frigivelse og genoptagelse og fortolkningerAf disse svar har overvejende anvendt en simpel model af stimuleret DA neurotransmission kaldet Michaelis-Menten (MM) model 12 . MM-modellen består af 3 variable til at beskrive DA-responser i form af en konstant DA-frigivelseshastighed og en konstant genoptagelseseffektivitet ( dvs. forholdet mellem DA-genoptagelseshastigheden og ekstracellulære DA-koncentrationer) som beskrevet ved ligning 1 : 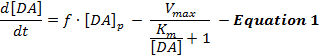
(DA frigivelse) (DA genoptagelse)
I ligning 1 er f frekvensen af stimulering; [DA] p er den estimerede DA koncentration stigning pr. Stimuleringsimpulser; V max repræsenterer den estimerede maksimale genoptagelsesrate; Og K m er den estimerede MM-konstant, som teoretisk svarer til den ekstracellulære DA-koncentration, der mætter 50% DAT, hvilket fører til en halv maksimal genoptagelseshastighed. Denne differentiAl ligning kan integreres for at simulere eksperimentelle DA responser ved at estimere [DA] p , V max og K m parametrene.
Selv om MM-modellen har lettet betydelige fremskridt inden for forståelsen af DA-neurotransmissionskinetik i forskellige eksperimentelle sammenhænge, gør MM-modellen enkle grundlæggende antagelser, som begrænser dets anvendelighed, når modellering DA-responser fremkaldes af supraphysiologiske stimuleringer 2 , 13 . For eksempel kan MM-modellen kun tilpasse DA-responsformer, hvis de stiger på en konveks måde, men den kan ikke tage højde for de gradvise (konkave) stigende responser, der findes i dorsale striatale regioner 12 . Således opfanger MM-modelantagelserne ikke nøjagtigt de dynamiske frigivelses- og genoptagelsesprocesser af stimuleret DA-neurotransmission.
At model stimulerede DA responser i henhold til en realistisk kvantItative ramme blev den kvantitative neurobiologiske (QN) ramme udviklet baseret på principper for stimuleret neurotransmissionskinetik stammer fra komplementær forskning og eksperimentering 2 . Forskellige linjer med neurotransmissionsforskning viser, at (1) stimuleret frigivelse af neurotransmitter er en dynamisk proces, der falder i hastighed i løbet af stimulering 14 , (2) frigivelsen fortsætter i post-stimuleringsfasen med bifasisk henfaldskinetik 15 og (3) DA Genoptagelseseffektivitet hæmmes progressivt i løbet af selve stimuleringen 2 , 16 . Disse tre begreber tjener som grundlaget for QN-rammen og de tre ligninger bestående af 12 parametre, der beskriver dynamikken i DA-frigivelse og genoptagelse ( tabel 1 ). QN-rammen kan nøje simulere heterogene eksperimentelle DA-svarstyper, såvel som pReducerede virkninger af eksperimentelle manipulationer af stimuleringsparametre og lægemiddeladministration 2 , 6 . Selv om yderligere forskning er nødvendig for at finjustere datamodelleringsmetoden, kan fremtidige eksperimenter i høj grad drage fordel af denne neurobiologisk orienterede modelleringsmetode, som væsentligt øger de afledninger, der er trukket fra det stimulerede DA neurotransmission paradigme.

Tabel 1: Modelleringsligninger og parametre . Klik her for at se en større version af denne figur.
Denne vejledning beskriver, hvordan man modellerer stimulerede DA-responsdata til at estimere DA-frigivelse og genoptage kinetik ved hjælp af QNsim 1.0. Den faktiske eksperimentelle dataindsamling og prOcessing er ikke beskrevet her og kræver kun tidsmæssige DA koncentrationsdata. Den teoretiske understøttelse og grundlag for QN-rammen er beskrevet i det væsentlige tidligere 2 , men et praktisk perspektiv på anvendelsen af QN-rammen på model DA-responsdata er beskrevet nedenfor.
QN-rammen modellerer det dynamiske samspil mellem: 1) dynamisk DA-frigivelse, 2) DA-genoptagelse og 3) virkningerne af suprafysiologiske stimuleringer på disse processer for at udtrække meningsfuld kinetisk information fra DA-responsdata. QN-rammen er bedst egnet til modellering af FSCV-data, der er erhvervet ved hjælp af stærkt suprafysiologiske stimuleringer af lang varighed ( f.eks. 60 Hz, 10 s stimuleringer), der producerer robuste DA-reaktioner, der kan anvendes til kinetisk analyse. Efter den nøjagtige modellering af de underliggende frigivelses- og genoptagelsesprocesser kan modelparametrene bruges til at simulere et DA-respons, der skal tilnærme formen af exPerimental DA respons.
Ligningerne af QN-rammen beskriver hastigheden af DA-frigivelse og genoptagelse i løbet af de stimulerede DA-reaktioner. QN-rammen beskriver den stimulerede DA-frigivelseshastighed som en funktion af tiden fra starten af stimulering (t- stim ), når DA-frigivelseshastigheden eksponentielt falder i løbet af stimuleringen. Dette er i overensstemmelse med udtømningen af en let frigivelig pool med en tilsat stabil DA-frigivelseshastighed (DARss) for at tage højde for vesikelpåfyldning, svarende til andre rapporter ( ligning 2 ) 14 , 17 .
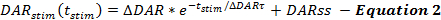
Manipulationer, der øger DA-frigivelseshastigheden, såsom forøgelse af Δ DAR, Δ DAR τ eller DARss, fører til øgede responsamplituder på DA versus tidstegninger. Hver parameTer bidrager forskelligt til DA responsformer. Forøgelse af DARss og Δ DAR τ gør begge stigende faser af svar mere lineære (mindre konvekse). Faldende Δ DAR τ fremmer konvexitet, som styres af størrelsen af Δ DAR. Baseret på modelleringserfaring er DARss generelt mindre end 1/5 af Δ DAR; Således er Δ DAR frigivelsesparameteren, der primært bestemmer den samlede responsamplitude af et DA-respons.
DA-frigivelseshastigheden efter stimulering modelleres af ligning 3 som en fortsættelse af den stimulerede DA-frigivelseshastighed fra slutningen af stimulering (DAR ES ) som en funktion af tiden efter stimulering (t- post ). Post-stimulation DA frigivelseshastigheden følger et bifasisk henfaldsmønster som tidligere beskrevet 15 med en hurtig eksponentiel henfaldsfase og en forlænget lineær henfaldsfase til model to ca.Lciumafhængige neurotransmitterfrigivelsesprocesser.
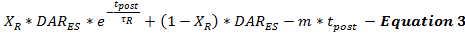
(Hurtig eksponentiel forfald) (langvarigt lineært forfald)
Det er i øjeblikket ikke muligt at bestemme, hvor meget poststimulering DA frigivelse finder sted. Denne begrænsning kan behandles ved systematisk minimering af estimater for poststimulering DA frigivelse og validering af modelparametre på tværs af et sæt eksperimentelle DA-reaktioner indsamlet fra det samme optagelsessted ved anvendelse af forskellige stimuleringsvarigheder. Denne minimering giver brugerne mulighed for at lave konservative estimater for frigivelse og genoptagelse. Fordi elektriske stimuleringer fører til kalciumakkumulering, der fremmer frigivelse efter stimulering af neurotransmitter, påvirker stimuleringstiden de post-stimulerende neurotransformerMitterfrigivelsesparametre 18 , 19 . Baseret på modelleringserfaring blev det konstateret, at som stimuleringsvarigheden stiger, øges τ R og X R falder, hvilket er i overensstemmelse med de forventede virkninger af en større calciumakkumulering 20 .
Ligning 4 beskriver DA-genoptagelseshastigheden som en forlængelse af MM-rammen og inkorporerer et dynamisk Km-udtryk, som forøges under stimulering for at modellere en gradvist faldende genoptagelseseffektivitet forårsaget af de suprafysiologiske stimuleringer 2 , 16 . Km efter stimulation holdes konstant ved Km-værdien ved stimulationens slutning (K mES ).
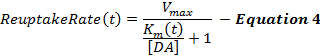
hvor,
<img alt = "Ligning 6" src = "/ files / ftp_upload / 55595 / 55595eq6.jpg" />
(Under stimulering) (Efter stimulation)
Stimulerede DA-reaktioner, især fra ventrale striatale regioner, er ofte ufølsomme over for ændringer i den indledende Km-værdi (K mi ), hvilket gør det muligt at definere en K mi- værdi problematisk. Således er, ligesom den oprindelige MM-ramme, K mi tilnærmelsesvis ved 0,1-0,4 μM for DA-reaktioner indsamlet fra kontrolbehandlede dyr 12 . Δ K m termen bestemmer omfanget af genoptagelseseffektivitetsændring under stimulering, hvilket fra vores erfaring er omkring 2081; M i løbet af en 60 Hz, 10 s stimulation. K- og K- minf-værdierne bestemmer, hvordan K m ændres over tid, og at øge en af disse vilkår fremmer koncaviteten af stigningsfasen. V max er den maksimale genoptagelseshastighed, der delvis vedrører lokal DA transportør densitet, som udviser en ventromedial til dorsolateral gradient 21 . Følgelig er Vmax-værdierne i dorsalstriatumet (D-Str) generelt større end 30 μM / s, men generelt mindre end 30 μM / s i de ventrale områder, som nukleinsummen (NAc) 6 .
De generelle retningslinjer ovenfor kan hjælpe med at modellere eksperimentelle DA-responsdata, men generering af en simulering, der nærmer sig det eksperimentelle DA-respons, kræver iterativt at justere modelparametre. Nøjagtigheden af modelparametrene kan forbedres ved at opnå DA-responser på suprafysiologiske stimuleringer, der tilvejebringerEa robust substrat til simulering samt ved at opnå og modellere flere DA-reaktioner på stimuleringer af varierende varighed på samme optagelsessted ( f.eks. 60 Hz, 5 s og 10 s stimuleringer) for at validere parameternes nøjagtighed ( Se eksempeldata). For at demonstrere er et datasæt inkluderet i softwarepakken indeholdende regiospecifikke stimulerede DA-responser indsamlet i nucleus accumbens og dorsal striatum før og efter en farmakologisk udfordring, der allerede var modelleret ved anvendelse af QN-rammen. I forlængelse heraf finder brugerne, at denne metode også kan anvendes til at karakterisere kinetikken af DA-neurotransmission i forskellige sygdomskontekster og farmakologiske manipulationer.
Protocol
Representative Results
Discussion
Brugen af FSCV til at studere in vivo- stimuleret DA-neurotransmission opstod i 1980'erne 30 og fortsætter stadig at være en rig kilde til in vivo- neurotransmissionsdata med enestående rumlig og tidsmæssig opløsning. Stimulerede DA-responser afspejler en kompleks balance af DA-frigivelse og genoptagelse, der moduleres af de elektriske stimuleringer selv. QN-modellen inkorporerer principper fra moderne neurotransmissionsforskning til model in vivo- stimul…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Vi anerkender UPMC Rehabilitation Institute for at støtte dette arbejde.
Materials
| MATLAB R2016a for Mac | Mathworks | ||
| QNsim1.0 | In house software package | Software to model FSCV data using the QN framework |
Riferimenti
- Taylor, I. M., et al. Kinetic diversity of dopamine transmission in the dorsal striatum. J Neurochem. 133 (4), 522-531 (2015).
- Harun, R., Grassi, C. M., Munoz, M. J., Torres, G. E., Wagner, A. K. Neurobiological model of stimulated dopamine neurotransmission to interpret fast-scan cyclic voltammetry data. Brain Res. 1599, 67-84 (2015).
- Taylor, I. M., Jaquins-Gerstl, A., Sesack, S. R., Michael, A. C. Domain-dependent effects of DAT inhibition in the rat dorsal striatum. Journal of neurochemistry. 122 (2), 283-294 (2012).
- Garris, P. A., Ciolkowski, E. L., Wightman, R. M. Heterogeneity of evoked dopamine overflow within the striatal and striatoamygdaloid regions. Neuroscienze. 59 (2), 417-427 (1994).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain Res. 487 (2), 311-320 (1989).
- Harun, R., et al. Fast-scan cyclic voltammetry demonstrates that L-DOPA produces dose-dependent regionally selective, bimodal effects on striatal dopamine kinetics in vivo. J Neurochem. , (2015).
- Jones, S. R., Garris, P. A., Wightman, R. M. Different effects of cocaine and nomifensine on dopamine uptake in the caudate-putamen and nucleus accumbens. The Journal of pharmacology and experimental therapeutics. 274 (1), 396-403 (1995).
- Budygin, E. A., John, C. E., Mateo, Y., Jones, S. R. Lack of cocaine effect on dopamine clearance in the core and shell of the nucleus accumbens of dopamine transporter knock-out mice. J Neurosci. 22 (10), RC222 (2002).
- Jones, S. R., et al. Loss of autoreceptor functions in mice lacking the dopamine transporter. Nat Neurosci. 2 (7), 649-655 (1999).
- Wagner, A. K., et al. Chronic methylphenidate treatment enhances striatal dopamine neurotransmission after experimental traumatic brain injury. J Neurochem. 108 (4), 986-997 (2009).
- Wagner, A. K., et al. Controlled cortical impact injury influences methylphenidate-induced changes in striatal dopamine neurotransmission. J Neurochem. 110 (3), 801-810 (2009).
- Wightman, R. M., et al. Real-time characterization of dopamine overflow and uptake in the rat striatum. Neuroscienze. 25 (2), 513-523 (1988).
- Moquin, K. F., Michael, A. C. Tonic autoinhibition contributes to the heterogeneity of evoked dopamine release in the rat striatum. J Neurochem. 110 (5), 1491-1501 (2009).
- Pyott, S. J., Rosenmund, C. The effects of temperature on vesicular supply and release in autaptic cultures of rat and mouse hippocampal neurons. J Physiol. 539 (Pt 2), 523-535 (2002).
- Atluri, P. P., Regehr, W. G. Delayed release of neurotransmitter from cerebellar granule cells. J Neurosci. 18 (20), 8214-8227 (1998).
- Wang, S. R., et al. Role of vesicle pools in action potential pattern-dependent dopamine overflow in rat striatum in vivo. J Neurochem. 119 (2), 342-353 (2011).
- Taschenberger, H., von Gersdorff, H. Fine-tuning an auditory synapse for speed and fidelity: developmental changes in presynaptic waveform, EPSC kinetics, and synaptic plasticity. J Neurosci. 20 (24), 9162-9173 (2000).
- Goda, Y., Stevens, C. F. Two components of transmitter release at a central synapse. Proc Nat Acad of Sci U S A. 91 (26), 12942-12946 (1994).
- Yao, J., Gaffaney, J. D., Kwon, S. E., Chapman, E. R. Doc2 is a Ca2+ sensor required for asynchronous neurotransmitter release. Cell. 147 (3), 666-677 (2011).
- Hagler, D. J., Goda, Y. Properties of synchronous and asynchronous release during pulse train depression in cultured hippocampal neurons. J Neurophysiol. 85 (6), 2324-2334 (2001).
- Ciliax, B. J., et al. The dopamine transporter: immunochemical characterization and localization in brain. J Neurosci. 15 (3 Pt 1), 1714-1723 (1995).
- Volz, T. J., Farnsworth, S. J., Rowley, S. D., Hanson, G. R., Fleckenstein, A. E. Methylphenidate-induced increases in vesicular dopamine sequestration and dopamine release in the striatum: the role of muscarinic and dopamine D2 receptors. J Pharm Exp Ther. 327 (1), 161-167 (2008).
- Dresel, S. H., Kung, M. P., Plossl, K., Meegalla, S. K., Kung, H. F. Pharmacological effects of dopaminergic drugs on in vivo binding of [99mTc]TRODAT-1 to the central dopamine transporters in rats. Eur J Nucl Med. 25 (1), 31-39 (1998).
- Near, J. A., Bigelow, J. C., Wightman, R. M. Comparison of uptake of dopamine in rat striatal chopped tissue and synaptosomes. J Pharm Exp Ther. 245 (3), 921-927 (1988).
- Michael, A. C., Ikeda, M., Justice, J. B. Dynamics of the recovery of releasable dopamine following electrical stimulation of the medial forebrain bundle. Neurosci Lett. 76 (1), 81-86 (1987).
- Fierro, L., DiPolo, R., Llano, I. Intracellular calcium clearance in Purkinje cell somata from rat cerebellar slices. The Journal of physiology. 510 (Pt 2), 499-512 (1998).
- Sandoval, V., Riddle, E. L., Hanson, G. R., Fleckenstein, A. E. Methylphenidate redistributes vesicular monoamine transporter-2: role of dopamine receptors. J Neurosci. 22 (19), 8705-8710 (2002).
- Daws, L. C., et al. Cocaine increases dopamine uptake and cell surface expression of dopamine transporters. Biochem Biophys Res Commun. 290 (5), 1545-1550 (2002).
- Little, K. Y., Kirkman, J. A., Carroll, F. I., Clark, T. B., Duncan, G. E. Cocaine use increases [3H]WIN 35428 binding sites in human striatum. Brain Res. 628 (1-2), 17-25 (1993).
- Ewing, A. G., Bigelow, J. C., Wightman, R. M. Direct in vivo monitoring of dopamine released from two striatal compartments in the rat. Science. 221 (4606), 169-171 (1983).
- Janezic, S., et al. Deficits in dopaminergic transmission precede neuron loss and dysfunction in a new Parkinson model. Proc Natl Acad Sci U S A. 110 (42), E4016-E4025 (2013).
- Macdonald, P. A., Monchi, O. Differential effects of dopaminergic therapies on dorsal and ventral striatum in Parkinson’s disease: implications for cognitive function. Parkinsons Dis. 2011, 572743 (2011).
- Kile, B. M., et al. Optimizing the Temporal Resolution of Fast-Scan Cyclic Voltammetry. ACS Chem Neurosci. 3 (4), 285-292 (2012).
- Venton, B. J., Troyer, K. P., Wightman, R. M. Response times of carbon fiber microelectrodes to dynamic changes in catecholamine concentration. Anal Chem. 74 (3), 539-546 (2002).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain research. 487 (2), 311-320 (1989).
- Wu, Q., Reith, M. E., Wightman, R. M., Kawagoe, K. T., Garris, P. A. Determination of release and uptake parameters from electrically evoked dopamine dynamics measured by real-time voltammetry. J Neurosci Methods. 112 (2), 119-133 (2001).

