Ved hjælp af trefarvet enkelt-molekyle FRET at studere sammenhængen af Protein interaktioner
Summary
Vi præsenterer her, en protokol for at opnå trefarvet smFRET data og sin analyse med en 3D ensemble skjulte Markov Model. Med denne tilgang, kan forskerne udtrække kinetic oplysninger fra komplekse protein systemer, herunder cooperativity eller korreleret interaktioner.
Abstract
Enkelt-molekyle Förster resonans energioverførsel (smFRET) er blevet en meget anvendt biofysiske teknik til at studere dynamikken i biomolekyler. For mange molekylære maskiner i en celle proteiner har til at handle sammen med interaktion partnere i en funktionel cyklus for at opfylde deres opgave. Udvidelse af to-farve til multi smFRET gør det muligt at samtidig sonde mere end én interaktion eller konformationel ændring. Dette ikke kun tilføjer en ny dimension til smFRET eksperimenter, men det giver også den unikke mulighed for at direkte studere sekvens af hændelser og registrere korreleret interaktioner, ved hjælp af et immobiliseret prøve og en total interne reflection fluorescens mikroskop (TIRFM). Multi-farve smFRET er derfor et alsidigt værktøj til at undersøge biomolekylære komplekser på en kvantitativ måde og i en tidligere uopnåelige detalje.
Vi viser her, hvordan man kan overvinde de særlige udfordringer, multi-farve smFRET eksperimenter på proteiner. Vi præsenterer detaljerede protokoller for at opnå data og udvinde kinetisk oplysninger. Dette omfatter trace udvælgelseskriterier, staten adskillelse og genvinding af staten baner fra den støjende data ved hjælp af en 3D ensemble skjulte Markov Model (HMM). Sammenlignet med andre metoder, er den kinetiske oplysninger ikke inddrives fra dwell tid histogrammer, men direkte fra HMM. Den maksimale sandsynlighed ramme tillader os at kritisk vurdere den kinetiske model og give meningsfulde usikkerhed for priser.
Ved at anvende vores metode til heat shock protein 90 (Hsp90), er vi i stand til at udrede nukleotid bindende og de globale konformationelle ændringer af protein. Dette tillader os at direkte observere cooperativity mellem de to nukleotid bindende lommer af Hsp90 dimer.
Introduction
Mange proteiner opfylde deres funktion i dynamisk komplekser med andre molekyler, medieret af konformationelle ændringer og forbigående foreninger på en bred vifte af tidsskalaer1,2,3. Koblet til en ekstern energikilde (fx ATP) disse dynamiske interaktioner kan føre til tekstretning i en funktionel cyklus og i sidste ende bevare ikke-ligevægt steady-state i en celle, en forudsætning for liv.
For fuldt ud at forstå disse molekylære maskiner, er en statisk beskrivelse styret af strukturelle undersøgelser ikke tilstrækkelig. Derudover er det vigtigt at have kendskab til de underliggende kinetiske model og at bestemme de kinetiske sats konstanter. Flere eksisterende metoder giver forskere til at studere dynamikken i binære interaktioner mellem to molekyler af interesse, fx overflade plasmon resonans, afslapning metoder med en spektroskopiske udlæsning (fx hop eller stoppet-flow teknikker), og Kernemagnetisk resonans. Deres anvendelighed er imidlertid i de fleste tilfælde begrænset til enkle to-stats systemer (f.eks. en bundet og en ubundet stat) på grund af den gennemsnit iboende til bulk eksperimenter. I tilfælde hvor flere stater eller mellemprodukter er involveret, giver de kun en kompleks blanding af sats-konstanter. Enkelt-molekyle metoder såsom optiske eller magnetisk pincet eller to-farve smFRET, dvs., én donor og en acceptor fluorophore, med en overflade-immobiliseret prøve kan gendanne sats konstanter for alle observerede konformationelle ændringer. Men når det kommer til interaktioner, der berører mere end én bindingssted, disse metoder være begrænset og oplysninger om mulige korrelationen mellem to (eller flere) interaktioner vil kun være tilgængelig via indirekte konklusioner fra et sæt af forsøg.
Multi-farve smFRET4,5,6,7,8,9 tilbyder mulighed for at studere samspillet mellem disse komponenter direkte, i realtid og under i nærheden af fysiologiske forhold10. Dette gør det muligt at undersøge eksempelvis strukturafhængigt bindingen af en ligand eller et andet protein8,9,11. Den samlede tilgang præsenteres her er at mærke de(n) af interesse på bestemte holdninger, til at vedhæfte en protein til overfladen af måling kammer og spore fluorescens-intensiteten over tid på en prisme-type TIRFM (for detaljer se 9 , 12). den geografiske nærhed af de forskellige farvestoffer kan derefter bestemmes fra energioverførsel mellem dem. Mærkning strategier kan variere fra protein til protein (gennemgik i 13) og retningslinjer for at undgå artefakter i smFRET målinger findes14.
Da en donor farvestof kan overføre energi til forskellige acceptor farvestoffer i en multi-farve smFRET eksperiment, er den relative placering af alle farvestoffer ikke tilgængeligt fra excitation af et farvestof alene15,16. Men i kombination med skiftevis laser excitation (ALEX17, og gennemgik i 18) denne metode giver alle spatio-temporale oplysninger på lynhurtige og sub nanometer opløsning.
Hovedstol, høj opløsning strukturelle oplysninger kan opnås ved hjælp af Inter farvestof afstande beregnes ud fra kombinationen af alle fluorescens intensiteter i en multi-farve smFRET eksperiment med ALEX. Men her vi fokusere på staten identifikation og adskillelse samt udvinding af kinetiske modeller, hvor multi-farve smFRET er uundværlig. Når “kun” struktur bestemmelse af triangulering ønskes, kan en række enklere tofarvet smFRET eksperimenter med høj signal-støj-forholdet være udført12,19.
Vi bruger den delvise fluorescens (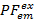 ) som en proxy for energioverførsel mellem to fluorophores7. PF er beregnet ud fra fluorescens intensitet svarer til FRET effektiviteten af en to-farvet eksperiment:
) som en proxy for energioverførsel mellem to fluorophores7. PF er beregnet ud fra fluorescens intensitet svarer til FRET effektiviteten af en to-farvet eksperiment:
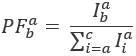
Hvor 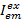 er intensiteten i emission kanal em efter excitation med farve ex, og c er acceptor med den længste bølgelængde. Opdagelse kanaler repræsenterer den samme holdning i prøve salen men optage forskellige spektrale intervaller lysets fluorescens. Den samme id for excitations- og anvendes i denne protokol (dvs., “blå”, “grønne” og “røde”).
er intensiteten i emission kanal em efter excitation med farve ex, og c er acceptor med den længste bølgelængde. Opdagelse kanaler repræsenterer den samme holdning i prøve salen men optage forskellige spektrale intervaller lysets fluorescens. Den samme id for excitations- og anvendes i denne protokol (dvs., “blå”, “grønne” og “røde”).
På grund af eksperimentelle mangler afhænger de målte fluorescens intensiteter ikke kun om energioverførsel, men også på fluorophore og setup egenskaber. For at opnå den sande energieffektivitet overførsel mellem to fluorophores, skal de målte intensitet korrigeres. Den følgende procedure er baseret på reference9. Korrektionsfaktorer for tilsyneladende lækage (lk, dvs, påvisning af fotoner fra en fluorophore i en kanal udpeget til en anden farve) og tilsyneladende gamma (ag, dvs., fluorescens kvanteudbytte af farvestoffet og den opdagelse effektivitet af kanalen) er fremstillet af enkelt-molekyle spor, der viser en acceptor blegning begivenhed.
Udsivning af donor farvestof i alle mulige acceptor kanal er beregnet ud fra alle datapunkter i de registrerede fluorescens spor hvor acceptor farvestof bleget men donor er stadig fluorescerende (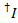 ):
):
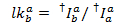
Medianværdien af lækage histogrammet bruges som tilsyneladende lækage faktor. Efter korrektion for lækage bestemmes den tilsyneladende gamma faktor fra det samme sæt af spor. Det beregnes ved at dividere ændringen af fluorescens i acceptoren kanal af ændringen af fluorescens i donor kanal ved blegning af acceptoren farvestof:
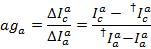
Hvor c er igen den opdagelse kanal for acceptor med den længste bølgelængde. Medianen af den resulterende distribution anvendes som tilsyneladende korrektionsfaktoren.
De korrigerede intensiteter i hver kanal er fremstillet af:
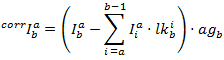
PF er derefter beregnes i henhold til:
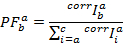
Forskellige populationer kan adskilles i multi-dimensionelle rum som PFs. Position og bredde i hver stat bestemmes af montering af data med multi-dimensional Gaussisk funktioner. Efterfølgende optimering af en global HMM baseret på alle PF spor giver en kvantitativ beskrivelse af de observerede kinetik. Selv små ændringer i satserne kan registreres.
HMMs give en måde at udlede en stat model fra en samling af støjende tid spor. Systemet anses for at være i en af et sæt af diskret, skjult stater på et givet tidspunkt og den faktiske observation (dvs. emissionen) er en probabilistisk funktion af denne skjulte tilstand20. I tilfælde af TIRFM smFRET data, kan den emission Sandsynligheder bjeg pr. stat, jeg modelleret af kontinuerlig Gaussisk betafordelingen funktioner. På regelmæssigt fordelte diskret tid point, kan overgange fra den ene til en anden stat forekomme efter overgangen sandsynligheden af, er tid-invariant og kun afhænger af den aktuelle tilstand. Overgangen matrix A indeholder disse overgang sandsynligheder enij mellem alle skjulte stater. Starttilstand fordeling 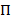 giver de statsspecifikke sandsynligheder
giver de statsspecifikke sandsynligheder 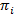 for den første tidspunkt for en tid spor. Bruger en maksimum-sandsynligheden tilgang, kan disse parametre være optimeret til at bedst beskriver dataene med den frem-tilbage og Baum-Welch algoritmer20,21. Dette giver maksimal sandsynligheden estimatorer (MLE). Endelig, den stat sekvens, der mest sandsynligt produceret bane af observationer kan udledes med Viterbi algoritme. I modsætning til andre HMM analyser af smFRET data24,25,26 bruger vi ikke HMM som en blot “udjævning” af data, men ekstrakt kinetic state-modellen fra datasættet uden behov for passende hviletid histogrammer27. HMM analyse er færdig med in-house scripts ved hjælp af Igor Pro. Gennemførelsen af kodeksen er baseret på reference21. Vi leverer en software kit og eksemplarisk data på vores webside for at følge afsnit 5 og 6 i denne protokol (https://www.singlemolecule.uni-freiburg.de/software/3d-fret). Fuld software er tilgængelig efter anmodning.
for den første tidspunkt for en tid spor. Bruger en maksimum-sandsynligheden tilgang, kan disse parametre være optimeret til at bedst beskriver dataene med den frem-tilbage og Baum-Welch algoritmer20,21. Dette giver maksimal sandsynligheden estimatorer (MLE). Endelig, den stat sekvens, der mest sandsynligt produceret bane af observationer kan udledes med Viterbi algoritme. I modsætning til andre HMM analyser af smFRET data24,25,26 bruger vi ikke HMM som en blot “udjævning” af data, men ekstrakt kinetic state-modellen fra datasættet uden behov for passende hviletid histogrammer27. HMM analyse er færdig med in-house scripts ved hjælp af Igor Pro. Gennemførelsen af kodeksen er baseret på reference21. Vi leverer en software kit og eksemplarisk data på vores webside for at følge afsnit 5 og 6 i denne protokol (https://www.singlemolecule.uni-freiburg.de/software/3d-fret). Fuld software er tilgængelig efter anmodning.
Tid punkter i data med PF < -1 eller PF > 2 i enhver opdagelse kanal er tildelt minimal emission sandsynligheden for alle stater (10-200). Dette forhindrer kunstige overgange på disse datapunkter.
Parametre for emission Sandsynligheder er fremstillet af anfald af 3D PF histogrammet med Gaussisk funktion som beskrevet i trin 5.7. Disse parametre holdes fast under optimering af HMM.
I metoden præsenteres starttilstand distribution vektor og overgangen matrix anvendes globalt til at beskrive hele ensemblet af spor. De opdateres baseret på alle N molekyler fra datasæt efter reference27.
Startparametre i den oprindelige tilstand distribution bestemmes ud fra 2D fremskrivninger af PF histogram (trin 5.3) og overgangen sandsynligheder er indstillet til 0,05 med undtagelse af sandsynligheder til ophold i den samme stat, som er valgt sådan at sandsynligheden for at forlade en bestemt stat er normaliseret til enhed.
En sandsynlighed profilering metode bruges til at give konfidensintervaller (CIs) for alle overgang priser21,22, der tjener som meningsfuld estimater for deres usikkerhed. For at beregne rammerne af CI for en bestemt frekvens, er overgang sandsynligheden af interesse fastgjort til en anden værdi end MLE. Dette giver test model λ’. En risiko ratio (LR) test sandsynligheden for 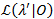 given datasæt 0 er udført i henhold til:
given datasæt 0 er udført i henhold til:
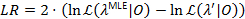
95% konfidensinterval bundet for parameteren er nået, når LR overstiger 3.841, 95% fraktil af en x2-fordelingen med en grad af frihed22,23.
Kraften i metoden er påvist ved hjælp af Hsp90. Dette rigeligt protein der findes i bakterier og eukaryoter og er en del af cellulært stress reaktion28. Det er en lovende drug target i cancer behandling29. Hsp90 er en homodimer med et nukleotid bindende lomme i hver underenhed30N-terminale domæne. Det kan gennemgå overgange mellem mindst to globalt forskellige konformationer, et lukket og et N-terminale åben, V-formet kropsbygning19,31,32. Dimerisk karakter rejser direkte spørgsmålet om samspillet mellem de to nukleotid-bindingssteder i Hsp90.
I følgende giver vi en trinvis protokol til dataopsamling og analyse af en trefarvet smFRET eksperiment på gær Hsp90 og nukleotid. Strukturafhængigt bindingen af fluorescently mærket AMP-PNP (AMP-PNP *, en ikke-hydrolyserbar analog af ATP) er analyseret. Anvendelse af den beskrevne procedure tillader undersøgelse af nukleotid bindende og samtidig Hsp90 konformationelle ændringerne og afslører dermed cooperativity mellem de to nukleotid bindende lommer af Hsp90.
Protocol
Representative Results
Discussion
Vi præsenterer den eksperimentelle procedure for at opnå trefarvet smFRET data for et komplekst protein system og en trinvis beskrivelse af analysen af disse målinger. Denne tilgang giver enestående mulighed for direkte vurdere sammenhængen mellem flere interaktion websteder eller konformationelle ændringer.
For at opnå passende flerfarvet enkelt-molekyle data proteiner er det vigtigt at udføre reproducerbare målinger på et lavt støjniveau. Dette kan opnås ved hjælp af en effektiv…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette arbejde er finansieret af den tyske Forskningsfonds (INST 39/969-1) og det Europæiske Forskningsråd gennem ERC tilskudsaftalen n. 681891.
Materials
| Setup | |||
| vibration-damped optical table | Newport, Irvine, CA, USA | RS2000 | |
| OBIS 473nm LX 75mW LASER | Coherent Inc, Santa Clara, CA, USA | 1185052 | |
| OBIS 532nm LS 50mW LASER | Coherent Inc, Santa Clara, CA, USA | 1261779 | |
| OBIS 594nm LS 60mW LASER | Coherent Inc, Santa Clara, CA, USA | 1233470 | |
| OBIS 637nm LX 140mW LASER | Coherent Inc, Santa Clara, CA, USA | 1196625 | |
| laser control unit | Coherent Inc, Santa Clara, CA, USA | 1234465 | Scientific Remote |
| aspheric telescope lenses | Thorlabs Inc, Newton, New Jersey, USA | d=25.4mm, f=50mm and f=100mm | |
| CF ex1 | AHF analysentechnik AG, Tübingen, Germany | ZET 473/10 | cleanup filter excitation |
| CF ex2 | AHF analysentechnik AG, Tübingen, Germany | ZET 532/10 | cleanup filter excitation |
| CF ex3 | AHF analysentechnik AG, Tübingen, Germany | ZET 594/10 | cleanup filter excitation |
| CF ex4 | Thorlabs Inc, Newton, New Jersey, USA | FL635-10 | cleanup filter excitation |
| DM ex1 | AHF analysentechnik AG, Tübingen, Germany | ZQ594RDC | dichroic mirror excitation |
| DM ex2 | AHF analysentechnik AG, Tübingen, Germany | 570DCXR | dichroic mirror excitation |
| DM ex3 | AHF analysentechnik AG, Tübingen, Germany | ZQ491RDC | dichroic mirror excitation |
| AOTFnC-Vis | AA Opto-Electronic, Orsay, France | ||
| λ/4 plate | Thorlabs Inc, Newton, New Jersey, USA | AQWP05M-600 | |
| CFI Apo TIRF 100x | Nikon Instruments Inc, Melville, NY, USA | high-NA objective | |
| piezo focus positioner MIPOS 250 CAP | piezosystem jena GmbH, Jena, Germany | Piezo Controller NV 40/1 CLE | |
| piezo stepper | Newport, Irvine, CA, USA | PZA12 | PZC200-KT NanoPZ Actuator Kit |
| achromatic aspheric lenses | Qioptiq Photonics GmbH & Co. KG, Göttingen, Germany | G322-304-000 | d=50mm, f=200mm |
| adjustable optical slit | Owis GmbH, Staufen i. Br., Germany | 27.160.1212 | max. aperture 12 x 12 mm |
| DM det1 | AHF analysentechnik AG, Tübingen, Germany | T 600 LPXR | dichroic mirror detection |
| DM det2 | AHF analysentechnik AG, Tübingen, Germany | H 560 LPXR superflat | dichroic mirror detection |
| DM det3 | AHF analysentechnik AG, Tübingen, Germany | HC BS R635 | dichroic mirror detection |
| BP det1 | AHF analysentechnik AG, Tübingen, Germany | 525/40 BrightLine HC | bandpass filter detection |
| BP det2 | AHF analysentechnik AG, Tübingen, Germany | 586/20 BrightLine HC | bandpass filter detection |
| BP det3 | AHF analysentechnik AG, Tübingen, Germany | 631/36 BrightLine HC | bandpass filter detection |
| BP det4 | AHF analysentechnik AG, Tübingen, Germany | 700/75 ET Bandpass | bandpass filter detection |
| optical shutters detection | Vincent Associates, Rochester, NY, USA | Uniblitz VS25S2T0 | |
| EMCCD iXon Ultra 897 | Andor Technology Ltd, Belfast, Northern Ireland | ||
| digital I/O card, PCIe-6535 | National Instruments, Austin, Texas, USA | ||
| syringe pump | Harvard Apparatus, Holliston, MA, USA | PHD22/2000 | |
| Name | Company | Catalog Number | Comments |
| Flow chamber | |||
| quartz slides | G. Finkenbeiner Inc, Waltham, MA, USA | Spectrosil2000, h=3mm | |
| TEGADERM film | 3M Deutschland GmbH, Neuss, Germany | 1626W | 10 x 12cm |
| spray adhesive | 3M Deutschland GmbH, Neuss, Germany | Photo Mount 050777 | |
| glycerol | Carl Zeiss AG, Oberkochen, Germany | Immersol G | |
| immersion oil | OLYMPUS EUROPA SE & CO. KG, Hamburg, Germany | IMMOIL-F30CC | |
| prism | Vogelsberger Quarzglastechnik GmbH, Hauzenberg, Germany | Suprasil1 | |
| aluminium prism holder | custom built | ||
| hollow setscrews | Thorlabs Inc, Newton, New Jersey, USA | with custom drilling | |
| Tygon S3 E-3603 tubing | neoLab Migge GmbH, Heidelberg, Germany | 2-4450 | ACF00001 |
| PTFE tubing | Bohlender GmbH, Grünsfeld, Germany | S1810-08 | |
| Name | Company | Catalog Number | Comments |
| Sample | |||
| yeast Hsp90 D61C, Q385C_biotin | UniProt ID P02829 | ||
| Maleimide derivatives of Atto488, Atto550 | ATTO-TEC GmbH, Siegen, Germany | ||
| AMP-PNP* | Jena Bioscience, Jena, Germany | γ-[(6-Aminohexyl)-imido]-AMP-PNP-Atto647N | |
| Fluospheres | Thermo Fisher Scientific, Waltham, MA, USA | F8764 | amine-modified, 0.2 μm, yellow-green fluorescent |
| Name | Company | Catalog Number | Comments |
| Software | |||
| Andor Solis | Andor Technology Ltd, Belfast, Northern Ireland | version 4.30 | |
| LabVIEW | National Instruments, Austin, Texas, USA | version 2012, 32bit; misc. hardware control | |
| MDS control software | AA Opto-Electronic, Orsay, France | version 2.03a | |
| Coherent Connection | Coherent Inc, Santa Clara, CA, USA | version 3 | |
| Igor Pro | WaveMetrics Inc, Portland, OR, USA | version 6.37 |
Riferimenti
- Nooren, I. M. A., Thornton, J. M. Diversity of protein-protein interactions. EMBO J. 22 (14), 3486-3492 (2003).
- Marsh, J. A., Teichmann, S. A. Structure, dynamics, assembly, and evolution of protein complexes. Annu Rev Biochem. 84, 551-575 (2015).
- Henzler-Wildman, K., Kern, D. Dynamic personalities of proteins. Nature. 450 (7172), 964-972 (2007).
- Hohng, S., Joo, C., Ha, T. Single-Molecule Three-Color FRET. Biophys J. 87 (2), 1328-1337 (2004).
- Person, B., Stein, I. H., Steinhauer, C., Vogelsang, J., Tinnefeld, P. Correlated movement and bending of nucleic acid structures visualized by multicolor single-molecule spectroscopy. ChemPhysChem. 10 (9-10), 1455-1460 (2009).
- Lee, J., Lee, S., Ragunathan, K., Joo, C., Ha, T., Hohng, S. Single-molecule four-color FRET. Angew Chem Int Ed. 49 (51), 9922-9925 (2010).
- Ratzke, C., Berkemeier, F., Hugel, T. Heat shock protein 90’s mechanochemical cycle is dominated by thermal fluctuations. Proc Natl Acad Sci U S A. 109 (1), 161-166 (2012).
- Ratzke, C., Hellenkamp, B., Hugel, T. Four-colour FRET reveals directionality in the Hsp90 multicomponent machinery. Nat Commun. 5, 4192 (2014).
- Götz, M., Wortmann, P., Schmid, S., Hugel, T. A Multicolor Single-Molecule FRET Approach to Study Protein Dynamics and Interactions Simultaneously. Methods Enzymol. 581, 487-516 (2016).
- Yengo, C. M., Berger, C. L. Fluorescence anisotropy and resonance energy transfer: Powerful tools for measuring real time protein dynamics in a physiological environment. Curr Opin Pharmacol. 10 (6), 731-737 (2010).
- Wortmann,P , ., Götz M, ., Hugel T , . Cooperative Nucleotide Binding in Hsp90 and Its Regulation by Aha1. Biophys J. 113, 1711-1718 (2017).
- Dörfler, T., Eilert, T., Röcker, C., Nagy, J., Michaelis, J. Structural Information from Single-molecule FRET Experiments Using the Fast Nano-positioning System. J Vis Exp. (120), e54782 (2017).
- Stephanopoulos, N., Francis, M. B. Choosing an effective protein bioconjugation strategy. Nature chemical biology. 7 (12), 876-884 (2011).
- Sánchez-Rico, C., Voith von Voithenberg, L., Warner, L., Lamb, D. C., Sattler, M. Effects of Fluorophore Attachment on Protein Conformation and Dynamics Studied by spFRET and NMR Spectroscopy. Chemistry (Weinheim an der Bergstrasse, Germany). , (2017).
- Roy, R., Hohng, S., Ha, T. A practical guide to single-molecule FRET. Nat Methods. 5 (6), 507-516 (2008).
- Lee, N. K., et al. Three-color alternating-laser excitation of single molecules: monitoring multiple interactions and distances. Biophys J. 92 (1), 303-312 (2007).
- Kapanidis, A. N., Lee, N. K., Laurence, T. A., Doose, S., Margeat, E., Weiss, S. Fluorescence-aided molecule sorting: analysis of structure and interactions by alternating-laser excitation of single molecules. Proc Natl Acad Sci U S A. 101 (24), 8936-8941 (2004).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chem Soc Rev. 43 (4), 1156-1171 (2014).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nat Methods. 14, 174-180 (2017).
- Rabiner, L. R. A tutorial on hidden Markov models and selected applications in speech recognition. Proc IEEE. 77 (2), 257-286 (1989).
- Fink, G. A. . Markov Models for Pattern Recognition. , (2014).
- Giudici, P., Ryden, T., Vandekerkhove, P. Likelihood-Ratio Tests for Hidden Markov Models. Biometrics. 56 (3), 742-747 (2000).
- Visser, I., Raijmakers, M. E. J., Molenaar, P. C. M. Confidence intervals for hidden Markov model parameters. Br J Math Stat Psychol. 53 (2), 317-327 (2000).
- McKinney, S. A., Joo, C., Ha, T. Analysis of Single-Molecule FRET Trajectories Using Hidden Markov Modeling. Biophys J. 91 (5), 1941-1951 (2006).
- Bronson, J. E., Fei, J., Hofman, J. M., Gonzalez, R. L., Wiggins, C. H. Learning Rates and States from Biophysical Time Series: A Bayesian Approach to Model Selection and Single-Molecule FRET Data. Biophys J. 97 (12), 3196-3205 (2009).
- Greenfeld, M., Pavlichin, D. S., Mabuchi, H., Herschlag, D. Single Molecule Analysis Research Tool (SMART): an integrated approach for analyzing single molecule data. PLoS ONE. 7 (2), e30024 (2012).
- Schmid, S., Götz, M., Hugel, T. Single-Molecule Analysis beyond Dwell Times: Demonstration and Assessment in and out of Equilibrium. Biophys J. 111 (7), 1375-1384 (2016).
- Taipale, M., Jarosz, D. F., Lindquist, S. HSP90 at the hub of protein homeostasis: emerging mechanistic insights. Nat Rev Mol Cell Biol. 11 (7), 515-528 (2010).
- Trepel, J., Mollapour, M., Giaccone, G., Neckers, L. Targeting the dynamic HSP90 complex in cancer. Nat Rev Cancer. 10 (8), 537-549 (2010).
- Wayne, N., Bolon, D. N. Dimerization of Hsp90 is required for in vivo function. Design and analysis of monomers and dimers. J Biol Chem. 282 (48), 35386-35395 (2007).
- Ali, M. M. U., et al. Crystal structure of an Hsp90-nucleotide-p23/Sba1 closed chaperone complex. Nature. 440 (7087), 1013-1017 (2006).
- Southworth, D. R., Agard, D. A. Species-dependent ensembles of conserved conformational states define the Hsp90 chaperone ATPase cycle. Mol Cell. 32 (5), 631-640 (2008).
- Blanchard, S. C., Kim, H. D., Gonzalez, R. L., Puglisi, J. D., Chu, S. tRNA dynamics on the ribosome during translation. Proc Natl Acad Sci U S A. 101 (35), 12893-12898 (2004).
- Aitken, C. E., Marshall, R. A., Puglisi, J. D. An Oxygen Scavenging System for Improvement of Dye Stability in Single-Molecule Fluorescence Experiments. Biophys J. 94 (5), 1826-1835 (2008).
- Swoboda, M., et al. Enzymatic oxygen scavenging for photostability without pH drop in single-molecule experiments. ACS Nano. 6 (7), 6364-6369 (2012).
- Rognoni, L., Stigler, J., Pelz, B., Ylänne, J., Rief, M. Dynamic force sensing of filamin revealed in single-molecule experiments. Proc Natl Acad Sci U S A. 109 (48), 19679-19684 (2012).
- Okumus, B., Wilson, T. J., Lilley, D. M. J., Ha, T. Vesicle encapsulation studies reveal that single molecule ribozyme heterogeneities are intrinsic. Biophys J. 87 (4), 2798-2806 (2004).
- Boukobza, E., Sonnenfeld, A., Haran, G. Immobilization in Surface-Tethered Lipid Vesicles as a New Tool for Single Biomolecule Spectroscopy. J Phys Chem B. 105 (48), 12165-12170 (2001).
- Levene, M. J., Korlach, J., Turner, S. W., Foquet, M., Craighead, H. G., Webb, W. W. Zero-mode waveguides for single-molecule analysis at high concentrations. Science. 299 (5607), 682-686 (2003).
- Panaretou, B., et al. ATP binding and hydrolysis are essential to the function of the Hsp90 molecular chaperone in vivo. EMBO J. 17 (16), 4829-4836 (1998).

